Гемостатические средства
Гемостатические средства — лекарственные средства, способствующие остановке кровотечений. Все гемостатики, в зависимости от механизма действия, подразделяются на три большие группы:
- ингибиторы фибринолиза (антифибринолитики);
- средства, усиливающие свертывание крови (коагулянты);
- средства, понижающие сосудистую проницаемость.
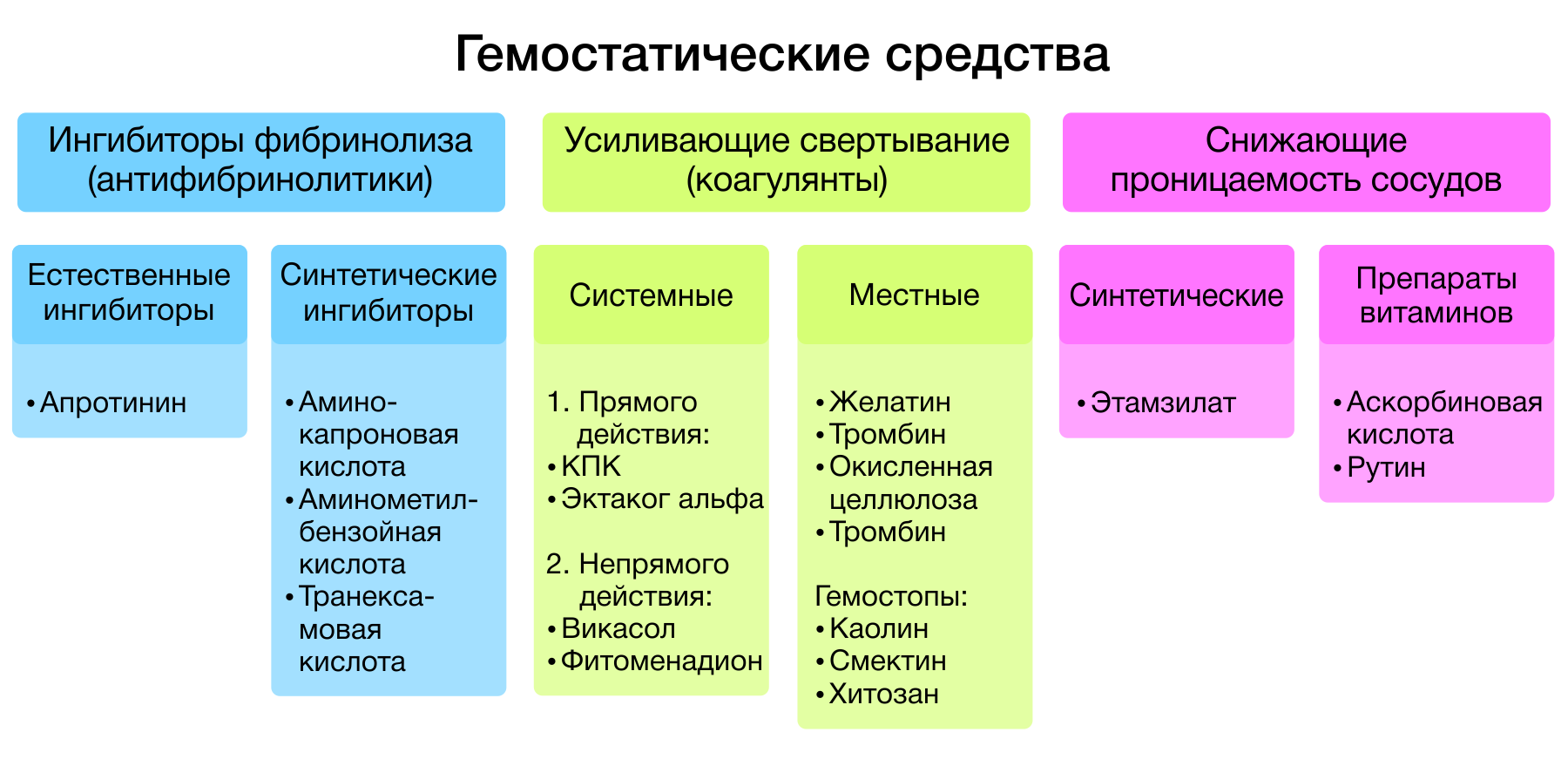
Рисунок 1 | Классификация гемостатиков.
1. Ингибиторы фибринолиза.
В клинической практике широкое распространение получили две группы препаратов ингибиторов фибринолиза: естественные ингибиторы фибринолиза (апротинин и его аналоги) и синтетические ингибиторы фибринолиза (аминокапроновая кислота, аминометилбензойная кислота, транексамовая кислота).
Апротинин — полипептид, получаемый из легких, поджелудочной и околоушной желез крупного рогатого скота, действующий аналогично α2-антиплазмину. Апротинин разрушает свободный плазмин, практически не взаимодействует со связанным плазмином, а также угнетает активацию тромбоцитов. Являясь сериновой протеазой, апротинин блокирует калликреин-кининовую систему путем разрушения калликреина, снижает активность отдельных протеолитических ферментов, таких как: трипсин, химотрипсин, кининогеназа. Изначально препарат был включен в рекомендации по лечению острого панкреатита и панкреонекроза, однако не подтвердил свою эффективность, и показания к его применению были пересмотрены.[1]
Аминокапроновая кислота – 6-аминогексановая кислота — синтетическое производное лизина. Присоединяясь к лизин-связывающему участку плазминогена, аминокапроновая кислота обратимо блокирует процесс фибринолиза, снижает активность стрептокиназы, урокиназы, тканевых киназ, калликреина, трипсина и гиалуронидазы. Аналогичным фармакологическим эффектом обладает производное аминокапроновой кислоты — аминометилбензойная кислота, отличающаяся улучшенной фармакокинетикой. Аминокапроновая кислота снижает активность тромболитических препаратов и может быть использована для нейтрализации их эффекта.
Транексамовая кислота — транс-4-(аминометил)-циклогексанкарбоновая кислота — обратимо блокирует эффект плазминогена, адгезию лейкоцитов и тромбоцитов на поверхность тромба за счет конкурентного ингибирования активатора плазминогена. Оказывает противоаллергическое и противовоспалительное действие посредством подавления образования кининов и других активных пептидов, участвующих в аллергических и воспалительных реакциях. По мощности антифибринолитического действия транексамовая кислота значительно превосходит аминокапроновую кислоту. Активность препарата в плазме сохраняется на протяжении 7-8 часов, в тканях — до 17 часов.[2]
У больных с высоким риском массивной кровопотери в плановой хирургии (сердечно-сосудистая хирургия, травматология и ортопедия, трансплантология) применение ингибиторов фибринолиза уменьшает интраоперационную кровопотерю и снижает потребность в трансфузии донорской крови. На протяжении 20 лет проводилось множество исследований, результаты которых были неоднозначны: мнения склонялись то в пользу апротинина, то в пользу синтетических производных лизина.
В 2007 году компания Bayer завершила исследование BART (Blood conservation using antifibrinolytics in a randomized trial), в котором было изучено действие апротинина у кардиохирургических больных высокого риска. Исследователи выявили большой риск летальных исходов и осложнений при использовании апротинина. В группе апротинина количество больных с массивной кровопотерей было несколько меньше, но 30-дневная летальность на 50% превышала аналогичный показатель в других группах.[3]
После публикации результатов BART компания Bayer уведомила Управление по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) о намерении изъять апротинин с рынка. Показания к назначению были пересмотрены, и препарат был исключен из списка безопасных лекарственных средств.
Огромный мета-анализ позволил сделать вывод, что транексамовая кислота обеспечивает такое же снижение периоперационной трансфузии, какое наблюдается при использовании апротинина, но более безопасна. Согласно рекомендациям Европейского общества анестезиологов по ведению пациентов с массивной периоперационной кровопотерей (2013 г.), при массивном кровотечении рекомендуется применение транексамовой кислоты (20-25 мг/кг); она может быть введена повторно или применяться в виде пролонгированной инфузии (1-2 мг/кг/ч).[4]
2. Препараты, усиливающие свертывание крови
Среди средств, повышающих скорость свертывания крови, выделяют: средства системного действия и для местного применения. К препаратам системного действия относят непрямые коагулянты (фитоменадион, менадиона натрия бисульфит) и коагулянты прямого действия (факторы свертывания: концентрат протромбинового комплекса, эптаког альфа).
Менадиона натрия бисульфит — синтетический водорастворимый аналог витамина К3. Субстратно стимулирует витамин K-редуктазу, активирующую витамин К и обеспечивающую его участие в печеночном синтезе витамин K-зависимых плазменных факторов гемостаза (II, VII, IX, X). Фитоменадион является синтетическим структурным аналогом витамина К1, обладает большей активностью и более ранним началом реализации эффектов (через 6-10 часов после перорального применения, против 18-24 часов у менадиона натрия бисульфита). Данная группа препаратов показана для коррекции нарушений системы гемостаза, вызванных дефицитом витамина К1, передозировкой антикоагулянтов непрямого действия (варфарина), а также для предоперационной профилактики кровотечений.
Концентрат протромбинового комплекса (КПК) — лекарственный препарат, содержащий факторы II, VII, IX, X, а также следовые концентрации антитромбина III, гепарина, протеинов С и S. Основным показанием к применению КПК служит коррекция приобретенного дефицита витамин К1-зависимых факторов в экстренных ситуациях (кровотечение, экстренная операция). Помимо этого, КПК широко используется как средство для лечения и профилактики кровотечений у пациентов с врожденным дефицитом одного из К1 зависимых факторов свертывания (врожденная гипопротромбинемия, врожденный дефицит фактора Стюарта – Прауэра).[5]
Эптаког альфа — рекомбинантный активированный VII фактор свертывания. Механизм действия препарата заключается в прямой активации фактора Х на поверхности активированных тромбоцитов. Это вызывает «тромбиновый взрыв» независимо от имеющейся концентрации факторов VIIIa и IXa. В результате образуется стабильный фибриновый сгусток. Считается, что эптаког альфа инициирует гемостаз только в месте повреждения ткани и не вызывает системной активации механизмов свертывания. Препарат был разработан для лечения кровотечений и проведения хирургических вмешательств у пациентов с наследственной или приобретенной гемофилией и высоким титром ингибитора факторов свертывания VIIIa или IXa. Его применение у пациентов с массивным кровотечением можно сформулировать согласно рекомендациям ESA (2013): «Применение рекомбинантного фактора VII возможно только при кровотечениях, которые не могут быть устранены хирургическими методами или путем комплексной гемостаз-корригирующей терапии». Необходимо серьезное обоснование для применения данного препарата [6].
3. Местные гемостатики
Местные гемостатики используются для остановки капиллярных и паренхиматозных кровотечений преимущественно в неотложной хирургии и стоматологии. Данная группа включает в себя широкий спектр препаратов с различным механизмом действия.
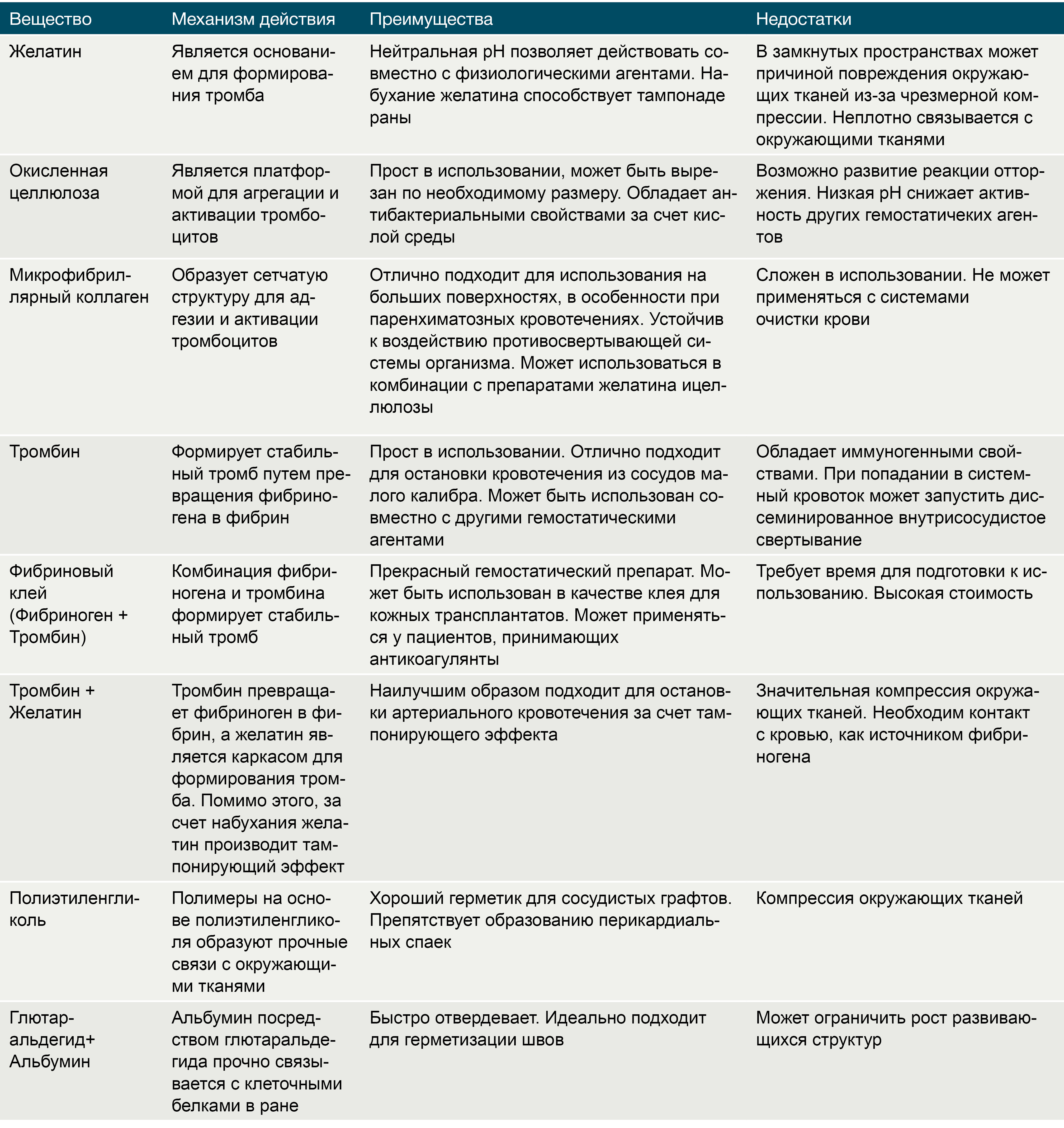
Препараты на основе желатина, получаемого из свиной кожи, существуют в трех формах: пленка, губка и порошок. Желатин чрезвычайно гигроскопичен, и за счет этого свойства он абсорбирует влагу, увеличиваясь в размерах и заполняя тканевой дефект. Существуют комбинации желатина с тромбином, которые помимо пассивного гемостатического эффекта напрямую запускают коагуляционный каскад и активируют тромбоциты в месте нанесения. Желатин разрушается протеиназами в течение 4-6 недель. Несмотря на абсолютную индифферентность, желатин может служить в качестве хронического очага инфекции. Помимо этого, одним из существенных недостатков данных препаратов является отсутствие прочных связей с окружающими тканями [7].
Тромбин является естественным компонентом свертывающей системы крови. Раствор тромбина используют только местно при капиллярных или паренхиматозных кровотечениях в ходе нейрохирургических вмешательств, операций на печени и почках, в стоматологической практике. Попадание тромбина в крупные кровеносные сосуды может вызвать распространенный тромбоз [7].
Окисленная целлюлоза выпускается в виде пленок, сеток, пучков и губок. Данный биологический агент играет роль субстрата для агрегации тромбоцитов и активации механизмов гемостаза. Целлюлоза значительно снижает рН среды, что приводит к лизису эритроцитов с образованием кислого гематина, который формирует дополнительный искусственный сгусток. Помимо этого окисленная целлюлоза обладает антибактериальным эффектом, в том числе в отношении антибиотикорезистентных микроорганизмов [7].
Микрофибриллярный коллаген, производимый из кожи крупного рогатого скота, имеет ряд преимуществ перед остальными топическими биологическими кровоостанавливающими агентами, среди которых: быстрый гемостатический эффект, минимальная реактивность тканей и высокая способность к реабсорбции. Аналогично целлюлозе, микрофибриллярный коллаген является матрицей для активации тромбоцитов, агрегации и образования тромбов [7].
Подвидом местных кровоостанавливающих средств являются гемостопы, получившие большое распространение в военной медицине. Это препараты внешнего воздействия, которые почти не влияют на свертывающую и противосвертывающую системы крови. Многообразие форм выпуска обеспечивает удобство применения в полевых условиях и полностью удовлетворяет потребностям оказания неотложной помощи при любых кровотечениях. На сегодняшний день наиболее эффективным средством считается хитозан.
Хитозан – это полисахаридный биополимер, получаемый из хитиновых панцирей ракообразных. Кровоостанавливающий эффект данного вещества достигается путем связывания хлопьев хитозана с отрицательно-заряженными эритроцитами и образования гелеобразного сгустка в месте контакта с кровью. Среди преимуществ препаратов на основе хитозана выделяют его антимикробные свойства, длительный срок хранения, стабильность при перепадах температур и безопасность при наружном использовании [8].
Наиболее известным представителем группы средств, понижающих сосудистую проницаемость, является этамзилат. Гемостатический эффект данного препарата обусловлен активацией тромбопластина в месте повреждения сосудов микроциркуляторного русла и снижением синтеза простациклина PGI-2 в эндотелии сосудов, что в конечном итоге приводит к усилению адгезии и агрегации тромбоцитов, остановке или уменьшению кровоточивости. За счет антигиалуронидазного действия этамзилат обладает ангиопротективным эффектом, улучшает микроциркуляцию и нормализует проницаемость сосудистой стенки при патологических процессах [9].
Источники
- Fergusson D. A. et al. A comparison of aprotinin and lysine analogues in high-risk cardiac surgery //New England Journal of Medicine. – 2008. – Т. 358. – №. 22. – С. 2319-2331.
- Williams-Johnson J. A. et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial //West Indian Medical Journal. – 2010. – Т. 59. – №. 6. – С. 612-624.
- Ferraris V. A. et al. Perioperative blood transfusion and blood conservation in cardiac surgery: the Society of Thoracic Surgeons and The Society of Cardiovascular Anesthesiologists clinical practice guideline //The Annals of thoracic surgery. – 2007. – Т. 83. – №. 5. – С. S27-S86.
- Sedrakyan A., Treasure T., Elefteriades J. A. Effect of aprotinin on clinical outcomes in coronary artery bypass graft surgery: a systematic review and meta-analysis of randomized clinical trials //The Journal of thoracic and cardiovascular surgery. – 2004. – Т. 128. – №. 3. – С. 442-448.
- Song H. K. et al. Safety and efficacy of prothrombin complex concentrates for the treatment of coagulopathy after cardiac surgery //The Journal of thoracic and cardiovascular surgery. – 2014. – Т. 147. – №. 3. – С. 1036-1040.
- Shapiro A. D. et al. Prospective, randomised trial of two doses of rFVIIa (NovoSeven) in haemophilia patients with inhibitors undergoing surgery //Thrombosis and haemostasis. – 1998. – Т. 79. – №. 05. – С. 773-778.
- Achneck H. E. et al. A comprehensive review of topical hemostatic agents: efficacy and recommendations for use //Annals of surgery. – 2010. – Т. 251. – №. 2. – С. 217-228.
- McManus J. G., Wedmore I. Modern Hemostatic Agents for Hemorrhage Control â A Review and Discussion of Use in Current Combat Operations. – 2005.
- Okuma M. et al. Effects of etamsylate on platelet functions and arachidonic acid metabolism //Thrombosis and haemostasis. – 1982. – Т. 48. – №. 3. – С. 330-333.
Источник
АНТИКОАГУЛЯНТЫ, ДЕЙСТВУЮЩИЕ НА ПРОЦЕСС СВЕРТЫВАНИЯ КРОВИ
Мы продолжаем знакомить с лекарственными средствами, действующими на процесс свертывания крови.
Преферанская Нина Германовна
Доцент кафедры фармакологии образовательного департамента Института фармации и трансляционной медицины Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Ранее читатели познакомились с фибринолитическими (тромболитическими) препаратами, которые используют для растворения уже образовавшихся тромбов. Настоящая статья посвящена средствам, которые препятствуют образованию тромбов и предупреждают возникновение тромбозов.
Повреждение сосудистой стенки инициирует процесс свертывания крови и таким образом останавливает кровотечение из поврежденного сосуда. Этот сложный многоступенчатый процесс требует комбинированной активации плазменных, сосудистых, тромбоцитарных факторов. Большинство из них — это белки плазмы крови, которые циркулируют в крови в неактивном состоянии, но последовательно активируются в процессе свертывания крови. В этом гемокоагуляционном каскаде задействованы важнейшие компоненты: фибриноген (фактор I), протромбин (фактор II), тканевой тромбопластин (III), ионы кальция (IV), проакцелерин (V), антифибринолизин или проконвертин (VII), антигемофильный глобулин А (VIII), Кристмас–фактор (IX) и фактор Стюарта–Прауэра (Х), и др. Факторы свертывания крови являются проферментами и в результате активации превращаются в протеолитические ферменты. На каждой стадии неактивный энзимоген превращается в более активный фермент.
Первым этапом формирования тромбов является прилипание (адгезия) тромбоцитов. Тромбоциты не прилипают к интактному эндотелию и не слипаются друг с другом (агрегация), если не поврежден эндотелий и не обнаружены субэндотелиальные структуры. Адгезия тромбоцитов происходит при участии гликопротеина, присутствующего в плазме крови, тромбоцитах и эндотелии сосудов, названного фактором фон Виллебранда. Фактор фон Виллебранда связывается с гликопротеиновыми рецепторами, тромбоциты приобретают шиповидно–сферическую форму, что облегчает их агрегацию и адгезию, т.е. взаимодействие их друг с другом и с поверхностью поврежденного эндотелия.
Фактор фон Виллебранда и проакцелерин после активации выполняют роль кофакторов, повышающих протеолитическую активность. Проконвертин изначально обладает невысокой протеолитической активностью, а в результате взаимодействия с тканевым фaктopoм eгo протеолитическая активность быстро возрастает. Активированный проконвертин (корвертин) вместе с тканевым фактором и ионами Са 2+ образует комплекс, который вызывает частичный протеолиз Кристмас-фактора и фактора Стюарта–Прауэра, они активируются. Активный фактор Кристмаса (IXа), в свою очередь, дополнительно активирует фактор Х. Активный фактор Стюарта–Прауэра (Ха) действует на протромбин (фактор II) и превращает его в активный тромбин (IIа). В дальнейшем тромбоциты активируются коллагеном и первыми порциями тромбина, образовавшегося в сосудистой стенке. Тромбин вызывает частичный протеолиз фибриногена с образованием фибрина.
Протеолитическая активация факторов свертывания крови в значительной степени ускоряется, когда эти факторы через ионы Са 2 + связываются с отрицательно заряженными фосфолипидами клеточных мембран. Эти фосфолипиды выполняют роль своеобразной матрицы, на которой факторы свертывания собираются в комплексы при участии ионов Са 2+ . При этом скорость активации факторов в этих комплексах возрастает в 50 и более раз. Необходимым условием формирования таких комплексов является способность факторов II, VII, IX, Х связываться с ионами Са 2 + . Фaктopы содepжaт отрицательно заряженные остатки γ–карбоксиглутаминовых кислот, которые и обеспечивают их связывание с Са 2 + . Образование γ-карбоксиглутаминовых кислот происходит в печени при участии витамина К. При дефиците витамина К в крови появляются неполноценные факторы свертывания крови и нарушается образование фибриновых нитей.
Для человеческого организма оптимальным является наличие равновесия между этими процессами (система гемостаза). Функция этой системы заключается в сохранении жидкого состояния крови, остановке кровотечений, при повреждениях стенок сосудов и растворении тромбов.
В зависимости от характера, механизма действия, скорости и длительности влияния на процесс тромбообразования лекарственные средства подразделяются на следующие подгруппы:
- Антикоагулянты прямого действия, действующие на факторы свертывания крови.
- Антикоагулянты непрямого действия, нарушающие образование протромбина в печени.
- Средства, влияющие на агрегацию тромбоцитов, понижающие уровень цитоплазматического Са 2+ и препятствующие слипанию тромбоцитов.
- Фибринолитики (тромболитики), стимулирующие превращение профибринолизина в фибринолизин и разрушающие нити фибрина (МА №11 – 12/16).
Антикоагулянтами называются средства, ингибирующие активные факторы свертывания непосредственно в сосудистом русле или нарушающие образование факторов свертывания в печени и, таким образом, препятствующие образованию тромбов. Нарушения процесса свертывания крови в ту или другую сторону вызывают тяжелые заболевания.
Показаниями к применению антикоагулянтов являются:
- профилактика и лечение тромбоэмболических заболеваний;
- предупреждение тромбоза коронарных и периферических артерий;
- нестабильная стенокардия, инфаркт миокарда;
- профилактика и лечение тромбоза глубоких вен;
- тромбоэмболии легочной артерии;
- профилактика тромбообразования, при фибрилляции предсердий;
- ангиопластика коронарных сосудов;
- предупреждение и ограничение тромбообразования, при оперативных вмешательствах;
- поддержание жидкого состояния крови в аппаратах искусственного кровообращения и промывании венозных катетеров;
- проведение гемодиализа, гемосорбции, перитонеального диализа.
Антикоагулянты прямого действия препятствуют образованию фибрина и способствуют действию на них фибринолитических факторов. Эти средства предупреждают появление тромбов или прекращают рост уже образовавшихся тромбов.
КЛАССИФИКАЦИЯ АНТИКОАГУЛЯНТОВ ПРЯМОГО ДЕЙСТВИЯ
1. Препараты гепарина: Гепарин стандартный (нефракционированный), Гепарин натрия (Лиотон 1000, Тромблесс);
1а. Комбинированные препараты, содержащие гепарин: Венолайф, Венабос, Венитан форте, Гепатромбин, Гепатромбин Г, Гепатромбин С, Гепариновая мазь, Долобене, Контрактубекс, Нигепан, Тромблесс Плюс, Троксевазин Нео;
2. Низкомолекулярные (фракционированные) гепарины: Надропарин–кальций (Фраксипарин), Далтепарин натрия (Фрагмин), Парнапарин натрия (Флюксум), Эноксапарин-натрий (Антифибра, Клексан);
3. Дегидрированный низкомолекулярный гепарин — Бемипарин натрия (Цибор 2500, Цибор 3500);
4. Гепариноиды мукополисахариды: Гепариноид Зентива, Гепариноид Лечива Сулодексид (Ангиофлюкс, Вессел Дуэ Ф);
5. Прямые ингибиторы фактора свертывания крови Ха (активированного фактора Стюарта–Прауэра): Апиксабан (Эликвис), Ривароксабан (Ксарелто), Фондапаринукс–натрия (Арикстра);
6. Избирательные прямые ингибиторы тромбина: Бивалирудин (Ангиокс), Дабигатрана этексилата мезилат (Прадакса);
7. Препарат антитромбина III — Антитромбина III человеческий (гликопротеин);
8. Препараты гирудина: Лепирудин;
9. Пиявка медицинская, Пиявит (порошок пиявок);
10. Натрия цитрат, для консервирования крови.
Антикоагулянты прямого действиядействуют непосредственно в крови, применяются парентерально и перорально. При применении этих препаратов могут возникать побочные эффекты: геморрагии, аллергические реакции (крапивница, ангионевротический отек и др.), тромбоцитопения, гиперкалиемия, при длительном применении — остеопороз и др.
Гепарин, сульфатированный гликозаминогликан (мукополисахарид), состоящий из остатков D–глюкозамина и D–уроновой кислоты. Образуется тучными клетками во многих тканях; в больших количествах содержится в печени, легких, слизистой оболочке кишечника. Для медицинских целей гепарин выделяют из слизистой оболочки свиного кишечника и из бычьих легких. В процессе выделения получается смесь фракций с различной длиной полисахаридной цепи и различной молекулярной массой (от 3000 до 40 000 Д). Фракции с различной молекулярной массой несколько отличаются друг от друга по биологической активности и фармакокинетическим свойствам.
Препараты гепарина, получаемые разными способами и из разных источников, могут обладать неодинаковой антикоагулянтной активностью, вследствие чего необходимо проводить их биологическую стандартизацию. Активность гепарина определяется по способности удлинять время свертывания крови (1 мг стандартного гепарина содержит 130 ЕД).
Механизм действия гепарина сложен. Гепарин собственно сам антикоагулянтным действием не обладает, он оказывает свое действие на факторы свертывания крови только после образования комплекса с эндогенным антикоагулянтом антитромбином III. Антитромбин III — это гликопротеин плазмы крови, синтезируемый в печени. Он является ингибитором сериновых протеаз, к которым относятся факторы свертывания крови IIа (тромбин), IХа и Ха (а также ХIа и ХIIа). Однако процесс инактивации факторов под действием одного антитромбина III протекает очень медленно. Гепарин вызывает конформационные изменения в молекуле антитромбина III, потенцирует его эффекты, что приводит к ускорению этого процесса примерно в 1000 раз. Основное действие комплекса гепарин–антитромбин III направлено против тромбина и фактора Ха, но механизмы ингибирования этих факторов имеют некоторые отличия. Для инактивации тромбина необходимо, чтобы гепарин связался как с молекулой антитромбина III, так и с молекулой тромбина. В то же время быстрая инактивация фактора Ха комплексом гепарин–антитромбин III не требует связывания этого фактора с гепарином. Фракции гепарина с относительно короткой полимерной цепью не могут одновременно присоединять антитромбин III и тромбин и поэтому не обладают антитромбиновой активностью. Их действие в основном связано с инактивацией фактора Ха и, следовательно, с нарушением превращения протромбина в тромбин.
Гепарин плохо всасывается при введении внутрь. В зависимости от показаний гепарин вводят внутривенно (иногда первые порции капельно), внутримышечно и подкожно. Дозируют гепарин в единицах действия, назначают от 2000 ЕД до 5000 ЕД в сутки. С лечебной целью вводят в/в, дозы и частоту введения определяют индивидуально, в зависимости от анализа протромбинового времени. При внутривенном введении действие наступает сразу и продолжается 4–6 час. При подкожном введении гепарин начинает действовать через 30–60 мин., продолжительность действия составляет 8–12 час. С профилактической целью его применяют подкожно, вводят каждые 8–12 час. в область живота, где меньше сосудов и меньше опасность развития гематом.
Гепарин в крови связывается со многими белками, в т.ч. с такими, которые его нейтрализуют (тромбоцитарный фактор). Высокий уровень этих белков в крови может вызвать относительную резистентность к препарату. Кроме того, гепарин связывается с макрофагами и эндотелиальными клетками, при этом происходит его деградация (деполимеризация). Гепарин биотрансформируется печенью, преимущественно клетками ретикулоэндотелиальной системы и выводится почками в виде метаболитов.
Применяют гепарин для профилактики и лечения тромбоза глубоких вен и тромбоэмболии легочной артерии, при нестабильной стенокардии и инфаркте миокарда, для предупреждения тромбоза периферических артерий, при протезировании клапанов сердца и экстракорпоральном кровообращении. Гепарин снижает уровень липидов в крови вследствие активации липопротеинлипазы, которая гидролизует триглицериды с освобождением свободных жирных кислот.
При одновременном применении гепарина с антиагрегантами (особенно аспирином), другими антикоагулянтами, фибринолитиками и нестероидными противовоспалительными средствами усиливается его противосвертывающая активность, повышается риск развития кровотечений. Средства, вызывающие гипопротромбинемию (цефамандол, цефоперазон, вальпроевая кислота), также повышают риск развития кровотечений. При применении с никотином, алкалоидами спорыньи, тироксином, тетрациклином и антигистаминными средствами действие гепарина снижается.
Наиболее частым осложнением гепаринотерапии являются кровотечения, причиной которых может быть угнетение функции тромбоцитов или уменьшение их количества (тромбоцитопения). Связывание гепарина с фактором фон Виллебранда, по–видимому, объясняет его ингибирующее воздействие на адгезию и агрегацию тромбоцитов. В таких случаях гепарин отменяют, а при серьезных кровотечениях необходимо внутривенно вводить гемостатик (антидот гепарина) — протамина сульфат, который нейтрализует гепарин, образуя с ним нерастворимый комплекс. Вводят 1 мг на 100 ЕД гепарина.
У 1–5% больных, получающих гепарин, на 7–14-й день наблюдается тромбоцитопения, причиной которой является появление антител против комплекса гепарин — фактор 4 тромбоцитов. Этот комплекс образуется на мембране тромбоцитов при нейтрализации гепарина фактором 4 (гликопротеин тромбоцитарного происхождения), который высвобождается при агрегации тромбоцитов. Менее чем у 1% больных с тромбоцитопенией наблюдается тромбоз вследствие активации тромбоцитов антителами к комплексу гепарин — фактор 4, что вызывает их агрегацию. Это состояние требует отмены гепарина и назначения антикоагулянтов, не вызывающих тромбоцитопению, таких как данапароид и лепирудин.
При длительном введении гепарина (более 3 мес.) может развиться остеопороз. Это особенно важно учитывать при назначении гепарина в постклимактерический период. Довольно редким осложнением гепаринотерапии является гиперкалиемия, связанная с ингибированием синтеза альдостерона в надпочечниках.
Гепарин противопоказан больным с кровотечениями, геморрагическими инсультами и диатезами, гемофилией, тромбоцитопенией, тяжелой гипертонией, больным с активным туберкулезом и язвенной болезнью, беременным только по жизненным показаниям.
При тромбофлебитах поверхностных вен ног, трофических язвах конечностей и др. тромбоэмболических заболеваниях гепарин используется местно, в виде мазей, гелей, суппозиториев. С этой целью применяют гепарин натрия и комбинированные препараты, содержащие гепарин.
Гепарин натрия (Лиотон 1000, Тромблесс) относится к группе среднемолекулярных гепаринов, оказывая противовоспалительное, антипролиферативное, противоотечное и обезболивающее действие. Уменьшает агрегацию тромбоцитов, связывается с антитромбином III, предупреждая переход протромбина в тромбин. Угнетает активность тромбина, снижает активность гиалуронидазы, повышает фибринолитические свойства крови. Улучшает микроциркуляцию и активирует тканевой обмен, благодаря чему ускоряет процессы рассасывания гематомы и тромбов, в конечном итоге восстанавливает проходимость вен, что сопровождается выраженным обезболивающим и противовоспалительным действием.
При наружном применении Лиотона 1000 его компоненты оказывают местное антитромботическое, противоэкссудативное, умеренное противовоспалительное действие. Препарат применяют с целью профилактики и лечения тромбоза глубоких вен, при заболеваниях периферических вен, тромбофлебите, в профилактике и терапии микротромбообразования и нарушения микроциркуляции. Лиотон 1000 в виде геля или мази для наружного применения наносят на пораженный участок (3–5 см в диаметре) 1–3 раза в сутки.
При тромбозе геморроидальных вен накладывают ректальные тампоны или бязевые прокладки с нанесенной мазью непосредственно на ущемленные узлы и фиксируют повязкой. С этой же целью можно использовать тампон, пропитанный мазью, который вводят в задний проход.
Курс лечения препаратом «Лиотон 1000» — 3–4 дня. В случае язвы голени осторожно смазывают воспаленную кожу вокруг язвы, применяя 2–3 раза в день, ежедневно, до исчезновения воспалительных явлений, в среднем от 3 до 7 дней, возможность проведения более длительного курса лечения определяется врачом.
Важно! Не следует наносить гель/мазь на открытые раны, на слизистые оболочки, при наличии гнойных процессов. Применение мази не рекомендуется и при глубоком венозном тромбозе.
Тромблесс — гель, действие которого направлено на уменьшение воспалительного процесса, свертываемости крови, снижение отека мягких тканей и болевых ощущений. Действует препарат посредством уменьшения агрегации тромбоцитов, связываясь с антитромбином III, что не позволяет перейти протромбину в тромбин.Под действием геля улучшается ток крови в мелких сосудах (капиллярах) тканей и тканевой обмен, что приводит к рассасыванию тромбов и гематом, снижению воспаления и интенсивности боли.
Тромблесс Плюс — комбинированный препарат, действующими веществами которого являются гепарин натрия, троксерутин, декспатенол и бензокаин.
Декспантенол провитамин В5 в коже превращается в пантотеновую кислоту, входящую в состав кофермента А, который участвует в процессах ацетилирования, обмене углеводном и жировом; стимулирует регенерацию кожи, нормализует клеточный метаболизм, увеличивает прочность коллагеновых волокон. Препарат оказывает регенерирующее, витаминное, метаболическое и противовоспалительное действие.
Троксерутин — производное рутина, обладает Р–витаминной активностью, оказывает венотонизирующее, ангиопротекторное, противоотечное, антиоксидантное и противовоспалительное действие. Участвует в окислительно–восстановительных процессах, блокирует гиалуронидазу, стабилизирует гиалуроновую кислоту клеточных оболочек и уменьшает проницаемость и ломкость капилляров, повышает их тонус. Увеличивает плотность сосудистой стенки, уменьшает экссудацию жидкой части плазмы и диапедез клеток крови. Снижает воспаление в сосудистой стенке, ограничивая прилипание к ее поверхности тромбоцитов.
Бензокаин — местный анестетик для поверхностной анестезии. Уменьшает проницаемость клеточной мембраны для ионов натрия, вытесняет ионы кальция из рецепторов, расположенных на внутренней поверхности мембраны, блокирует проведение нервных импульсов. Препятствует возникновению болевых импульсов в окончаниях чувствительных нервов и их проведению по нервным волокнам. Препарат расширяет поверхностные сосуды, способствуя всасыванию гепарина.
К средствам с антитромбическим и местноанестезирующим действием, содержащим бензокаин, относятся Гепариновая мазь и Нигепан, суппозитории ректальные. Ректальные суппозитории Гепазолон содержат лидокаина гидрохлорид.
Гепатромбин (гель, мазь) – препарат, в состав которого входят гепарин натрия, аллантоин и декспантенол, обладает антитромботическим, кератолитическим и противовоспалительным действием, улучшает регенерацию тканей.
При геморрое с осложнениями в виде тромбоза, при трещинах и свищах заднего прохода, при аногенитальном зуде применяют Гепатромбин Г — средство с антитромбическим, местноанестезирующим, веносклерозирующим, противоотечным, противозудным и противовоспалительным действием, в состав которого входят гепарин натрия, лауромакрогол и преднизолон. Выпускается в виде ректальных суппозиториев, мази для ректального и наружного применения.
Гепатромбин С и Долобене (гель), в состав которых входят гепарин натрия, декспантенол и диметилсульфаксид, применяются при гематомах, воспалении мягких тканей, мышц, сухожилий, сухожильных влагалищ, связок после ушибов, сдавлений, травм (в т.ч. спортивных); при бурситах, невралгиях, периартритах, при наличии поражения периартикулярных тканей. Обладают антитромботическим, противовоспалительным действием, улучшают регенерацию тканей.
При варикозном расширении вен нижних конечностей и тромбофлебитах применяют комбинированные препараты с гепарином, содержащие троксерутин, — гели «Венолайф», «Троксевазин Нео», «Венитан форте». Препараты оказывают антитромботическое, венотонизирующее, ангиопротекторное действие, обладают Р–витаминной активностью, снижают сосудисто–тканевую проницаемость и ломкость капилляров, нормализуют микроциркуляцию и трофику тканей, уменьшают застойные явления в венах и паравенозных тканях, вызывая противоотечный и противовоспалительный эффект.
Источник