Лекарственные растительные средства защиты
На протяжении всей своей истории человечество соприкасалось с царством растений, используя последние для удовлетворения своих хозяйственных, пищевых и лекарственных целей. Поэтому неудивительно, что даже современные лекарственные препараты разработаны на основе природных соединений. Среди них наиболее известны витамин С, аспирин, хинин, морфин и кодеин. В последние десятилетия большое внимание уделяется изучению свойств таксола, арглабина, винбластина и некоторых других соединений, полученных на основе растительных препаратов.
Поиск новых биологически активных соединений растительного происхождения для лечения и профилактики иммуносупрессии, инфекционных заболеваний, онкологии и метаболических заболеваний остается активной частью фармацевтических исследований [15]. В последние годы на рынке появилось более 40 новых препаратов природного происхождения, прошедших полный путь от исследования до клинических испытаний [2]. Такое внимание исследователей к природным соединениям обусловлено в первую очередь меньшей токсичностью растительных препаратов и более широким спектром действия. Некоторые лекарственные соединения растительного происхождения обнаружили способность эффективно блокировать развитие различных вирусов, включая вирус простого герпеса, гриппа, вирус иммунодефицита человека, вирусы гепатита С и В и многие другие [4, 8, 17, 19,].
Целью данного сообщения является систематизация данных по действию различных соединений растительного происхождения, способных ингибировать репродукцию вирусов.
Основой противовирусной терапии является воздействие на вирус или его составляющие компоненты на той или иной стадии репродукции. Весь процесс репродукции вирусов может быть условно разделен на три фазы [15]. Первая фаза охватывает события, которые ведут к адсорбции и проникновению вируса в клетку, освобождению его внутренних структурных компонентов и модификации его таким образом, что он способен вызвать инфекцию. Вторая фаза репродукции связана со сложными процессами, в течение которых происходит экспрессия вирусного генома. Заключительной стадией репродукции является выход вирусного потомства из клетки путем почкования или за счет лизиса, причем в последнем случае клетка погибает [12]. Имеющийся на сегодняшний день арсенал противовирусных средств способен оказывать воздействие на любой из этапов репродукции вируса.
Адсорбция и проникновение вируса в клетку
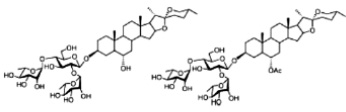
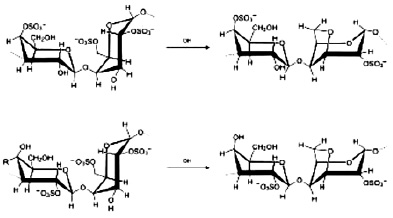
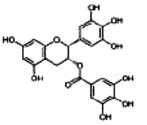
Взаимодействие вируса с клеткой начинается с процесса адсорбции, т.е. прикрепления вирусных частиц к клеточной поверхности. Этот процесс протекает при наличии соответствующих рецепторов на поверхности клетки и «узнающих» их субстанций на поверхности вируса. Прикрепление вируса к клетке происходит в два этапа, один из которых неспецифический, другой ‒ специфический. Поэтому химиотерапия этого этапа инфекции может быть также разделена на специфическую и неспецифическую. Неспецифическая стадия блокирования адсорбции вируса в первую очередь связана с электростатическими взаимодействиями между вирусом и клеткой, поэтому использование полисахаридов и некоторых пептидов, выделенных из растений и несущих большой отрицательный заряд, эффективно ингибирует адсорбцию вирусов. В подобных препаратах необходимы, как минимум, две сульфатные группы на один моносахарид. При этом противовирусная активность возрастает с возрастанием молекулярной массы в интервале от 1 до 10 kD. При меньших, а также больших массах полисахаридов противовирусная активность резко снижена. Не менее интересной группой химических соединений, подавляющих адсорбцию вирусов, можно назвать тритерпеновые сапонины, которые в силу своих структурных особенностей, связываясь с холестерином мембраны, способны изменять пространственную структуру мембраны клетки [13]. Установлено, что наличие у подобных препаратов трех сахарных остатков 3-O-β-хакотриозила увеличивает противовирусную активность соединений. Другой группой препаратов, блокирующих репликацию вирусов, являются полифенольные соединения, не только изменяющие заряд поверхности клетки, но и препятствующие специфической сорбции вируса на рецепторы (рис. 1).
Рис. 1. Соединения, блокирующие стадию адсорбции вируса [4, 8, 13]
Освобождение внутреннего компонента вируса
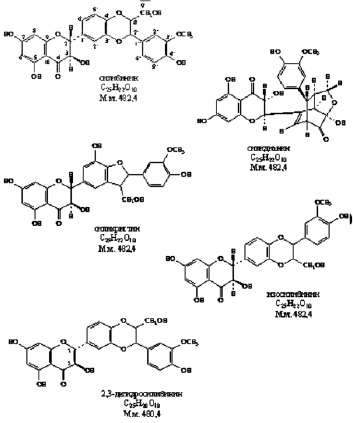
После проникновения вириона в клетку происходит целый комплекс превращений вируса, смысл которых заключается в удалении вирусных защитных оболочек, препятствующих экспрессии вирусного генома. Этот процесс сопровождается рядом характерных особенностей: исчезает инфекционность вируса, появляется чувствительность к нуклеазам, возникает устойчивость к нейтрализующему действию антител. Основной группой растительных соединений, способных подавлять репродукцию вирусов на этой стадии, являются аналоги силимарина, лютеолина и кверцетина (рис. 2) [4, 20, 21].
Рис. 2. Соединения, блокирующие освобождение внутреннего компонента вируса
Экспрессия вирусного генома и сборка вирусных частиц
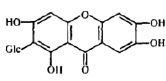
Экспрессия вирусного генома и сборка вирионов являются самыми сложными этапами, включающими транскрипцию нуклеиновых кислот, трансляцию белков, посттрансляционные модификации вирусных белков, репликацию нуклеиновых кислот, сборку вирусных частиц. Этот этап репродукции вирусов успешно блокируется 2 основными группами растительных соединений: ингибиторами РНК полимераз и ингибиторами посттрансляционных модификаций белков. К таким препаратам относятся алпизарин, госсипол, эпиген и др (рис. 3).
Механизм действия подобных препаратов связан с образованием ацил-ферментных производных и основан на блокировании одной из трех основных областей, критичных для активности аспарагиновой протеазы вируса: каталитическое ядро фермента, содержащее пару Asp-Thr/Ser-Gly триад, мобильная flap-область и домен димеризации на N- и С-концах протеазы [1, 10, 14].
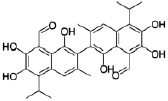
Рис. 3. Соединения, блокирующие экспрессию вирусного генома
Выход вирусного потомства
Завершающим этапом репродукции вируса является выход вирионов из инфицированной клетки. Этот процесс может протекать с помощью почкования вируса и лизиса клетки. Лизис клетки, как правило, сопровождается гибелью клетки. Блокировать такой механизм выхода вируса практически невозможно.
Выход из клетки путем почкования осуществляют вирусы с липопротеиновой оболочкой. При этом способе клетка может длительное время сохранять жизнеспособность и продуцировать вирусное потомство, пока не произойдет полное истощение ее ресурсов. Одним из механизмов блокирования этого этапа репродукции вируса является использование ингибиторов ферментативной активности вируса, участвующей в почковании вируса. Разработка препаратов группы ингибиторов фермента вируса гриппа – нейраминидазы (NA) ‒ является успешным достижением современной вирусологической науки последних лет – так называемого «рационального лекарственного дизайна», поскольку при синтезе данного препарата были использованы современные знания третичной структуры NA как антигена и фермента [3, 6].
Препараты с антинейраминидазным действием «имитируют» структуру натуральных субстратов каталитического сайта NA (рис. 4), что «привлекает» вирус к большему взаимодействию с ними [5, 18]. К подобным соединениям относятся коричные и оксикоричные кислоты, галлаты и др.
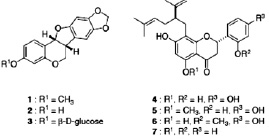
Рис. 4. Структура ингибиторов нейраминидазы [7, 9, 16]
На сегодняшний день практическая медицина обладает достаточно внушительным арсеналом противовирусных средств, способных подавлять репродукцию вируса на любой стадии процесса. Однако, несмотря на определенные успехи, достигнутые в вирусной химиотерапии, клиническая практика сталкивается с серьезной проблемой появления вариантов вируса, устойчивых к тем или иным препаратам.
Изучение растительных препаратов, обладающих антивирусными свойствами (алпизарин, эпиген, протефлазид, госсипол), показало, что за счет разных механизмов действия препаратов (противовирусное и иммуностимулирующее) появление вирусов, устойчивых к данным препаратам, не наблюдается. Большое разнообразие биологически активных соединений, находящихся в растениях, позволяет рассчитывать на возможность получения новых высокоактивных препаратов, обладающих способностью блокировать различные вирусы, в том числе, резистентные к существующим коммерческим химиопрепаратам. Подобные препараты, сочетающие в себе свойства иммуностимулирующих и противовирусных соединений, можно рекомендовать для лечения и профилактики инфекционных заболеваний, ассоциированных с иммунодефицитным состоянием, в том числе таких, как грипп, ВИЧ, гепатит С и др. [11, 17].
Рецензенты:
Саятов М.Х., д.б.н., академик НАН РК, профессор, главный научный сотрудник, РГП «Институт микробиологии и вирусологии» КН МОН РК, г. Алматы;
Жуматов К.Х., д.б.н., профессор, главный научный сотрудник, РГП «Институт микробиологии и вирусологии» КН МОН РК, г. Алматы.
Источник
ГАСТРОЦИТОПРОТЕКТОРЫ: ДЛЯ ЗАЩИТЫ СЛИЗИСТОЙ ОБОЛОЧКИ ЖКТ
Для защиты слизистой оболочки желудочно–кишечного тракта (ЖКТ) от воздействия всевозможных агрессивных раздражителей применяют гастроцитопротекторные средства.
Преферанская Нина Германовна
Доцент кафедры фармакологии института фармации им. А.П. Нелюбина Первого МГМУ им. И.М. Сеченова (Сеченовский университет), к.фарм.н.
Они повышают резистентность слизистых оболочек ЖКТ к действию повышенной активности пепсина или сильнокислой реакции желудка (рН 0,8–1,5). Гастроцитопротекторные средства стимулируют образование муцина железистыми клетками и слизистой оболочкой желудка, тем самым сохраняют целостность его защитного барьера. Препараты способствуют поддержанию рН желудочного сока на уровне 3,0-3,5 за счет повышения секреции бикарбонатов. При их применении повышается синтез защитных факторов (простагландинов) и уменьшается их инактивация. Улучшается регенерация клеток слизистой желудка за счет уменьшения повреждения микрососудов и улучшения регионарного кровотока. Стимулируется эпидермальный фактор роста, повышается барьерная функция слизистой оболочки. Стимулируется пролиферация и обмен эпителиальных клеток. Все это значительно улучшает репаративные процессы и способствует восстановлению дескваминированного (лат. desquamo — удаляю, отслаиваю) эпителия в желудке.
С этой целью применяют несколько подгрупп гастроцитопротекторных лекарственных средств:
1. Синтетические аналоги простагландинов — Мизопростол.
2. Препараты, повышающие синтез простагландинов — Ребамипид.
3. Препараты, образующие комплексные соединения (хелаты), — Висмута трикалия дицитрат, Сукралфат.
4. Препараты висмута: Висмута субнитрат, Викалин, Викаир.
5. Препараты природного происхождения — Солкосерил, Мумие и др.
Гастроцитопротекторные ЛС отличаются между собой не только составом, но и фармакологическими эффектами. Каждое лекарственное средство по-разному защищает слизистую оболочку и стимулирует восстановление клеток стенки желудка.
ГОРМОНОПОДОБНЫЕ ЛИПИДНЫЕ МЕДИАТОРЫ
Многочисленные исследования показали, что простагландины повышают устойчивость слизистой оболочки желудка к воздействию травмирующих факторов (соляной кислоте, пепсину, желчи, этанолу, НВПС, ГКС). Связано это с их влиянием на физиологические функции организма. НПВС и ГКС нарушают образование простагландинов Е и I2 Первым препаратом этой группы является синтетический аналог простагландина Е1 — Мизопростол (Misoprostol) — ТН «Миролют» —активирует регенерацию слизистой оболочки, усиливает кровообращение в микрососудах стенки желудка, подавляет выработку пищеварительного фермента пепсина и уменьшает продукцию желудочного сока. Он повышает воспроизводимость особыми (добавочными) клетками желудочной слизи, которая защищает его стенки от агрессивных факторов. Препарат оказывает слабое стимулирующее действие на гладкую мускулатуру ЖКТ антисекреторной активностью. Повышается устойчивость слизистой оболочки желудка, что предупреждает развитие эрозивно–язвенных поражений. Прием чаще назначают для профилактики НПВС–гастропатий. Самостоятельно Мизопростол лучше не назначать, даже если в качестве основного лекарства был назначен аспирин, который почему-то многие пациенты принимают не по назначению и довольно часто. У больных, принимающих НПВС, уменьшается частота развития язв желудка и двенадцатиперстной кишки, снижается риск язвенного кровотечения.
Важно! Препарат противопоказан при ИБС, гипертонической болезни, нарушении функции печени, беременности. Не рекомендуют принимать детям и подросткам. Простагландины опасны побочными эффектами, они вызывают: метеоризм, диарею, тошноту, головную боль, нарушение менструального цикла, вагинальные кровотечения и др.
Перед приемом препарата необходимо обязательно проконсультироваться у лечащего врача.
Ребамипид (Rebamipidum) — ТН «Ребагид» — оказывает цитопротекторное действие в отношении слизистой желудка при повреждающем воздействии этанола, кислот, щелочей и лекарственных средств (НПВС, ГКС). Способствует активации энзимов, ускоряющих биосинтез высокомолекулярных гликопротеинов, и повышает содержание слизи на поверхности стенки желудка. Ребамипид повышает содержание простагландина Е2 (PGE2) в слизистой желудка и повышает содержание PGI2 в желудке. Способствует улучшению кровоснабжения слизистой желудка, активизирует ее барьерную функцию, активизирует щелочную секрецию желудка, усиливает пролиферацию и обмен эпителиальных клеток желудка. При приеме препарата ингибируются продукты окислительного стресса, воспалительных цитокинов и хемокинов, при этом очищает слизистую от гидроксильных радикалов и подавляет супероксиды, продуцируемые полиморфноядерными лейкоцитами и нейтрофилами в присутствии Helicobacter pylori. Абсорбция при приеме внутрь — высокая. После приема в дозе 100 мг максимальная концентрация достигается приблизительно через 2 ч и составляет 340 нг/мл. Период полувыведения равен приблизительно 1 ч. Повторные приемы препарата не приводят к его кумуляции в организме. Приблизительно 10% препарата выводится почками, преимущественно в неизмененном виде.
Препарат принимают внутрь по 1 табл. 3 раза в сутки, запивается небольшим количеством жидкости. Курс лечения составляет 2-4 недели, в случае необходимости может быть продлен до 8 недель.
Важно! При применении препарата могут возникать побочные эффекты со стороны желудочно-кишечного тракта: запор, метеоризм, диарея, тошнота, боль в области живота, нарушение вкусовых ощущений, а также аллергические реакции и нарушение менструального цикла.
ЛП, ОБРАЗУЮЩИЕ ЗАЩИТНУЮ ПЛЕНКУ ИЗ МЕТАЛЛООРГАНИЧЕСКИХ КОМПЛЕКСОВ
Висмута трикалия дицитрат (Bismuthi trikalii dicitras) — ТН «Де–нол«, ТН «Новобисмол«,табл. 120 мг. В кислой среде желудка препарат образует нерастворимые висмута оксихлорид и дицитрат. Соединение дицитрата с гидроокисью висмута образует молекулярные комплексы различной структуры и размеров, что приводит к переходу водного раствора в коллоидную форму. Коллоидная форма препарата позволяет ему эффективно пенетрировать в желудочную слизь. Препарат хорошо проникает в глубь желудочных ямок, что позволяет ему уничтожать бактерии, находящиеся в недосягаемости для других антибактериальных препаратов. Обладает антихеликобактерным действием, которое проявляется в виде коагуляции белков микробной клетки и гибели спиралевидной жгутиковой грамотрицательной бактерии Helicobacter pylori. При применении препарат практически не всасывается из ЖКТ, выводится в основном с экскрементами.
Сукральфат (Sucralfatum) — ТН «Вентер«, табл. 1,0 г — препарат смешанного типа действия: в желудке распадается на два активных метаболита: алюминия гидроокись, обладающую антацидным действием и сульфат сахарозы, который взаимодействует с белками некротизированной ткани, образуя хелатный комплекс, в виде клейкой массы, которая выстилает и защищает язву от повреждения. Алюминия гидроокись оказывает антацидное действие, нейтрализует соляную кислоту и повышает рН содержимого желудка. Основными побочными эффектами являются диспептические расстройства и аллергические реакции.
Препараты висмута обладают вяжущим, адсорбирующим и обволакивающим действием.
Висмута субнитрат (Bismuthi subnitras) — препарат на поверхности слизистой оболочки желудка коагулирует белки, образуя защитную пленку из денатурированных белков с образованием плотного альбумината. Оказывает сосудосуживающий эффект, уменьшает местный воспалительный процесс, подавляет рост и развитие Helicobacter pylori. Кроме того, препараты висмута обладают местной антимикробной активностью, действуя непосредственно на клеточную стенку бактерий, нарушают ее целостность. Висмут оказывает непосредственное бактерицидное действие, его минимальная ингибирующая концентрация в отношении Helicobacter pylori достаточна высокая.
При применении этого препарата могут возникать тошнота, рвота, головная боль, пигментации на языке и аллергические реакции.
Викалин (Vicalin), табл., покр. обол., — комбинированный препарат, в одной таблетке которого содержатся активные компоненты: висмута субнитрат (350 мг), магния карбонат — 400 мг, натрия гидрокарбонат (200 мг), кора крушины ольховидной (25 мг), корневище аира болотного (25 мг), рутозида + келлина по 5 мг.
Препарат обладает репаративными свойствами, оказывает вяжущее, адсорбирующее, обволакивающее действие. Дополнительно викалин проявляет спазмолитический, слабительный, притивовоспалительный эффект. При применении препарата снижается кислотность желудочного сока и уменьшается активность пепсина, возникает антацидное и бактерицидное действие. При применении викалина могут возникать учащение стула, тошнота, головная боль и аллергические реакции Таблетки применяют внутрь через 30-60 мин. после еды, запивая достаточным количеством теплой воды (0,5 стакана). Отмечается быстрое действие, хорошая переносимость и доступная стоимость препарата. Применение препарата запрещено больным детям в возрасте до 18 лет, при почечной недостаточности, беременным и во время кормления грудью.
Препарат назначается взрослым по 1–2 таблетки 3-4 раза в сутки за 30 мин. до или через 2 часа после последнего приема пищи; детям от 6 до 14 лет можно по 1 табл. 2 раза в день, запивая небольшим количеством воды. Курс лечения — 28-56 дней, перерыв — 8 недель.
Важно! Во избежание накопления в организме висмута, особенно при снижении выделительной функции почек, длительные курсы приема препарата не рекомендуются. При применении препарата может возникать тошнота, рвота и металлический привкус во рту.
Викаир (Vicair) — препарат в комбинации висмута субнитрата (350 мг), коры крушины ольховидной (400 мг), корневища аира болотного (200 мг), магния карбонат + натрия гидрокарбонат по 25 мг. Эффект препарата обусловлен свойствами его компонентов. В состав данного средства входит аир, обладающий спазмолитическим действием, крушина, обладает слабительным действием, способствуя улучшению пассажа по кишечнику. Препарат проявляет вяжущее, антацидное действие.
Режим дозирования индивидуальный, в зависимости от показаний, возраста пациента и клинической ситуации. Препарат противопоказан при гипоацидном гастрите, хронической почечной недостаточности, хроническом аппендиците, энтероколите, детском возрасте до 18 лет, беременности, в период лактации и при повышенной чувствительности к компонентам комбинации.
Важно! Длительно принимать препараты висмута нельзя, т.к. они вызывают различные побочные эффекты: дисфункцию кишечника, проявляющуюся запором или поносом, нарушают работу почек, печени, могут стать причиной бессонницы, энцефалопатии, снижения памяти.
ПРЕПАРАТЫ РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ
Препараты, с успехом используемые для улучшения репаративных процессов: Солкосерил, Алоэ, Зверобой, Прополис, Мумие.
Солкосерил — зарекомендовавшее себя эффективное средство при язве желудка, изготовленное из телячьей крови. Это средство изобретено давно и используется как сильнодействующее ранозаживляющее средство и сейчас.
Это биогенный стимулятор, он быстро и эффективно устраняет симптомы болезни, уменьшает воспалительный процесс. Он активизирует процессы регенерации и метаболизма в организме, убирает воспаление. Солкосерил запускает механизм самооздоровления, происходит саморегуляция нарушений слизистой пищеварительного органа. И не только желудку становится легче, но и печени. Препарат выводит из организма накопившиеся из-за недуга токсичные вещества.
Его основное назначение — стимулировать кровоснабжение слизистой пищеварительного органа, ускорять рубцевание язв; активировать регенеративные возможности клеток, предупреждать атрофию слизистой желудка; улучшать обмен веществ и иммунитет.
Метилметионинсульфония хлорид (Витамин U) оказывает обезболивающий эффект и стимулирует заживление поражений слизистых оболочек. При его применении организм больного насыщается метильными группами, которые необходимы для биохимических процессов синтеза. Участвует в метилировании гистамина, превращая его в неактивную форму, что способствует уменьшению желудочной секреции. Назначают внутрь 2 табл. 3 раза в день, курс лечения — месяц, при необходимости курс повторяют.
Фитопрепараты, содержащие цветы ромашки аптечной, слизь семян льна, листья подорожника, траву зверобоя, обладают обволакивающим и вяжущим действием. Они менее эффективны, но их можно применять в качестве профилактического средства, предварительно посоветовавшись с гастроэнтерологом, аллергологом (у растительных препаратов также есть противопоказания к применению).
Биогенные стимуляторы — экстрат алоэ, сок каланхоэ, ФИБС, масло облепихи и шиповника — улучшают тканевую регенерацию.
Облепиховое масло благодаря содержанию токоферолов защищает биологические мембраны от повреждения, обладает умеренным ингибирующим влиянием на секрецию желудочного сока и ускоряет процесс заживления язв. Больным с локализацией язвы в желудке и двенадцатиперстной кишке назначают по 1 ч. л. за 30 мин. до еды 2–3 раза в день и на ночь. Для внутреннего применения противопоказано при воспалительных процессах в желчном пузыре, печени, поджелудочной железе и при желчнокаменной болезни.
Врач-гастроэнтеролог перед назначением препарата учитывает все его характеристики: механизмы и эффекты действия, отрицательные виды действия, побочные эффекты, противопоказания и индивидуально подбирает необходимое средство. Своевременное обращение к гастроэнтерологу и правильное применение гастроцитопротекторных средств позволяет больным нивелировать фазу обострений и оптимизировать фазу ремиссий.
Источник