Лекарственные препараты уравнение реакции
Управление солюбилизационными характеристиками лекарственных веществ является одним из основных направлений в разработках современных систем доставки лекарств (Drug Delivery Systems) [22]. В этом направлении наиболее востребованы методы повышения растворимости и скорости растворения активных фармацевтических субстанций – лекарственных веществ (ЛВ). Растворимость играет существенную роль в действии лекарств, прежде всего предназначенных для перорального приема, так как максимальная скорость пассивного транспорта препарата через биологические мембраны – основной путь для поглощения ЛВ – зависит от проницаемости мембраны и концентрации раствора/растворимости. Учитывая, что
40 % выпускающихся лекарственных субстанций классифицируются как практически нерастворимые, а
85 % самых продаваемых препаратов в США и Европе принимаются перорально, актуальность исследований в данном направлении становится очевидной.
В настоящее время FDA принята система биофармацевтической классификации лекарств [24, 26] для прогнозирования биодоступности при пероральном приеме. Эта система основана на использовании соотношений параметров растворимости и проницаемости стенок желудочно-кишечного тракта (ЖКТ). Растворимость классифицирована на основании стандартов Фармакопеи США (USP) [23]. Так, лекарственное вещество считается хорошо растворимым, когда максимальная разрешенная его доза растворяется в 90 процентов его дозы проникает в кровоток при пероральном введении. Ниже приводятся основные классы ЛВ по критериям «проницаемость стенок ЖКТ – растворимость».
Класс I – высокая проницаемость, высокая растворимость. Эти соединения хорошо всасываются и скорость абсорбции, как правило, выше, чем выведение.
Класс II – высокая проницаемость, низкая растворимость. Пример: большинство нестероидных противовоспалительных средств. Биодоступность таких продуктов ограничена скоростью их растворения (кинетический барьер) и растворимостью (термодинамический барьер). К этому классу относится
> 30 % выпускающихся и разрабатываемых лекарств.
Класс III – низкая проницаемость, высокая растворимость. Пример: большинство антибиотиков бета-лактамного типа. Низкая скорость абсорбции ограничивает проникновение в кровоток, но препараты растворяются очень быстро.
Класс IV – низкая проницаемость, низкая растворимость. Пример: антигельминтики – альбендазол, карбендацим, фенбендазол; растительные флавоноиды – рутин, кверцетин, дигидрокверцетин. Эти соединения имеют низкую биодоступность. Обычно они плохо поглощаются слизистой оболочкой кишечника. К этому классу относится
10 % выпускающихся и разрабатываемых лекарств.
Таким образом, ЛВ, относящиеся к II и IV классам, нуждаются в технологиях повышения их водорастворимости. К этим классам относятся до 50 % разрабатываемых и выпускающихся фармацевтической промышленностью ЛВ.
Для повышения растворимости лекарств используют различные физико-химические подходы: уменьшение размеров частиц, модификация кристаллической структуры, получение твердых дисперсий ЛВ с наполнителями и т.д. [20, 18]. Так, при измельчении субстанций антигельминтных препаратов «карбендацим» (бензимидазолил-2-метил карбамат) и «альбендазол» (5-тиопропилбензимидазолил-2-метилкарбамат) в планетарно-центробежном активаторе АГО–2 в «жестких» условиях активации (40 – 60g) было показано не только уменьшение размера частиц, но также стабильность химической структуры, а именно, при сравнении ИК-спектров исходных и измельченных субстанций не было обнаружено изменений в расположении полос поглощения основных функциональных групп (NH, C = N, C = O, OCH3). В спектрах измельченных субстанций наблюдалось увеличение интенсивности этих сигналов, что позволило предполагать лишь о разрушении межмолекулярных водородных связей [11]. Изучение растворения исходного и измельченного образцов карбендацима в среде «желудочного сока» показало, что скорость растворения измельченной субстанции выше, нежели неизмельченной субстанции.
Однако, по нашему мнению, наиболее значимые результаты достигаются за счет перевода ЛВ в их водорастворимые соли (если ЛВ имеет выраженные кислотно-основные свойства), а также за счет включения молекул ЛВ в супрамолекулярные водорастворимые образования (межмолекулярные комплексы, мицеллы) со специально подобранными «вспомогательными» веществами.
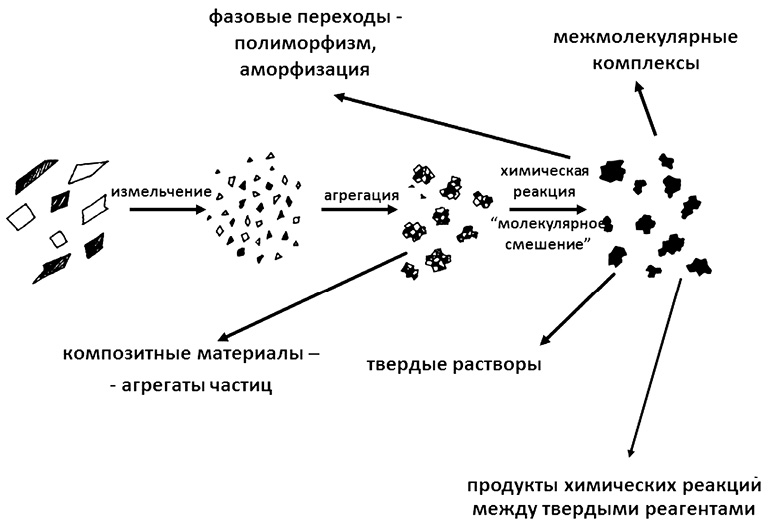
Механохимия является разделом химии твердого тела, в котором изучаются физико-химические превращения твердых веществ и их смесей в условиях интенсивных ударно-истирающих воздействий, обычно реализующихся в специальных мельницах. На рис. 1 показаны возможные пути трансформаций в смесях твердых веществ при их механохимической обработке [3].
Суть нашей технологии заключается в получении твердых дисперсий лекарственных веществ со вспомогательными веществами различной химической природы. Увеличение растворимости ЛВ и повышение эффективности фармакологического действия в зависимости от их физико-химических свойств достигается:
– образованием твердых дисперсий, в которых ЛВ диспергировано в молекулярной форме или находится в аморфном состоянии;
– образованием водорастворимых солей;
– образованием водорастворимых комплексов включения с полисахаридами по типу «гость-хозяин», а также мицелл.
Далее мы рассмотрим вышеуказанные случаи.
Рис. 1. Схема механохимических превращений в смесях твердых веществ (ЛВ + вспомогательные вещества) при их механической обработке ударно-истирающими воздействиями
Получение и свойства твердых дисперсий, в которых ЛВ находится в аморфизованном состоянии или диспергирована в молекулярной форме
Высвобождение в раствор фармакологически активного вещества из твердых лекарственных форм (порошков, таблеток и т.д.) во многом определяется скоростью растворения его кристаллической фазы. Однако многие фармакологические активные вещества крайне медленно растворяются в воде во многом за счет плохой смачиваемости и «прочности» кристаллической решетки. Очевидно, что получение твердых растворов – молекулярных дисперсий – таких веществ в хорошо растворимом наполнителе либо разупорядочение их кристаллических фаз будет способствовать ускорению процесса растворения. Именно этот принцип был применен нами к модификации антигельминтика карбендацима и ряда транквилизаторов бензодиазепинов – диазепама, оксазепама и медазепама, лекарственные субстанции которых практически нерастворимы в воде.
Для модификации солюбилизационных характеристик бензодиазепинов нами механохимическим способом были получены их твердые дисперсии с лактозой и микрокристаллической целлюлозой в весовых соотношениях 1:5, 1:10 и 1:15. В дифрактограммах механически активированных образцов наблюдалось резкое падение интенсивности рефлексов (без их заметного уширения) кристаллических фаз ЛВ вплоть до их полного исчезновения. Рефлексы веществ – наполнителей (лактозы и отчасти целлюлозы) претерпевали уширение, что свидетельствовало о накоплении дефектов и уменьшении кристалличности. К сожалению, методы термического анализа оказались неэффективны из-за относительно низких температур разложения веществ-наполнителей.
Проведенные исследования растворимости образцов продемонстрировали во всех случаях увеличение скорости растворения ЛВ в механохимически полученных образцах по сравнению со смесями, не подвергавшимися механохимической обработке и тем более измельченными исходными субстанциями [5]. Проведенные испытания биологической доступности образцов модифицированных препаратов оксазепама на лабораторных животных – кроликах – показали увеличение действующей концентрации оксазепама в крови и сокращение времени достижения ее максимального значения. Биодоступность оксазепама по сравнению с неактивированной смесью увеличивается в 1,56 ± 0,25 раза. Таким образом повышается эффективность действия лекарственного средства.
Получение и свойства твердых дисперсий, образующих водорастворимые соли ЛВ
Многие малорастворимые ЛВ обладают кислотными или основными свойствами и способны к ионизации в водных растворах и образованию соответствующих солей. Как правило, ионизированная форма является более гидрофильной и имеет более высокую водорастворимость. Многие ЛВ с целью повышения их растворимости выпускаются в виде их солей [9, 12]. Так, лекарственные вещества, имеющие основной характер, – в виде гидрохлоридов, а органические кислоты – в виде солей металлов или органических оснований. Соли получают реакцией жидкофазной нейтрализации с последующим выделением (сушкой). При этом требуются большие объемы растворителей, громоздкое оборудование, значительные производственные площади. Кроме того, в процессе сушки возможно разложение целевого продукта.
Рассмотрим возможности этого подхода на примере ацетилсалициловой кислоты (аспирина). Малая растворимость в воде ( Примечания:
Cmax – максимальная концентрация в крови;
Tmax – время достижения максимальной концентрации в крови;
AUC – площадь под фармакокинетической кривой, в относительных единицах;
* – навески препаратов взяты в эквивалентных по действующему веществу концентрациях.
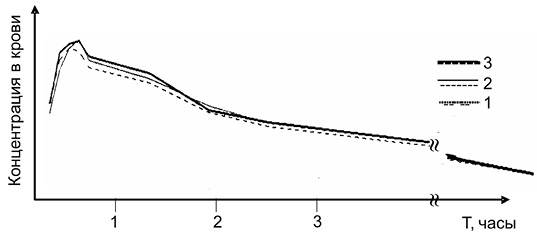
Рис. 3. Фармакокинетика препаратов «АСК – Na2CO3» и «Аспирин + С» при разных способах приема препаратов. Прием раствора таблеток «Аспирин + С» (1), раствора таблеток нашего препарата (2) и таблеток нашего препарата без предварительного растворения (3) в эквивалентных по АСК дозах
В соответствии с действующими правилами нами были разработаны фармакопейные статьи на таблетки и субстанцию, проведены фармакологические испытания [1, 2] и препарат зарегистрирован для применения в РФ.
Композиция состава АСК/CaCO3 = 78/22 вес. % также представляет значительный интерес. Она обладает высокой химической стабильностью при хранении и меньшей гигроскопичностью, но замедленной скоростью растворения. Методом прямого прессования из нее были получены таблетки с двумя дозировками АСК – 0,1 г (вес таблетки 0,128 г) и 0,5 г (вес таблетки 0,64 г). По своим характеристикам – химическая чистота, время растворения, кислотонейтрализующая емкость (для таблеток по 0,5 г) – эти таблетки соответствуют требованиям USP к так называемым «буферированным» таблеткам ацетилсалициловой кислоты. Разработанный нами препарат, получивший название «Антиагрегин», показал при сравнительных опытах с применяемыми в медицинской практике импортными препаратами практически равнозначную эффективность и безопасность для лечения и профилактики сердечно-сосудистых заболеваний (табл. 2).
Сравнительные характеристики разработанных в ИХТТМ СО РАН растворимых таблеток и их импортных аналогов
Источник
ВИДЫ ФАРМАКОЛОГИЧЕСКОГО ДЕЙСТВИЯ ЛС (ЧАСТЬ 3)
Индивидуальная несовместимость организма с ЛС может быть врожденной (идиосинкразия) или приобретенной (сенсибилизация).
Идиосинкразия (греч. idios — своеобразный, synkrasis — смешение) — врожденная индивидуальная непереносимость ЛВ. Она обусловлена отсутствием или снижением активности ферментов, либо отсутствием систем обезвреживания веществ определенной химической группы.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Идиосинкразия возникает при первом приеме вещества (агента) и при этом иммунитет не развивается, антитела не образуются, не возникает реакции «АГ+АТ». Например, врожденная аномалия фермента псевдохолинэстеразы удлиняет миорелаксирующее действие суксаметония йодида (Дитилин). У ряда больных с наследственной недостаточностью фермента глюкозо–6–фосфатдегидрогеназы может возникать гемолиз эритроцитов при применении противомалярийного препарата «Примахин» или антибиотика «Хлорамфеникол».
Аллергические реакции являются одними из наиболее часто встречающихся отрицательных видов действия ЛС. Многие из них (антибиотики, сульфаниламиды, препараты инсулина и др.) при попадании в организм людей с повышенной чувствительностью приводят к образованию и накоплению специфических антител. При повторных введениях этих ЛС происходит их взаимодействие с антителами и в результате возникают аллергические реакции. Лекарственная аллергия обусловлена нарушением иммунологических свойств организма, это приобретенная повышенная чувствительность организма к лекарственным веществам. Она протекает в виде аллергических реакций по немедленному или замедленному типу. К аллергическим реакциям немедленного типа относятся крапивница, отек Квинке, поллинозы, бронхиальная астма, сывороточная болезнь, лекарственный анафилактический шок. Они возникают при повторных курсах терапии, через несколько минут (≈20–30 мин.) после приема лекарства. Из аллергических реакций немедленного типа наиболее опасным является анафилактический шок. Анафилактический шок — быстроразвивающаяся реакция организма на повторное введение лекарства при имеющейся повышенной чувствительности к данному лекарственному веществу. Симптомы: боль за грудиной, отек гортани, спазм бронхов и удушье, снижение АД и ослабление сердечной деятельности, возможна потеря сознания. Если вовремя не оказать помощь, может наступить гибель организма. Аллергические реакции немедленного типа могут вызвать антибактериальные препараты (в частности, введение антибиотиков пенициллинового ряда), НПВС, анестетики, введение сывороток, вакцин.
Аллергические реакции замедленного типа развиваются через 24–48 часов и более, после повторного введения лекарственного вещества, к которому имеется сенсибилизация организма. Сенсибилизацией (лат. sensibilis — чувствительный) называется иммунологически опосредованная повышенная чувствительность организма к экзогенным или эндогенным антигенам. К ним относятся: лекарственная аллергия, вызывающая цитотоксический эффект в виде дерматитов, васкулитов, флебитов, аллергические реакции на пробы Манту, Пирке.
К отрицательным видам действия ЛС относится также «синдром отмены» — абстиненция (лат. abstinentia — воздержание), физическое и психическое состояние пациента после внезапного или полного прекращения препаратозависимой терапии. Синдром отмены может наблюдаться после прекращения приема опиоидных наркотических анальгетиков (Морфин, Тримеперидин); гормональных препаратов (Инсулин, глюкокортикостероиды); антигипертензивного средства «Клофелин», адреноблокатора «Анаприлин» и некоторых психотропных средств.
Всесоюзная организация здравоохранения (ВОЗ) рассматривает все случаи неблагоприятных реакций на организм зарегистрированных ЛС. Согласно определению ВОЗ, побочное нежелательное действие — это непредвиденные вредные (губительные) эффекты, которые возникают при использовании доз лекарственного средства, рекомендованных для профилактики и лечения заболеваний. При однократном введении лекарства неблагоприятные реакции могут не развиваться, не проявляться и никак не выявляться. При длительном применении ЛС побочный нежелательный эффект может стать причиной различных осложнений, в т.ч. обострения наследственных заболеваний. Различают нежелательные реакции, связанные с применением ЛС, на:
- побочные (негативные) реакции;
- серьезные нежелательные реакции (приводящие к различным осложнениям, инвалидности, угрозе жизни человека или к летальному исходу);
- непредсказуемые нежелательные реакции;
- серьезные непредвиденные нежелательные реакции.
Нежелательные эффекты, возникающие при применении ЛС в дозах, превышающих терапевтические, называются токсическими, как правило, это связано с передозировкой того или иного лекарственного препарата.
Согласно международной классификации выделяют 4 типа отрицательных побочных эффектов или нежелательных реакций на ЛС.
Тип А — предсказуемые реакции организма на введенное лекарство. Как правило, это дозозависимые побочные реакции, возникающие в 75% случаев от всех нежелательных реакций и приблизительно наблюдаются более чем у 1 из 100 больных. Эти реакции связывают с лекарственным взаимодействием, абсолютной, относительной передозировкой, индивидуальными особенностями организма. Летальность пациентов невысокая.
Тип В — непредсказуемые реакции организма, как правило, нечастые и возникают только у чувствительных людей. Это — дозонезависимые реакции, в
25% случаев неизвестного генеза, иммунологические или неиммунологические (иммунопатии, энзимопатии, идиосинкразия, сенсибилизация, гиперчувствительность). Возникновение таких реакций — менее 1 на 1000 больных, высокая летальность.
Тип С — реакции организма, связанные с длительной терапией заболевания. Возникает синдром отмены, кумуляция, лекарственная зависимость, подавление выработки эндогенных веществ. Диагностика таких реакций затруднительна.
Тип D — тяжелые необратимые побочные эффекты на вводимое лекарство. Как правило, чаще всего наблюдаются отсроченные эффекты: мутагенность, канцерогенность и тератогенность. Предсказать такие реакции организма крайне трудно. В настоящее время все лекарства, которые регистрируются, проходят тестирование на вышеперечисленные необратимые побочные эффекты.
Одновременное использование нескольких ЛС с мало прогнозируемым результатом их совместного взаимодействия может привести к полипрагмазии (греч. poli, polys — многий, pragma — действие). У больных старше 60 лет нередко диагностируют одновременно несколько заболеваний. В норме врач назначает не более 3–5 лекарств. Использование 3–5 лекарств одновременно приводит к развитию нежелательных реакций у 4% пациентов. Применение 16–20 лекарств одновременно может вызвать развитие побочных нежелательных эффектов в 54% случаев.
Токсическое действие возникает также при абсолютной или относительной передозировке ЛС и проявляется в значительном, иногда обратимом нарушении функций отдельных органов или систем органов. Абсолютная передозировка бывает при повышении высших, суточных и курсовых доз, а относительная передозировка – при назначении средних (обычных) доз лицам с поражениями печени, почек, что сопровождается накоплением в организме применяемого действующего вещества, т.к. замедляется его инактивация и выделение из организма. Хорошо известно токсическое действие аминогликозидных антибиотиков (Стрептомицин, Канамицин) на слуховой нерв, когда поражается восьмая пара черепно-мозговых нервов и возникает ототоксический эффект. У больных наблюдается снижением слуха, шум, звон или заложенность в ушах, вплоть до глухоты.
Токсическое действие, кроме общего и местного, может обозначаться как ориентированное на определенные органы: нейро–, нефро–, гепато–, гемато– или кардиотоксический эффект и т.д.
При нейротоксическом эффекте повреждаются ткани нервной системы (ЦНС, периферическая нервная система). Примером нейротоксического действия является повреждающее действие ЦНС местным анестетиком «Новокаином» и близким к нему по химической структуре антиаритмическим препаратом 1А класса — «Новокаинамидом». При в/в введении возможно развитие головокружения, двигательного возбуждения или неприятные ощущения (чаще в конечностях), парестезии, которые проявляются онемением, покалыванием, жжением или эффектом «ползание мурашек». Антибиотик «Циклосерин», применяемый для лечения больных туберкулезом, может вызвать развитие психозов, галлюцинаций, псевдоэпилептических припадков.
Антибиотики из группы аминогликозидов вызывают нефротоксический эффект. Повреждение клубочкового аппарата или канальцевой системы нефрона почек могут возникать при применении полимиксинов и некоторых цефалоспоринов.
Гепатотоксическое действие — повреждение паренхимы печени и нарушение ее метаболической функции и др. Например, при применении Метациклина, Рифампицина.
Гематотоксическое действие (угнетение кроветворения) оказывают большинство цитостатиков, т.к. оказывают прямое угнетающее влияние на быстро размножающиеся ткани и в т.ч. на кроветворную систему (костный мозг). Это токсическое действие возникает только при резорбтивном применении хлорамфеникола (левомицетина). После местного применения препаратов, в состав которых входит левомицетин: 0,25% раствор левомицетина в глазных каплях, 1% глазной линимент, линимент синтомицина, содержащий рацемическую смесь (1 ч. хлорамфеникола + 1 ч. — его правовращающий изомер), комбинированная мазь «Левомиколь» и антибактериальный аэрозоль «Олазоль», таких побочных эффектов не возникает.
При назначении ЛС беременным женщинам возможно отрицательное действие на развивающийся плод. Эти отрицательные действия возникают при применении ЛС, проникающих через плацентарный барьер. Наиболее серьезными являются тератогенное и эмбриотоксическое действия.
Тератогенное действие (греч. teras — урод) проявляется врожденными уродствами, развившимися в результате влияния некоторых ЛС на организм плода (наиболее опасный период с 3 по 12 неделю беременности). Хорошо известна история применения в некоторых зарубежных странах успокаивающего и снотворного средства «Талидомид». У женщин, принимавших в первую треть беременности этот препарат, рождались дети, имевшие врожденные уродства (дефекты конечностей, их недоразвитие, пороки сердца, почек, нарушение функций желудочно–кишечного тракта и др. органов). Известны случаи уродств от применения некоторых гормональных препаратов, антибиотиков. Для предупреждения тератогенного действия рекомендуется воздерживаться от приема ЛС в первые три месяца беременности, особенно когда происходит закладка органов ребенка.
Эмбриотоксическое действие ЛС проявляется нарушением развития эмбриона, процессов имплантации (1–2 неделю беременности) и образования плаценты (3–6 неделю). В результате эмбриотоксического действия беременность или не развивается, или заканчивается самопроизвольным абортом.
Фетотоксическое действие связано с изменением функции органов и систем плода, а также обмена веществ в период с 9 по 38 неделю.
Мутагенное действие связано со стойким повреждением зародышевой клетки в период эмбриогенеза и ее генетического аппарата (до 12 недели беременности). Мутации могут проявляться в половых клетках, изменяя генотип потомства. Мутации в соматических клетках могут привести к развитию злокачественных образований (канцерогенному действию).
Безопасность ЛС должна изучаться на всех этапах продвижения препарата на фармацевтическом рынке (даже после тщательно проведенных доклинических и клинических испытаний). Одно только официальное разрешение на применение лекарства не является гарантией его безопасности для всех больных.
Источник