Угроза выкидыша — причины, симптомы, лечение

Что такое угроза выкидыша
Ситуация самопроизвольного прерывания беременности и есть угроза выкидыша. На сегодня с угрозой прерывания сталкиваются женщины в 20% случаев. Самая распространенная угроза приходится на ранние сроки беременности, от зачатия до 12-ти недель. Также существует угроза прерывания на сроке 22-23 недель. На сроке с 22 по 37 неделю, это уже преждевременные роды.
Симптомы угрозы выкидыша
- Кровотечение. Иногда оно сильное, иногда выражается периодическими кровянистыми выделениями;
- Различной интенсивности боли внизу живота, которые могут опоясывающими, частыми или преходящими; боли могут появляться и в районе крестца;
- Ощущение напряжения матки (изменения тонуса). Ощущается дискомфорт, позднее могут начаться схваткообразные или тянущие вниз боли;
- Повышение температуры. Этот симптом часто свидетельствует о наличии в организме инфекции и может спровоцировать выкидыш. Температура в пределах 37.3 является гипертермическим воздействием прогестерона, считается нормой и явлением временного характера (появляется в основном на ранних сроках).
Любые перечисленные симптомы являются угрозой для вынашивания плода и требуют немедленной врачебной консультации, осмотра и принятия специальных мер для предотвращения выкидыша. Бывают случаи, когда при отсутствии перечисленных симптомов при осмотре гинекологом выявляется увеличенный тонус матки, нарушения сердечного ритма плода при осмотре на УЗИ, или обнаруживается опасная инфекция в крови, которой до зачатия не было. Количество угроз для выкидыша существует очень много, но если женщина находится под постоянным контролем специалиста и выполняет все рекомендации, то и опасность сводится к нулю.
Распространенные причины угрозы выкидыша
- Патология женских половых органов (например, двурогая или седловидная матка);
- наличие миомы матки, кисты, опухоли;
- повреждение эндометриальной ткани матки (особенно после частых абортов или перенесенной операции на матке);
- гормональные (нехватка гормонов или их высокий уровень);
- генетические сбои у плода;
- нарушение у беременной режима труда и отдыха;
- стрессовые ситуации, волнения, недосыпания, страхи, повышенная эмоциональность;
- вредные привычки;
- тяжелые физические нагрузки, поднятие тяжелого;
- употребление некоторых химических препаратов;
- инфицирование.
Иногда беременность женщины становится случайной, женщина не подозревает о ней, потому не бережет себя. А первый триместр является наиболее важным и уязвимым, ведь оплодотворенная яйцеклетка имплантируется в эндометрий матки и этот процесс могут прервать множество факторов: от употребления спиртного до активной половой жизни. Половая жизнь в первые месяцы после зачатия нежелательна из-за сокращений матки.
Любой сильный толчок, прыжки, передвигание тяжелого, нечаянное падение женщины могут спровоцировать угрозу выкидыша. При возникновении любого из перечисленных симптомов необходимо срочно обратиться к врачу для осмотра и сдачи анализов, мазков.
При наличии подозрений на опасность угрозы выкидыша берется моча на кетостероиды, анализы крови на инфекцию, мазок на наличие половой инфекции, исследуется гормональный фон. Если предыдущие беременности заканчивались выкидышами, то проводится коагулограмма. Чтобы определить точную причину угрозы выкидыша, необходима комплексная диагностика.
Как предотвратить угрозу выкидыша
- Планировать беременность заранее, проведя комплексное обследование для подготовки организма женщины к зачатию. Если присутствуют какие-либо заболевания, нужно пролечить и устранить их возможное влияние на течение беременности;
- оберегать свое здоровье от возможных стрессов и волнений, не переутомляться, достаточно высыпаться и расслабляться;
- хорошо питаться, употребляя в достаточном количестве витамины, микро- и макроэлементы, необходимые для нормального внутриутробного развития плода и поддержания здоровья женского организма;
- ни в коем случае не подымать тяжелого;
- выбирать удобную обувь без высоких каблуков (минимизируется возможности случайного падения и появления тромбофлебита);
- с учетом рекомендации специалиста постоянно выполнять специальные физические упражнения для беременных, которые помогут впоследствии при родах.
Для сохранения нормальной беременности витамины следует принимать не синтетические, а с учетом продуктов, богатых ими, с живой молекулярной структурой. Особенно важны свежие натуральные фрукты и овощи, соки из них, богатые клетчаткой, кальцием, витаминами группы В и витамином С для общего укрепления иммунной системы женщины.
Несмотря на достаточно распространенную угрозу выкидыша на сегодня существует много возможностей помощи для женщины, желающей выносить и родить здорового малыша. Главное, это постоянно проходить консультацию, своевременно сдавать анализы, выполнять все рекомендации гинеколога.
Источник
Лекарственные препараты угрожающие беременности
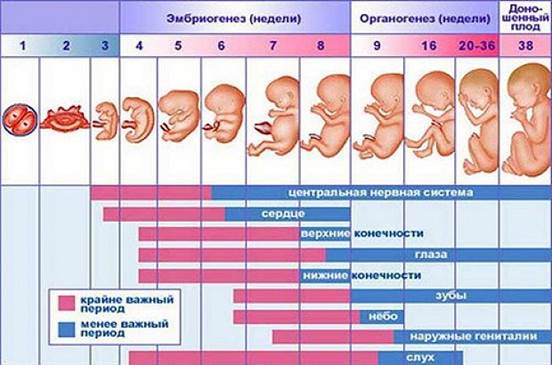
Врожденные аномалии у детей имеют широкий этиологический спектр. В настоящее время актуальность проблемы высока как на всем земном шаре, так и в России. Статистически частота врожденных пороков развития в России составляет 5-6 случаев на 1000 детей, тогда как в странах Европы 3-4 случая на 1000 родов. В настоящее время медицина не до конца выяснила причины врожденных аномалий у детей. Известно, что 10% врожденных пороков вызваны хромосомными и генетическими изменениями, 1% пороков вызваны действием лекарственных препаратов, в остальных 89% случаев изменения повлекли иные факторы. Путем рандомизированного исследования в странах мира лекарственные препараты во время беременности принимали более 80% опрошенных по данным Всемирной организации здравоохранения[2, 5]. Лекарства, которые выписывают доктора беременным, необходимы для нормального протекания беременности и развития здорового ребенка. Однако, есть определенный процент женщин, которые прибегают к самолечению, не выполняя указания врача. Во время беременности выделяют 3 триместра, в каждом из которых бесконтрольный и неправильный прием лекарственных средств может привести к врожденным порокам развития. Анализируя периоды беременности можно отметить, что отклонения от нормы будущего ребенка связаны с приемом лекарственных препаратов. Так, в первый триместр беременности, с 1-ой по 12-13-ю гинекологическую неделю, зародыш претерпевает ряд изменений, среди которых образование наружных половых органов, появляется точечно окостенение в хрящевом скелете, а также начинают функционировать мышцы, происходит окончание формирования плаценты[3]. (Рис.1) Во время 1-2 недели беременности, которые являются критическим периодом, эмбрион чувствителен к действию лекарств и при неправильном их приеме может произойти внутриутробная смерть зародыша. Второй триместр беременности длительностью с 14-ой по 26-ю гинекологическую неделю отличается относительным спокойствием, для этого периода характерно совершенствование органов и систем органов, которые начали закладываться в первом триместре. Третий триместр продолжается с 27-ой недели до родов. На данном этапе происходит формирование плода в плаценте. Происходит совершенствование нервной системы, почек, печени, органов чувств. Развиваются дыхательный, глотательный рефлексы. Плод набирает массу и активно растет в длину [3]. (Рис.1)
Рис.1 Внутриутробное развитие
Различают 3 вида патологических вариантов воздействия лекарственных средств на развитие плода: эмбриотоксический, тератогенный,фетотоксический. Эмбриотоксическое действие лекарственных препаратов, возникающее в первые 2-3 недели беременности, отмечается в негативном влиянии на зиготу и бластоцисту. Как следствие, может возникнуть гибель плода или морфофункциональные нарушения клеточных систем. Среди препаратов, которые вызывающие эмбриотоксическое действие выделяют противоопухолевые средства, противосудорожные препараты, никотин, эстрогены, гестогены, минералокортикоиды, антибиотики, сульфаниламиды, мочегонные препараты. (Табл. 1) Тератогенные эффекты, возникающие с 3 недели эмбриогенеза, вызывают нарушения биохимического, морфологического и функционального характера. Действие зависит от химической структуры, способности проникать через плаценту, дозировки препарата и скорость выведение лекарства из организма матери. По опасности препараты с тератогенными эффектами делятся на 3 группы: препараты, высоко опасные для плода, их употребление категорически запрещается даже за 6 месяцев до беременности, лекарства с определенной тератогенной опасностью, препараты, вызывающие отклонения при наличии определенных условий, например, высокий возраст беременной женщины, дозы применяемых лекарств [6]. Препараты с тератогенными эффектами являются наиболее опасными, так как они действуют на плод во время гистогенеза и органогенеза. Таким образом нарушение дифференцировки тканей может привести к порокам опорно-двигательной системы, а также внутренних органов. К таким средствам относятся: противоэпилептические средства, препараты половых гормонов, антибиотики, антикоагулянты, анальгетики, антидепрессанты, противомалярийные и противоопухолевые средства. Также известно, что прием ретиноидов, которые оказывают тератогенный эффект, вызывал врожденные аномалии развития, даже если курс лечения был завершен до начала беременности. (Табл. 1) [2,7]. Фетотоксическое действие наблюдается с 14-ой по 38-ую неделю беременности. Вызывают дисфункцию жизненно-важных систем органов. Примеры препаратов: аминогликозидные антибиотики, бета-адреномиметики и т.д. ( Табл. 1) [2,7] Лекарственные препараты проникают в организм плода через систему «мать-плацента-плод». Безусловно, самым важным органом во время беременности является плацента. Она служит своеобразным барьером между организмом матери и плода. Изначально толщина плаценты достигает 25мкм, но ближе к завершению беременности плацента становится заметно тоньше, ее толщина достигает 2 мкм. Этот факт способствует более легкому проникновению лекарств через плацентарный барьер в кровь плода. Также на ослабление плацентарного барьера влияют различные заболевания, например, сахарный диабет. Способность к проникновению различных веществ через плаценту обусловлена различными факторами, среди которых морфофункциональное состояние плаценты, плацентарный кровоток, физико-химическая характеристика лекарственных веществ и т.д. Известно, что большей проницаемостью через плаценту обладают низкомолекулярные вещества. Проникновение различных веществ через плаценту возможно различными путями, среди которых пиноцитоз, диффузия, активный транспорт. После проникновения лекарственного препарата происходит его дальнейшее попадание в пупочную вену, поэтому препарат достигает главных органов, например, сердце и мозг, минуя печень. Также важной проблемой является то, что некоторые препараты могут несколько раз циркулировать по организму плода, вызывая у него больший риск возникновения аномалий и пороков [8].
Таблица 1. Влияние лекарственных препаратов на развитие плода в первом, втором и третьем триместре беременности [4,5,9].
Источник
Терапия угрозы прерывания беременности в I триместре
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Этиологическая структура различных гестационных осложнений, в том числе и прерывания беременности на ранних сроках, разнообразна [1,4,5,7,8]. Причинно–следственные механизмы, обусловливающие развитие патологии в каждом отдельном случае при наличии прочих равных условий до настоящего времени остаются в стадии изучения. I триместр беременности является наиболее значимым, поскольку в этот период происходит эмбриогенез, формирование плаценты и сложных взаимоотношений между матерью и плодом. Угроза прерывания беременности в I триместре часто осложняет нормальное течение этих процессов, что может приводить к спонтанным абортам, развитию плацентарной недостаточности, внутриутробному страданию плода [3,5,12]. Несмотря на большое количество научных исследований [1,2,3,6,8], посвященных данной проблеме, до настоящего времени вопросы, посвященные ведению данного контингента беременных, особенно на первых, самых ответственных этапах гестации, остаются до конца не решенными.
На сегодняшнем этапе научного поиска многие исследователи приходят к выводу о тесной взаимосвязи и взаиморегуляции между эндокринной и иммунной системами на ранних этапах имплантации [4,5,8,10,11,12]. Неоспорим тот факт, что прогестерон играет очень важную роль в организме женщины. Еще до наступления беременности он вызывает децидуальную трансформацию эндометрия, подготавливая его к имплантации оплодотворенной яйцеклетки, а в период гестации способствует росту и васкуляризации миометрия, снижает возбудимость матки путем нейтрализации действия окситоцина, подавляет тканевые иммунологические реакции и др. [1,5,6,13]. Доказано, что прогестерон способствует полноценной секреторной трансформации эндометрия, необходимой для внедрения бластоцисты. Кроме того, во время беременности гестагены обеспечивают рост и развитие миометрия, его васкуляризацию и релаксацию путем нивелирования влияния окситоцина и снижения синтеза простагландинов [3,7,8,14].
Осложнения на начальных этапах гестации могут быть следствием как неполноценного стероидогенеза, так и недостаточности рецепторного аппарата эндометрия. Для успешной имплантации эмбриона необходимо согласование во времени готовности эндометрия к имплантации с развитием эмбриона (так называемое «имплантационное окно») [3,6,8]. В подобных ситуациях терапевтический подход должен учитывать этиологию формирования неполноценной лютеиновой фазы и нивелировать неблагоприятные предрасполагающие факторы. При хроническом воспалительном процессе в матке и придатках, помимо назначения индивидуально подобранной этиологической терапии, иммуномодулирующей терапии, необходима коррекция гормонального фона, что позволяет нормализовать состояние эндометрия и обеспечить адекватный бластогенез и плацентацию.
Принципиальную роль в подготовке слизистой оболочки матки к имплантации играет прогестерон. Общепризнано, что для нормального исхода беременности иммунная система женщины должна распознать ее. При нормально протекающей беременности в лимфоцитах периферической крови присутствуют рецепторы прогестерона, причем доля клеток, содержащих такие рецепторы, возрастает по мере увеличения срока гестации. В случае угрозы прерывания беременности доля клеток, содержащих рецепторы прогестерона, существенно ниже, чем у здоровых женщин, находящихся на том же сроке беременности. Ряд ученых полагают, что увеличение числа рецепторов прогестерона при беременности может быть вызвано присутствием эмбриона, который выступает в роли хорионического аллоантигенного (чужеродного) стимулятора [6,9,11].
По мнению A.R. Genazzani [10], около 15% всех наступивших беременностей завершается самопроизвольным абортом, который является одним из наиболее частых осложнений беременности. По данным статистики, примерно у одной из четырех беременных женщин возникают один и более самопроизвольных выкидыша.
О привычном невынашивании говорят в случае, если имели место три и более повторных самопроизвольных выкидыша. Данная патология, по данным В.М. Сидельниковой [5], встречается примерно у 1–3% всех женщин. При этом риск невынашивания беременности после трех повторных самопроизвольных выкидышей достигает 55%. В большинстве случаев (50–60%) причиной выкидышей являются гормональные нарушения, структурные аномалии хромосом зародыша, инфекции, эндокринные расстройства, анатомические дефекты у матери и др. Многие исследователи [1,3,5,7,14] полагают, что большая часть выкидышей, имеющих неясную этиологию, может быть вызвана ненормальной иммунной реакцией организма матери на отцовские антигены зародыша. В настоящее время появляется все больше данных, свидетельствующих о том, что прогестерон, по–видимому, играет важную роль в нормализации иммунного ответа на ранних стадиях беременности. При нормально протекающей беременности желтое тело, а позже плацента вырабатывают достаточное количество прогестерона. В его присутствии активируемые лимфоциты вырабатывают специальный белок – прогестерон–индуцированный блокирующий фактор (ПИБФ), который оказывает антиабортивное действие.
Как известно, при сохранении беременности на фоне лютеиновой недостаточности в дальнейшем формируется первичная плацентарная недостаточность. Для ее профилактики необходима полноценная подготовка к беременности и правильное ведение пациенток с угрожающим и привычным невынашиванием.
Для лечения угрожающего и привычного выкидыша практичным и высокоэффективным является прямое воздействие на рецепторы прогестерона за счет восполнения недостатка эндогенного прогестерона при помощи лекарственных средств – прогестагенов. Современным эффективным гестагенным препаратом является Дюфастон (дидрогестерон), в структуре которого метильная группа в позиции 10 расположена в a–позиции, водород при углероде 9 находится в b–позиции, кроме того, между углеводами 6 и 7 имеет место двойная связь. Изменение конфигурации молекулы приводит к тому, что Дюфастон легко абсорбируется при пероральном введении. Дидрогестерон в дозе 20–30 мг вызывает в эндометрии полноценную фазу секреции. Исследования, проведенные на животных, подтверждают высокую способность дидрогестерона поддерживать беременность.
Дюфастон является сильнодействующим гестагеном, эффективным при приеме внутрь, который по своей молекулярной структуре и фармакологическому действию близок к эндогенному прогестерону и вследствие этого обладает высокой аффинностью (сродством) к рецепторам прогестерона.
В отличие от многих прогестагенов он не является производным тестостерона, его структура отличается от структуры большинства синтетических прогестагенов, вследствие чего не вызывает ни одного из побочных эффектов, характерных для большинства этих препаратов.
Преимуществами химической структуры дидрогестерона является более высокая биодоступность препарата после перорального применения и отсутствие метаболитов с андрогенной или эстрогенной активностью. Основным метаболитом Дюфастона является 20 a–дигидроксидидрогестерон, который также обладает прогестагенной активностью.
Последние данные показали, что антиабортные эффекты прогестерона в течение ранней беременности вызваны также модуляцией материнского иммунного ответа. Доказано, что в присутствии Дюфастона активизированные лимфоциты синтезируют белок (блокирующий фактор, индуцированный прогестероном). Последний предотвращает воспалительные и вторичные тромботические реакции отторжения трофобласта за счет увеличения асимметричных нетоксичных блокирующих антител, а также блокады дегрануляции клеток естественных киллеров и за счет индукции T–лимфоцит–2 (Th2) зависящих цитокинов, перемещая баланс в сторону Th2 клеток, т.е. цитопротективного иммунного ответа [4,7]. Возмещая недостаточность лютеиновой фазы при угрозе или привычном прерывании беременности, Дюфастон оказывает также расслабляющий эффект на мускулатуру матки.
В отличие от других синтетических прогестагенов Дюфастон не вызывает феминизации плода мужского пола и не оказывает побочного действия на функции печени и свертываемость крови, таких проявлений, как угревые высыпания, огрубение голоса, гирсутизм и маскулинизации половых органов плода женского пола, не имеет метаболических эффектов (например, изменения липидного спектра крови и концентрации глюкозы), а также не влияет на активность гипофизарно–яичниковой системы и не вызывает атрофии надпочечников.
Одна таблетка Дюфастона содержит 10 мг дидрогестерона. После перорального приема дигидрогестерона 63% введенной дозы элиминируется с мочой, причем 85% от этого количества выводится в течение 24 часов. Практически полная почечная экскреция введенной дозы заканчивается через 72 часа.
При угрожающем выкидыше в комплекс лечения рекомендуется включать прием 40 мг данного препарата одномоментно, затем по 10 мг каждые 8 ч до исчезновения симптомов прерывания беременности. При привычном выкидыше назначают 10 мг Дюфастона 2 раза в сутки до 18–20–й недели беременности.
Появляется все большее количество данных в пользу того, что иммуномодулирующее действие гормонов имеет важное значение для поддержания нормальной функции эндометрия. Результаты исследований, проведенных A.R. Genazzani [10], показывают роль иммунной системы при беременности и, в частности, увеличение количества рецепторов прогестерона на лимфоцитах по мере развития беременности. В присутствии прогестерона или его аналога Дюфастона лимфоциты вырабатывают прогестерон–индуцированный блокирующий фактор. В результате иммунологических эффектов ПИБФ увеличивается активность Т–хелперных клеток II типа (Тh2), способствующих нормальному протеканию беременности, и снижается активность Т–хелперных клеток I типа (ТМ), оказывающих неблагоприятное действие на беременность. Авторы показали, что дидрогестерон (Дюфастон) также способен сместить соотношение Тh2/Th1 в благоприятную сторону и тем самым повысить вероятность успешной беременности. Этот эффект был подтвержден в двух клинических исследованиях, показавших, что дидрогестерон снижает частоту самопроизвольных абортов у женщин с угрозой выкидыша или привычным выкидышем в анамнезе.
Углубленные исследования о роли ПИБФ в поддержании беременности проводились J. Szekeres–Bartho и соавт. [13,14]. Общепризнано, что для нормального исхода беременности необходимо, чтобы иммунная система была способна ее распознать. При нормально протекающей беременности в лимфоцитах периферической крови присутствуют рецепторы прогестерона, причем доля клеток, содержащих такие рецепторы, увеличивается по мере увеличения срока гестации. Однако у женщин с высоким риском преждевременного прекращения беременности доля клеток, содержащих рецепторы прогестерона, существенно ниже, чем у здоровых женщин, находящихся на том же сроке беременности. После пересадки трансплантата или переливания крови количество клеток, содержащих рецепторы прогестерона, сравнимо с аналогичным показателем у беременных женщин. Это позволяет предположить, что у беременных увеличение числа рецепторов прогестерона на лимфоцитах может быть вызвано присутствием зародыша, который выступает в роли аллоантигенного стимулятора. В присутствии прогестерона эти лимфоциты продуцируют особый медиаторный белок 34–kD, или ПИБФ. Концентрация ПИБФ растет по мере увеличения срока гестации, но исчезает по истечении 40 недель при нормально протекающей беременности. Благодаря иммунологическому влиянию ПИБФ сохраняется беременность. ПИБФ изменяет баланс цитокинов в иммунной системе. При этом существуют два типа цитокинов: цитокины, вырабатываемые Т–хелперными клетками Th1, которые оказывают неблагоприятное действие на беременность, и цитокины, вырабатываемые Т–хелперными клетками Тh2, которые способствуют нормальному течению беременности. В присутствии ПИБФ происходит сдвиг в сторону преобладания цитокинов Тh2. Одновременное уменьшение выработки цитокинов Тh1 влечет за собой снижение активности естественных киллерных клеток (ЕКК) и нормальному исходу беременности. На фоне приема Дюфастона происходит достоверное повышение концентрации ПИБФ–позитивных лимфоцитов, что влечет за собой вышеописанные изменения в иммунной системе, направленные на сохранение беременности. В случаях же отсутствия ПИБФ концентрация цитокинов ТМ повышается и одновременно активизируются естественные киллерные клетки, что повышает вероятность аборта.
При угрозе выкидыша или преждевременных родах уровень ПИБФ значительно ниже, чем при нормально протекающей беременности. При недостатке ПИБФ активность естественных киллерных клеток возрастает примерно в 4 раза. В настоящее время считается, что повышенная активность ЕКК является одним из факторов, обусловливающих досрочное прекращение беременности.
M.Y. El–Zibdeh [9] публикует данные о результатах двух исследований, целью которых было выяснить, возможно ли с помощью дидрогестерона улучшить исход беременности у женщин, страдающих привычным выкидышем. 114 женщин с привычным выкидышем в анамнезе (среднее количество предыдущих выкидышей 3,3) были методом случайной выборки разделены на три группы и получали: дидрогестерон (Дюфастон) внутрь по 10 мг два раза в сутки; или хорионический гонадотропин человека (ХГЧ) внутримышечно по 5000 ME каждые 4 дня; или не получали никакого лечения. Терапию начинали сразу после подтверждения наступления беременности и прекращали при сроке гестации 12 недель. В группе женщин, принимавших Дюфастон, частота абортов достоверно (р
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Источник