Лекарственные препараты состав растения
НИИ фармации ММА им. И.М. Сеченова, Москва
Лекарственные сборы — смеси нескольких видов измельченного, реже – цельного, растительного сырья. В состав сборов входят различные части растений: корни, кора, трава, листья, цветки, плоды, семена. Многокомпонентные лекарственные растительные сборы давно используются в медицинской практике, что объясняется эффективностью и мягкостью их действия, отсутствием, как правило, нежелательных побочных явлений при длительном применении, а также удобством приготовления. В России имеются достаточная сырьевая база по многим видам лекарственных растений, опыт их производства и клинического применения. Лекарственные растительные сборы являются наиболее популярной и широко используемой формой переработки лекарственного растительного сырья.
Композиции из лекарственного растительного сырья, иногда с добавлением минеральных веществ, с глубокой древности применялись в медицине всего мира. Особенно популярны сборы в восточной медицине: китайской, тибетской и др. Прописи этих сборов отличаются сложностью состава, большим числом компонентов, относящихся к различным морфологическим группам сырья. В народной медицине России сборы применялись менее широко, т. к. предпочтение отдавалось индивидуальным лекарственным растениям.
Многокомпонентные смеси из лекарственного растительного сырья обладают ценными преимуществами перед другими фитопрепаратами: возможность обеспечить основной фармакологический эффект в сочетании с комплексным воздействием на организм больного в целом, мягкость действия и отсутствие, как правило, нежелательных побочных явлений. Они достаточно просты в промышленном производстве и относительно дешевы.
Лечение многокомпонентными лекарственными растительными сборами обычно более эффективно, чем одиночными растениями. При составлении сбора необходимо учитывать индивидуальные особенности больного и наличие сопутствующих заболеваний. При выборе сбора нужно знать показатели артериального давления и учитывать основную тенденцию его изменения. Например, при выборе сбора для больного холециститом с артериальной гипертензией необходимо, чтобы в сбор входили растения не только с желчегонным, но и с гипотензивным действием, иначе лечение может спровоцировать гипертонический криз, ухудшить общее состояние. Кроме того, следует учитывать склонность к запорам либо поносам; соответственно, эффект должен быть слабительного или вяжущего характера. Действие лекарственного растительного сырья во многом зависит от доз. Корень ревеня, например, в больших дозах применяется как слабительное средство, а в малых, наоборот, оказывает закрепляющее действие. Различные дозы пряно-горького сырья стимулируют или угнетают выделение желудочного сока. Некоторые растения действуют на мускулатуру матки и могут быть опасными при беременности. Растительные сборы и средства не рекомендуется принимать во время менструаций. Лекарственное растительное сырье обладает разносторонним действием. Этим объясняется тот факт, что в прописях, разных по назначению, часто встречаются одинаковые компоненты, но в разных количествах и различных сочетаниях. Предусмотреть нежелательное побочное действие лекарственных растений может только врач после всестороннего обследования больного.
В зависимости от входящих в состав сбора видов сырья на его основе готовят настои или отвары. Если в состав сбора входят пахучие эфирномасличные растения, то из них, как правило, готовят настой. Кипячение при этом не допускается, т. к. эфирные масла являются летучими веществами, испаряющимися вместе с водой. Лекарственные сборы содержат различные биологически активные соединения, которые одновременно с лечением основного заболевания дополнительно обогащают организм различными витаминами, минеральными соединениями и другими компонентами растений, способствующими повышению сопротивляемости организма, благотворно влияющими на центральную нервную систему, улучшающими процессы кроветворения, нейтрализующими шлаки и ускоряющими выведение их из организма. Воздействие на физиологические процессы осуществляется в этом случае природными, более приемлемыми для организма органическими веществами. Аллергические осложнения при лечении лекарственными растительными сборами наблюдаются гораздо реже, чем при применении других медикаментов (например, химического происхождения). Разностороннее воздействие биологически активных веществ растений часто достигает цели. Так, при назначении сложного сбора при заболеваниях печени вещества бессмертника усиливают секрецию желчи, желудочного и панкреатического сока, повышают тонус желчного пузыря, изменяют химический состав желчи. Вещества, содержащиеся в кукурузных рыльцах, благотворно влияют на обмен веществ, улучшают желчеотделение. Вещества барбариса уменьшают и снимают боли, что связано с присутствием алкалоида берберина, обладающего спазмолитическим действием. С той же целью часто в такой сбор вводят и лист мяты перечной.
Кроме органических веществ сборы содержат макро- и микроэлементы, которые участвуют в обмене веществ, находятся в функциональном взаимодействии с ферментами, витаминами, гормонами и другими биологически активными веществами. Марганец, медь, цинк, кобальт в микродозах стимулируют выработку антител, повышают сопротивляемость организма. Медь, железо, цинк, кобальт уменьшают проницаемость биологических мембран. При лечении больного многокомпонентными лекарственными сборами в организм вводятся белки, аминокислоты, углеводы, липиды, ферменты, витамины, органические кислоты, спирты, альдегиды и кетоны, сложные эфиры фосфорной кислоты и других кислот, фитостерины, смолистые и дубильные вещества, гликозиды, терпеноиды, кумарины, амиды и амины, бетаины, холин и холиновые сложные эфиры, пурины и пиримидины, алкалоиды, горькие вещества и многие другие.
Наиболее популярны следующие лекарственные растительные сборы: антимикробный, желудочно-кишечный, урологический, грудной, успокоительный, желчегонный, противосклеротический, спазмолитический, ветрогонный, мочегонный, противоастматический.
Заболевания желудочно-кишечного тракта довольно широко распространены, на их долю приходится 35–37 % общей заболеваемости населения. Наиболее распространенными среди них являются гастриты, язвенная болезнь, энтероколиты. Терапия воспалительных и деструктивных заболеваний желудочно-кишечного тракта направлена на коррекцию нарушений желудочной секреции, моторной функции желудка и кишечника, кишечного пищеварения, а также предусматривает воздействие на измененную слизистую оболочку желудка и кишечника. Применение синтетических лекарственных препаратов не всегда оказывает должное воздействие при указанной патологии; кроме того, возможно развитие побочных реакций и осложнений. В таких случаях, а также для профилактики обострений хронических заболеваний желудочно-кишечного тракта весьма перспективны растительные сборы. Желудочно-кишечный сбор – это комбинированный препарат растительного происхождения, содержащий пять видов растительного лекарственного сырья. Настой сбора обладает спазмолитическим, противовоспалительным, желчегонным седативным, регенерирующим действием. Эффект обусловливают содержащиеся в цветках ромашки эфирное масло, полисахариды, флавоноиды; эфирное масло из листьев мяты, основными компонентами которого является ментол, флавоноиды, витамины; эфирное масло из плодов укропа.
Воспалительные заболевания бронхов в настоящее время широко распространены и являются одной из наиболее частых причин потери работоспособности. Антибиотикотерапия, применяемая для их лечения, нередко приводит к развитию аллергии, формированию резистентности микроорганизмов с потерей чувствительности к антибиотикам при последующих курсах лечения, развитию дисбактериоза и росту числа грибковых заболеваний. Опыт клинического применения грудного сбора демонстрирует его эффективность и целесообразность использования при инфекционно-воспалительных процессах в бронхах в качестве вспомогательного или альтернативного лекарственного средства, свободного от нежелательных побочных явлений. Лечебный эффект сбора обусловлен антибактериальным эффектом цветков ромашки, побегов багульника, цветков календулы, отхаркивающим и обволакивающим действием корней солодки, травы фиалки и побегов багульника, противовоспалительными и спазмолитическими эффектами корней солодки, цветков ромашки, календулы и листьев мяты.
В последнее время наблюдается значительный рост распространенности состояний, вызванных повышенной физической или умственной нагрузкой, воздействием неблагоприятных факторов окружающей среды, растущими информационными нагрузками, стрессами. В таких условиях развивается хроническое переутомление, которое приводит к развитию бессонницы, повышенной нервной возбудимости, раздражительности, неврастении, сердечно-сосудистых неврозов, тахикардии, истерии, мигрени, вегетососудистой дистонии, климактерических расстройств, артериальной гипертензии. Лекарственных растений, обладающих успокоительным действием, достаточно много. Седативное, спазмолитическое, гипотензивное действие успокоительного сбора обусловлено входящими в него лекарственными травами. Эффект определяют содержащиеся в траве пустырника эфирные масла, сапонины, дубильные вещества, алкалоиды; в листьях мяты перечной – ментол; в корневищах с корнями валерианы – сложный эфир борнеола и изовалериановой кислоты, свободная валериановая и другие органические кислоты, алкалоиды (валерин и хатинин), дубильные вещества, сахара; в корнях солодки – ликуразид, тритерпены, глицирризиновая кислота и флавоноиды; в траве чабреца – эфирное масло, дубильные и горькие вещества; в траве душицы – тимол, флавоноиды, дубильные вещества; в шишках хмеля – эфирное масло, органические кислоты, алкалоиды, флавоноиды, лупулин; в траве донника – кумарины, мелилотозид, полисахариды.
Приготовление из сборов лекарственных растений настоев и отваров принципиально не отличается от получения этих препаратов из сырья отдельных лекарственных растений. В конкретных указаниях по приготовлению из сборов настоев и отваров обычно приводится такое соотношение: 1–2 столовая ложка смеси на 200 мл воды.
Во всех случаях для полного извлечения действующих веществ воды берут гораздо больше, чем при приготовлении аналогичных лекарств в условиях аптеки. Поэтому принимают изготовленное лекарство чаще всего не ложками, а по 1/3–1/2 стакана. Если настой или отвар готовят ежедневно, он не подвергается микробной контаминации и может храниться при комнатной температуре в течение дня. При большем количестве его следует хранить в холодильнике, но не более двух суток.
Обычно при лечении лекарственными растениями улучшение наступает через несколько дней, но стойкого эффекта удается достичь лишь при длительном и регулярном применении лекарственных трав. Отсутствие положительного эффекта в течение 2–3 недель, как правило, является основанием для замены сбора. Курс лечения сборами должен определять лечащий врач при постоянном наблюдении за здоровьем больного.
При лечении хронических больных сборами растений их принимают длительное время. Во избежание привыкания к ним и снижения эффективности лечебного воздействия рекомендуют после каждого курса лечения (1,0–1,5 месяца) делать перерыв на 1–2 недели. По тем же соображениям желательно после 2–3 курсов лечения одним из сборов перейти на лечение другим, обладающим аналогичным действием.
Информация об авторах:
Самылина Ирина Александровна – доктор фармацевтических наук, профессор, член-корреспондент РАМН,
директор НИИ фармации; заведующая кафедрой фармакогнозии ММА им. И.М. Сеченова.
Тел. 8 (499) 128-57-88;
Сорокина Алла Анатольевна – доктор фармацевтических наук,
профессор кафедры фармакогнозии ММА им. И.М. Сеченова.
Тел. 8 (495) 120-20-20;
Пятигорская Наталья Валерьевна – кандидат фармацевтических наук, доцент,
заместитель директора НИИ фармации по научной работе.
Тел. 8 (499) 128-57-55
Источник
Лекарственные препараты состав растения
Одним из перспективных источников фитопрепаратов считаются лекарственные растения, содержащие флавоноиды, которые в силу широкого распространения в растениях и большого структурного разнообразия в настоящее время находятся в центре внимания исследователей в области фармакогнозии, фармации и медицины [1–3, 8–11]. Флавоноиды – наиболее многочисленный класс природных фенольных соединений, для которых характерно структурное многообразие, высокая и разносторонняя активность и малая токсичность. Широкая амплитуда биологической активности флавоноидов связана с многообразием их химических структур и вытекающих из них различных физико-химических свойств. Этот интерес связан с тем обстоятельством, что флавоноиды, будучи эволюционно адекватными организму человека, обусловливают антиоксидантные, ангиопротекторные, гепатопротекторные, желчегонные, диуретические, нейротропные и другие важнейшие фармакологические свойства [1, 5–13]. Причем именно вышеперечисленные фармакологические эффекты в наибольшей степени привлекают ученых в области создания новых растительных лекарственных препаратов.
При этом важно отметить, что только за последние 10–15 лет число фармакопейных растений, содержащих флавоноиды, увеличилось с 11 до 30 видов [4, 6, 8]. Вместе с тем созданию лекарственных препаратов на основе флавоноидных растений препятствует недостаточная степень изученности их химического состава, зависимостей в ряду «химическая структура – спектральные характеристики» и «компонентный состав – фармакологические свойства». Это приводит к отсутствию системного подхода в трактовке совокупной значимости действующих веществ в плане проявления фармакологических эффектов, а также научно обоснованных технологий получения и анализа лекарственных средств. Кроме того, в настоящее время остро стоит проблема объективной стандартизации сырья лекарственных растений и фитопрепаратов, содержащих флавоноиды, поскольку во многих случаях в методиках анализа отсутствует доказательная база или же не используются современные инструментальные возможности. В этом контексте весьма актуальной проблемой является совершенствование имеющейся нормативной документации, а также разработка новых стандартов качества на ЛРС, лекарственные субстанции и препараты, особенно в связи с подготовкой к изданию Государственной Фармакопеи Российской Федерации XII издания.
Цель настоящих исследований – разработка методологических подходов к созданию и стандартизации лекарственного растительного сырья и фитопрепаратов, содержащих флавоноиды.
Материалы и методы исследования
В качестве объектов исследования служили фармакопейные растения, лекарственное растительное сырье, флавоноиды, выделенные из ЛРС. При этом исследовали цветки бессмертника песчаного [Helichrysum arenarium (L.) Moench.], цветки пижмы обыкновенной (Tanacetum vulgare L.), траву эрвы шерстистой (Aerva lanata L.), цветки василька синего (Centaurea cyanus L.), траву полыни эстрагон (Artemisia dracunculus L.), траву горца почечуйного (Polygonum persicaria L.), траву перца водяного (Polygonum hydropiper L.), листья гинкго двулопастного (Ginkgo biloba L.), траву репешка аптечного (Agrimonia eupatoria L.), плоды и цветки боярышника кроваво-красного (Crataegus sanguinea Pall.), цветки липы сердцевидной (Tilia cordata Mill.).
В работе использованы тонкослойная хроматография, колоночная хроматография, высокоэффективная жидкостная хроматография, спектрофотомерия, 1Н-ЯМР-спектроскопия, масс-спектрометрия, различные химические превращения. 1Н-ЯМР- спектры получали на приборах «Bruker AM 300» (300 МГц), масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Воздушно-сухое растительное сырье подвергали исчерпывающему экстрагированию 70 % спиртом этиловым, полученные водно-спиртовые экстракты упаривали под вакуумом до густого остатка и далее подвергали хроматографическому разделению на силикагеле L 40/100. Контроль за разделением веществ осуществляли с помощью ТСХ-анализа на пластинках «Сорбфил ПТСХ-АФ-А-УФ» в системах хлороформ-этанол (9:1), хлороформ-этанол-вода (26:16:3), а также н-бутанол-ледяная уксусная кислота-вода (4:1:2).
Результаты исследования и их обсуждение
С целью систематизации фармакопейных растений, содержащих флавоноиды, нами разработана классификация (таблица), позволяющая учитывать всю совокупность биологически активных соединений (БАС) с точки зрения биологической активности, стандартизации и технологии получения лекарственных препаратов.
Классификация фармакопейных растений, содержащих флавоноиды
Наименование группы фармакопейных растений
Наименование лекарственного растения
Фармакопейные растения, содержащие флавоноиды в качестве ведущей группы БАС
Бархат амурский, бессмертник песчаный, бессмертник итальянский, боярышник кроваво-красный, бузина черная, василек синий, володушка многожильчатая, володушка круглолистная, гибискус сабдариффа, гинкго двулопастный, горец перечный, горец почечуйный, горец птичий, гречиха посевная, датиска коноплевая, десмодиум канадский, зверобой продырявленный, зверобой пятнистый, земляника лесная, золотарник канадский, лабазник вязолистный, лапчатка серебристая, леспедеца двухцветная, леспедеца копеечниковая, лимон, расторопша пятнистая, овес посевной, очиток большой, репешок аптечный, солянка холмовая, софора японская, стальник полевой, фасоль обыкновенная, фиалка трехцветная, хвощ полевой шлемник байкальский, эрва шерстистая
Фармакопейные эфиромасличные растения, содержащие флавоноиды
Арника горная, береза повислая, береза бородавчатая, липа сердцевидная, мята перечная, пижма обыкновенная, полынь эстрагон, ромашка аптечная, ромашка душистая, тополь черный, тысячелистник обыкновенный
Фармакопейные растения, содержащие горечи и флавоноиды
Одуванчик лекарственный, пустырник пятилопастный, трилистник водяной
Фармакопейные растения, содержащие сапонины и флавоноиды
Астрагал шерстистоцветковый, каштан конский обыкновенный, солодка голая, солодка уральская
Фармакопейные растения, содержащие витамины и флавоноиды
Арония черноплодная, календула лекарственная, смородина черная, сушеница топяная, череда трехраздельная, шиповник коричный, шиповник собачий
Фармакопейные растения, содержащие простые фенолы и флавоноиды
Фармакопейные растения, содержащие дубильные вещества и флавоноиды
Сабельник болотный, скумпия кожевенная, черемуха обыкновенная, черника обыкновенная
Фармакопейные алкалоидоносные растения, содержащие флавоноиды
Пассифлора инкарнатная, чай китайский, чистотел большой
В соответствии с данной классификацией в первой группе находятся лекарственные растения, содержащие флавоноиды в качестве ведущей группы БАС. В группах 2-8 флавоноиды выступают второй группы БАС, причем в данном случае акцент сделан не только на вкладе флавоноидов в фармакологический эффект, но и на их использовании в качестве критерия подлинности, качества сырья, а также как источника получения лекарственных средств.
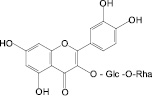
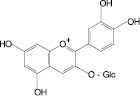
На основе результатов сравнительного изучения химического состава сырья и лекарственных препаратов фармакопейных растений научно обоснованы методологические подходы к стандартизации ЛРС, содержащего флаваноны, халконы, флавоны, флавонолы, антоцианы, наиболее широко распространенные в растениях. Эти подходы заключаются в комплексном и обоснованном использовании методов ТСХ, ВЭЖХ, спектрофотометрии и использовании соответствующих ГСО (изосалипурпозид, пиностробин, цинарозид, гиперозид, рутин, цианидин-3-О-глюкозид).
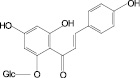
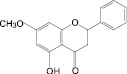
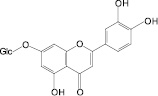
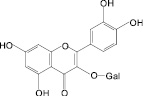
Обосновано использование в методиках качественного и количественного анализа сырья и препаратов, содержащих преимущественно флаваноны (перца водяного трава), халконы (бессмертника песчаного цветки), флавоны (пижмы обыкновенной цветки, полыни эстрагон трава), флавонолы (горца почечуйного трава, боярышника кроваво-красного цветки и плоды, липы цветки, эрвы шерстистой трава, репешка аптечного трава), антоцианы (василька синего цветки), соответствующих ГСО изосалипурпозида (халкон), пиностробина (флаванон), цинарозида (флавон), гиперозида и рутина (флавонолы), цианидин-3-О-глюкозида (антоцианы).
На основе результатов фармакогностических, химических, технологических и фармакологических исследований сырья флавоноидосодержащих фармакопейных растений обоснована целесообразность создания антиоксидантных, гепатопротекторных, диуретических, ноотропных, анксиолитических фитопрепаратов, в том числе импортозамещающих лекарственных средств.
Особого внимания заслуживают нейротропные свойства флавоноидов, которые стали привлекать исследователей сравнительно недавно. Среди фармакопейных растений, содержащих флавоноиды, в качестве источника нейротропных лекарственных препаратов применяются два вида – зверобой продырявленный и гинкго двулопастный [4–6, 8]. При изучении флавоноидов листьев гинкго двулопастного выявлено, что вклад в ноотропную активность вносит гинкгетин, являющийся одним из характерных и диагностических компонентов сырья данного растения [8]. Впервые обнаружена анксиолитическая активность для лекарственного препарата «Гинкго двулопастного настойка», при этом показана значимость всего флавоноидного комплекса листьев гинкго двулопастного для проявления наиболее полного спектра нейротропной активности.
Уточнен характер антиоксидантного действия для индивидуальных соединений, относящихся к разным классификационным группам флавоноидов, на ферментативные и неферментативные звенья антиоксидантной защиты, что позволило сформулировать рекомендации по созданию комбинированных гепатопротекторных лекарственных препаратов, в случае которых антиоксидантная составляющая актуальной в плане проявления терапевтического эффекта. При этом необходимо отметить, что именно благодаря изучению воздействия флавоноидов, а именно флаволигнанов плодов расторопши пятнистой [3, 7] на функцию печени, особенно гепатоцитов, появилось понятие «гепатопротекторные свойства» и, как следствие, фармакологическая группа – гепатопротекторы, причем произошло это сравнительно недавно – в 90-е годы XX столетия [3, 4, 6].
В ходе исследований выявлены также особенности влияния на выделительную функцию почек водных и водно-спиртовых извлечений. Проведено сравнительное исследование диуретической активности водно-спиртовых извлечений из листьев толокнянки обыкновенной (препараты сравнения), травы эрвы шерстистой, цветков пижмы обыкновенной, травы репешка аптечного аптечного и цветков бессмертника песчаного. Установлено, что настой и препарат «Эрвы шерстистой настойка» обладают быстрым развитием диуретического эффекта и короткой продолжительностью действия. Для препаратов «Пижмы настойка» и «Бессмертника песчаного настойка», а также соответствующих настоев характерно быстрое развитие эффекта и длительное диуретическое действие, тогда как в случае препарата «Толокнянки настойка» наблюдается длительный латентный период в сочетании с продолжительным диуретическим действием.
Результаты проведенных исследований позволили создать методологическую базу для совершенствования стандартизации ЛРС, содержащего флавоноиды, а также расширить возможности целенаправленного поиска новых сырьевых источников для получения эффективных отечественных фитопрепаратов и лекарственных субстанций с антиоксидантной, диуретической, ноотропной и анксиолитической активностью. Внедрение результатов данных исследований будет способствовать успешной реализации Стратегии лекарственного обеспечения населения Российской Федерации на период до 2025 года, одним из главных приоритетов которой является разработка новых конкурентоспособных импортозамещающих лекарственных препаратов, в том числе растительного происхождения.
Рецензенты:
Первушкин С.В., д.фарм.н., профессор, заведующий кафедрой фармацевтической технологии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара;
Дубищев А.В., д.м.н., профессор, зав. кафедрой фармакологии им. заслуженного деятеля науки РФ, профессора А.А. Лебедева, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара.
Источник