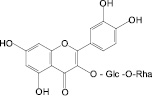
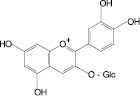
Лекарственное растительное сырье содержащие фенольные соединения флавоноиды
Одним из перспективных источников фитопрепаратов считаются лекарственные растения, содержащие флавоноиды, которые в силу широкого распространения в растениях и большого структурного разнообразия в настоящее время находятся в центре внимания исследователей в области фармакогнозии, фармации и медицины [1–3, 8–11]. Флавоноиды – наиболее многочисленный класс природных фенольных соединений, для которых характерно структурное многообразие, высокая и разносторонняя активность и малая токсичность. Широкая амплитуда биологической активности флавоноидов связана с многообразием их химических структур и вытекающих из них различных физико-химических свойств. Этот интерес связан с тем обстоятельством, что флавоноиды, будучи эволюционно адекватными организму человека, обусловливают антиоксидантные, ангиопротекторные, гепатопротекторные, желчегонные, диуретические, нейротропные и другие важнейшие фармакологические свойства [1, 5–13]. Причем именно вышеперечисленные фармакологические эффекты в наибольшей степени привлекают ученых в области создания новых растительных лекарственных препаратов.
При этом важно отметить, что только за последние 10–15 лет число фармакопейных растений, содержащих флавоноиды, увеличилось с 11 до 30 видов [4, 6, 8]. Вместе с тем созданию лекарственных препаратов на основе флавоноидных растений препятствует недостаточная степень изученности их химического состава, зависимостей в ряду «химическая структура – спектральные характеристики» и «компонентный состав – фармакологические свойства». Это приводит к отсутствию системного подхода в трактовке совокупной значимости действующих веществ в плане проявления фармакологических эффектов, а также научно обоснованных технологий получения и анализа лекарственных средств. Кроме того, в настоящее время остро стоит проблема объективной стандартизации сырья лекарственных растений и фитопрепаратов, содержащих флавоноиды, поскольку во многих случаях в методиках анализа отсутствует доказательная база или же не используются современные инструментальные возможности. В этом контексте весьма актуальной проблемой является совершенствование имеющейся нормативной документации, а также разработка новых стандартов качества на ЛРС, лекарственные субстанции и препараты, особенно в связи с подготовкой к изданию Государственной Фармакопеи Российской Федерации XII издания.
Цель настоящих исследований – разработка методологических подходов к созданию и стандартизации лекарственного растительного сырья и фитопрепаратов, содержащих флавоноиды.
Материалы и методы исследования
В качестве объектов исследования служили фармакопейные растения, лекарственное растительное сырье, флавоноиды, выделенные из ЛРС. При этом исследовали цветки бессмертника песчаного [Helichrysum arenarium (L.) Moench.], цветки пижмы обыкновенной (Tanacetum vulgare L.), траву эрвы шерстистой (Aerva lanata L.), цветки василька синего (Centaurea cyanus L.), траву полыни эстрагон (Artemisia dracunculus L.), траву горца почечуйного (Polygonum persicaria L.), траву перца водяного (Polygonum hydropiper L.), листья гинкго двулопастного (Ginkgo biloba L.), траву репешка аптечного (Agrimonia eupatoria L.), плоды и цветки боярышника кроваво-красного (Crataegus sanguinea Pall.), цветки липы сердцевидной (Tilia cordata Mill.).
В работе использованы тонкослойная хроматография, колоночная хроматография, высокоэффективная жидкостная хроматография, спектрофотомерия, 1Н-ЯМР-спектроскопия, масс-спектрометрия, различные химические превращения. 1Н-ЯМР- спектры получали на приборах «Bruker AM 300» (300 МГц), масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Воздушно-сухое растительное сырье подвергали исчерпывающему экстрагированию 70 % спиртом этиловым, полученные водно-спиртовые экстракты упаривали под вакуумом до густого остатка и далее подвергали хроматографическому разделению на силикагеле L 40/100. Контроль за разделением веществ осуществляли с помощью ТСХ-анализа на пластинках «Сорбфил ПТСХ-АФ-А-УФ» в системах хлороформ-этанол (9:1), хлороформ-этанол-вода (26:16:3), а также н-бутанол-ледяная уксусная кислота-вода (4:1:2).
Результаты исследования и их обсуждение
С целью систематизации фармакопейных растений, содержащих флавоноиды, нами разработана классификация (таблица), позволяющая учитывать всю совокупность биологически активных соединений (БАС) с точки зрения биологической активности, стандартизации и технологии получения лекарственных препаратов.
Классификация фармакопейных растений, содержащих флавоноиды
Наименование группы фармакопейных растений
Наименование лекарственного растения
Фармакопейные растения, содержащие флавоноиды в качестве ведущей группы БАС
Бархат амурский, бессмертник песчаный, бессмертник итальянский, боярышник кроваво-красный, бузина черная, василек синий, володушка многожильчатая, володушка круглолистная, гибискус сабдариффа, гинкго двулопастный, горец перечный, горец почечуйный, горец птичий, гречиха посевная, датиска коноплевая, десмодиум канадский, зверобой продырявленный, зверобой пятнистый, земляника лесная, золотарник канадский, лабазник вязолистный, лапчатка серебристая, леспедеца двухцветная, леспедеца копеечниковая, лимон, расторопша пятнистая, овес посевной, очиток большой, репешок аптечный, солянка холмовая, софора японская, стальник полевой, фасоль обыкновенная, фиалка трехцветная, хвощ полевой шлемник байкальский, эрва шерстистая
Фармакопейные эфиромасличные растения, содержащие флавоноиды
Арника горная, береза повислая, береза бородавчатая, липа сердцевидная, мята перечная, пижма обыкновенная, полынь эстрагон, ромашка аптечная, ромашка душистая, тополь черный, тысячелистник обыкновенный
Фармакопейные растения, содержащие горечи и флавоноиды
Одуванчик лекарственный, пустырник пятилопастный, трилистник водяной
Фармакопейные растения, содержащие сапонины и флавоноиды
Астрагал шерстистоцветковый, каштан конский обыкновенный, солодка голая, солодка уральская
Фармакопейные растения, содержащие витамины и флавоноиды
Арония черноплодная, календула лекарственная, смородина черная, сушеница топяная, череда трехраздельная, шиповник коричный, шиповник собачий
Фармакопейные растения, содержащие простые фенолы и флавоноиды
Фармакопейные растения, содержащие дубильные вещества и флавоноиды
Сабельник болотный, скумпия кожевенная, черемуха обыкновенная, черника обыкновенная
Фармакопейные алкалоидоносные растения, содержащие флавоноиды
Пассифлора инкарнатная, чай китайский, чистотел большой
В соответствии с данной классификацией в первой группе находятся лекарственные растения, содержащие флавоноиды в качестве ведущей группы БАС. В группах 2-8 флавоноиды выступают второй группы БАС, причем в данном случае акцент сделан не только на вкладе флавоноидов в фармакологический эффект, но и на их использовании в качестве критерия подлинности, качества сырья, а также как источника получения лекарственных средств.
На основе результатов сравнительного изучения химического состава сырья и лекарственных препаратов фармакопейных растений научно обоснованы методологические подходы к стандартизации ЛРС, содержащего флаваноны, халконы, флавоны, флавонолы, антоцианы, наиболее широко распространенные в растениях. Эти подходы заключаются в комплексном и обоснованном использовании методов ТСХ, ВЭЖХ, спектрофотометрии и использовании соответствующих ГСО (изосалипурпозид, пиностробин, цинарозид, гиперозид, рутин, цианидин-3-О-глюкозид).
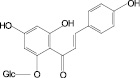
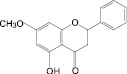
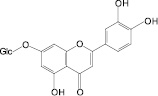
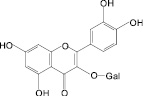
Обосновано использование в методиках качественного и количественного анализа сырья и препаратов, содержащих преимущественно флаваноны (перца водяного трава), халконы (бессмертника песчаного цветки), флавоны (пижмы обыкновенной цветки, полыни эстрагон трава), флавонолы (горца почечуйного трава, боярышника кроваво-красного цветки и плоды, липы цветки, эрвы шерстистой трава, репешка аптечного трава), антоцианы (василька синего цветки), соответствующих ГСО изосалипурпозида (халкон), пиностробина (флаванон), цинарозида (флавон), гиперозида и рутина (флавонолы), цианидин-3-О-глюкозида (антоцианы).
На основе результатов фармакогностических, химических, технологических и фармакологических исследований сырья флавоноидосодержащих фармакопейных растений обоснована целесообразность создания антиоксидантных, гепатопротекторных, диуретических, ноотропных, анксиолитических фитопрепаратов, в том числе импортозамещающих лекарственных средств.
Особого внимания заслуживают нейротропные свойства флавоноидов, которые стали привлекать исследователей сравнительно недавно. Среди фармакопейных растений, содержащих флавоноиды, в качестве источника нейротропных лекарственных препаратов применяются два вида – зверобой продырявленный и гинкго двулопастный [4–6, 8]. При изучении флавоноидов листьев гинкго двулопастного выявлено, что вклад в ноотропную активность вносит гинкгетин, являющийся одним из характерных и диагностических компонентов сырья данного растения [8]. Впервые обнаружена анксиолитическая активность для лекарственного препарата «Гинкго двулопастного настойка», при этом показана значимость всего флавоноидного комплекса листьев гинкго двулопастного для проявления наиболее полного спектра нейротропной активности.
Уточнен характер антиоксидантного действия для индивидуальных соединений, относящихся к разным классификационным группам флавоноидов, на ферментативные и неферментативные звенья антиоксидантной защиты, что позволило сформулировать рекомендации по созданию комбинированных гепатопротекторных лекарственных препаратов, в случае которых антиоксидантная составляющая актуальной в плане проявления терапевтического эффекта. При этом необходимо отметить, что именно благодаря изучению воздействия флавоноидов, а именно флаволигнанов плодов расторопши пятнистой [3, 7] на функцию печени, особенно гепатоцитов, появилось понятие «гепатопротекторные свойства» и, как следствие, фармакологическая группа – гепатопротекторы, причем произошло это сравнительно недавно – в 90-е годы XX столетия [3, 4, 6].
В ходе исследований выявлены также особенности влияния на выделительную функцию почек водных и водно-спиртовых извлечений. Проведено сравнительное исследование диуретической активности водно-спиртовых извлечений из листьев толокнянки обыкновенной (препараты сравнения), травы эрвы шерстистой, цветков пижмы обыкновенной, травы репешка аптечного аптечного и цветков бессмертника песчаного. Установлено, что настой и препарат «Эрвы шерстистой настойка» обладают быстрым развитием диуретического эффекта и короткой продолжительностью действия. Для препаратов «Пижмы настойка» и «Бессмертника песчаного настойка», а также соответствующих настоев характерно быстрое развитие эффекта и длительное диуретическое действие, тогда как в случае препарата «Толокнянки настойка» наблюдается длительный латентный период в сочетании с продолжительным диуретическим действием.
Результаты проведенных исследований позволили создать методологическую базу для совершенствования стандартизации ЛРС, содержащего флавоноиды, а также расширить возможности целенаправленного поиска новых сырьевых источников для получения эффективных отечественных фитопрепаратов и лекарственных субстанций с антиоксидантной, диуретической, ноотропной и анксиолитической активностью. Внедрение результатов данных исследований будет способствовать успешной реализации Стратегии лекарственного обеспечения населения Российской Федерации на период до 2025 года, одним из главных приоритетов которой является разработка новых конкурентоспособных импортозамещающих лекарственных препаратов, в том числе растительного происхождения.
Рецензенты:
Первушкин С.В., д.фарм.н., профессор, заведующий кафедрой фармацевтической технологии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара;
Дубищев А.В., д.м.н., профессор, зав. кафедрой фармакологии им. заслуженного деятеля науки РФ, профессора А.А. Лебедева, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара.
Источник
Лекарственное растительное сырье содержащие фенольные соединения флавоноиды
Лекарственные растения рассматриваются как перспективный источник биологически активных соединений (БАС), обладающих антиоксидантной активностью, однако в Государственный реестр лекарственных средств, разрешенных к применению в Российской Федерации, включен лишь антиоксидант диквертин, представляющий собой дигидрокверцетин (таксифолин) – флавоноид из древесины лиственницы сибирской [9, 13]. Если на этом фоне рассматривать значимость антиоксидантных свойств сквозь призму механизма действия некоторых витаминных препаратов (витамины А, С, Е, Р и др.), гепатопротекторов и ангиопротекторов, то актуальность исследований, направленных на поиск новых антиоксидантов, является тем более бесспорной.
В последнее время внимание исследователей привлекают фенольные соединения, среди которых наиболее активно изучаются флавоноиды [1-11, 13-15]. При этом флавоноиды, содержащиеся в лекарственных растениях, представляют интерес не только как потенциальные антиоксидантные препараты, но и как БАС, которые могут оказывать в суммарных растительных средствах, включая галеновые препараты, сопутствующий антиоксидантный эффект, способствующий успешному лечению какого-либо заболевания, причиной или следствием которого являются нарушения в системе антиоксидантной защиты организма [1, 9]. Лекарственное растительное сырье (ЛРС), содержащее флавоноиды, широко применяется в медицинской практике в качестве источника желчегонных, гепатопротекторных, антиоксидантных, ангиопротекторных, диуретических, противовоспалительных, противоязвенных, спазмолитических лекарственных средств [2, 7, 9, 14, 15]. За последние 15-20 лет число фармакопейных видов сырья, отнесенных к флавоноидам, увеличилось с 11 до 30 наименований [10]. Кроме того, флавоноиды имеют статус второй группы БАС в 35 видах лекарственных растений, включая эфиромасличное сырье (цветки пижмы обыкновенной, листья мяты перечной, трава полыни эстрагон и др.), а также виды, содержащие фенилпропаноиды, в частности, гидроксикоричные кислоты (цветки бессмертника песчаного и др.), в случае которых подходы к химической стандартизации достаточно противоречивы, а используемые методики анализа не всегда отвечают параметрам валидации [10].
Цель настоящих исследований – компьютерное прогнозирование активности антиоксидантной активности некоторых флавоноидов, широко встречаемых в лекарственных растениях.
Материал и методы исследования
В качестве объектов исследования служили фармакопейные растения, лекарственное растительное сырье, флавоноиды, выделенные из травы гречихи посевной (Fagopyrum sagittatum Gilib.) (рутин), травы зверобоя продырявленного (Hypericum perforatum L.) (бисапигенин), травы зверобоя пятнистого (Hypericum maculatum Grantz.) (гиперозид) листьев березы бородавчатой (Betula verrucosa Ehrh.) (гиперозид), древесины лиственницы сибирской (Larix sibirica L.) (дигидрокверцетин). Кверцетин, будучи агликоном рутина (3-О-рутинозид кверцетина), получен в результате кислотного гидролиза рутина при нагревании на водяной бане с последующей перекристаллизацией полученного осадка в водном этиловом спирте.
В работе использованы тонкослойная хроматография, колоночная хроматография, спектрофотомерия, 1Н-ЯМР-спектроскопия, масс-спектрометрия, различные химические превращения. 1Н-ЯМР- спектры получали на приборах «Bruker AM 300» (300 МГц), масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Воздушно-сухое растительное сырье подвергали исчерпывающему экстрагированию 70 % этиловым спиртом, полученные водно-спиртовые экстракты упаривали под вакуумом до густого остатка и далее подвергали хроматографическому разделению. Хроматографическую колонку (силикагель L 40/100) элюировали хлороформом и смесью хлороформ-этиловый спирт в различных соотношениях. Контроль за разделением флавоноидов осуществляли с помощью ТСХ-анализа на пластинках «Сорбфил ПТСХ-АФ-А-УФ» в системах хлороформ-этанол (9:1), хлороформ-метанол-вода (26:14:3), а также н-бутанол-ледяная уксусная кислота-вода (4:1:2).
Компьютерное прогнозирование антиоксидантной активности осуществляли с использованием программы PASS в виде списка активностей с двумя вероятностями Pa («быть активным») и Pi («быть неактивным») [12]. При этом только активности с Pa>Pi считаются возможными для анализируемого соединения [12].
Результаты исследования и их обсуждение
В ходе исследований с использованием программы PASS определено, что наиболее вероятное проявление антиоксидантной активности (Pa > Pi) возможно в случае флавоноловых гликозидов — рутина и гиперозида (табл. 1), что согласуется с экспериментальными данными по изучению антиоксидантной активности [3, 8]. Достаточно велика вероятность проявления антиоксидантной активности кверцетина (0.681 > 0.005) и бисапигенина (0.665 > 0.005), хотя в меньшей степени, чем в случае препарата сравнения – дигидрокверцетина (0.718 > 0.004) (табл. 1). Следует отметить, что данный прогноз коррелирует с результатами соответствующих экспериментальных исследований антиоксидантной активности [3, 8].
Прогноз антиоксидантной активности некоторых флавоноидов (Pa > Pi)
Источник