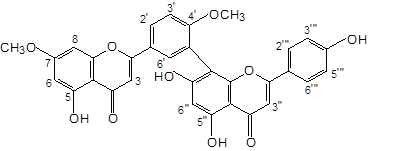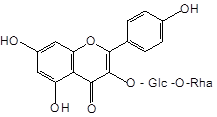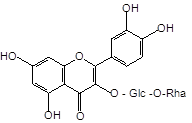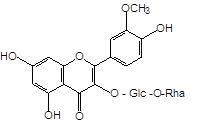- ФС.2.5.0010.15 Гинкго двулопастного листья
- ФС.2.5.0010.15 Гинкго двулопастного листья
- ПОДЛИННОСТЬ
- Внешние признаки
- Микроскопические признаки
- Определение основных групп биологически активных веществ
- Тонкослойная хроматография
- ИСПЫТАНИЯ
- Влажность
- Зола общая
- Зола, нерастворимая в хлористоводородной кислоте
- Измельченность сырья
- Посторонние примеси
- Тяжелые металлы
- Радионуклиды
- Остаточные количества пестицидов
- Микробиологическая чистота
- Количественное определение
- Лекарственное растительное сырье гинкго двулопастного листья анализируют по содержанию
ФС.2.5.0010.15 Гинкго двулопастного листья
Содержимое (Table of Contents)
ФС.2.5.0010.15 Гинкго двулопастного листья
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Гинкго двулопастного листья ФС.2.5.0010.15
Ginkgo biloba folia Вводится впервые
Cобранные в течение вегетационного периода и высушенные листья многолетнего культивируемого древесного растения гинкго двулопастного – Ginkgo biloba L., сем. гинкговых – Ginkgoaceae.
ПОДЛИННОСТЬ
Внешние признаки
Цельное сырье. Цельные или частично измельченные черешковые листья без прилистников светло-зелёного, желтовато-зеленого или желтого цвета, в очертании листовой пластинки веерообразные, на верхушке двулопастные с дихотомическим жилкованием и низбегающим основанием, кожистые, голые, слегка гофрированные по краю. Размер листьев варьирует от 4 до 10 см. Изредка встречаются части укороченных побегов. Листовая пластинка рассечена и имеет сверху глубокий V-образный вырез, рассекающий пластинку на 2 симметричные половинки. Запах характерный. Вкус водного извлечения специфический, кисловатый, слегка вяжущий с горьким послевкусием.
Измельчённое сырьё. Кусочки цельнокрайних листовых пластинок, черешков различной величины и формы, проходящих сквозь сито с отверстиями размером 7 мм. Цвет сырья зелёный, желтовато-зеленый или желтый. Запах характерный. Вкус водного извлечения специфический, кисловатый, слегка вяжущий с горьким послевкусием.
Микроскопические признаки
Цельное и измельченное сырье. При рассмотрении листа с поверхности видны клетки верхнего и нижнего эпидермиса неправильной, вытянутой формы, клетки верхнего эпидермиса с сильноизвилистым краем и чётковидно-утолщенными стенками; устьица встречаются только на нижней стороне листа и расположены группами по 2 – 4, замыкающие клетки устьиц содержат крахмал. На поперечном срезе листовой пластинки видна кутикула с обеих сторон листа. Под эпидермисом находится мезофилл. Мезофилл состоит из однотипных паренхимных клеток округлой, изодиаметрической формы с небольшими межклетниками; содержит хлоропласты, крахмальные зерна, вместилища. Клетки эпидермиса черешка листа, расположенные над жилкой прозенхимной формы, сильно вытянутые вдоль жилки, а между жилками – паренхимные. Под эпидермисом находится 2-3-слойная гиподерма, состоящая из плотно сомкнутых клеток с сильно утолщенными одревесневшими оболочками. На поперечном срезе черешка видны 2 пучка, ограниченные клетками паренхимы, а также вместилища; клетки хлоренхимы черешка округлой изодиаметрической формы. На продольном срезе черешка в основной паренхиме видны крупные друзы, а между гиподермой и ксилемой – друзы небольшого размера. Ксилема черешка представлена кольчатыми сосудами и сосудами с окаймленными порами.
ФС.2.5.0010.15 Гинкго двулопастного листья микроскопия
» data-image-caption=»» data-medium-file=»https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?fit=300%2C192&ssl=1″ data-large-file=»https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?fit=700%2C449&ssl=1″ loading=»lazy» src=»https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya-300×192.png?resize=552%2C353″ alt=»ФС.2.5.0010.15 Гинкго двулопастного листья микроскопия» width=»552″ height=»353″ srcset=»https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?resize=300%2C192&ssl=1 300w, https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?resize=768%2C492&ssl=1 768w, https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?resize=660%2C423&ssl=1 660w, https://i0.wp.com/pharmacopoeia.ru/wp-content/uploads/2016/09/FS.2.5.0010.15-Ginkgo-dvulopastnogo-listya-mikroskopiya.png?w=1101&ssl=1 1101w» sizes=»(max-width: 552px) 100vw, 552px» data-recalc-dims=»1″/>
Рисунок – Гинкго двулопастного листья.
1 – фрагмент верхнего эпидермиса (400×); 2 – фрагмент нижнего эпидермиса с устьицами аномоцитного типа (400×); 3 – фрагмент продольного среза листовой пластины с устьичным комплексом (а) (400×); 4 – фрагмент поперечного среза листовой пластины: выстилающие клетки (a), полость вместилища (б) (400×); 5 – фрагмент радиального среза черешка листа: смоляной ход (а), проводящий пучок (б) (100×)
Определение основных групп биологически активных веществ
Тонкослойная хроматография
На линию старта аналитической хроматографической пластинки со слоем силикагеля с флуоресцентным индикатором на алюминиевой подложке размером 10×15 см наносят 10 мкл испытуемого раствора (см. раздел «Количественное определение» приготовление раствора А испытуемого раствора) и рядом 10 мкл раствора стандартного образца (СО) рутина (см. раздел «Количественное определение» приготовление раствор А СО рутина). Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру, предварительно насыщенную в течение не менее 24 ч смесью растворителей хлороформ – метанол – вода (26:14:3), и хроматографируют восходящим способом. Когда фронт растворителей пройдет 80 – 90 % длины пластинки от линии старта, ее вынимают из камеры, сушат до удаления следов растворителей и просматривают в УФ-свете при длине волны 254 нм.
На хроматограмме испытуемого раствора должны обнаруживаться 2 зоны адсорбции фиолетового цвета, расположенные выше зоны на хроматограмме раствора СО рутина.
Затем пластинку обрабатывают раствором диазореактива и просматривают при дневном свете.
На хроматограмме испытуемого раствора должны обнаруживаться 2 зоны адсорбции желто-оранжевого цвета, расположенные выше зоны на хроматограмме раствора СО рутина.
ИСПЫТАНИЯ
Влажность
Цельное сырье, измельченное сырье – не более 12 %.
Зола общая
Цельное сырье, измельченное сырье – не более 10 %.
Зола, нерастворимая в хлористоводородной кислоте
Цельное сырье, измельченное сырье – не более 5 %.
Измельченность сырья
Цельное сырье: частиц, проходящих сквозь сито с отверстиями размером 2 мм, — не более 5 %. Измельченное сырье: частиц, не проходящих сквозь сито с отверстиями размером 7 мм, — не более
5 %; частиц, проходящих сквозь сито с отверстиями размером 0,5 мм, — не более 5 %.
Посторонние примеси
Части укороченных побегов. Цельное сырье – не более 2 %.
Органическая примесь. Цельное сырье, измельченное сырье – не более 0,5 %.
Минеральная примесь. Цельное сырье, измельченное сырье – не более 0,5 %.
Тяжелые металлы
Радионуклиды
В соответствии с требованиями ОФС «Определение содержания радионуклидов в лекарственном растительном сырье и лекарственных растительных препаратах».
Остаточные количества пестицидов
Микробиологическая чистота
Количественное определение
Цельное сырье, измельченное сырье: cумма флавоноидов в пересчете на рутин — не менее 0,5 %.
Раствор СО рутина. Около 0,025 г (точная навеска) предварительно высушенного до постоянной массы при температуре 100 – 105 °С СО рутина помещают в мерную колбу вместимостью 50 мл, растворяют в 30 мл спирта 70 % при нагревании на водяной бане. После охлаждения до комнатной температуры содержимое колбы доводят спиртом 70 % до метки и перемешивают (раствор А СО рутина). Срок годности раствора не более 3 мес при хранении в прохладном, защищенном от света месте.
1,0 мл раствора А СО рутина помещают в мерную колбу вместимостью 25 мл, прибавляют 1 мл алюминия хлорида спиртового раствора 2 % и 1 каплю уксусной кислоты разбавленной 30 %, доводят объем раствора спиртом 96 % до метки и перемешивают (раствор Б СО рутина). Срок годности раствора 3 мес при хранении в прохладном, защищенном от света месте.
Аналитическую пробу сырья измельчают до величины частиц, проходящих сквозь сито с отверстиями размером 2 мм.
Около 1,0 г (точная навеска) измельченного сырья помещают в колбу со шлифом вместимостью 100 мл, приливают 30 мл спирта 70 % и взвешивают с точностью до ± 0,01 г. Колбу с содержимым присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 1 ч. После охлаждения до комнатной температуры колбу взвешивают, доводят ее содержимое спиртом 70 % до первоначальной массы, перемешивают и фильтруют через бумажный фильтр «красная полоса» (раствор А испытуемого раствора).
1,0 мл раствор А испытуемого раствора помещают в мерную колбу вместимостью 25 мл, прибавляют 2 мл алюминия хлорида спиртового раствора 2 % и 1 каплю уксусной кислоты разбавленной 30 %, доводят объем раствора спиртом 96 % до метки и перемешивают (раствор Б испытуемого раствора).
Оптическую плотность раствора Б испытуемого раствора измеряют через 40 мин на спектрофотометре при длине волны 406 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют раствор, состоящий из 1 мл раствора А испытуемого раствора, 1 капли уксусной кислоты разбавленной 30 %, доведенный спиртом 96 % до метки в мерной колбе вместимостью 25 мл.
Параллельно измеряют оптическую плотность раствора Б СО рутина. В качестве раствора сравнения используют раствор, состоящий из 1 мл раствора А СО рутина, 1 капли уксусной кислоты разбавленной 30 %, доведенный спиртом 96 % до метки в мерной колбе вместимостью 25 мл.
Содержание суммы флавоноидов в пересчете на рутин в абсолютно сухом сырье в процентах (X) вычисляют по формуле:
A – оптическая плотность раствора Б испытуемого раствора;
Ao – оптическая плотность раствора Б СО рутина;
a – навеска сырья, г;
Р – содержание основного вещества в СО рутина, %;
W – влажность сырья, %.
Допускается содержания суммы флавоноидов в пересчете на рутин вычислять с использованием удельного показателя поглощения комплекса рутина с алюминия хлоридом по формуле:
А — оптическая плотность раствора Б испытуемого раствора;

а – навеска сырья, г;
W – влажность сырья, %.
Источник
Лекарственное растительное сырье гинкго двулопастного листья анализируют по содержанию
Гинкго двулопастный Ginkgo biloba L. — единственный реликтовый вид класса Гинкговых (сем. Ginkgoaceae), который сохранился до нашего времени с пермского периода палеозойской эры [1, 6, 11]. Гинкго двулопастный произрастает в странах с субтропическим климатом, однако возможности к адаптации этого растения очень высоки, о чем свидетельствует его успешное культивирование в Российской Федерации, в частности, в Краснодарском, Ставропольском краях, в Московской обл. [3, 4]. Листья гинкго двулопастного (Ginkgo biloba L.) входят в Европейскую и Американскую фармакопеи, а также включены в Государственный реестр лекарственных средств РФ [1, 3, 6]. На основе субстанций из листьев гинкго двулопастного в Российской Федерации применяются такие препараты, как танакан, билобил, мемоплант, гинкор форт, гинкор гель, однако они производятся за рубежом и являются дорогостоящими. Это обусловливает актуальность исследований в плане обоснования целесообразности создания импортозамещающих ноотропных препаратов на основе листьев гинкго двулопастного. Для успешного решения данной проблемы необходимой является разработка методов стандартизации, позволяющих объективно оценивать качество сырья и лекарственных препаратов данного растения.
На данный момент в Российской Федерации отсутствуют какие-либо виды нормативной документации на сырье «Гинкго двулопастного листья», причем до сих пор не решены в полной мере вопросы стандартизации сырья и препаратов гинкго, хотя определенный опыт в этом отношении имеется [3]. На основе результатов изучения компонентного состава флавоноидов листьев гинкго двулопастного ранее была разработана методика количественного определения суммы флавоноидов с использованием дифференциальной спектрофотометрии и Государственного стандартного образца рутина [2]. В плане дальнейшего совершенствования методов стандартизации листьев гинкго двулопастного особый интерес представляют такие методы, как тонкослойная хроматография (ТСХ) и высокоэффективная жидкостная хроматография (ВЭЖХ) [3, 12].
Цель исследования – научное обоснование новых подходов к стандартизации листьев гинкго двулопастного с использованием метода ВЭЖХ.
Материал и методы исследования
В качестве объектов исследования образцы листьев гинкго двулопастного, культивируемого в различных регионах Российской Федерации: Московская обл. (Ботанический сад Института физиологии растений РАН, г. Москва), Краснодарский край (Ботанический сад г. Краснодара), Ставропольский край (окр. г. Пятигорска).
В работе использованы тонкослойная хроматография, высокоэффективная жидкостная хроматография и спектрофотомерия. Регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Воздушно-сухое растительное сырье подвергали исчерпывающему экстрагированию 70 % этиловым спиртом в соотношении «сырье – экстрагент» — 1:30. Анализ полученных водно-спиртовых извлечений осуществляли с помощью ТСХ на пластинках «Сорбфил ПТСХ-АФ-А-УФ» в системе хлороформ-этанол-вода (26:16:3). В качестве стандартных веществ использовали гинкгетин (7,41-диметиламентофлавон) (1), никотифлорин (3-О-рутинозид кемпферола) (2), рутин (3-О-рутинозид кверцетина) (3) и нарциссин (3-О-рутинозид изорамнетина (4) (рис. 1).
Рис. 1. Химические структуры важнейших флавоноидов листьев гинкго двулопастного.
Исследование водно-спиртовых извлечений из листьев гинкго двулопастного с помощью ВЭЖХ осуществляли с использованием хроматографа «Стайер» (ООО «НПО Аквилон», г. Подольск) и колонки размером 4,6 х 250 мм (стационарная фаза — октадецил силан С-18), объем вводимой пробы – 25 мкл. В качестве подвижной фазы использовали смеси «ацетонитрил-вода» в соотношении (70:30). Скорость подачи элюента составила 2 мл/мин. Детектирование веществ осуществляли УФ-детектором при длине волны 270 нм. Скорость подачи элюента составила 2 мл/мин. Детектирование веществ осуществляли УФ-детектором при длине волны 270 нм. Качественный анализ проводили посредством регистрации времен удерживания веществ и сравнения спектральных отношений, причем как в условиях метода внутреннего стандарта, так и путем введения растворов индивидуальных веществ в хроматографическую колонку.
Результаты исследования и их обсуждение
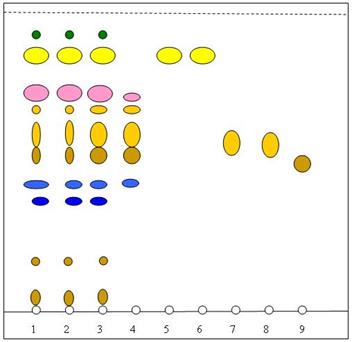
Результаты сравнительного исследования методом ТСХ свидетельствуют о том, что на хроматограммах водно-спиртовых извлечений различных образцов являются гинкгетин (1) и никотифлорин (2) (рис. 2). После проявления хроматограммы щелочным раствором диазобензолсульфокислоты гинкгетин и изогинкгетин обнаруживаются в виде доминирующего пятна желто-оранжевого цвета с величиной Rf около 0,8, а никотифлорин — в виде желтого пятна с величиной Rf около 0,6. Следует отметить, что на уровне гинкгетина обнаруживается изогинкгетин, что соответствует данным зарубежных ученых, в работах которых близкие по химической структуре флавоноиды обнаруживаются в виде одного пятна [10]. Сопоставимую хроматографическую подвижность имеют также никотифлорин и нарциссин, которые в водно-спиртовых извлечениях и в лекарственном препарате «Танакан» обнаруживаются в виде одного пятна желтой окраски с величиной Rf около 0,6.
На наш взгляд, заслуживает внимания тот факт, что во всех исследуемых образцах листьев одним из доминирующих компонентов является соединение фенольной природы с величиной Rf около 0,7, тогда как в лекарственном препарате «Танакан» оно содержится в незначительных количествах. Что касается одного из доминирующих флавоноидов листьев — гинкгетина, то это вещество в танакане не обнаруживается.
Рис. 2. Схема тонкослойной хроматограммы веществ и водно-спиртового извлечения из листьев гинкго двулопастного.
Обозначения: 1 – водно-спиртовое извлечение из сырья (Ботанический сад г. Краснодара); 2 – водно-спиртовое извлечение из сырья (Ботанический сад Института физиологии растений РАН, г. Москва); 3 – водно-спиртовое извлечение из сырья (окр. г. Пятигорска); 4 – раствор препарата «Танакан»; 5 – гинкгетин; 6 – изогинкгетин; 7 – никотифлорин; 8 – нарциссин; 9 – рутин.
Изогингетин обнаружен нами в качестве примеси в образце гинкгетина, что соответствует данным зарубежных ученых, которые получили эти соединения в виде смеси [9]. Примечательно, что и в другой зарубежной работе гинкгетин (7,41-диметиламентофлавон) и изогинкгетин (41,4111-диметиламентофлавон), будучи близкими по химической структуре, обнаруживаются в виде одного пятна [6]. На наш взгляд, определение гинкгетина как одного из доминирующих и характерных флавоноидов листьев гинкго двулопастного имеет принципиальное значение. Во-первых, для гинкгетина выявлена ноотропная активность, свойственная препаратам гинкго [4, 7, 10], а во-вторых, имеются примеры, когда стандартизацию сырья данного растения осуществляют без учета наличия гинкгетина: методом ВЭЖХ обнаруживаются лишь продукты кислотного гидролизата – кемпферол, кверцетин и изорамнетин [5], что, на наш взгляд, является ошибочным подходом. Что касается рутина, описанного в литературе для данного растения, то он относится к минорным компонентам и едва обнаруживается на хроматограммах (ТСХ). Интересно, по данным зарубежных ученых, в исследуемых образцах листьев гинкго двулопастного рутин относительно четко обнаруживается методом ТСХ лишь в сырье из Италии [8].
Учитывая то обстоятельство, что гинкгетин (1), как один из доминирующих флавоноидов, имеет диагностическое значение, на наш взгляд, ТСХ-анализ может быть использован для целей идентификации сырья и препаратов данного растения.
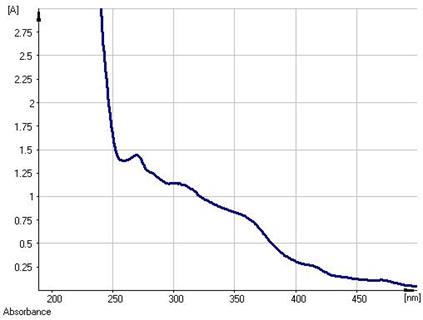
Результаты сравнительного исследования электронных спектров водно-спиртовых извлечений образцов листьев гинкго двулопастного, культивируемого в различных регионах России, свидетельствуют о том, что для всех образцов сырья характерен основной максимум поглощения в области 270 нм + 1 нм (рис. 3).
Гинкгетин (1), имея максимумы поглощения при 270 и 330 нм, в значительной мере определяет спектральные характеристики водно-спиртового извлечения из листьев гинкго двулопастного (рис. 3), может быть также использовано для целей идентификации сырья данного растения.
Рис. 3. Электронный спектр водно-спиртового извлечения из листьев гинкго двулопастного.
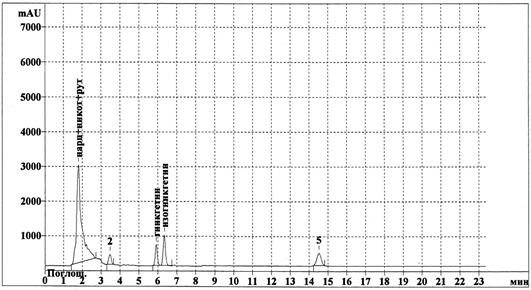
В последнее время для целей стандартизации активно внедряется метод ВЭЖХ, позволяющий одновременно осуществлять качественный и количественный анализ ЛРС. На наш взгляд, в условиях ВЭЖХ в качестве маркера может выступать доминирующий флавоноид гинкгетин (1). Результаты ВЭЖХ-анализа свидетельствуют о том, что в исследуемых условиях хроматографирования гинкгетин (1) с величиной времени удерживания около 12,5 мин хорошо отделяется от других компонентов листьев гинкго двулопастного (рис. 4), что позволяет данный метод рекомендовать как для целей идентификации листьев гинкго двулопастного, так и для целей стандартизации препаратов на основе сырья данного растения.
Рис. 4. ВЭЖХ-хроматограмма водно-спиртового извлечения из листьев гинкго двулопастного.
Учитывая специфичность гинкгетина для листьев гинкго двулопастного, считаем целесообразным использование метода ВЭЖХ для определения подлинности сырья и препаратов данного растения по обнаружению данного флавоноида, имеющего диагностическое значение. Метод ВЭЖХ имеет принципиальное значение с точки зрения создания импортозамещающих ноотропных препаратов, которые в отличие зарубежных аналогов содержат гинкгетин, обладающий ноотропной активностью и характеризующий их происхождение в силу специфичности.
1. Разработаны новые подходы к стандартизации подхода к стандартизации листьев гинкго двулопастного, заключающиеся в комплексном использовании спектрофотометрии, ТСХ и ВЭЖХ.
2. С учетом специфичности гинкгетина для листьев гинкго двулопастного, является целесообразным использование методов ВЭЖХ и ТСХ для определения подлинности сырья и препаратов данного растения по обнаружению данного флавоноида, имеющего диагностическое значение.
Рецензенты:
Шаталаев Иван Федорович, доктор биологических наук, профессор, заведующий кафедрой химии фармацевтического факультета государственного бюджетного образовательного учреждения высшего профессионального образования «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г.Самара.
Правдивцева Ольга Евгеньевна, доктор фармацевтических наук, доцент кафедры фармакогнозии с ботаникой и основами фитотерапии государственного бюджетного образовательного учреждения высшего профессионального образования «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г.Самара.
Источник