- Стафилококк: чего ждать и что делать?
- Стафилококк: как выявить и вылечить
- Что такое стафилококк
- Виды патогенных стафилококков
- Как проявляется стафилококковая инфекция
- Как лечить стафилококк
- Антибиотики прямо под нашим носом
- Антибиотики прямо под нашим носом
- Семейные разборки
- Золотистый стафилококк
- Секретное оружие
- Нерибосомные пептиды
- Строение
- Синтез
- Испытания в боевых условиях
- Перспективы
Стафилококк: чего ждать и что делать?
Стафилококки широко распространены в природе.
В воде, почве, на коже и слизистых людей и животных. Но патогенными, т.е. потенциально опасными могут быть золотистые стафилококки (Staphilococcus aureus) и в меньшей степени эпидермальные стафилококки (Staphilococcus epidermidis). Эти микробы относятся к условно-патогенным микроорганизмам, т. е. вызывать заболевание они могут только при определенных условиях, а в основном спокойно проживают на слизистых и коже человека, не причиняя вреда.
У человека золотистые стафилококки живут в кишечнике, преддверии носа, в промежности, подмышечных впадинах, в области пупка. В преддверии носа они обнаруживаются у 40-50% здоровых взрослых, в кишечнике у 60-70% здоровых людей.
Эпидермальные стафилококки считаются непатогенными, но у больных с иммунодефицитом, протезированными клапанами сердца, сосудистыми катетерами они могут вызывать внутрибольничную инфекцию.
Возбудитель может передаваться от больного или носителя воздушно-капельным, контактным путем, а также фекально-оральным.
Перечень заболеваний, вызываемых стафилококками очень велик.
Это инфекции кожи и подкожной клетчатки (ячмени, фурункулы, карбункулы, абсцессы кожи, иметиго, флегмоны).
Стафилококки причастны к разнообразным инфекциям ЛОР-органов (синуситы, ангины, аденоидиты, отиты), также вызывают бронхиты, пневмонии.
Опасно, если заражение происходит в стационаре, т. к. внутрибольничные стафилококки обладают устойчивостью ко многим антибиотикам и лечить такую инфекцию становится очень проблематично.
Иногда, особенно у маленьких детей, возникают стафилококковые кишечные инфекции, энтероколиты. У взрослых людей чаще случаются пищевые токсикоинфекции, когда заболевание вызывается не самим стафилококком, а его токсинами, скопившимися в недоброкачественном продукте, который был инфицирован стафилококками.
Если в роддоме или родильном отделении появляется вирулентный (очень заразный) штамм стафилококка, то инфекция может быстро распространяться. Чаще инфекция у новорожденных протекает легко, проявляется в основном пустулами вокруг ногтевых валиков, изредка поражаются более глубокие ткани.
У новорожденных некоторые штаммы стафилококка могут вызвать тяжелую инфекцию кожи — синдром ошпаренной кожи (болезнь Риттера). У женщин при кормлении больного ребенка может развиться стафилококковый гнойный мастит.
Стафилококк причастен и к такому тяжелому заболеванию, как остеомиелит (воспаление костей и костного мозга). Стафилококки чаще попадают в кость из очагов в коже или носоглотке, но иногда входные ворота инфекции остаются не выявленными.
Если стафилококки проникают через, так называемый, гематоэнцефалический барьер, то развивается грозное заболевание — менингоэнцефалит.
Также, при выраженном иммунодефиците может развиться стафилококковый сепсис. При этом стафилококк проникает в кровоток из любого очага инфекции на коже или подкожной клетчатки.
Все же, вышеперечисленные тяжелые заболевания возникают редко, т. к. в большинстве случаев защитные барьеры срабатывают, и инфекция или ограничивается локальными формами и легко лечится, или вообще не развивается. Но может оставаться в виде носительства, что не мешает человеку чувствовать себя абсолютно здоровым.
Если в анализах выявляется стафилококк, это не значит, что его надо лечить.
Лечить мы должны только заболевание, а не анализы. И если жалоб у человека нет, то и волноваться понапрасну не надо.
Работники некоторых профессий, предприятий и организаций (пищевой промышленности, роддомов, хирургических отделений и др.) подлежат периодическому осмотру и обследованию на стафилококки. И вот у них, в случае выявления возбудителей, проводится профилактическая санация возможных очагов инфекции, чтобы их носительство стафилококка не стало фактором риска для окружающих.
Источник
Стафилококк: как выявить и вылечить
Это особая категория бактериальных культур, многие виды которой опасны для человеческого здоровья. Стафилококки принято называть условно-патогенными микробами. Обитая в организме постоянно, они находятся под контролем иммунитета. Но при ослаблении защиты могут спровоцировать воспалительный процесс. Некоторые бактерии чрезвычайно устойчивы к антимикробным средствам и нередко становятся причиной суперинфекций.
Что такое стафилококк
Это неподвижный грамположительный микроорганизм шаровидной формы, образующий многочисленные колонии. Стафилококки анаэробны — могут существовать и размножаться без участия кислорода, в закрытой среде. Штаммов бактерий насчитывается более двадцати. Некоторые из них довольно безобидны, а другие вызывают мощные патологические реакции в человеческом организме. Части тела и органы, наиболее уязвимые перед стафилококками:
Поражая их, микробы вырабатывают токсичные вещества, провоцируют воспаления, в тяжелых случаях приводящие к сепсису, необратимым изменениям структур или стойким нарушениям функций.
Виды патогенных стафилококков
Для человека опасны несколько разновидностей бактерий. Самые распространенные:
Staphylococcus aureus: золотистый. Название получил из-за характерного желтого пигмента на поверхности. Проникая в организм, синтезирует фермент коагулазу, может вызывать гнойные воспаления почти любых внутренних органов. Этот вид патогена быстро приспосабливается к воздействию антибиотиков, образуя резистентные формы.
Staphylococcus epidermidis: эпидермальный. Поражает обычно кожные покровы слизистые оболочки. Часто становится фактором воспаления повреждений, послеоперационных швов, развития гнойного конъюнктивита, инфекций дыхательных путей.
Staphylococcus saprophyticus: сапрофитный. Его специфика: поражать слизистые мочевыводящих органов, провоцировать цистит, уретрит, почечные воспаления.
Staphylococcus haemolyticus: гемолитический. Опасен для слизистых и тканей внутренних органов. Становится провокатором развития эндокардита, пневмоний, нефритов и других тяж елых патологий.
Практически все типы патогенных стафилококков склонны к мутациям в результате неправильного или недостаточно продолжительного лечения.
Как проявляется стафилококковая инфекция
Симптоматика, ее длительность и интенсивность зависят от штамма возбудителя, общего физического состояния больного и особенностей его иммунитета. Два характерных признака поражения стафилококком: воспаления различной локализации и интоксикация.
При пиодермии воспаляются потовые, сальные железы, волосяные фолликулы, из-за чего на коже образуются болезненные выпуклые узелки, наполняемые гноем. Фурункулы и карбункулы обычно окружены участками покрасневшей отекшей кожи. При интенсивном воспалении вероятно появление лихорадки, набухание близко расположенных к очагам воспаления лимфоузлов.
Поражение пазух носа стафилококком проявляется банальным насморком с вязкими желтоватыми или зел еными выделениями. Проникновение инфекции глубже вызывает развитие синуситов. Их симптомы характерны:
заложенность в области переносицы;
ощущение тяжести, распирания с пораженной стороны;
густые гнойные выделения из носа;
повышение температуры тела выше +37°С.
Нередко инфекция распространяется на среднее ухо, вызывая отит: резкие стреляющие боли, снижение слуха. При поражении слизистых глаз развивается нагноение конъюнктивы, склеры краснеют и отекают.
При атаке стафилококком верхних дыхательных путей неизбежны гнойные фарингиты или ларингиты. Их признаки:
сильная отечность, покраснение глотки;
затрудненное болезненное глотание;
сухой навязчивый кашель, дискомфорт в горле.
Часто стафилококковые фарингиты поражают детей младше 12 лет. У взрослых эта патология контролируется иммунитетом.
При развитии воспалений в нижних отделах дыхательных путей «актуальны» бронхит и пневмония с характерным лающим или мокрым кашлем, высокой температурой температурой и физической слабостью.
Менее распространенные признаки поражений стафилококком:
воспаления суставных тканей, мышц;
нарушения работы сердца.
Среди грозных осложнений, вызываемых стафилококком: менингит, абсцессы л егких, остеомиелит, синдром токсического шока, генерализованный сепсис.
Как лечить стафилококк
Точный диагноз — виновен ли микроб в патологии, можно установить только после лабораторного анализа. Обнаружить и идентифицировать его в пробах мочи, мазках и соскобах с кожных покровов и слизистых не составляет труда. А вот избавиться от заразы намного тяжелее. Печально известный стафилококк аурум (золотистый) чрезвычайно устойчив к воздействию дезинфекторов, в том числе к хлорке и «зеленке». Почти 15%всех случаев заражения им происходят внутри больниц.
Применение антибиотиков тоже не всегда оправдано. К пенициллинам, например, стафилококки приспосабливаются очень быстро. А золотистый давно к ним устойчив, как ко многим другим медикаментам. Для быстрого подавления активности патогенов применяют комбинации различных групп препаратов. Относительно новые и эффективные: макролиды и фторхинолоны. Лекарства этих категорий разрушают и уничтожают белковые оболочки бактерий, не давая им времени для развития резистентности.
Чтобы терапия оказалась действенной, важно применять антимикробным средства только по назначению врача, четко следовать указанной схеме. Запрещено прерывать курс по своему разумению, менять без разрешения один препарат на другой, корректировать дозировку.
В качестве профилактики заражения необходимо соблюдать общие правила гигиены. Важно избегать употребления непроверенных продуктов, вовремя санировать полость рта, лечить насморк. Полезно закаляться, принимать иммуномодуляторы. А главное — не применять антимикробные средства без веских причин.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Источник
Антибиотики прямо под нашим носом
16 августа 2016
Антибиотики прямо под нашим носом
Структурная формула нового пептидного антибиотика.
Автор
Редакторы
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром — мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее — в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Доступные населению антибиотики теряют эффективность, а их частое и необоснованное применение приводит к отбору устойчивых форм бактерий внутри организмов людей и животных. MDRO в человеческом микробиоме трудно выявить, ведь обычно их носительство бессимптомно. Однако в стрессовых условиях (после хирургических операций, при травмах или иммуносупрессии) оно может перерасти в агрессивную инфекцию, побороть которую будет крайне сложно. А если еще учесть и частую устойчивость подобных бактерий к классическим дезинфектантам, становится понятным, почему MDRO считают настоящим бичом стационаров и роддомов. Они — куда более осязаемая угроза для населения всех континентов, чем тот же вирус Эбола, поэтому огромные усилия сейчас направляются на поиск и производство новых антибиотиков, способных «взломать» защитные системы MDRO.
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик — лактоциллин [3].
Может показаться странным, что человеческая микробиота производит антибиотики, ведь индустрия поиска противомикробных веществ всегда была сосредоточена на почвенных бактериях: считалось, что именно там бурлит жизнь и активно идет борьба за существование. Однако в микробиоме человека насчитывается более тысячи видов бактерий, конкурирующих за место и питательные вещества. Это способствует появлению настоящего «оружия массового поражения» — бактериоцинов, производимых с помощью ферментов двух типов — поликетидсинтаз и нерибосомных пептидсинтетаз [5].
Семейные разборки
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
Золотистый стафилококк
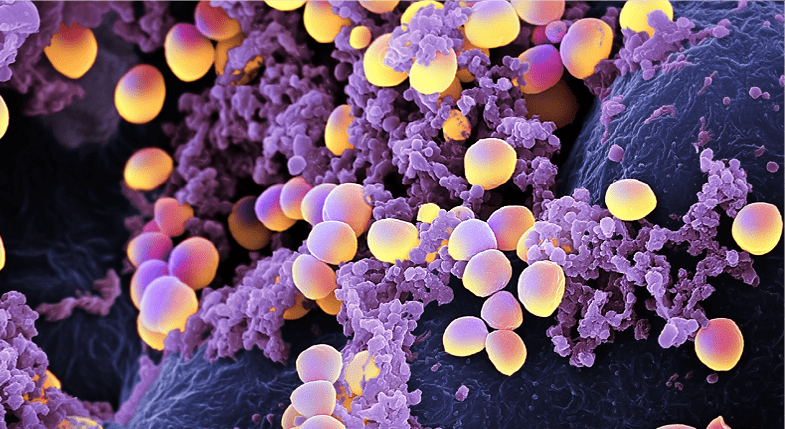
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus — шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6], [7].
Рисунок 1. Staphylococcus aureus и лейкоциты.
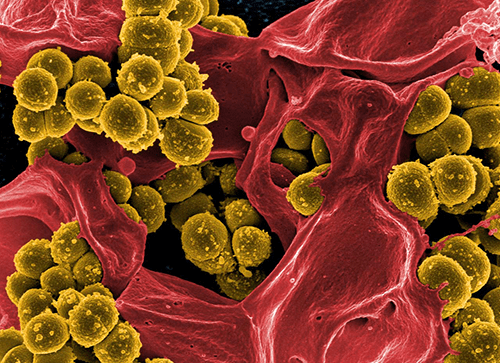
Рисунок 2. Метициллин-резистентные золотистые стафилококки.
Staphylococcus aureus — бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5], [7], [8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S. aureus — это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7], [9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S. aureus, MRSA) (рис. 2). Метициллин — это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам. В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6], [9], [10].
Основные источники заражения золотистым стафилококком — больные со стертой формой инфекции и бессимптомные носители. Наибольшая опасность исходит от медицинского персонала: по некоторым данным, носительство среди медиков может достигать 35% и, в сравнении с основной популяцией, они гораздо чаще «населены» антибиотикорезистентными штаммами. S. aureus может передаваться через руки медперсонала и нестерильные медицинские инструменты, при использовании внутривенных катетеров и проведении искусственной вентиляции легких. После госпитализации носителями золотистых стафилококков становятся 20–30% пациентов, принимавших антибиотики, больных сахарным диабетом или проходивших гемодиализ [7], [10]. В том числе поэтому грамотные врачи призывают обдуманно подходить к госпитализации — прибегать к ней только в случае реальной необходимости и выписываться как можно скорее. Помимо стафилококка и других потенциально мультирезистентных бактерий, среди пациентов, посетителей и персонала там молниеносно распространяются очень неприятные вирусы — рото- и норо-, — только вот предупреждать о внутрибольничных вспышках «туалетных» инфекций редко где считают нужным. Поэтому «пойти полежать для профилактики, прокáпаться» может обернуться немного неожиданной стороной.
Штамм S. lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма — чтобы выявить ген, ответственный за синтез смертельного для S. aureus вещества.
Рисунок 3. Антибактериальная активность S. lugdunensis против метициллин-резистентного S. aureus. Слева — дикий штамм IVK28 образует зону лизиса на культуре S. aureus. В центре — штамм IVK28ΔlugD (с «выключенным» встраиванием транспозона геном lugD) не оказывает влияния на золотистого стафилококка. Справа — штамм с восстановленной активностью гена lugD снова лизирует клетки конкурента.
В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S. lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S. lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий — путем горизонтального переноса .
Разношерстные участники и пикантные подробности бактериального горизонтального генетического переноса описаны в статье «Мобильные генетические элементы прокариот: стратификация „общества“ бродяжек и домоседов» [11].
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S. lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Секретное оружие
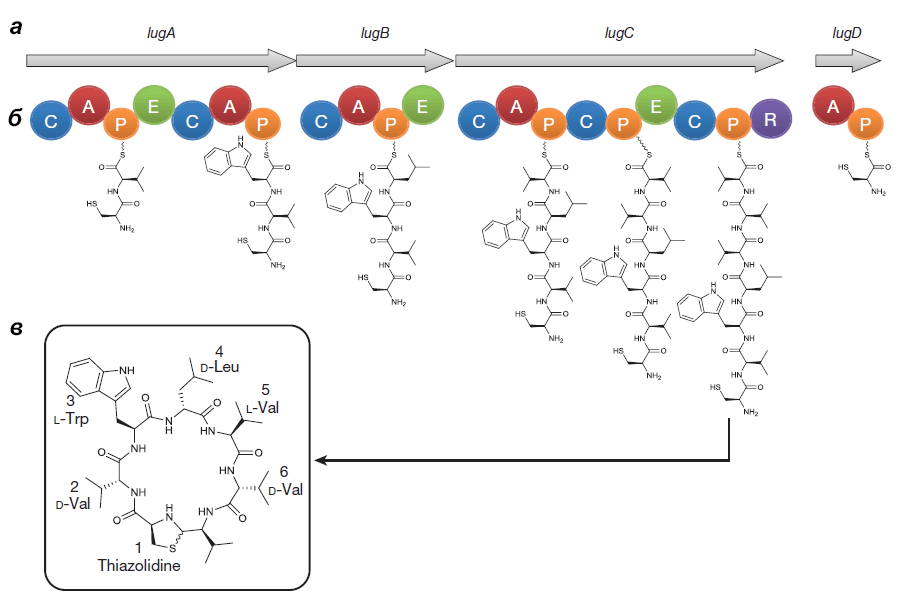
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.
Рисунок 4. Кластер генов, биосинтетический путь и химическая структура лугдунина. а — Гены «субъединиц» (не модулей!) нерибосомной пептидсинтетазы S. lugdunensis: lugA, B, C и D. б — Функциональные домены продуктов оперона: А — аденилирующий, Р — пептидильный, С — конденсирующий, Е — эпимеризующий, R — редуктазный. Их специфические комбинации составляют модули — обособленные каталитические единицы фермента. Биосинтез лугдунина начинается, видимо, в инициирующем модуле LugD и продолжается последовательно с помощью LugA-C. в — Структурная формула лугдунина.
Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров — белков, ДНК и пептидогликанов [5].
Нерибосомные пептиды
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид — предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Строение
Нерибосомные пептиды имеют длину от 2 до 50 аминокислот и часто циклическую или разветвленную структуру. Они содержат как «обычные», протеиногенные, так и непротеиногенные аминокислоты — D-формы или остатки, модифицированные присоединением N-метильных и N-формильных групп, гликозилированием, гидроксилированием, ацилированием или галогенированием. Циклизация происходит путем образования в пептидном остове оксазолинов и тиазолинов [12].
Синтез
НРП синтезируются нерибосомными пептидсинтетазами (НРПС), которые в своей работе не следуют «чужим» инструкциям, то есть обходятся без мРНК. НРПС — это гигантские мультимодульные ферменты, каждый из которых может синтезировать только один вид пептидов. Отдельный модуль фермента отвечает за включение одной аминокислоты в пептидную цепь, поэтому количество модулей соответствует длине пептида [14].
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина — 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S. aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) |
|---|---|---|
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 |
| + 50% человеческой сыворотки крови | 1,5 | |
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 |
| Staphylococcus aureus Mu50 | GISA | 3 |
| Staphylococcus aureus SA113 | 3 | |
| Staphylococcus aureus RN4220 | 3 | |
| Enterococcus faecium BK463 | VRE | 3 |
| Enterococcus faecalis VRE366 | VRE | 12 |
| Listeria monocytogenes ATCC19118 | 6 | |
| Streptococcus pneumoniae ATCC49619 | 1,5 | |
| Bacillus subtilis 168 (trpC2) | 4 | |
| Pseudomonas aeruginosa PAO1 | >50 | |
| Escherichia coli DH5α | >50 | |
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | ||
Испытания в боевых условиях
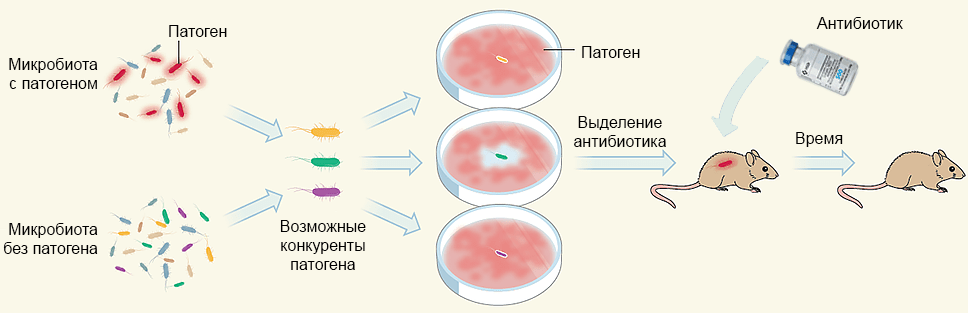
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S. aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.
Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях.
[5], рисунок модифицирован и адаптирован
Чтобы понять, может ли S. lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S. aureus + S. lugdunensis IVK28 и S. aureus + S. lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S. aureus + S. lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S. aureus + S. lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S. lugdunensis в носу человека колонизацию бактериями S. aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) — S. lugdunensis. И только у одного пациента с S. lugdunensis в носу обитал S. aureus. У всех выделенных штаммов S. lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S. aureus оказались восприимчивы к лугдунину.
Перспективы
Из-за высокой эффективности лугдунина авторы обсуждаемой работы предлагают использовать S. lugdunensis в борьбе с золотистым стафилококком, особенно у пациентов с высокими рисками развития инфекции — после операций, иммуносупрессии или гемодиализа. Ранее пробиотическими, как правило, называли бактерий, активно действующих на благо макроорганизма в желудочно-кишечном тракте. Группа Ципперера выступает за расширение понятия «пробиотики» — включение туда бактерий, борющихся с инфекциями и в других местах человеческого тела, таких как носовая полость или кожа.
В очень редких случаях и сам S. lugdunensis может вызывать заболевания, но если удастся создать мутантов, полностью утративших факторы вирулентности, или встроить lug-оперон в абсолютно «мирные» бактерии, можно разработать безопасный пробиотический препарат.
Лугдунин оказался первым обнаруженным бактериоцином нового класса — макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S. aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.
Источник