Виды вакцин
Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
- Живые вакцины. Защищают от полиомиелита, кори, краснухи, гриппа, эпидемического паротита, ветряной оспы, туберкулеза, ротавирусной инфекции. Основу препарата составляют ослабленные микроорганизмы — возбудители болезней. Их сил недостаточно для развития значительного недомогания у пациента, но хватает, чтобы выработать адекватный иммунный ответ.
- Инактивированные вакцины. Прививки против гриппа, брюшного тифа, клещевого энцефалита, бешенства, гепатита А, менингококковой инфекции и др. В составе мертвые (убитые) бактерии или их фрагменты.
- Анатоксины (токсоиды). Особым образом обработанные токсины бактерий. На их основе делают прививочный материал от коклюша, столбняка, дифтерии.
В последние годы появился еще один вид вакцин — молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
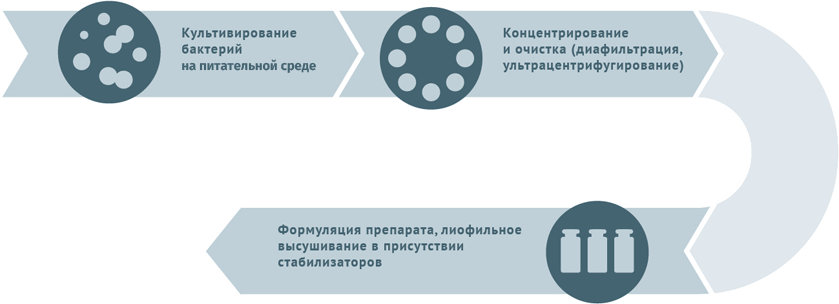
Живые бактериальные
Схема подходит для вакцины БЦЖ, БЦЖ-М.
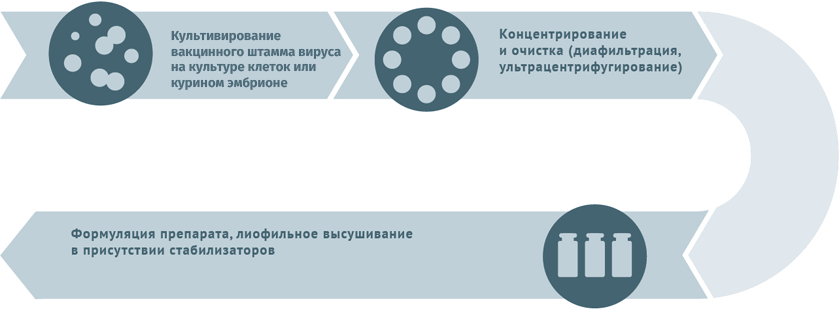
Живые противовирусные
Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
- куриные эмбрионы;
- перепелиные эмбриональные фибробласты;
- первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков);
- перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293).
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
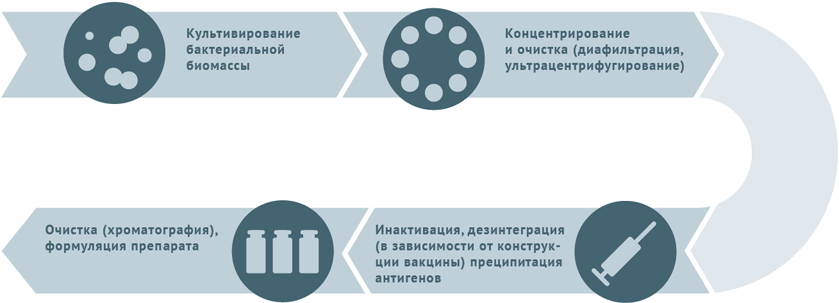
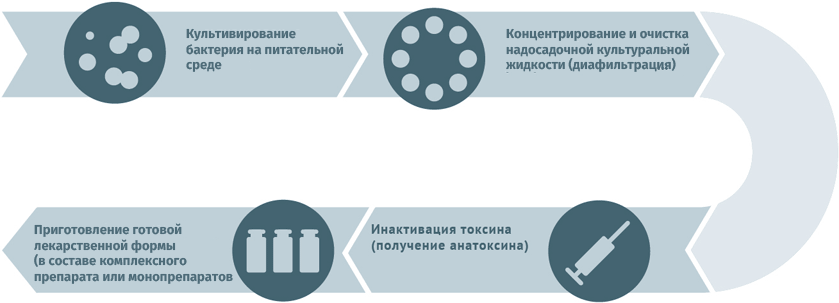
Инактивированные антибактериальные вакцины
- Культивация и очистка штаммов бактерий.
- Инактивация биомассы.
- Для расщепленных вакцин клетки микробов дезинтегрируют и осаждают антигены с последующим их хроматографическим выделением.
- Для конъюгированных вакцин полученные при предыдущей обработке антигены (как правило, полисахаридные) сближают с белком-носителем (конъюгация).
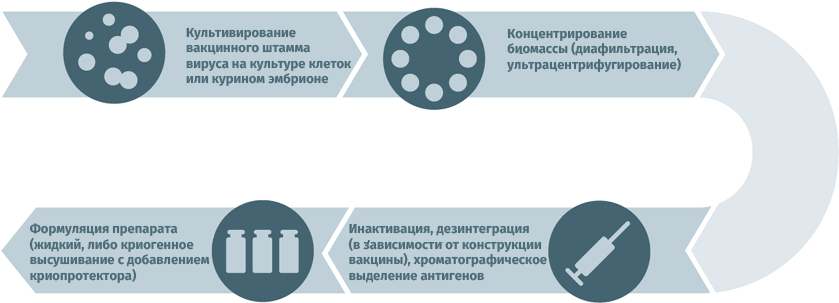
Инактивированные противовирусные вакцины
- Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться куриные эмбрионы, перепелиные эмбриональные фибробласты, первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков), перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293). Первичная очистка для удаления клеточного дебриса проводится методами ультрацентрифугирования и диафильтрации.
- Для инактивации используются ультрафиолет, формалин, бета-пропиолактон.
- В случае приготовления расщепленных или субъединичных вакцин полупродукт подвергают действию детергента с целью разрушить вирусные частицы, а затем выделяют специфические антигены тонкой хроматографией.
- Человеческий сывороточный альбумин применяется для стабилизации полученного вещества.
- Криопротекторы (в лиофилизатах): сахароза, поливинилпирролидон, желатин.
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
Анатоксины
Для дезактивации вредного воздействия токсинов используют методы:
- химический (обработка спиртом, ацетоном или формальдегидом);
- физический (подогрев).
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
По материалам: «Наука и жизнь» № 3, 2006, «Вакцины: от Дженнера и Пастера до наших дней», академик РАМН В. В. Зверев, директор НИИ вакцин и сывороток им. И. И. Мечникова РАМН.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Я много лет вакцинируюсь от гриппа вакциной французского производителя. В этом году терапевт предложила мне сделать прививку российской вакциной. Я ничего не знаю об отечественных вакцинах, какая из них качественная?
Отвечает Полибин Роман Владимирович
Российские препараты, которыми проводится вакцинацию в рамках ОМС, эффективны и безопасны. Для массовой иммунизации населения Минздравом используются вакцины Совигрипп (НПО «Микроген»), Ультрикс (ООО ФОРТ), УльтриксКвадри (ООО «ФОРТ» иФлю-М (СПбНИИВС ФМБА России). Препараты доказали высокий профиль безопасности и эффективности в ходе полного объема обязательных доклинических и клинических исследований, проведенных в соответствии с требованиями, предъявляемыми регуляторными органами РФ и Европы, а также длительного опыта успешного применения в России и динамики снижения заболеваемости. Подробнее о вакцинах можно узнать на официальных сайтах разработчиков.
Вакцина «Менюгейт» зарегистрирована в России? С какого возраста разрешена к применению?
Отвечает Харит Сусанна Михайловна
Да, зарегистрирована, вакцина – от менингококка С, сейчас также есть вакцина конъюгированная, но уже против 4 типов менингококков – А, С, Y, W135 – Менактра. Прививки проводят с 9 мес.жизни.
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Вы абсолютно правы, если в контейнере был лед. Но если там была смесь воды и льда- вакцина не должна замерзать. Однако живые вакцины, к которым относится ротавирусная, не увеличивают реактогенность при температуре менее 0, в отличие от неживых, а, например, для живой полиомиелитной допускается замораживание до -20 град С.
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму. В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска.
Отвечает Полибин Роман Владимирович
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Реакция Манту. По Приказу № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерациии» и Санитарным правилам СП 3.1.2.3114-13 «Профилактика туберкулеза», несмотря на наличие новых тестов, детям необходимо ежегодно делать реакцию Манту, но так как этот тест может давать ложноположительные результаты, то при подозрении на тубинфицирование и активную туберкулезную инфекцию проводят Диаскин-тест. Диаскин-тест является высоко чувствительным (эффективным) для выявления активной туберкулезной инфекции (когда идет размножение микобактерий). Однако полностью перейти на Диаскин-тест и не делать реакцию Манту фтизиатры не рекомендуют, так как, он не «улавливает» раннее инфицирование, а это важно, особенно для детей, поскольку профилактика развития локальных форм туберкулеза эффективна именно в раннем периоде инфицирования. Кроме того, инфицирование микобактерией туберкулеза необходимо определять для решения вопроса о ревакцинации БЦЖ. К сожалению, нет ни одного теста, который бы со 100% точностью ответил на вопрос, есть инфицирование микобактерией или заболевание. Квантифероновый тест также выявляет только активные формы туберкулеза. Поэтому при подозрении на инфицирование или заболевание (положительная реакция Манту, контакт с больным, наличие жалоб и пр.) используются комплексные методы (диаскин-тест, квантифероновый тест, рентгенография и др.).
Что касается «иммунитета и как он работает», в настоящее время иммунология — это высокоразвитая наука и многое, в частности, что касается процессов на фоне вакцинации – открыто и хорошо изучено.
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
Источник
Научная электронная библиотека
Перетрухина А. Т., Блинова Е. И.,
Глава 4. ВАКЦИНЫ
Среди различных микробных препаратов, применяемых для профилактики, лечения и диагностики инфекционных заболеваний большое место занимают вакцины — биопрепараты, предназначенные для создания активного искусственного иммунитета.
В качестве антигенов вакцины могут содержать убитые или живые микробные тела, либо извлеченные из них химическим путем полные антигены -глюцидо-липоидные полипептидные комплексы. В зависимости от количества антигенов различают моно-, ди-, три-, тетра- и поливакцины.
Для изготовления вакцин применяются такие штаммы микробов, которые удовлетворяют требованиям специальных инструкций по отбору, проверке и хранению культур, применяемых для изготовления вакцин. Изучение и апробация штаммов на предмет соответствия их требованиям инструкций производится Государственным контрольным институтом медицинских биологических препаратов, там же они хранятся в музее живых культур как эталонные, от них отвивают дубликаты и рассылают в сопровождении специального паспорта в институты, изготавливающие вакцины, для использования в производстве. В паспортах, сопровождающих такие штаммы, указываются основные их свойства — морфологические, культуральные, биохимические, антигенные.
Штаммы, полученные из контрольного института, используются в производстве вакцин только после проверки на местах. В производственных институтах проводится большая работа по изучению условий стабилизации свойств штаммов, предназначенных для изготовления вакцин. В настоящее время стабильность свойств культур обеспечивается хранением их в высушенном состоянии в условиях вакуума в запаянных ампулах. Бактериальные культуры, кроме того, можно хранить в пробирках на плотной питательной среде, оптимальной для данного вида микроба. Пробирки в этом случае запаивают, либо заливают пробки расплавленным воском или парафином, чтобы предохранить культуру от высыхания при длительном хранении. Штаммы, хранящиеся в лаборатории, регистрируются в специальных журналах, где записывают паспортные данные, а также результаты текущих проверок, регламентируемых инструкциями.
Требования инструкций к производственным штаммам разных видов и различных групп микроорганизмов направлены к одной цели — обеспечению малой реактогенности, полной безвредности и высокой эпидемиологической эффективности приготовленных из них вакцин. Методы определения этих свойств производственных штаммов в зависимости от того, к какому виду микробов они применяются, имеют специфические особенности, которые отражены в специальной части. В принципе иммуногенность их определяется путем выявления устойчивости животных, иммунизированных опытными вакцинами, приготовленными из этих штаммов, к заражению заведомо смертельными дозами соответствующих культур.
Вирулентность штаммов изучается путем заражения чувствительных животных, чаще всего мышей, и характеризуется заведомо смертельными, минимальными смертельными и 50 %-ными смертельными дозами культур испытуемых штаммов.
Для выявления токсичности животным вводится убитая нагреванием культура производственных штаммов.
Конкретные показатели иммуногенности, вирулентности и токсичности для разных видов микробов определяются инструкциями. Штаммы, обладающие меньшей иммуногенностью и вирулентностью или большей токсичностью, чем это установлено инструкцией, для производства вакцин не применяются.
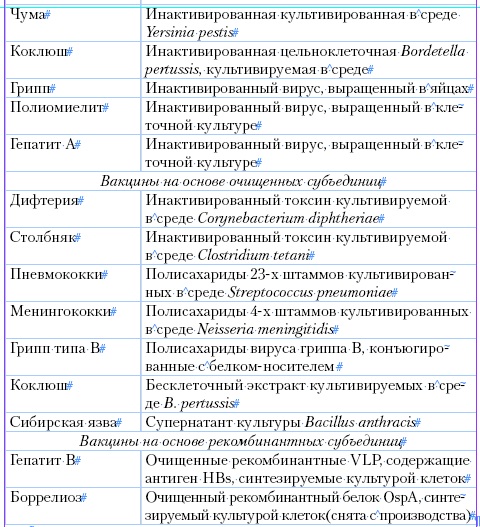
Таблица 1
Основные типы вакцин
Способы приготовления вакцин отличаются выраженным разнообразием, что связано с особенностями тех микробов, из которых они готовятся. Для удобства изложения целесообразно выделить четыре группы вакцин, которые имеют общие принципы приготовления:
1) вакцины из убитых бактерий;
2) вакцины из инактивированных риккетсий и вирусов;
3) химические вакцины;
4) живые вакцины.
Вакцины из убитых бактерий
Процесс изготовления вакцин из убитых бактерий состоит из следующих операций:
1) заготовка посевного материала;
2) массовый посев и выращивание микробов;
3) сбор и обработка бактерийной массы (инактивирование, консервирование и стандартизация);
4) разведение маточной взвеси для получения вакцины.
Заготовка посевного материала. Материалом для посева обычно служит суточная бактерийная культура — бульонная или агаровая, приготовленная в виде суспензии из штаммов определенного вида, удовлетворяющих требованиям инструкции. Для достижения большей эпидемиологической эффективности некоторые вакцины изготавливаются из нескольких (3-5) штаммов одного и того же вида микробов. Такие вакцины называются поливалентными. Каждый штамм бактерий засевается и выращивается отдельно. Бактерийная суспензия для посева может быть приготовлена из высушенной культуры производственного штамма; в этом случае ампулу вскрывают, сухую бактерийную массу разводят стерильным, физиологическим раствором и используют для посева.
Массовый посев и выращивание бактерий. В настоящее время получение бактерийной массы для изготовления вакцин производят посевом культуры в жидкую питательную среду в специальных котлах-реакторах (новый метод) или массовым посевом на плотную среду в матрацах или четвертях (старым метод). Детали нового метода изложены в разделе культивирования микроорганизмов. Выращивание ведется при оптимальной для данного микроба температуре в течение 12-18-20 часов. Иногда срок инкубации удлиняется.
Сбор и обработка микробной бактерийной массы. По истечении срока культивирования производится сбор бактерийной массы и инактивирование ее. Последовательность этих операций определяется методом выращивания. Так, при использовании жидких питательных сред культура вначале инактивируется в том же реакторе, где производилось выращивание, а затем микробная масса отделяется от жидкой части культуры путем центрифугирования на суперцентрифугах. Если применялись плотные питательные среды, то выросшая на них культура смывается физиологическим раствором и собирается- с помощью сифонной трубки в стерильные градуированные бутыли, в которых затем производится инактивирование культуры.
Как в том, так и в другом случаях инактивирование осуществляется чаще всего прогреванием микробной взвеси при 54-58 °С
(в зависимости от вида микроба) в течение одного часа с постоянным помешиванием. Применяется для этой цели также воздействие химических веществ — формалина, добавляемого в концентраций 0,1-1 %, спирта, мертиолята и других. Полученная — инактивированная, так называемая маточная, взвесь подвергается дальнейшей обработке. После проверки стерильности определяется густота полученной суспензии. Это осуществляется либо путем сравнения со стандартами мутности, изготовляемыми и рассылаемыми производственным институтам Государственным контрольным институтом биологических медицинских препаратов, либо с помощью нефелометра. В настоящее время для целей стандартизации вакцин выпускаются стеклянные стандарты, представляющие собой взвесь мельчайших частиц пирекс-стекла в дистиллированной воде. Они выпускаются в виде набора эталонов различной степени мутности, фотометрически подогнанной к мутности взвеси живых тифозных бактерий определенной концентрации.
Инактивированная и стандартизированная маточная взвесь может сохраняться в хранилище при температуре не выше 8-10 °С 3-6 месяцев; в течение этого времени она должна быть переведена в вакцину.
Маточные взвеси разводятся стерильным физиологическим раствором так, чтобы получить суспензии определенной густоты, установленной для каждого вида вакцин специальными инструкциями. Исходя из общего количества маточной взвеси и ее густоты, рассчитывают необходимое количество физиологического раствора, которое нужно взять для разведения, чтобы получить вакцину нужной густоты. После произведенных расчетов к специально заготовленному физиологическому раствору, содержащему 0,25-0,5 % карболовой кислоты, добавляют необходимое количество маточной взвеси. Густоту полученной суспензии проверяют и окончательно коррегируют, если в этом есть необходимость, по стандартам мутности.
Для получения серии, которая должна содержать несколько разных антигенов, смешивают исходные маточные взвеси разных видов в количествах, определяемых густотой каждой взвеси и тем соотношением микробов, которое установлено для готовой вакцины.
Каждый этап обработки вакцины заканчивается контролем стерильности. В качестве консерванта к вакцине добавляют химически чистую карболовую кислоту (0,5 %) либо мертиолят (1:10000). Помимо проверки стерильности и соответствия стандарту, на разных этапах приготовления контролируют безвредность, иммуногенность и переносимость вакцин. Детали проведения этих контролей изложены в разделе контроля препаратов вообще и в частном разделе применительно к особенностям каждой вакцины. Проконтролированные вакцины передаются в РФО, где разливаются и фасуются в соответствии с положениями инструкции по выпуску каждого вида вакцины.
Вакцины из убитых бактерий применяются для профилактики брюшного тифа, паратифов А и В, дизентерии, холеры, лептоспирозов, коклюша. К их числу могут быть присоединены вакцины, применяемые для лечебных целей, при некоторых хронических и вяло протекающих инфекциях, как то: бруцеллез, туляремия, дизентерия, гонорея, коклюш. При некоторых гнойных заболеваниях применяются стафилококковые и стрептококковые вакцины, которые иногда рекомендуют готовить из штаммов, выделенных от больного. В таких случаях препарат называют аутовакциной.
Вакцины из инактивированных риккетсий и вирусов
Отличительной особенностью вакцин из инактивированных риккетсий и вирусов является способ накопления микробной массы. Этот процесс осуществляется путем заражения чувствительных животных, членистоногих, куриных эмбрионов или культур тканей, что в деталях изложено в разделе культивирования микробов.
Таким образом, вирусные и риккетсиозные вакцины представляют собой суспензии тканей, в которых размножались микроорганизмы или, если говорить о некоторых вирусных вакцинах — вируссодержащую жидкость, в которой размножались те или иные клетки, инфицированные вирусами.
Процессы приготовления этих вакцин отличаются выраженным своеобразием, определяемым особенностями микроба. В связи с этим в деталях они изложены в соответствующих частных разделах.
К числу инактивированных риккетсиозных и вирусных вакцин относятся вакцины против сыпного тифа, клещевого и комариного энцефалита, геморрагической лихорадки.
Химические вакцины
Описанные до сих пор вакцины в качестве антигенов содержат убитые тела соответствующих микробов. Между тем известно, что из микробных тел химическим путем могут быть извлечены активные, иммуногенные фракции. Использование этих специфических фракций, свободных от балластных веществ клетки, положено в основу приготовления бескорпускулярных химических вакцин.
Извлечение соматических антигенов из микробных тел осуществляется различными методами: экстрагированием трихлоруксусной кислотой, кислотным гидролитом или ферментативным перевариванием микробных тел с последующим осаждением антигена спиртом или сернокислым аммонием и очисткой диализом.
Входящие в состав химических вакцин растворимые антигены адсорбируются на фосфате кальция. Благодаря этому в месте введения вакцины создается «депо» антигена, что удлиняет срок пребывания препарата в организме, повышает иммуногенность и позволяет, следовательно, сократить число прививок. Кроме того, замедленное всасывание снижает реактогенность препарата. Получение химическим путем микробных антигенов представляет ряд преимуществ, так как дает возможность извлекать из культуральной жидкости максимальное количество антигенов и концентрировать их в небольшом объеме.
Живые вакцины
Впервые вакцина, содержащая в качестве антигена живые вирусы, была предложена Дженнером. Это была вакцина против оспы и представляла собой лимфу из пустул, возникающих на вымени коров, больных оспой.
Открытие принципа приготовления живых вакцин принадлежит Л. Пастеру, и, поскольку эти препараты являются наиболее эффективными, этот принцип разрабатывается многими исследователями с целью создания живых вакцин против различных инфекционных заболеваний.
Основной особенностью живых вакцин является то, что они изготавливаются из, так называемых, аттенуированных штаммов, которые утратили свои патогенные свойства под влиянием тех или иных воздействий, но сохранили способность, будучи введенными в организм, приживаться в нем и вызывать иммунологические сдвиги, которые являются характерными для состояния резистентности организма к инфекции.
Такие штаммы можно получить путем селекции, либо с помощью воздействия на микробы различными, неблагоприятными для них факторами (необычной температурой, бактериофагами, антителами, антибиотиками, неблагоприятными питательными средами, проведением через организм животных). В качестве факторов последней могут быть использованы: необычная температура, бактериофаги, антитела, антибиотики, неблагоприятные питательные среды, организм животных.
Получение вакцинных штаммов для вирусных вакцин осуществляется более или менее длительным пассированием микроба через организм животных. Применяемый для изготовления антирабической вакцины фиксированный вирус бешенства, был получен Пастером путем длительного пассирования вируса уличного бешенства, выделенного от больной коровы через мозг кролика. В результате этого микроб, повысив до предела свою вирулентность для кролика при внутримозговом введении, снизил ее до минимума для человека, собак и сельскохозяйственных животных.
В принципе все вакцинные штаммы отличаются значительной утратой вирулентности и сохранением антигенной структуры исходного штамма.
Первый признак — значительная утрата вирулентности не позволяет им вызвать заболевание в организме привитого. Однако, благодаря остаточной вирулентности, они приживаются в нем и вызывают доброкачественное заболевание, так называемую вакцинальную реакцию. Благодаря этому, а также антигенной тождественности с соответствующим возбудителем заболевания, в организме привитого появляются специфические антитела, изменяется реактивность, что выявляется положительными аллергическими реакциями, развивается специфический иммунитет;
Измененные штаммы могут быть названы вакцинными только в том случае, если указанные выше признаки, приобретенные ими, стойко удерживаются, передаются по наследству и если полностью исключена возможность реверсии — возврата к исходному состоянию.
Все живые вирусные вакцины содержат не только специфические антигены соответствующих микроорганизмов, но и элементы разрушенной ими и гомогенизированной в процессе приготовления ткани, в которой они размножались. Так, оспенная вакцина состоит из растертых пустул, развившихся на коже привитого теленка, антирабическая вакцина — из измельченной ткани головного мозга кролика, инфицированного фиксированным вирусом бешенства, гриппозная вакцина содержит аллантоисную жидкость и измельченные аллантоисные оболочки куриного эмбриона и т.д.
В настоящее время, в связи с развитием вирусологической техники, получена возможность накапливать значительные количества вируса in vitro, на размножающихся культурах различных клеток. Вируссодержащая жидкость, полученная таким образом, и является основой для приготовления вакцины. Такие вакцины, освобождение от ненужных элементов тканей, являются препаратами более высокого качества.
Эффективность живых вакцин в значительной степени обусловливается количеством содержащихся в них живых микроорганизмов; по мере отмирания их иммуногенность вакцины снижается. Для стабилизации живых вакцин и удлинения срока годности они выпускаются в сухом виде. Высушивание вакцин производится методом лиофилизации. Срок годности сухих вакцин значительно удлиняется, что дает возможность применять их даже в самых отдаленных районах страны. Правильно высушенные вакцины представляют собой плотные или пористые таблетки полушаровидной формы. Перед употреблением их растворяют в стерильной воде, физиологическом растворе или в смеси физиологического раствора с глицерином. Плохо растворяющаяся вакцина к употреблению не годна.
В настоящее время применяются:
1) живые бактериальные вакцины: против бруцеллеза, чумы, туляремии, туберкулеза, сибирской язвы.
2) живые вирусные и риккетсиозные вакцины: против оспы, гриппа, бешенства, полиомиелита, кори, коревой краснухи и желтой лихорадки.
Живые вакцины имеют неоспоримое преимущество перед аналогичными вакцинами из убитых микробов, в некоторых случаях они являются единственными эффективными профилактическими препаратами.
Ассоциированные вакцины
Применение комплексных препаратов позволяет уменьшить количество прививок и получить при этом иммунологический эффект не меньший, чем при использовании монопрепаратов. В настоящее время проводятся широко поставленные исследования, направленные на разработку ассоциированных вакцин различной сложности.
Изучается возможность комплексирования не только однотипных вакцин, но и препаратов разного типа. В практику уже давно вошли сложные вакцины против кишечных инфекций (ди-, три- и тетравакцины), химические вакцины также представляют собою сложные препараты, состоящие из антигенов нескольких видов микробов и в ряде случаев столбнячного анатоксина. Из области экспериментальной разработки вышли в практику дифтерийно-столбнячный анатоксин (ДС) и коклюшно-дифтерийно-столбнячная вакцина (КДС и АКДС).
Объединение в состав ассоциированных вакцин различных антигенов диктуется эпидемиологической целесообразностью. Так, известно, что дети могут заболевать столбняком, что коклюш является одной из наиболее распространенных инфекций в детском возрасте и что одной из задач, стоящих перед органами здравоохранения, является ликвидация дифтерии. В связи с этим, эпидемиологически вполне целесообразно объединить антигены, создающие иммунитет против этих инфекций в один препарат. Целесообразно также комплексировать анатоксины против столбняка и других анаэробных инфекций и др.
При создании ассоциированных вакцин исследователям приходится учитывать особенности взаимодействия разных антигенов в организме привитого, важное значение имеет количественное соотношение антигенов, входящих в состав ассоциированного препарата. Нерациональное дозирование может снижать ответную реакцию организма к отдельным антигенам, различным по своей иммунологической активности.
Возможность извлечения антигенов из микробной клетки химическими путями, достижения в области очистки их, а также анатоксинов, от балластных веществ с последующей концентрацией действующих начал, открывает перед иммунологами широкие перспективы дальнейшего развития этого, чрезвычайно важное и весьма перспективного раздела прикладном иммунологии.
Источник