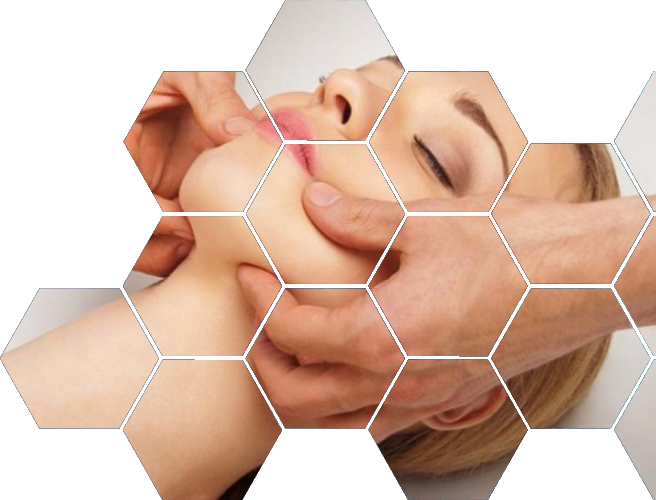
Лечебная миорелаксация
Более чем у половины пациентов при осмотре выявляются болезненные уплотнения в мышцах шеи и лица, так называемые триггерные точки, 
Особенности процедуры
Метод заключается в охлаждении мышцы специальным спреем или льдом с последующим легким растяжением, при помощи специальных приемов (разных для каждой мышцы). При этом, триггерные точки инактивируются, то есть мышца расслабляется, и спазм исчезает. Лечебная миорелаксация безболезненна и абсолютно безопасна.
В особых случаях проводятся инъекции лидокаина в триггерные точки и разрушение триггерной точки очень тонкой (акупунктурной) иглой. Также для инактивации триггерных точек мы успешно применяем ударно-волновую терапию (УВТ). Аппарат УВТ создает мощную вибрацию, которая расслабляет мышцу и устраняет триггерные точки.

Стоимость
Цена за 1 сеанс лечебной миорелаксации составляет 1500 рублей, продолжительность сеанса до 60 минут. Необходимое количество процедур рассчитывается индивидуально каждому пациенту.
Как записаться
Записаться на консультацию к неврологу для проведения лечебной миорелаксации вы можете у администраторов нашего центра:
Ул. Шейнкмана, 134 А, тел: (343) 286-80-24,
Источник
Есть ли польза от миорелаксации?
Самым распространенным сиптомокомплексом в клинической практике является синдром болезненного рефлекторного мышечного спазма. Характеризуется он повышением мышечного тонуса с длительными непроизвольными сокращениями скелетной мускулатуры, вызывающими сильнейшую, порой невыносимую боль. Ведущим звеном в его терапии является миорелаксация.
В нашей клинике представлены лучшие мировые физиотерапевтические бренды, позволяющие достигать самых быстрых результатов, поэтому вы сможете увидеть положительный эффект уже с первого сеанса!
Что такое миорелаксация?
Это снижение тонуса скелетных мышц, что может достигаться с помощью специальных психофизиологических методов, физиотерапии и медикаментов. Расслабление помогает уменьшить психическое напряжение, поэтому оно широко используется в йоге, гипнозе, психотерапии и иных оздоровительных системах.
Медитация и релаксация очень популярны как средство лечения психосоматических болезней и стресса. Особенно эффективны они для людей с повышенным мышечным тонусом, который, как было доказано, приводит к развитию заболеваний. Сильное прогрессирующее снижение или повышение мышечного тонуса может быть результатом заболевания.
Как провести миорелаксацию?
К нам часто обращаются с вопросом, «Как провести миорелаксацию?»
Мы рекомендуем высокоинтенсивную магнитотерапию, которая обладает эффектом мышечного расслабления и обезболивания. Воздействие при помощи инновационной методики Super Inductive System ускорит вымывание кислых метаболитов, вызывающих болезненное раздражение в мышцах и местах хронического воспаления. Таким образом уменьшается боль и снижаются болезненные мышечные спазмы (контрактуры). Кроме того, было доказано существенное замедление нервной проводимости в нижних конечностях у спортсменов, что также способствует расслаблению мышц.
Эффект миорелаксанта устройств Super Inductive System на мышечную ткань спины устраняет ряд проблем, таких как затвердение шейного отдела позвоночника, головные боли, головокружение, потеря слуха, ограниченный диапазон движений, боль в конечностях и пр. Поможет методика купировать колики и приносить релаксацию скелетной мышечной ткани, что является необходимым условием для лечения всех болезненных состояний опорно-двигательного аппарата.
По эффективности этот метод лечения пациентов в разы результативнее остальных, запишитесь на курс и убедитесь в этом прямо сегодня!
Источник
Миорелаксация челюстно-лицевой области
Так, нарушение работы жевательных и лицевых мышц приводит к изменению положения нижней челюсти, дисфункциям нижнечелюстного сустава, невралгиям, невропатиям и общему нарушению баланса тела в пространстве. Чем сильнее напряжена мышца, тем большей компрессии подвергаются близлежащие структуры (нервы, сосуды, связки, фасции).
* Цены на сайте не являются публичной офертой и имеют информационный характер.
Патологическое миофасциальное напряжение челюстно-лицевой области вызывает асимметрию мышечного тонуса с возникновением ряда биомеханических нарушений, куда относятся и функциональные блоки височно-нижнечелюстного сустава. Под этим понятием подразумевается ограничение подвижности сустава, обусловленное рефлекторной околосуставной миофиксацией. Сочленение в такой ситуации испытывает перегрузку, в капсулярном аппарате начинают развиваться дистрофические изменения. Нарушения не ограничиваются локальными негативными эффектами, они последовательно распространяются на «нижние» этажи тела.
Фасциальные напряжения в челюстно-лицевой области часто сопровождаются нарушениями осанки, изменениями двигательного стереотипа, перекосом таза. В блокированных, напряженных структурах прогрессирует раздражение многочисленных рецепторов, что обусловливает возникновение локальных и иных видов боли, отдающих в разные зоны тела.
Методика миорелаксации челюстно-лицевой области основана на принципе обратной взаимосвязи между структурами организма. Это значит, что приемы врача направлены на изменение пластичности тканей, но положительные изменения отражаются в гораздо более широких пределах. Используемые техники не требуют специальной подготовки и физических затрат со стороны пациента, хорошо помогают при многих соматических патологиях. Врач-постуролог не ограничивается исключительно механическим эффектом, его действия затрагивают нейромышечные рефлекторные связи, отвечающие за правильные взаимоотношения проприоцептивных и биомеханических механизмов в патологически измененных тканях.
Грамотная миофасциальная релаксация челюстно-лицевой области способна на многое:
- улучшение кровотока в зонах триггерных точек;
- восстановление нервно-мышечных связей;
- ликвидация фокусов сверхраздражимости в мышце;
- расширение диапазона движений мышечного волокна;
- облегчение состояния при невралгиях и невропатиях;
- купирование лицевых и отраженных болей.
Миорелаксация хорошо устраняет локальные спазмы в мышечном пучке или сухожилии, хорошо проявляет себя в комплексном лечении дисфункции височно-нижнечелюстного сустава.
Наши специалисты успешно сочетают современные релаксирующие техники с другими методиками, направленными на восстановление постурального баланса. Понимание клинической значимости ручных приемов и умение применять их на практике расширяет показания метода в лечении многих заболеваний челюстно-лицевой области, особенно в сочетании с нейромышечной стоматологией.
Мы практикуем комплексный подход для эффективного лечения пациентов со стоматологическими, неврологическими, двигательными и другими проблемами.
Не откладывайте визит к врачу при появлении жалоб! –
Лечение в нашей клинике проходит максимально комфортно и быстро.
Источник
Место миорелаксантов в лечении болевого синдрома
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Болевой синдром – один из основных компонентов защитной системы организма. Боль – важнейший сигнал о повреждении ткани и развитии патологического процесса. Многие острые и хронические заболевания, медицинские вмешательства и травмы сопряжены с болью, требующей применения анальгетических средств [1].
Ощущение боли формирует целый комплекс защитных реакций, направленных на устранение повреждения [2]. Острая (преходящая) боль обусловлена острым заболеванием, травмой и прекращается по мере выздоровления и заживления ран. Хроническая (персистирующая) боль связана с длительно существующим патологическим процессом или посттравматическим состоянием, продолжается от 1–3 мес. до многих лет [3]. Хроническая боль – это больше, чем физический симптом. Ее постоянное присутствие имеет множество проявлений, включая поглощенность пациента болью, ограничение личной, социальной и профессиональной деятельности, аффективные расстройства, использование большего количества медикаментов и частое обращение за медицинской помощью, когда в целом человек сживается с «ролью больного» [4, 5].
В клинической и амбулаторной практике при болевом синдроме чаще всего используют нестероидные противовоспалительные препараты (НПВП), обладающие обезболивающим действием, которое сочетается с противовоспалительным и жаропонижающим эффектом. Анальгетическое действие данных средств, так же как и всех НПВП, обусловлено подавлением активности циклооксигеназы (ЦОГ) и снижением продукции простагландинов E2 и F2, повышающих чувствительность ноцицепторов как при воспалении, так и при повреждении тканей. Более выраженным анальгетическим, чем противовоспалительным эффектом обладают те НПВП, которые вследствие своей химической структуры нейтральны, меньше накапливаются в воспалительной ткани, быстрее проникают через гематоэнцефалический барьер и подавляют ЦОГ в ЦНС, а также влияют на таламические центры болевой чувствительности [6, 7].
В мировой медицинской литературе представлено огромное количество данных о побочных эффектах терапии НПВП. У 30–40% больных, получающих НПВП, отмечаются диспептические расстройства, у 10–20% – эрозии и язвы желудка, двенадцатиперстной, тонкой, а иногда и толстой кишки, у 2–5% – кровотечения и перфорации. Причем гастро- и энтеротоксичность могут иметь место при любом пути введения НПВП. Также отмечают нефро-, гепато- и гемотоксичность некоторых НПВП [6–9].
Снизить вероятность развития и выраженность проявления нежелательных лекарственных реакций при назначении НПВП, а также повысить эффективность проводимой терапии возможно при комбинированном подходе к лечению болевого синдрома. Это позволяет сократить дозы противовоспалительных препаратов и сроки их назначения [6–9].
В патогенезе болей различной локализации (мышечно-тонические боли в спине вследствие остеохондроза или спондилоартроза, миофасциальный синдром, головная боль напряжения (ГБН) и др.) часто можно отметить мышечно-спастический компонент. Боль, обусловленная мышечно-тоническим и/или миофасциальным болевым синдромом, очень часто является основной причиной обращения пациента к врачу. Нередко болевые синдромы становятся причиной ограничения и даже утраты трудоспособности. В этой связи важно заметить, что при адекватной и своевременной терапии болевой синдром может довольно быстро купироваться. Врачебная тактика при лечении подобных пациентов заключается, с одной стороны, в ослаблении боли и в стремлении к как можно более быстрому возвращению пациента к активному образу жизни и, с другой стороны, в предупреждении повторных обострений и хронического течения болевого синдрома [7, 10–13].
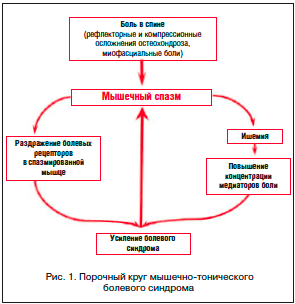
Применение миорелаксантов обосновано признанием важной роли мышечного спазма в патогенезе боли в нижней части спины. Доказано, что при острой поясничной боли добавление к стандартной терапии (НПВП) миорелаксантов приводит к более быстрому регрессу боли, мышечного напряжения и улучшению подвижности позвоночника. Боль различного генеза (вследствие поражения межпозвонковых дисков, фасеточных суставов позвоночника, самих мышц и других причин) повышает активность двигательных нейронов спинного мозга, что приводит к мышечному спазму, который, в свою очередь, играет значительную роль в поддержании самой боли. Патогенез возникновения хронических болевых мышечно-тонических синдромов обусловлен механизмом порочного круга: боль и напряжение мышцы – перевозбуждение спинальных нейронов (вставочных и мотонейронов) – напряжение мышц и изменение позы – еще большее усиление боли. При этом ухудшается кровоснабжение мышц, повышается концентрация медиаторов боли, раздражаются болевые рецепторы в спазмированной мышце. Миорелаксанты разрывают порочный круг «боль → мышечный спазм → боль» и вследствие этого способны ускорять процесс выздоровления (рис. 1) [10, 11, 14].
Большое значение в патогенезе болевых мышечно-тонических синдромов имеют вставочные спинальные нейроны. Их состояние определяется влиянием нисходящих супраспинальных путей, среди которых особое место принадлежит структурам среднего и продолговатого мозга. Регуляция проведения ноцицептивных стимулов на спинальном уровне осуществляется при участии супраспинальных адренергических структур. Ингибирующее действие тормозящих спинальных нейронов реализуется с участием различных нейромедиаторных систем (глутаматергической, ГАМК-ергической*, адренергической и др.). Именно с этими структурами связано действие большинства миорелаксирующих препаратов. Наиболее важные положительные эффекты миорелаксантов: уменьшение боли, снижение болезненного мышечного напряжения, улучшение двигательной активности, уменьшение дозы обезболивающих препаратов, в т. ч. НПВП. Лечение миорелаксантами начинают с обычной терапевтической дозы и продолжают при наличии болевого синдрома; как правило, курс лечения составляет несколько недель. Для лечения острых болей в нижней части спины в качестве эффективных миорелаксантов применяются тизанидин, дантролен, диазепам, баклофен, толперизон и др. [7, 10, 14].
Эффективным препаратом для лечения миофасциальных болевых синдромов, мышечно-тонических синдромов и спастичности различного генеза является релаксант скелетной мускулатуры центрального действия, агонист α2-адренергических рецепторов тизанидин (Сирдалуд, «Новартис Фарма АГ», Швейцария). В основе патогенетического действия препарата лежит комплексный механизм: сочетание миорелаксантного, уменьшающего болевой поток из перикраниальных мышц, и центрального умеренно выраженного анальгезирующего эффекта.
По механизму своего действия и особенностям применения он выгодно отличается от других миорелаксантов, поскольку обладает и миорелаксирующим, и анальгезирующим действием. Обезболивающий эффект препарата при болевых мышечно-тонических синдромах обусловлен как расслаблением патологически напряженных мышц, так и непосредственным антиноцицептивным действием, которое реализуется на спинальном и супраспинальном уровнях и связано с адренергической активностью препарата. Тизанидин, угнетая стимуляцию NMDA-рецепторов, блокирует механизм, отвечающий за избыточный мышечный тонус; подавляя полисинаптические рефлексы на уровне спинного мозга, угнетает высвобождение возбуждающих аминокислот и активирует глицин, снижающий возбудимость интернейронов спинного мозга. В результате снижается мышечный тонус. Тизанидин обладает и непосредственным, не связанным со снижением мышечного тонуса, обезболивающим действием. Миорелаксирующий и анальгетический эффекты тизанидина (Сирдалуда) носят дозозависимый характер. При приеме внутрь максимальная концентрация Сирдалуда в крови достигается через 1 ч. Прием пищи не влияет на его фармакокинетику. Начальная доза препарата варьирует от минимальной – 2 мг на ночь до 6 мг/сут в 3 приема. Средняя терапевтическая доза – 12–24 мг/сут. Максимальная доза – 36 мг/сут. Использование Сирдалуда наиболее эффективно в острую фазу заболевания. Положительный эффект (уменьшение выраженности мышечного спазма, боли в покое, при движении, ночью) отмечается уже на 3-й день терапии. Оптимальная доза Сирдалуда – 8–12 мг/сут (2–4 мг утром, 2–4 мг днем и 4 мг вечером). Подбор индивидуально эффективной дозы (от 2 мг до максимальной дозы 24–36 мг/сут) обычно осуществляется в течение 2–4 нед. [10, 15–17].
Эффективность и безопасность Сирдалуда при лечении острых болей в спине были убедительно доказаны почти 20 лет назад в плацебо-контролируемом исследовании. Применение тизанидина по 4 мг 3 р./сут в течение 7 дней при острой боли в нижней части спины имело достоверное преимущество над плацебо в отношении снижения боли в покое, болевых ощущений в ночное время, увеличения двигательной активности. В исследовании, проведенном D. Hutchinson (1990), осложнения со стороны ЖКТ отмечались у 6% больных, получавших по поводу боли в спине Сирдалуд и ибупрофен, и у 20% – комбинацию плацебо и ибупрофена. Важно отметить, что тизанидин (Сирдалуд) усиливает обезболивающее и противовоспалительное действие НПВП (нимесулида, диклофенака, мелоксикама и др.), позволяет снизить их дозу и, обладая гастропротекторной эффективностью, снижает риск возникновения гастропатий, обусловленных НПВП [7, 10, 18].
В настоящее время Сирдалуд представляет собой один из наиболее широко используемых миорелаксантов при лечении болей различной локализации, его эффективность и безопасность подтверждаются в современных исследованиях. Даже при выраженных и трудно поддающихся лечению болевых синдромах удается достигнуть улучшения. Антиспастический эффект тизанидина (Сирдалуда), связанный с несколькими механизмами действия (пресинаптическое и постсинаптическое ингибирование вставочных нейронов, возможное влияние на глутаматергическую систему), делает возможным его использование при патофизиологически различных заболеваниях, приводящих к спастике, в т. ч. при рассеянном склерозе, хронической миелопатии и спастичности после инсульта. Уменьшая выраженность спастики, Сирдалуд не снижает мышечную силу. Выраженные анальгетические свойства α2-агонистов позволяют успешно использовать Сирдалуд в лечении хронических болевых состояний, включая болевые спазмы, миофасциальную боль, нейропатическую боль и хроническую ежедневную головную боль, в т. ч. цервикогенные головные боли, связанные с мышечным спазмом.
Сирдалуд успешно используется в реабилитационной практике. Отмечаются снижение повышенного мышечного тонуса, нарастание объема пассивных движений в суставах, уменьшение выраженности контрактур, реже возникают клонусы. Препарат эффективен при спастичности как спинального, так и церебрального генеза, что подтверждается клиническими данными [10, 17–26].
Одним из показаний для назначения Сирдалуда является ГБН – самый часто встречающийся вид головной боли (45–80% среди ее других типов). Она представляет собой особый вид реакции на эмоциональный стресс и развивается в результате непроизвольного напряжения перикраниальных мышц или психического напряжения. В работе Е.Г. Филатовой и соавт. (1997) было показано уменьшение головной боли в 75% случаев у пациентов с ГБН при применении тизанидина в суточной дозе 4–6 мг в течение 14 дней. Об эффективности тизанидина (Сирдалуда) при ГБН свидетельствуют уменьшение выраженности головной боли, реактивной тревоги и депрессии, нормализация ночного сна, уменьшение выраженности вегетативных расстройств [15, 27, 28].
Монотерапия ГБН Сирдалудом может быть рекомендована больным с наличием напряжения перикраниальных мышц, мышц шеи и верхнего плечевого пояса при средней выраженности депрессивных эмоциональных нарушений. Двойное слепое плацебо-контролируемое исследование, проведенное R. Fogelhom, K. Murros et al. (1992), показало, что лечение тизанидином (Сирдалудом) в дозе 6–18 мг/сут на протяжении 6 нед. достоверно снижало интенсивность хронической ГБН. Меньшие дозы Сирдалуда (3 мг/сут, разделенные на 3 приема), по данным японских исследователей, также дают хороший эффект: значительное уменьшение интенсивности, частоты и продолжительности хронической ГБН в ходе 4-недельного курса лечения отмечено у 2/3 больных. Лечение рекомендуется начинать с малых доз: 2 мг/сут (на ночь) в течение первых 3-х дней, затем постепенно повысить дозу до 2 мг 2 р./сут (утром и на ночь). При недостаточном эффекте доза может быть повышена до 6–8 мг/сут (по 2 мг 3 р./сут или по 2 мг утром и днем и 4 мг на ночь). Продолжительность лечения может составлять от 2 нед. до 2 мес. [15, 28–30].
Нарушения мышечного тонуса, связанные с ними болевые синдромы, ограничения двигательных функций, вторичные изменения суставов и мышц составляют часть клинических проявлений многих заболеваний нервной системы. Как правило, клиническое значение приобретает проблема повышения мышечного тонуса. Наиболее широко применяется тизанидин (Сирдалуд) в лечении спастичности при травматических повреждениях головного и спинного мозга, рассеянном склерозе, инсульте. При спастичности, связанной с дистоническими нарушениями, паркинсонизмом, более целесообразно использование других средств (например, клоназепама, диазепама). Достаточно широкий диапазон эффективно действующих доз тизанидина (Сирдалуда) (от 2 до 36 мг/сут) позволяет использовать препарат для коротких и длительных курсов лечения болевых синдромов и спастичности в виде монотерапии или в сочетании с другими лекарственными средствами [15, 31–33].
Побочные эффекты на фоне приема Сирдалуда минимальны и чаще заключаются в легкой преходящей сонливости, сухости во рту, диспепсии и общей слабости. Тизанидин (Сирдалуд) оказывает анксиолитическое и седативное действие. Седативный эффект полезен больным с болевыми синдромами и сопутствующими нарушениями сна. В случае, когда седативный эффект нежелателен, его можно контролировать путем титрации дозы. Могут отмечаться артериальная гипотония, брадикардия. При приеме более высоких доз вышеперечисленные побочные действия возникают чаще и более выражены, однако они редко бывают настолько тяжелыми, чтобы лечение пришлось прервать. Частота возникновения побочных реакций коррелирует с уровнем препарата в плазме крови и достигает пика в течение 1 ч после приема [15, 26, 34].
Заключение
Благодаря высокой эффективности и благоприятному спектру побочных эффектов Сирдалуд рассматривается как препарат первой очереди выбора для лечения острой и подострой миофасциальной боли в монотерапии, а также хронического миофасциального синдрома в комбинации с другими медикаментами, чаще антидепрессантами.
Сирдалуд отличается от других миорелаксантов, поскольку обладает и миорелаксирующим, и анальгезирующим действием. Важным свойством тизанидина (Сирдалуда) является способность предохранять повреждение слизистой желудка при приеме НПВП. Назначение Сирдалуда в комплексной терапии болевого синдрома способствует уменьшению не только доз НПВП, но и проявлений ульцерогенного действия противовоспалительных препаратов за счет доказанного гастропротективного эффекта.
Обезболивающий эффект препарата при болевых мышечно-тонических синдромах обусловлен как расслаблением патологически напряженных мышц, так и непосредственным антиноцицептивным действием, которое реализуется на спинальном и супраспинальном уровнях и связано с адренергической активностью препарата. Стоит подчеркнуть, что снижение мышечного тонуса на фоне назначения Сирдалуда не сопровождается уменьшением мышечной силы, и это особенно важно для пациентов с центральными парезами (рассеянный склероз, остаточные явления перенесенного инсульта и т. д.). Сирдалуд, являясь агонистом α2-адренергических рецепторов, угнетает полисинаптические спинальные рефлексы и практически не влияет на моносинаптические рефлексы. Поэтому на фоне действия Сирдалуда уменьшается лишь тонический компонент мышечного сокращения при сохранности фазической реакции. Это отлично от действия других миорелаксантов (особенно баклофена), уменьшающих тонический и фазический компоненты, что сопровождается нежелательным снижением силы мышц.
* ГАМК – γ-аминомасляная кислота.
- Осипова Н.А., Абузарова Г.Р., Петрова В.В. Принципы применения анальгетических средств при острой и хронической боли. Клинические рекомендации. М.: ФГБУ «МНИОИ им. П.А. Герцена Минздравсоцразвития России», 2010. 67с.
- Кукушкин М.Л., Табеева Г.Р., Подчуфарова Е.В. Болевой синдром: патогенез, клиника, лечение. Клинические рекомендации / под ред. акад. РАМН Н.Н. Яхно. М.: ИМА-пресс, 2011. 79 с.
- IASP Committee on Taxonomy, 2012. Международная ассоциация по изучению боли IASP http://www.iasp-pain.org.
- Данилов А.Б. Биопсихосоциальная модель и хроническая боль // Российский журнал боли. 2010. № 1 (26). С. 3–7.
- Parsons T. Definitions of health and illness in the light of American values and social structure. — In: E.G. Jaco (ed.). Patients, physicians, and illness. 1958. P. 3–29.
- Клиническая фармакология и фармакотерапия / под ред. В.Г. Кукеса, А.К. Стародубцева М.: ГЭОТАР-Медиа, 2012. 832 с.
- Клиническая фармакология (серия «Национальные руководства»). М.: ГЭОТАР-Медиа, 2014. 976 с.
- Евсеев М.А. Повреждение кишечной трубки нестероидными противовоспалительными препаратами: клиническое значение, патогенез, возможности профилактики // Неврология, нейропсихиатрия, психосоматика. 2013. № 1. С. 79–87.
- Страчунский Л.С., Козлов С.Н. Нестероидные противовоспалительные средства http://www.antibiotic.ru/rus/all/metod/npvs.
- Парфенов В.А. Диагноз и лечение при острых болях в нижней части спины // РМЖ. 2007. № 6.
- Подчуфарова Е.В., Яхно Н.Н. Боли в спине и конечностях / В кн.: Болезни нервной системы. Руководство для врачей / под ред. Н.Н. Яхно. М., 2005. Т. 2. С. 306–331.
- Bogduk N., McGuirk B. Medical management of acute at chronic low back pain. Amsterdam: Elsevier, 2002.
- Dugan S.A. The role of exercise in the prevention and management of acute low back pain // Clin Occup Environ Med. 2006. Vol. 5. P. 615–632.
- Van Tulder M., Becker A., Bekkering T. et al. European guidelines for the management of acute nonspecific low back pain in primary care // Eur Spine J. 2006. Vol. 15. (Suppl. 2). Р. 169–.191.
- Данилов А.Б. Возможности применения тизанидина (Сирдалуда) в клинической практике // РМЖ. 2009. Т. 17. № 19.
- Coward D.M. Tizanidine: Neuropharmacology and mechanism of action // Neurology. 1994. Vol. 44 (Suppl. 9). Р. 6–11.
- Боль (практическое руководство для врачей) / под ред. Н.Н. Яхно, М.Л. Кукушкина. М., 2012. 512 c.
- Berry H., Hutchinson D.R. A multicentre placebo-controlled study in general practice to evaluate the efficacy and safety of tizanidine in acute low-back pain // J Int Med Res. 1988. Vol. 16. Р. 75–82.
- Ketenci A., Ozcan E., Karamursel S. Assessment of efficacy and psychomotor performances of thiocolchicoside and tizanidine in patients with acute low back pain // Int J Clin Pract. 2005. Vol. 59. Р. 764–770.
- Meythaler J.M., Guin-Renfroe S., Johnson A., Brunner R.M. Prospective assessment of tizanidine for spasticity due to acquired brain injury // Arch Phys Med Rehabil. 2001. Vol. 82. Р. 1155–1163.
- Smith C., Birnbaum G., Carter J.L., Greenstein J., Lublin F.D. Tizanidine treatment of spasticity caused by multiple sclerosis: results of a double-blind, placebo-controlled trial. US Tizanidine Study Group // Neurology. 1994. Vol. 44 (11. Suppl 9). Р. 34–43.
- Rosenthal M. et al. Die Behandlung chronisch rezidivierender Ruckenproblem mit tizanidin // Therapiewoche. 1988. Vol. 38. P. 2597–2601.
- Ревматология. Клинические рекомендации / под ред. Е.Л. Насонова. М., 2010. 752 с.
- Bettucci D., Testa L., Calzoni S. et al. Combination of tizanidine and amitriptyline in the prophylaxis of chronic tension-type headache: evaluation of efficacy and impact on quality of life // J Headache Pain. 2006. Vol. 7 (1). Р. 34–36.
- Smith H., Elliott J. Alpha2 receptors and agonists in pain management // Curr Opin Anaesthesiol. 2001. Vol. 14 (5). Р. 513–518.
- Воробьева О.В. Возможности альфа2-адренергических агонистов в лечении миофасциальной боли // Русский медицинский журнал. 2007. № 5. C. 445–448.
- Wagstaff AJ., Bryson HM. Tizanidine. A review of its pharmacology, clinical efficacy and tolerability in the management of spasticity associated with cerebral and spinal disorders // Drugs. 1997 Mar. Vol. 53 (3). Р. 435–452.
- Филатова Е.Г., Соловьева А.Д., Данилов А.Б. Лечение головной боли напряжения // Журнал неврол. и психиатр. 1996. № 4. С. 21–25.
- Осипова В.В. Головная боль напряжения: практическое руководство для врачей. М., 2009. 44 c.
- Fogelholm R., Murros K. Tizanidine in chronic tension–type headache: a placebo controlled double–blind crosss–over study // Headache. 1992. Vol. 32. Р. 509–513.
- Shimomura T., Awaki E., Kowa H., Takahashi K. Treatment of tension–type headache with tizanidine hydrochloride: its efficacy and relationship to the plasma MHPG concentration // Headache. 1991 Oct. Vol. 31 (9). Р. 601–604.
- Широков Е.А. Сирдалуд: области клинического применения // Русский медицинский журнал. 2004. № 14. C. 874–875.
- Гусев Е.И., Бойко А.Н. Рассеянный склероз: от новых знаний к новым методам лечения // Русский медицинский журнал. 2001. № 1. С. 4–10.
- Парфенов В.А. Постинсультная спастичность и ее лечение // Русский медицинский журнал. 2006. Т. 14. № 9.
- Nance P. W. Relationship of the antispasticity effect of tizanidine to plasma concentration in patients with multiple sclerosis / P.W. Nance, W.A. Sheremata, S.G. Lynch et al. // Arch. Neurol. 1997. Vol. 54. N 6. P. 731–736.
Только для зарегистрированных пользователей
Источник