Стенты для стентирования коронарных артерий
Ангиопластика и стентирование
Ангиопластика — это изменение формы сосуда. Наиболее часто этот термин употребляется для обозначения процедуры, направленной на расширение суженного участка сосуда. Сосуды, несущие кислород и питательные вещества во все органы и ткани, называются артериями. Они нередко поражаются атеросклерозом, болезнью при которой стенки сосудов утолщаются, сужая просвет. Сужение артерии, или стеноз, вызывает снижение кровотока и кислородное голодание, которое называется ишемией.
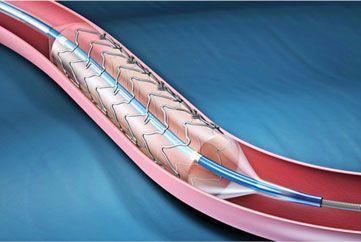
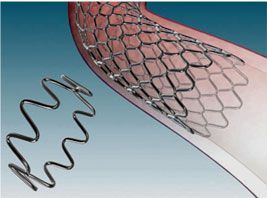
Наиболее часто применяемый вид ангиопластики — это расширение баллонным катетером суженного участка сосуда механическим путем. Несмотря на то, что баллонная ангиопластика не лечит причину болезни, она очень эффективно устраняет симптомы ишемии. Но недостаток метода состоит в том, что после расширения артерия, нередко, вновь сужается из-за эластических свойств. А иногда для достижения эффективного расширения приходится прилагать усилие, вызывающее расслоение стенки сосуда. Выход был найден около 30 лет тому назад, когда в клинической практике стали применять трубчатые распорки, называемые стентами. Стент — это трубка из тонкого металла ячеистой структуры, насаживаемая на баллонный катетер. После расширения баллоном, стент вживляется в стенку сосуда.
Стенты также не лишены определенных недостатков. При внедрении в живую ткань инородного тела, а таковой является стенка сосуда, нередко возникает ответная реакция в виде воспаления. Воспаление может привести к повторному сужению просвета, но уже не из-за роста атеросклеротических бляшек, а из-за размножения клеток, выстилающих внутреннюю поверхность стента. Так бывает, примерно, у каждого третьего пациента. Повторное сужение, рестеноз, может привести к сужению, еще большему чем исходно.
Ученные долго ломали голову над проблемой рестеноза. Применяли и противовоспалительные препараты и противоопухолевые цитостатики и локальное облучение, однако, эффективного метода профилактики рестеноза не было. Выход был найден только тогда, когда появились стенты, покрытые тонким полимерным покрытием, в толщу которого внедрили препарат, подавляющий избыточное размножение клеток. Такой «сэндвич» позволил дозировано, в течение длительного времени создавать высокую концентрацию препарата в «нужном месте и в нужное время». Препараты эти давно применяют в трансплантологии для профилактики отторжения чужеродной ткани и в онкологии для подавления роста опухолевых клеток.
Стенты с лекарственным покрытием
Стенты с лекарственным покрытием или стенты, выделяющие лекарственные препараты, совершили революцию в ангиопластике. Вероятность рестеноза при лечении , например, ишемической болезни сердца снизилась на порядок и составляет менее 5%. Это означает, что эффект полученный при стентировании практически гарантирован на всю жизнь. Стенты с лекарственным покрытием оказались средством выбора у определенной категории пациентов, например с сахарным диабетом, при поражениях большой длины и на развилках артерий, при которых «обычные» стенты почти наверняка «зарастают». Также, незаменимы стенты с лекарственным покрытием и для лечения больных с трофическими язвами, с поражениями артерий голени. Конечно не бывает методов лечения, лишенных недостатков. В связи с тем, что стенты с лекарственным покрытием выделяют препараты, противодействующие размножению клеток, они медленнее приживаются. Клетки, выстилающие изнутри поверхность стента обеспечивают наиболее совершенную защиту от тромбов. Поэтому после имплантации стентов с лекарственным покрытием необходимо длительно принимать препараты против тромбообразования. Кроме того, точность подбора диаметра и длины стента, аккуратность в выполнении процедуры приобретают решающее значение и несмотря на кажущуюся простоту в применении, стенты с лекарственным покрытием требуют высокого мастерства оператора. Технология развивается, появились стенты с лекарственным покрытием второго и третьего поколения, стенты на основе биорастворимых материалов и временные стенты. Все они также выделяют лекарственные препараты. На сегодня, стенты с лекарственным покрытием — основной инструмент в руках врачей. В сочетании с медикаментозной терапией современные стенты позволяют быстро, «малой кровью», эффективно и безопасно устранять симптомы, вызванные заболеваниями артерий.
Какие стенты используются в клинике ЦЭЛТ при стентировании артерий?
Стент BIOMATRIX (производитель — компания BIOSENSORS INTERNATIONAL (Швейцария)
Состав: материал 316 L — нержавеющая медицинская сталь.
Покрытие: имеет покрытие эффективным лекарством Biolimus A9, препятствующий повторному сужению внутри имплантированного стента.
Препарат вместе с полимером PLA полностью растворяется через 6-9 мес, обеспечивая эффективное вживление стента в стенку артерии без повторного сужения.
Отдаленные результаты: Два самых крупных исследования (LEADERS и регистр е — Biomatrix) с включением более 2 000 пациентов показали хорошие 5-ти летние отдаленные результаты с низкой частотой сердечно — сосудистых осложнений и повторных сужений внутри стента менее 7%
СТЕНТ BIOMIME (производитель — компания MERIL LIFE SCIENCES)(Индия)
Состав: материал L 605 — сплав кобальта и хрома.
Покрытие: Имеет специальное лекарственное (сиролимус) покрытие со стороны просвета сосуда для подавления избыточного роста тканей для профилактики повторных сужений на месте имплантации стента. Примерно через 90 дней полностью завершается процесс вживления в стенку сосуда.
Отдаленные результаты: в большом исследовании, в котором учавствовали 12 крупных клинических центров, показали высокую эффективность стента. Через 1 год после установки частота тромбозов стентов — 0%, сердечно — сосудистых происшествий — 2,6%, повторные операции всего в 1,7% случаев.
В результате эффективного подавления избыточного роста тканей, просвет артерии в отдаленном периоде (через 8 мес) сужается всего на 0,18 мм, что соответствует толщине новой ткани на поверхности стента.
Биоабсорбируемые (рассасывающиеся) стенты ABSORB (производитель — компания ABBOT VASCULAR (США)
Состав: PLLA — полимер из полилактозной кислоты.
Покрытие: стент сверху покрыт одним из самых эффективных лекарств эверолимусом, препятствуя образованию повторных сужений в стенте.
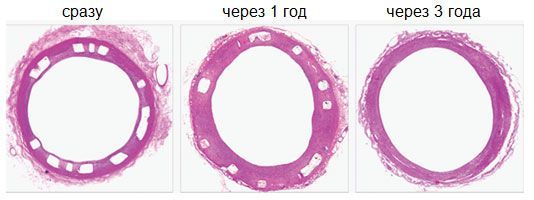
Несмотря на материал изготовления (полимер) стент обладает хорошей поддерживающей способностью. Многочисленные исследования доказали полное исчезновение структуры стента через 2-3 года после имплантации, оставляя просвет артерии в раскрытом виде и стенку сосуда заживленной. Absorb имеет потенциальные преимущества перед постоянно имплантируемыми металлическими стентами. Сохраняют вазомоторику сосуда, отсутствуют рубцовые изменения в стенке артерии, отсутствует основа для возможных воспалительных процессов в стенке сосуда, как при постоянных металлических стентах.
Отдаленные результаты: получены в результате многочисленных исследований в разных странах мира. Самые большие исследования ABSORB II и ASSURE REGISTRY показывают хорошие результаты. Повторные вмешательства потребовались лишь в 2,2-2,8 %, тромбозов рассасываемого стента в этих исследованиях не наблюдали. Многочисленные исследования по внутрисосудистой визуализации также подтверждают полное исчезновение (рассасывание) структуры стента через 3 года.
Стент EndeavorSprint – стент I поколения производитель Metronic (США)
Состав: МатериалL-605 – сплав кобальта и хрома.
Покрытие: лекарство Зотаролимус (Zotarolimus)
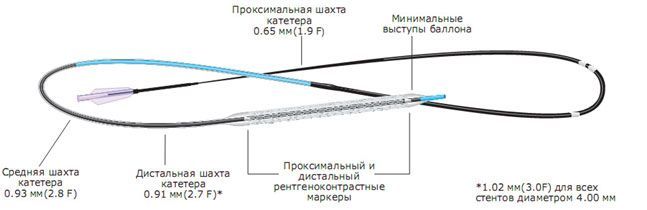
Технические характеристики: коронарный стент EndeavorSprint на системе доставки rapidexchange (RX) обладает низкопрофильным, модульным дизайном, сочетая в себе эффективность и безопасность стента Endeavor с гибкостью и доставляемостью баллона Sprinter. СтентEndeavorSprint установлен на системе доставки быстрой смены (RX) с раздуваемым полуподатливым баллоном, минимально выступающим за границы стента. Лекарство Зотаролимус содержится в биосовместимом, в менее сенситивном полимерном (PCPolymer) покрытии стента. Полимерное покрытие вызывает минимамальную воспалительную реакцию стенки сосуда. На сегодняшний день и покрытие и лекарство считается одним из наименее тромбогенным сочетанием из всех лекарственных стентов.
Отдаленные результаты: стент один из наиболее полноценно изученных из всех современных типов стентов. Более 1000 пациентов изучены в многочисленных сравнительных исследованиях, более 2000 были включены включены в исследовательскую программу Endeavortrialprogram. Исследования показали 37% снижение риска сердечных осложнений в сравнении с другими типами стентовI поколения. Необходимость в повторных вмешательствах через 5 лет после операции – всего 7,7%. Тромбоз стента через 2 года – 0,7%
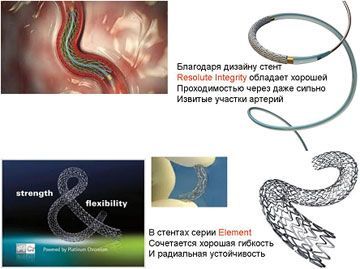
Стент TAXUS element – стент III поколения производитель BostonScientific (США)
Состав: Сплав Платины и хрома (PtCr).
Покрытие: лекарство Паклитаксель (paclitaxel)
Технические характеристики: сплав платины и хрома обеспечивает отличную визуализацию и способствует точной установки стента, а также изучению структуры после имплантации.Кроме того, улучшены механические каркасные функции одновременно с уменьшением толщины стента (всего 81 мкм).
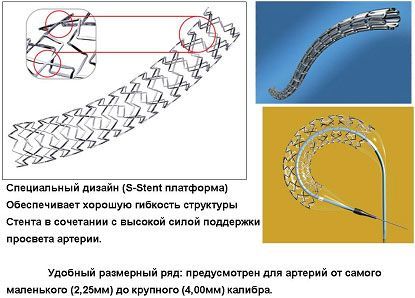
Дизайн стента: двойная синусоида с присутствием закрытых и открытых ячеек для оптимального сочетания гибкости и радиальной упругости (каркасной функции).
Отдаленные результаты : стент очень хорошо изучен в многочисленных сравнительных исследованиях. Более 1200 пациентов из 90 клиник мира изучены в исследование PERSEUS, где было выявлено снижение частоты повторных операции (5,5%) и тромбозов стентов (0,3%) в сравнении со стентами предыдущего поколения. В сосудах маленького диаметра (2,25мм) taxuselementобеспечивает меньший объем образования тканей, что уменьшает частоту повторных сужений внутри стента в этой сложной категории пациентов в сравнении с ранними типами стентов (7,3% против 19,3%).
Стенты 2-го поколения:
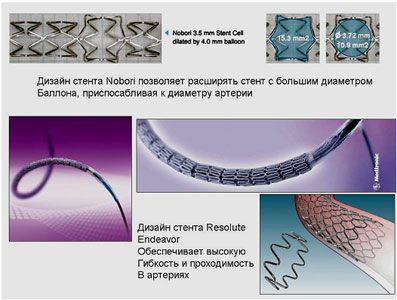
- NOBORI (производитель — компания ТЕRUMO (Япония)
- ENDEAVOR RESOLUTE (производитель — компания MEDTRONIC (США)
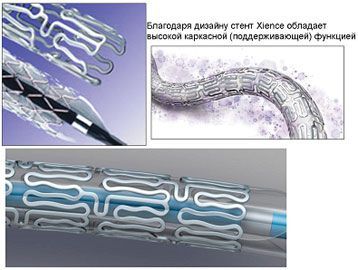
- XIENCE V (производитель — компания ABBOT VASCULAR (США)
Состав: материал 316L — нержавеющая медицинская сталь (Nobori стент)
Покрытие:
- Nobori стент имеет специальное покрытие, которое обеспечивает точное и дозированное во времени высвобождение лекарственного препарата (biolimus A9).
- Стент Endeavor покрыт нецитотоксичным лекарством Zotarolimus с инновационной технологией доставки препарата BioLinx.
- Стент XienceV покрыт одним из самых эффективных лекарственных средств на сегодняшний день — Эверолимусом. Обладает очень высоким поддерживающим (каркасным) свойством. Примерно через 180 дней полностью завершается процесс вживления в стенку сосуда.
Отдаленные результаты: Получены в результате многочисленных исследований по всем стентам второго поколения (более 15.000 пациентов). Случай тромбозов стентов не превышают 0.5% в год. Повторные сужения (рестенозы) в области установки стентов ограничиваются однозначным числом (до 10%). Отмечена также низкая чистота повторных операций в течение 5-ти лет (до 10-12 %).
Отдаленные результаты: получены в результате многочисленных исследований по всем стентам третьего поколения. На сегодняшний день результаты применения стентов 3-го поколения оценены в самой большой когорте пациентов (более 15 000 пациентов). Случай трамбозов стентов не превышает 0.2% в год. Частота повторных сужений (рестенозы) в области установки стентов очень низкая — около 3%. Соответственно отмечена также низкая частота повторных операций в течение 3-х лет (до 5%). Такие результаты неизменно показывают ВСЕ (!) исследования, проведенные с целью оценки результатов стентов 3-го поколения.
SYNERGY (производитель компания BOSTON SCIENTIFIC (США)
Состав: материал металл Р 6051-сплав платины и хрома.
Покрытие: Стент SYNERGY имеет уникальное биорассасываемое покрытие толщиной всего 4 мкм (человеческий волос -70 мкм) и только со стороны стенки сосуда, что улучшает заживление (поверхность стента со стороны просвета сосуда быстро и легко покрывается собственными тканями). В покрытие используется один из эффективных лекарственных препаратов (эверолимус).
Лекарство и рассасываемое покрытие рассчитаны на 3 месяца действия. Это ровно столько, сколько нужно для завершения заживления в стенке артерии. Стент SYNERGY самый тонкий (4 мкм) из известных на сегодняшний день стентов, что обеспечивает превосходную гибкость, проходимость в сочетании с оригинальным дизайном стента, придающим большую поддерживающую способность структуре стента.
Отдаленные результаты: Получены в результате более чем 10 исследований в разных странах на выборке из более чем 10.000 пациентов с имплантированными стентами SYNERGY. Стент показал уменьшение риска и частоты осложнений (тромбоз) в сравнении с другими типами стентов предыдущих поколений. Через 12 мес частота повторных операций составила всего 2,5 %, частота тромбозов стента — всего 0,4 %.
Источник
Биорезорбируемые коронарные стенты
Закарян Н.В., Панков А.С.
В поисках идеального коронарного стента ученые всего мира постоянно разрабатывают новые идеи. Так, с целью снижения риска позднего тромбоза были разработаны стенты с биодеградируемым покрытием на основе полимолочной кислоты. Полимолочная кислота (ПМК), она же полилактид, PLA и ее форма poly-L-lactide (PLLA) — биоразлагаемый, биосовместимый, термопластичный, алифатический полиэфир, мономером которого является молочная кислота. Сырьем для производства служат возобновляемые ресурсы, такие как кукуруза и сахарный тростник. В природных условиях срок разложения составляет от 2-х месяцев до 2-х лет. К подобным устройствам относятся стенты “Biomatrix” фирмы “Biosensors”, “Nobori” (“Terumo”), “Orsiro” (“Biotronik”). Особенностью этих металлических стентов является покрытие полимером с цитостатическим препаратом биолимусом А9. Даный препарат обеспечивает своевременную эндотелизацию стентированного участка артерии, а управляемое размывание полимера при этом уменьшает пролиферативный ответ в острый период формирования рестеноза. Исследования FUTURE I и FUTURE II показали безопасность и надежность этих стентов (1).
Следующим этапом стало появление на свет целиком биорезорбируемых (биодеградируемых) стентов (2-5). Идея создателей заключалась в том, что материал, из которого изготавливается каркас стента, был способен в течение нескольких месяцев после имплантации полностью раствориться, при этом выполнив свою функцию. Как и другие изобретения, биорезорбируемые стенты (“скаффолды”), вначале скептически воспринимались многими специалистами. Однако уже первые результаты использования стента Igaki-Tamai, сделанного из полимолочной кислоты, показали их высокую эффективность (6,7). Так, в работе Tsuji и соавт. показано, что после имплантации скаффолда Igaki-Tamai 50 пациентам, госпитальных осложнений и летальных исходов отмечено не было. Через год после вмешательства частота развития значимого рестеноза составила 19%, во всех случаях проблемы в отдаленном периоде были корригированы эндоваскулярно; через 4 года частота повторных рестенозов была минимальной (8).
В настоящее время для широкого использования одобрен только биорезорбируемый стент “Absorb” фирмы “Abbott”. За последние было проведено много исследований на тысячах пациентов, подтвердившие эффективность и безопасность данного скаффолда (3-5). Некоторые специалисты указывают, что при использовании стента “Absorb” частота тромбоза в отдаленном периоде несколько выше по сравнению с современными металлическими стентами с лекарственным покрытием, но большинство авторов считают, что это было связано с неправильным отбором пациентов (3). Также постепенно расширяются показания к использованию данного устройства – все чаще скаффолды “Absorb” имплантируют при острых инфарктах и сложных поражениях коронарных артерий (8).
Существуют также металлические биорезорбируемые стенты, чаще всего изготовленные из магния. Например, в исследовании PROGRESS оценивались результаты использования нового магниевого стента AMS (Absorbable Metal Stent) фирмы “Biotronik” (Германия) (9). Всего данный скаффолд был имплантирован 63 пациентам со стабильной стенокардией напряжения. Осложнений и летальных исходов на госпитальном этапе отмечено не было. К сожалению, через 4 месяца частота рестеноза составила целых 38%. Тем не менее, в настоящее время ученые продолжают разработку металлических биорезорбируемых стентов с целью улучшить результаты их использования.
1. Grube E. et al. Everolimus for stent-based intracoronary applications // Rev Cardiovasc Med. – 2004. – vol. 5(Suppl 2). — P3-8.
2. Ellis S. et al. Everolimus-Eluting Bioresorbable Scaffolds for Coronary Artery Disease // N Engl J Med. – 2015. – Vol. 373. – P.1905-1915
3. Serruys PW, Chevalier B, Dudek D et al. A bioresorbable everolimus-eluting scaffold versus a metallic everolimus-eluting stent for ischaemic heart disease caused by de-novo native coronary artery lesions (ABSORB II): an interim 1-year analysis of clinical and procedural secondary outcomes from a randomized controlled trial // Lancet. – 2015. – Vol. 385(9962). – P. 43-54.
4. Cassese S, Byrne RA, Ndrepepa G et al. Everolimus-eluting bioresorbable vascular scaffolds versus everolimus-eluting metallic stents: a meta-analysis of randomised controlled trials // Lancet. – 2016. – Vol. 387. – P. 537-544.
5. Kereiakes DJ, Ellis SG, Popma J. et al. Evaluation of a fully bioresorbable vascular scaffold in patients with coronary artery disease: design of and rationale for the ABSORB III randomized trial // Am Heart J. – 2015. – Vol. 170(4). P. 641-651.
6. Tamai H. et al. Initial and 6-month results of biodegradable polylactic acid coronary stents in humans // Circulation. – 2000. – Vol.102. – P. 399-404.
7. Tsuji T, Tamai H, Igaki K. Biodegradable stents as a platform to drug loading // Int J Cardiovasc Intervent. – 2003. – Vol. 5(1). P. 1-6.
8. Costopoulos C, Latib A, Naganuma T. et. al. Comparison of early clinical outcomes between ABSORB bioresorbable vascular scaffold and everolimus-eluting stent implantation in a real-world population // Catheter Cardiovasc Interv. – 2015. – Vol. 85(1). – E10-5.
9. Waksman R, Erbel R, Di Mario C. et al. PROGRESS-AMS (Clinical performance angiographic results of coronary stenting with Absorbable Metal Stents) Investigators. Early- and long-term intravascular ultrasound and angiographic findings after bioabsorbable magnesium stent implantation in human coronary arteries // JACC Cardiovasc Interv. – 2009. – Vol. 2(4). P. 312-320.
Источник