Концепция основных лекарственных средств
Лекарственные средства (ЛС) относятся к числу наиболее востребованных продуктов, поэтому совсем не удивительно то, что люди очень чувствительны ко всему тому, с чем связано потребление ЛС: их качеству, безопасности, доступности и стоимости. И именно поэтому существующие в большинстве стран проблемы, связанные с ненадлежащим потреблением ЛС и недостаточным лекарственным обеспечением, настолько болезненны для общества.
Однако если в развитых странах основной проблемой является избыток препаратов на рынке и обусловленное этим их нерациональное (избыточное) потребление, а соответственно и увеличение расходов здравоохранения на их оплату, то в развивающихся существует противоположная проблема. Жители этих стран испытывают острую нехватку ЛС, им недоступны многие препараты не только вследствие их высокой стоимости, но и просто из-за элементарного их отсутствия; в развивающихся странах несовершенна система распределения ЛС; не менее часто у пациентов отсутствует доступ к новым и инновационным препаратам; развивающиеся страны также чаще сталкиваются с проблемой контрафактных и некачественных ЛС. В то же время если в развитых странах существует отлаженная система возмещения пациентам стоимости ЛС, то в государствах с ограниченными ресурсами, в том числе и в Украине, бoльшая часть расходов на фармакотерапию ложится на плечи самих пациентов. По данным ВОЗ, расходы на лечение в странах с ограниченным бюджетом, выделяемым на здравоохранение, значительно выше, чем в государствах с развитой экономикой. Так, если в последних они составляют 15–30% общих расходов на нужды здравоохранения, то в странах с переходной экономикой они достигают 30%, а в развивающихся — 66%. При этом в странах с самым низким национальным доходом расходы на ЛС составляют бoльшую часть расходов семейного бюджета, затрачиваемых на лечение (ВОЗ, 2007). В то же время в результате нерационального применения ЛС доступ пациентов ко многим жизненно важным (называемым еще основными) лекарственным средствам до сих пор остается ограниченным. ВОЗ отмечает, что в странах с ограниченными финансовыми ресурсами 50–90% расходов на фармакотерапию пациенты оплачивают за счет личных средств. Именно поэтому, по мнению экспертов ВОЗ, рациональное применение ЛС, в частности таких, которые были бы эффективными и безопасными, но при этом недорогими, будет способствовать значительному снижению заболеваемости и спасет миллионы жизней.
Опыт многих стран свидетельствует, что наиболее эффективным способом экономного расходования бюджетных средств, выделяемых на фармакотерапию, является рациональный отбор ЛС медицинскими учреждениями и их правильное применение.
Для этого еще в середине 1970-х годов ВОЗ приступила к разработке концепции основных ЛС, и в 1977 г. был опубликован первый Примерный перечень основных ЛС, в который было включено 208 препаратов. В течение 30 лет с момента появления первого Примерного перечня основных ЛС 156 из 193 развитых и развивающихся государств — членов ВОЗ создали собственные перечни. По мнению ВОЗ, это позволило значительно повысить качество медицинской помощи и сэкономить средства национальных бюджетов здравоохранения. Этому также способствовало внедрение во многих странах формулярной системы, создание национальных формуляров.
Нынешний Примерный перечень основных ЛС, выпущенный ВОЗ в марте 2007 г., содержит 340 препаратов, предназначенных для лечения приоритетных патологических состояний, таких как малярия, туберкулез, состояний, связанных с репродуктивным здоровьем, и в возрастающих масштабах таких хронических заболеваний, как рак, сахарный диабет и ВИЧ/СПИД (с последним, 15-м изданием Примерного перечня основных ЛС на русском языке можно ознакомиться на сайте ВОЗ ( www.who.int ), а также на страницах «Еженедельника АПТЕКА» (см. № 47 (668) от 1 декабря 2008 г.).
Что же такое основные ЛС?
Основные ЛС – это ЛС, предназначенные для удовлетворения первоочередных потребностей населения в области здравоохранения. Эти ЛС отбирают на основе фактических данных, надлежащим образом учитывая их значимость для общественного здравоохранения, доказанной клинической эффективности, безопасности, качества, а также стоимости. В нормально функционирующих системах здравоохранения основные ЛС должны быть в наличии в любое время, в достаточном количестве, в соответствующих лекарственных формах, гарантированного качества, с достаточной информацией и по цене, доступной для каждого пациента и населения в целом (ВОЗ, 2007).
Концепция основных ЛС является главным звеном национальной лекарственной политики, поскольку она направлена на защиту прав пациентов и определяет приоритетные задачи в сфере лекарственного обеспечения и основные пути их решения.
В Украине основой национальной лекарственной политики является Государственная программа обеспечения населения лекарственными средствами на 2004–2010 годы ( zakon.rada.gov.ua ), утвержденная постановлением КМУ от 25.07.2003 г. № 1162 (изменения в которое, внесенные постановлением КМУ от 17.11.2008 г. № 955, приостановлены Указом Президента Украины от 03.12.2008 г. № 1139/2008).
Однако, как справедливо замечают многие, ни одна государственная система или система медицинского страхования не в состоянии возместить стоимость всех ЛС. Именно поэтому основа концепции основных ЛС состоит в применении ограниченного количества препаратов, тщательно отобранных с учетом клинических руководств, что способствует улучшению обеспечения ЛС, более правильному их назначению и снижению стоимости. Таким образом, использование основных ЛС, которые отобраны исходя из принципов терапевтической эффективности и рентабельности, позволяет повысить качество лечения и уменьшить финансовые затраты. Приобретая меньшее число наименований препаратов, но в большем количестве, становится возможным добиться значительной экономии на макроэкономическом уровне благодаря усилению ценовой конкуренции. С уменьшением количества наименований препаратов облегчается контроль их качества, упрощаются условия приобретения, хранения, распределения и реализации. Кроме того, появляется возможность сделать информацию о ЛС более понятной и доступной. При уменьшении количества наименований ЛС врачу легче отслеживать случаи взаимодействия препаратов и побочных явлений.
Таким образом, ключевые вопросы политики основных ЛС включают несколько аспектов. Так, доступ к основным ЛС зависит от 4 факторов: рационального выбора, доступности по цене, стабильного финансирования и надежной системы здравоохранения; следующий аспект – выбор основных ЛС, желательно с учетом стандартизованных клинических руководств, является важнейшим шагом в обеспечении доступа к медицинской помощи и в содействии рациональному использованию ЛС как специалистами, так и самими пациентами; официальное утверждение концепции основных ЛС определяет приоритеты для деятельности правительства в фармацевтическом секторе в целом и для снабжения ЛС в государственном секторе в частности, включая льготное получение препаратов в рамках системы медицинского страхования; для составления Национального перечня основных ЛС необходимо создание национального комитета, проведение систематических и прозрачных процедур и использование научно обоснованных клинических руководств.
Тщательный выбор ограниченного количества основных ЛС обеспечивает более качественную медицинскую помощь, более качественное производство ЛС, более эффективное использование ресурсов здравоохранения.
Согласно данным ВОЗ, клинические руководства и перечни основных ЛС оказывают влияние на наличие и надлежащее использование препаратов в системе здравоохранения, что приобретает еще большую актуальность в условиях ограниченных ресурсов, когда могут происходить перебои с ЛС в госсекторе. В таких обстоятельствах меры по обеспечению регулярных поставок основных ЛС приведут к реальному улучшению показателей здоровья и повысят доверие населения к медицинской помощи.
Критериями выбора ЛС для включения в такой перечень являются их применение для профилактики и лечения приоритетных заболеваний, доказанная эффективность и безопасность, учет соотношения стоимости и эффективности этих препаратов.
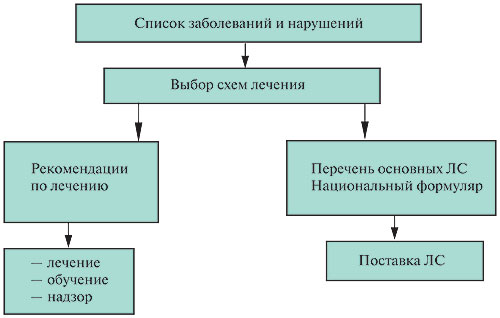
Процедура выбора препарата в перечень основных ЛС в первую очередь зависит от его использования в рекомендованных ВОЗ схемах лечения (схема). После включения в схемы лечения приоритетных заболеваний препарат вносится в перечень основных ЛС согласно АТС-классификации с указанием международного непатентованного названия, лекарственной формы и дозировки. В Формулярное руководство включают указанные сведения для всех препаратов перечня, а также информацию об условиях отпуска, основном фармакологическом действии и показаниях, противопоказаниях, возможных побочных эффектах, сведения о фармакодинамике и фармакокинетике, об условиях хранения и сроках, торговые названия, а иногда и стоимость ЛС. Важно также отметить, что Примерный перечень основных ЛС, принимаемый ВОЗ, носит рекомендательный характер и не является регуляторным документом, несущим какую-либо разрешительную или обязующую функцию.
 |
Каждое государство должно разработать собственный национальный перечень основных ЛС, который приспособлен к реалиям конкретной страны, уровню заболеваемости, ресурсам и т.д. Примерный перечень основных ЛС ВОЗ – это определенная универсальная модель минимальных потребностей базисной системы здравоохранения. Другими словами, это – авторитетнейший экспертный вывод, на международном уровне устанавливающий определенные границы, расставляющий определенные акценты на тех ЛС, наличие которых необходимо для действенного функционирования системы здравоохранения и эффективного оказания полноценной медицинской помощи.
В Украине Национальный перечень основных лекарственных средств и изделий медицинского назначения был утвержден постановлением КМУ от 29.03.2006 г. № 400 (с изменениями, внесенными согласно постановлениям КМУ от 30.05.2007 г. № 789 и от 09.07.2008 г. № 620) ( zakon.rada.gov.ua ), а совсем недавно были подготовлены и утверждены приказами МЗ Украины некоторые разделы Формулярного руководства лекарственных средств в Украине, которые, в частности, представлены на сайте Государственного фармакологического центра ( www.pharma-center.kiev.ua ).
По большому счету перечень основных ЛС должен являться не только исходным пунктом для определения стоимости схем лечения и потребности в препаратах, но и краеугольным камнем качества предоставляемой медико-санитарной помощи. Приобретет ли когда-либо концепция основных ЛС это значение в нашей стране – покажет время.
Источник
Концепция основные лекарственные средства
Автор: К.С.ДАВЫДОВА, филиал «Клиническая фармакология» НЦ БМТ РАМН
Большая часть лекарственных средств ( ЛС ) на современном фармрынке являются воспроизведенными (генерическими) препаратами. Согласно данным розничного аудита (IMS Health и DSM Group) доля дженериков в настоящее время составляет от 77 до 88% в натуральном выражении [5] (существуют данные и про долю в 95% [9], однако ее достоверность вызывает сомнения), при этом согласно прогнозам эта доля будет неуклонно расти. По объему генерического сектора Россия занимает 3 место в мире после Китая и Индии [2,3]. В то же время структура рынка стран большой семерки формируется следующим образом: в США — 12% дженериков, в Японии — 30%, в Германии — 35%, во Франции — 50%, в Англии — 55%, в Италии — 60%, в Канаде — 64% (рис. 1) [8].
Среди препаратов, которые ежегодно регистрируются в России, отмечается значительно большее количество дженериков, чем оригинальных препаратов. Отдельные оригинальные препараты имеют значительное количество воспроизведенных ЛС. Так, оригинальное лекарственное средство Вольтарен (действующее вещество – диклофенак натрия) сегодня имеет 207 дженериков, зарегистрированных к медицинскому применению. Также в РФ зарегистрировано около 150 генерических ЛС эналаприла, около 100 — нифедипина, атенолола, ципрофлоксацина и порядка 50 – нитроглицерина, аспирина и парацетамола (причем количество комбинированных генерических последних двух ЛС превышает 300) [1,4]. В ряде стран с развитой системой контроля качества, эффективности и безопасности ЛС, число дженериков инновационного препарата в большинстве случаев не превышает 4-5 [10,19].
Генерические ЛС выводятся на рынок после истечения срока патентной защиты. Они должны полностью соответствовать оригинальному продукту по составу действующих веществ (вспомогательные вещества могут быть иными) и лекарственной форме, соответствовать фармакопейным требованиям, быть произведенными в условиях GMP. В Федеральном законе о лекарственных средствах №86-ФЗ от 1998 г. дается определение воспроизведенных ЛС: «воспроизведенные лекарственные средства — лекарственные средства, поступившие в обращение после истечения срока действия исключительных патентных прав на оригинальные лекарственные средства». Однако такое определение не характеризует дженерик как копию или аналог инновационного препарата. В новом Федеральном законе «Об обращении лекарственных средств» №61-ФЗ от 2010 г. смысл термина раскрывается более полно, согласно современным международным рекомендациям: «воспроизведенное лекарственное средство — лекарственное средство, содержащее такую же фармацевтическую субстанцию или комбинацию таких же фармацевтических субстанций в такой же лекарственной форме, что и оригинальное лекарственное средство, и поступившее в обращение после поступления в обращение оригинального лекарственного средства».
Воспроизведенные ЛС имеют ряд равнозначных общеупотребляемых синонимов – «генерики», «дженерики», «генерические лекарственные средства», «многоисточниковые (мультиисточниковые) лекарственные средства» [8,9], однако согласно Федеральному закону № 61-ФЗ именно термин «воспроизведенные лекарственные средства» должен применяться в первую очередь. В то же время Всемирная организация здравоохранения в качестве основного понятия таких ЛС рекомендует употреблять термин «многоисточниковые лекарственные средства» (multisource drugs) [20]. Оригинальное (инновационное) лекарственное средство – это ЛС, которое было впервые зарегистрировано на основе полной документации в отношении его качества, безопасности и эффективности, защищенное патентом на срок до 20 лет [11].
Основными характеристиками оригинального ЛС являются: длительность разработки (10-15 лет) на основании отбора действующего вещества из значительного количества молекул; фармакологический эффект, токсичность, мутагенность и тератогенность которого проверены в доклинических исследованиях на животных; прохождение всех фаз клинических исследований в соответствии со стандартами GСP.
Несмотря на то что инновационное и воспроизведенное ЛС содержат одно и то же действующее вещество в одинаковой дозировке и лекарственной форме, эффективность и безопасность генерических препаратов может существенно различаться. Основными причинами таких различий могут быть фармацевтическая технология производства лекарственного препарата, вспомогательные вещества (неактивные ингредиенты, наполнители, консерванты, красители и др.), их природа и количество, полиморфизм, солевая форма, упаковка препарата, условия его хранения и транспортировки. Из-за этих отличий эффективность генерических препаратов и выраженность их побочных эффектов может сильно варьировать.
При этом следует отметить, что стоимость воспроизведенного ЛС ниже, чем оригинального, что определяется рядом причин. Для этого необходимо рассмотреть, из чего складывается стоимость оригинальных ЛС и дженериков. 80% стоимости оригинального ЛС составляет стоимость исследований эффективности и безопасности препарата, а 20% стоимости – это стоимость синтеза лекарственного вещества. Процесс создания оригинального ЛС является очень длительным и дорогостоящим. Сначала создается молекула, потом она оценивается в исследованиях на клетках и тканях, затем на животных. После этого следуют три этапа клинических исследований на здоровых добровольцах и пациентах. После завершения клинических исследований ЛС проходит регистрацию. Исследование оригинального ЛС продолжается и после регистрации. С соблюдением правил GCP проводятся и пострегистрационные исследования [23].
Известно, что только 1 из 5 000 молекул доходит до рынка в виде ЛС. Этот путь продолжается 12-15 лет, его стоимость составляет от 800 млн. до 1 млрд. долл. Прибыльными являются только 1-2 из вновь созданных ЛС [8]. Объяснением более низкой стоимости генерических ЛС являются: отсутствие клинических исследований; отсутствие масштабных доклинических исследований фармакологической активности, поисковых исследований; отсутствие изучения полного профиля безопасности.
Несмотря на широкое использование понятия эквивалентность, «эквивалентности» дженериков как термина не существует. Всемирная организация здравоохранения предлагает применять термин «взаимозаменяемость» (interchangeability) воспроизведенных лекарственных препаратов [23]. Взаимозаменяемое генерическое ЛС – это терапевтически эквивалентное генерическое ЛС, которым можно заменить препарат сравнения в клинической практике [22]. Видов «эквивалентности» воспроизведенных ЛС выделяют несколько – терапевтическая, фармацевтическая, биологическая, а также т.н. «эквивалентность in vitro» (in vitro equivalence), введенная в употребление в документе «WHO Technical Report Series 937. WHO Expert Committee on Specifications for Pharmaceutical Preparations (2006). Annex 7. Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability» [23].
Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями инструкции по применению [7,22]. Терапевтическая эквивалентность означает, что два препарата обеспечивают одинаковый терапевтический эффект и безопасность. Терапевтически эквивалентные лекарственные препараты должны отвечать следующим требованиям: иметь доказанную эффективность и безопасность; быть фармацевтически эквивалентными; быть биоэквивалентными; иметь сходные инструкции по применению; производиться в условиях стандарта GMP [6]. Доказанную клиническую эффективность и безопасность устанавливают на основании клинических исследований.
ЛС считаются фармацевтически эквивалентными, если они содержат одни и те же действующие вещества в одинаковом количестве и в одинаковой лекарственной форме и отвечают требованиям одних и тех же или сходных стандартов [1]. То есть фармацевтическая эквивалентность – это полное соответствие состава и лекарственной формы препаратов. Для некоторых лекарственных форм фармацевтическая эквивалентность будет обеспечивать терапевтическую эквивалентность и, соответственно, взаимозаменяемость двух препаратов (препараты для местного применения, порошки для изготовления растворов, инъекционные растворы и некоторые другие) [23].
Отдельно стоит выделить фармацевтическую альтернативность ЛС. Лекарственные средства являются фармацевтически альтернативными, если они содержат одинаковое количество одной и той же активной субстанции (субстанций), но различаются по лекарственной форме (например, таблетки и капсулы) и/или по химической форме (различные соли, эфиры) [1].
Оценка биоэквивалентности ЛС является основным видом медико-биологического контроля воспроизведенных (генерических) ЛС, не отличающихся лекарственной формой и содержанием действующих веществ от соответствующих оригинальных ЛС. Биоэквивалентность ЛС обозначает их одинаковую биодоступность. Под биодоступностью понимают количество неизмененного действующего вещества, достигающего системного кровотока (степень всасывания) относительно исходной дозы ЛС. Исследования биоэквивалентности позволяют сделать обоснованные заключения о качестве сравниваемых препаратов по относительно меньшему объему первичной информации и в более сжатые сроки, чем при проведении клинических исследований [17,18,21].
В некоторых международных руководствах введено понятие регуляторной процедуры «биовейвер», в соответствии с которой определение взаимозаменяемости генерических ЛС проводится на основании оценки их биофармацевтических свойств и эквивалентности in vitro (изучение сравнительной кинетики растворения) либо другими методами in vitro в качестве альтернативы исследованиям биоэквивалентности in vivo при их государственной регистрации [16].
Самое главное, к чему надо стремиться, — дженерики, как и инновационные (оригинальные) препараты, должны отвечать требованиям, предъявляемым в рамках Общего (или единого) технического документа (CTD): эффективность, безопасность, качество 13, поэтому весь объем исследований должен быть достаточным для подтверждения данных требований.
Литература
1. Арзамасцев А.П., Дорофеев В.Л. Эквивалентность воспроизведенных лекарственных средств: фармацевтические аспекты. // Ведомости НЦЭСМП. – М., 2007. – №1. – С. 27-35.
2. Баула О.Ю. Современные регуляторные требования к исследованиям и регистрации генерических лекарственных средств. – М., «Фармсодружество», 2007.
3. Белоусов Ю.Б. Дженерики – мифы и реалии. «Ремедиум». – 2003. — № 7–8. — С. 4–9.
4. Верткин А.Л., О.Б.Талибов. Генерики и эквивалентность – что стоит за терминами. Неотложная терапия. — 2004; — № 1–2. – С.16–17.
5. Новикова Н.Н. // Фармацевтический Вестник. – М., 2008. – №4. – С. 4.
6. Рудык Ю.С. К вопросу о терапевтической эквивалентности лекарственных средств // Рациональная фармакотерапия. – Киев, 2007. — №2. – С. 40-48.
7. Семинар-тренинг ВОЗ по проведению теста растворения, взаимозаменяемости лекарственных средств и системе биофармацевтической классификации. // Аптека, — Киев, 2007. – № 31. – С. 10-17.
8. Талибов О.Б. Генерики и эквивалентность лекарственных препаратов. // Медицинская газета «Здоровье Украины». – Киев, 2008. – №5. – С. 12-16.
9. Тарловская Е.И. Генерики и оригинальные препараты: взгляд практического врача. // Российский Медицинский Журнал. – М., 2008, – т. 16. – №5. – С. 30 – 35.
10. Чумак В.Т. Оборот лекарственных средств в Украине. Проблемы и перспективы. Материалы І Международной конференции «Клинические испытания лекарственных средств в Украине». — Киев, 2006.
11. Directive 2004/27/EC of the European Parliament and of the Council, Art. 10.1. – 2004.
12. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Quality M4Q (R1). – Geneva: ICH, 2002.
13. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Safety. M4S (R2). – Geneva: ICH, 2002.
14. ICH Harmonised Tripartite Guideline: The Common Technical Document for the Registration of Pharmaceuticals for Human Use: Efficacy. M4E (R1). – Geneva: ICH, 2002.
15. Interchangeability of multisource drug products containing highly variable drugs. WHO/FIP Training Workshop on Dissolution, Pharmaceutical Product Interchangeability and Biopharmaceuticals Classification System (BCS) — Kiev, 2007.
16. Yu G., Amidon J. Polli. Biopharmaceutics Classification System: The Scientific Basis for Biowaiver Extensions. // Pharmaceutical Research. – 2002. – Vol. 19, №. 7.
17. Chen M., Lesko L. Individual bioequivalence revisited. // Clin Pharmacokinet – 2001. – № 40: – pp. 701-706.
18. Chen M., Shah V., Patnaik R. Bioavailability and Bioequivalence: An FDA Regulatory Overview. // Pharmaceutical Research. – 2001. – Vol. 18, №. 12.
19. Laroche M., Merle L. Generic and brand-name drugs. Are different criteria sufficiently taken into account before granting market authorisation? // Acta Clin Belg Suppl. – 2006. – № 1: – pp. 48-50.
20. Multisource (Generic) Pharmaceutical Products: Guidelines on Registration Requirements to Establish Interchangeability. — WHO Technical Report Series, № 937. – WHO, 2006.
21. Quality of bioequivalence data. WHO workshop on assessment of bioequivalence data submitted to regulatory authorities – Kiev, 2009.
22. WHO Technical Report Series 937. WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
23. WHO Technical Report Series 937, annex 7 « Multisource (generic) pharmaceutical products: guidelines on registration requirements to establish interchangeability». WHO Expert Committee on Specifications for Pharmaceutical Preparations. – WHO, 2006.
Рисунок — в приложении
Файл: Загрузить (85 кбайт)
Источник


