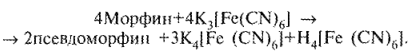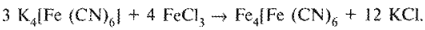- Количественное определение. Тема: «Контроль качества лекарственных средств, производных изохинолина.
- Методическая разработка теоретического занятия на тему «Контроль качества лекарственных средств, производных изохинолина»
- Дистанционное обучение как современный формат преподавания
- Химия: теория и методика преподавания в образовательной организации
- Биология и химия: теория и методика преподавания в образовательной организации
- Оставьте свой комментарий
- Подарочные сертификаты
- Производные изохинолина. Анализ лекарственных средств
Количественное определение. Тема: «Контроль качества лекарственных средств, производных изохинолина.
Тема: «Контроль качества лекарственных средств, производных изохинолина.
Контроль качества лекарственных средств, производных тропана»
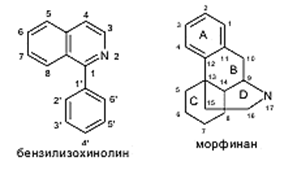
Широкое применение в медицине лекарственных веществ производных изохинолина связано с изучением алкалоидов мака снотворного. В млечном соке зеленых коробочек мака содержится около 25 алкалоидов. Важнейшие из них: морфин, кодеин, тебаин, наркотин, папаверин. Алкалоиды группы изохинолина (и лекарственные вещества, созданные на их основе) относятся, главным образом, к производным бензилизохинолина, морфинана. Морфинан относится к группе фенантренизохинолина:
Papaverini hydrochloridum.
Папаверина гидрохлорид.
Белый кристаллический порошок без запаха. Растворим в хлороформе, умеренно растворим в воде, мало растворим в спирте.
Drotaverini hydrochloridum (Nospanum).
Дротаверина гидрохлорид (Но-шпа).
Зеленовато-желтый кристаллический порошок со слабым запахом.
Папаверин впервые был выделен из опия, который содержит 0,4 – 1,5% этого алкалоида.
Подлинность.
1. Реакции окисления:
— нагревание папаверина с концентрированной серной кислотой – фиолетовое окрашивание;
— нагревание папаверина с концентрированной азотной кислотой – желтое окрашивание, переходящее в оранжевое;
— нагревание дротаверина с концентрированной серной кислотой в присутствии следов хлорида железа (III) приводит к появлению зеленого окрашивания, которое от добавления азотной кислоты переходит в коричнево-красное.
2. Реакция с реактивом Марки.
При взаимодействии с реактивом Марки возникает желтое окрашивание, переходящее в оранжевое. Дальнейшее добавление бромной воды и раствора аммиака приводит к образованию грязно-фиолетового осадка, растворяющегося в этаноле с образованием раствора окрашенного в фиолетовый или красно-фиолетовый цвет (реакция О.Н. Соболевой). Сущность реакции: образуется сульфат метиленбиспапаверина, который легко окисляется, приобретая окрашивание.
3. Каролиновая проба.
При проведении пробы к порошку папаверина гидрохлорида добавляют концентрированную серную кислоту, уксусный ангидрид и нагревают. Возникает ярко- желтое окрашивание с зеленой флуоресценцией:
Количественное определение.
1.Кислотно-основное титрование вневодной среде.
Среда – уксусный ангидрид+муравьиная кислота, титрант – 0,1М раствор кислоты хлорной HClO4. Для связывания хлорид-иона добавляют ртути (II) ацетат.
Количественное определение дротаверина гидрохлорида проводят также, как у папаверина гидрохлорида.
2. Алкалиметрия (при внутриаптечном контроле). Титруют щелочью по остатку кислоты хлороводородной.
Источник
Методическая разработка теоретического занятия на тему «Контроль качества лекарственных средств, производных изохинолина»
Новые аудиокурсы повышения квалификации для педагогов
Слушайте учебный материал в удобное для Вас время в любом месте
откроется в новом окне
Выдаем Удостоверение установленного образца:
Смоленское областное государственное бюджетное профессиональное образовательное учреждение «Вяземский медицинский колледж Е.О. Мухина»
Технологическая карта теоретического занятия
ТЕМА: Контроль качества лекарственных средств, производных изохинолина
УД или ПМ (МДК): ПМ. 02 «Изготовление лекарственных форм и проведение обязательных видов внутриаптечного контроля»
МДК 02.02. Контроль качества лекарственных средств.
методов и методик фармакопейного анализа конденсированных
гетероциклических соединений – производных изохинолина
способствовать развитию познавательного интереса обучающихся, внося в
содержание элементы новизны
использовать специальные приемы поддержания работоспособности
обучающихся, содействовать формированию нравственного воспитания
З1 — нормативно-правовую базу по изготовлению лекарственных форм и
З2 — порядок выписывания рецептов и требований;
З3 — требования производственной санитарии;
З4 — правила изготовления твердых, жидких, мягких, стерильных, асептических
З5 — физико-химические свойства лекарственных средств;
З6 — методы анализа лекарственных средств;
З7 — виды внутриаптечного контроля;
У1 — готовить твердые, жидкие, мягкие, стерильные, асептические
У2 — проводить обязательные виды внутриаптечного контроля качества
средств, регистрировать результаты контроля, упаковывать и оформлять
лекарственные средства к отпуску, пользоваться нормативной
Интеграционные связи УД, ПМ:
ОП.09. Органическая химия
Время – 2 часа (90 минут)
Место проведения – лекционный зал
Оснащение (технические средства): проектор
1. Беликов В.Г. Фармацевтическая химия.- М.: М ЕДпресс-информ , 2007
2.Фармацевтическая химия. Под ред. Арзамасцева А.П. – М.:
ГЭОТАР- Медиа, 2006.
1.Государственная фармакопея XII, М. «Медицина», 2007 г.
2.Машковский М.Д. Лекарственные средста. – 15-е изд., – М.: ООО
«Издательство Новая Волна», 2005.
3. Г осударственная фармакопея СССР: Вып. 1, ХI изд. , – М.: Медицина ,
4. Г осударственная фармакопея СССР: Вып. 2, ХI изд. , – М.: Медицина ,
— приветствие обучающихся, обращение внимания на внешний вид, санитарное состояние кабинета;
— сообщение темы, плана, целей занятия.
Введение (сообщение темы, плана, литературных источников, поставленных целей)
Тема: Контроль качества лекарственных средств, производных изохинолина
Цель: теоретическое обоснование для практического применения методов и методик фармакопейного анализа конденсированных гетероциклических соединений – производных изохинолина
Основная часть (изложение учебного материала по вопросам).
Характеристика и классификация производных изохинолина
Алколоиды, производные морфинана
Синтетические аналоги морфина
Заключительная часть (подведение итогов, ответы на вопросы)
Лекарственные вещества производные изохинолина подразделяются на группы:
1-бензилизохинолин морфинан апорфин
Производные 1– бензилизохинолина
Clorhidrat de papaverină
Получение . Алкалоид глауцин выделяют из травы мачка желтого – ( Glaucium flavum ) семейства маковых – Papaveraceae.
УФ-спектр – максимум поглощения при 300 нм (растворитель вода);
Реакция с реактивом Марки – появляется интенсивное зеленое окрашивание, которое последовательно переходит в сине-зеленое, сиреневое, а затем в вишневое;
Реакции с общеалкалоиднами реактивами (реактивы Драгендорфа и Майера);
Выделение основания и определение т. пл. 115-119 0 С;
метод неводного титрования в смеси ледяной уксусной кислоты и ртути ацетата ( II ) (индик. кристаллический-фиолетовый). Титровать можно и без добавления ртути ацетата ( II ), нов таком случае в качестве растворителя используют смесь муравьиной кислоты и уксусного ангидрида (1:10);
может быть выполнено косвенным комплексонометрическим методом, основанном на осаждении глауцина раствором иодида кадмия в иодиде калия (реактив Марме). Избыток реактива оттитровывают раствором трилона Б с использованием индикатора кислотного хром темно-синего;
фотометрическое определение глауцина выполняют, используя реакции с фосфорномолибденовой и азотной кислотами, а также с реактивом Марки.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
Курс профессиональной переподготовки
Химия: теория и методика преподавания в образовательной организации
Курс профессиональной переподготовки
Биология и химия: теория и методика преподавания в образовательной организации
Международная дистанционная олимпиада Осень 2021
Номер материала: ДБ-292540
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Около 50% россиян поддерживают использование цифровых технологий в школе
Время чтения: 1 минута
Большинство учителей считают, что поступить на бюджет без репетитора не получится
Время чтения: 1 минута
В ОНФ назвали допустимые ограничения на внешний вид школьников
Время чтения: 1 минута
В пяти регионах России протестируют новую систему оплаты труда педагогов
Время чтения: 2 минуты
Студент устроил стрельбу в Пермском государственном университете
Время чтения: 1 минута
Число бюджетных мест на IT-направлении к 2024 году увеличат вдвое
Время чтения: 2 минуты
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Источник
Производные изохинолина. Анализ лекарственных средств
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
ПРОИЗВОДНЫЕ ИЗОХИНОЛИНА
Широкое применение в медицине производных изохинолина связано с изучением алкалоидов мака снотворного. В млечном соке зеленых коробочек мака содержится около 25 алкалоидов: морфин, кодеин, тебаин, наркотин, папаверин и др. Алкалоиды группы изохинолина (и лекарственные вещества, созданные на их основе) относятся главным образом к производным бензилизохинолина, морфинана и апорфина. Морфинан и апорфин относятся к группе фенантренизохинолина:
Производные бензилизохинолина
К данной группе относятся папаверина гидрохлорид и дротаверина гидрохлорид (являющийся производным 1,2,3,4-тетрагидроизохинолина) (табл. 61).
Папаверина гидрохлорид — соль слабого азотистого основания, не растворимого в уксусной кислоте. Поэтому при добавлении к раствору препарата раствора ацетата натрия выделяется осадок основания. Это испытание позволяет отличить папаверина гидрохлорид от солей более сильных оснований.
Папаверин взаимодействует с общеалкалоидными осадительными реактивами.
Восстановительные свойства папаверина гидрохлорида объясняются наличием в структуре 2 ароматических фрагментов, связанных метиленовой группой, а также 4 метоксидных групп. Лекарственное вещество легко окислятся на свету и в присутствии примеси ионов тяжелых металлов. Первыми продуктами окисления являются спирт папаверинол и кетон папаверальдин (окисление происходит по метиленовому фрагменту).
При добавлении к папаверину гидрохлориду сильных окислителей и последующем нагревании образуются различно окрашенные продукты. Так, взаимодействие с кислотой азотной концентрированной приводит к появлению желтого окрашивания, переходящего в оранжево-красное при нагревании. Нагревание с концентрированной Н2SО4 приводит к образованию продукта, окрашенного в фиолетовый цвет:
Известны и другие реакции окисления папаверина. При взаимодействии с реактивом Марки возникает желтое окрашивание, переходящее в оранжевое. Дальнейшее добавление бромной воды и раствора аммиака приводит к образованию грязно-фиолетового осадка, растворяющегося в этаноле с образованием раствора, окрашенного в фиолетовый или красно-фиолетовый цвет (реакция О.Н. Соболевой).
Одной из наиболее известных реакций на папаверин, включенной в некоторые национальные фармакопеи, является каролиоевая проба: к порошку папаверина гидрохлорида добавляют концентрированную Н2SО4, уксусный ангидрид и нагревают. Возникает ярко-желтое окрашивание с зеленой флюоресценцией:
Количественное определение папаверина гидрохлорида проводят в среде уксусного ангидрида и муравьиной кислоты; титрант – 0,1 М раствор кислоты хлорной.
Дротаверина гидрохлорид является синтетическим спазмолитиком, близким по химическому строению к папаверину, но с более выраженными спазмолитическими свойствами. Молекулу дротаверина можно рассматривать как продукт конденсации 6,7-диэтокситетрагидроизохинолина и 3,4-диэтоксибензальдегида. Препарат имеет характерный спектр поглощения в УФ-области.
Дротаверин проявляет более выраженные основные свойства, чем папаверин, поэтому для выделения основания из раствора препарата следует добавить раствор щелочи.
Как и папаверин, дротаверин обладает выраженными восстановительными свойствами. При добавлении к навеске препарата концентрированной Н2SО4 с дальнейшим добавлением капли разведенной азотной кислоты возникает темно-коричневое окрашивание.
Количественное определение дротаверина гидрохлорида проводят так же, как и папаверина гидрохлорида.
Производные фенантренизохинолина
Большинство лекарственных веществ этой группы относится к подгруппе морфинана (табл. 62). К подгруппе апорфина относится апоморфина гидрохлорид.
Производные морфинана
Морфинан является частично гидрированным октагидрофенантренизохинолином. Сочетание циклов А,В,С образует частично гидрированный фенантрен; С,D — гидрированный изохинолин; цикл D – пиперидин.
У морфина появляется еще один цикл, образованный эпоксигруппой и соседними атомами углерода. Наличие 5 асимметрических атомов углерода (5,6,9,13,14) придает соединению оптическую активность.
Кислотно-основные свойства морфина объясняются наличием третичного атома азота (центр основности) и фенольного гидроксила (центр кислотности). Основные свойства морфина выражены слабее, чем у аммиака, а кислотные – несколько сильнее, чем у фенола.
ГФ регламентирует как одно из испытаний подлинности морфина гидрохлорида взаимодействие его раствора с раствором аммиака (выпадает белый осадок основания). Дальнейшее прибавление раствора натрия гидроксида приводит к растворению осадка (образование фенолята).
Как и соли других оснований, морфина гидрохлорид взаимодействует с общеалкалоидными осадительными реактивами.
Выраженные восстановительные свойства обусловлены принадлежностью морфина к частично гидрированной системе фенантрена, а также наличием фенольного гидроксила и вторичной спиртовой группы.
Растворы морфина гидрохлорида очень легко окисляются, особенно на свету и в щелочной среде. Наибольшая устойчивость растворов препарата наблюдается при pH 2,5.
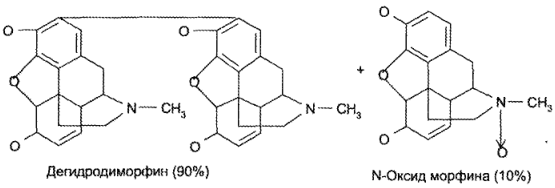
При свободном окислении морфина гидрохлорида образуются дегидродиморфин (псевдоморфин) и N-оксид морфина в соотношении 9:1.
Взаимодействие морфина гидрохлорида и других препаратов группы морфинана с сильными окислителями приводит к образованию различно окрашенных продуктов окисления.
ГФ в качестве испытаний подлинности морфина гидрохлорида приводит реакции препарата с реактивом Марки и с раствором молибдата аммония в концентрированной Н2SО4 (реактив Фреде). При взаимодействии морфина с реактивом Марки образуется пурпурное окрашивание, переходящее в фиолетовое:
В результате взаимодействия препарата с реактивом Фреде появляется фиолетовое окрашивание, переходящее в синее и (при стоянии) в зеленое.
Известны и другие (неофицинальные) реакции морфина гидрохлорида с различными окислителями. Так. при взаимодействии е реактивом Эрдмана (смесь концентрированных серной и азотной кислот) образуется продукт красного цвета:
Окисление морфина реактивом Манделина (раствор ванадата аммония в концентрированной Н2SО4) приводит к образованию продукта фиолетового цвета.
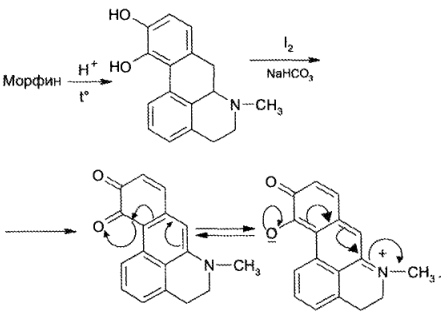
Окисление морфина раствори йода (реакция Пеллагри) проходит в 2 стадии. На 1-й морфин переводят в апоморфин нагреванием с концентрированной Н2SО4. Затем кислоту нейтрализуют и добавляют раствор йода и натрия гидрокарбонат. В результате образуется мезомерно стабилизированный красного цвета о-хинон:
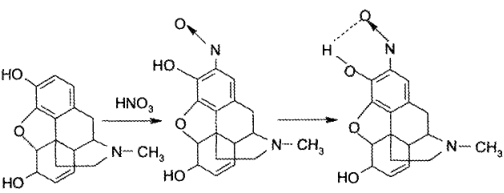
Реакция морфина с кислотой азотной концентрированной приводит к образованию оранжево-красного внутримолекулярного хелата:
При добавлении к раствору препарата раствора калия гексацианоферрата (III) образуются псевдоморфин и калия гексацианоферрат (II):
Дальнейшее прибавление раствора железа (III) хлорида приводит к образованию берлинской лазури синего цвета:
Известны реакции морфина гидрохлорида и другими окислителями.
Наличием в молекуле морфина фенольного и вторичного спиртового гидроксилов обусловлены характерные для этих функциональных групп реакции. Так, при взаимодействии раствора препарата с раствором железа (III) хлорида появляется сине-фиолетовое окрашивание (образование комплексного соединения по фенольному гидроксилу), быстро исчезающее из-за окисления морфина реактивом.
Как и другие фенолы, морфин вступает в SE-реакции (галогенирование, азосочетание с солями диазония и др.).
Возможно окисление вторичного спиртового гидроксила до кетона с последующим образованием оксимов, гидразонов, семикарбазонов.
Морфин легко этерифипируется и по фенольному, и по вторичному спиртовому гидроксилам.
ГФ регламентирует также определение величины удельного вращения морфина гидрохлорида.
Количественное определение морфина гидрохлорида проводят методом кислотно-основного титрования в среде ледяной уксусной кислоты с добавлением ртути (II) ацетата.
Содержание кодеина в опии невелико, поэтому препарат получают полусинтетически — метилированием морфина. Особенностью кодеина, отличающей его от других алакалоидов и синтетических оснований, является растворимость в воде, с чем связаны выраженные основные свойства препарата.
Структурным сходством кодеина с морфином можно объяснить взаимодействие препаратов с одинаковыми окислителями. Но различие в окрашивании получающихся продуктов реакций позволяет различать эти препараты.
Реакция кодеина с реактивом Марки приводит к образованию сине-фиолетового окрашивания, усиливающегося при стоянии.
С концентрированной Н,SО4 в присутствия железа (III) хлорида как катализатора получается продукт синего цвета, переходящий после добавления небольшого количества разведенной азотной кислоты в красный.
При реакции кодеина с концентрированной азотной кислотой возникает оранжевое окрашивание, переходящее в желтое.
С реактивом Фреде кодеин реагирует с образованием фиолетового окрашивания, а с реактивом Эрдмана — красного.
Как и морфин, кодеин легко этерифииируется по вторичному спиртовому гидроксилу.
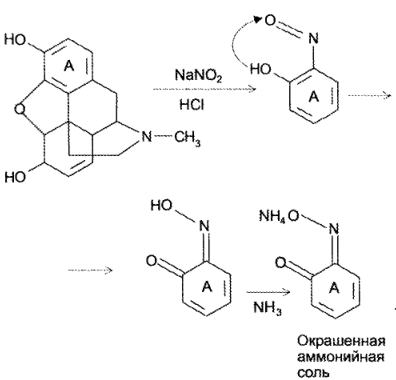
Специфической примесью в кодеине (по ГФ – до 0,0001 %) является морфин. Его примесь определяется в определенной навеске кодеина по реакции с раствором натрия нитрита в кислой среде и при последующем добавлении раствора аммиака. Интенсивность возникшего при реакции окрашивания сравнивают с окрашиванием эталонного раствора морфина после взаимодействия с теми же реактивами:
Кодеин, являющийся метиловым эфиром морфина по фенольному гидроксилу, в реакцию с натрия нитритом не вступает.
Количественное определение кодеина — ацидиметрия. Кодеин отличается от многих алкалоидов и синтетических оснований не только растворимостью в воде, но и силой основности. Значение pH водного раствора препарата находится в пределах 9,0, Это позволяет определять количественно кодеин методом кислотно-основного титрования в водной среде. Титрант — 0,1 М раствор кислоты хлороводородной, индикатор — метиловый красный.
Кодеина фосфат количественно определяют методом кислотноосновного титрования в неводной среде (растворитель – кислота уксусная ледяная; титрант — 0,1 М кислоты хлорной).
Этилморфина гидрохлорид анализируется в тех же условиях, что и морфина гидрохлорид и кодеин. При взаимодействии препарата с концентрированной Н2SО4 в присутствии железа (III) хлорида как катализатора возникает зеленое окрашивание, переходящее в фиолетово-синее, а при добавлении 1 капли кислоты азотной разведенной — в красное.
Синтетические аналоги морфина по фармакологическому действию
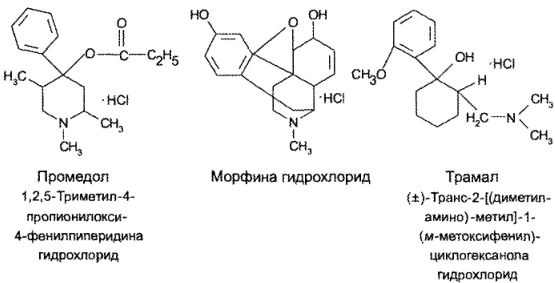
С учетом степени социального зла, связанного с опиоидными анальгетиками, во многих лабораториях мира проводится большая работа по созданию синтетических аналогов морфина по фармакологическому действию. Одним из первых в этом ряду был синтезирован промедол, а сравнительно недавно – трамал:
Сравнение приведенных структур показывает сходство химического строения промедола и трамала с таковым предшественника – морфина, хотя трамал не является даже гетероциклическим соединением.
Следует, однако, отметить, что промедол и трамал действуют, по-видимому, на те же центры коры головного мозга, что и морфин. Поэтому их длительное применение также вызывает привыкание.
Производные апорфина
Апоморфин следует рассматривать как продукт промежуточного окисления морфина, с учетом внешнего вида и химических свойств препарата. Апоморфина гидрохлорид неустойчив при хранении, особенно на свету, и легко окисляется как в нейтральной, так и в кислой и щелочной среде.
Окисление в кислой и нейтральной среде (pH 2—7) приводит к образованию дикетона (реакция Пеллагри — см. выше), а в щелочной – к ортохинону (10%) и хиноидному аниону (70%):
Подлинность апоморфина гидрохлорида определяют взаимодействием препарата с азотной кислотой (см. Химизм нитрования морфина) и реакцией Пеллагри.
Другие реакции апоморфина связаны с его амфотерным характером и наличием в его молекуле 2 фенольных гидроксилов.
Количественное определение апоморфина гидрохлорида — кислотно-основное титрование в неводной среде
Источник