Кажущийся объем распределения лекарственных средств это
Если лекарственное средство предназначено для того, чтобы вызвать системный эффект или реакцию со стороны какого-либо органа, на который невозможно воздействовать непосредственно, оно должно попасть в системный кровоток и другие «камеры» организма. Большинство препаратов широко распределяется в организме, так как некоторые из них растворяются в плазме, другие связываются с ее белками, третьи — с тканевыми структурами.
Иногда они распределяются неравномерно, так как избирательно связываются с белками плазмы или тканей или накапливаются в определенных органах. Безусловно, местное накопление лекарственного средства влияет на его действие. Например, если оно проникает через гематоэнцефалический барьер, то способно действовать на мозг, а степень (количество) и сила (прочность) связывания с белками или тканями влияют на время, в течение которого препарат остается в организме, и, следовательно, на длительность его действия.
Объем распределения лекарственного вещества — это кажущийся объем, в котором оно распределяется (или могло бы распределиться) при условии, что концентрация его в организме была бы равна его концентрации в плазме, т.е. если бы весь организм представлял собой как бы единую камеру.
Распределение лекарственного вещества из плазмы в другие жидкости и ткани организма имеет свои особенности для каждого препарата, попадающего в кровоток, и широко варьирует в зависимости от лекарственного средства. Точную его концентрацию в разных тканях и жидкостях организма можно определить путем биопсии тканей и забора жидких сред, что по понятным причинам невозможно произвести у человека. Обычно концентрацию препарата определяют в плазме.
Ее сопоставляют с введенной дозой, и на основании полученного результата делается вывод, остается ли препарат в системе кровообращения или переходит из плазмы в ткани. Если лекарственное вещество остается преимущественно в плазме, его объем распределения небольшой; если же оно распределяется главным образом в других тканях, его объем распределения будет большим.
Подобная информация важна для клинициста, в частности, при передозировке препарата. Удаление лекарственного средства путем гемодиализа эффективно только в том случае, если большая его часть находится в плазме (салицилаты, имеющие небольшой объем распределения). В то же время при передозировке петидина гемодиализ неэффективен из-за очень большого объема его распределения. Однако это общие положения, а для практических целей необходимо определять его количественно.
Для определения объема распределения препарата в организме используется принцип оценки объема распределения красителя в контейнере, заполненном жидкостью. Масса добавленного в контейнер красителя, разделенная на его концентрацию после смешивания, дает представление об объеме его распределения. Аналогично можно определить объем распределения препарата в организме после одноразового внутривенного болюсного введения его дозы, разделив эту дозу на его концентрацию в плазме.
На основании этих расчетов значение объема распределения по существу редко соответствует физиологическому объему внеклеточной жидкости или общему объему жидкости в организме, так как измеренный объем представляет собой лишь кажущийся объем распределения, определяемый но введенной дозе препарата и получаемой концентрации его в плазме; при этом предполагают, что объем плазмы соответствует всему объему распределения. В связи с этим часто пользуются понятием кажущийся объем распределения.
В действительности для некоторых препаратов, в значительной степени связывающихся в тканях, кажущийся объем распределения, рассчитываемый на основании низкой концентрации препарата в плазме, во много раз превосходит общий объем организма.
Объем распределения — это объем жидкости, в котором кажется распределенным лекарственное вещество при его концентрации, равной таковой в плазме.
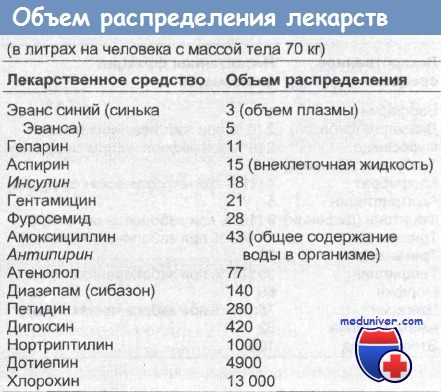
В таблице приведены кажущиеся объемы распределения. Курсивом выделены названия препаратов, использованных для параллельного определения физиологического пространства распределения.
Избирательное распределение в организме происходит благодаря особому сродству лекарственного вещества к определенным компонентам организма. Многие препараты связываются с белками плазмы: например, фенотиазины и хлорохин — с меланинсодержащими тканями, в том числе и в сетчатке глаза, что объясняет развитие ретинопатии при приеме этих препаратов. Избирательное накопление лекарственных веществ в определенных тканях (например, йода в щитовидной железе) может происходить с участием специальных транспортных систем.
Источник
Кажущийся объем распределения лекарственных средств это
Распределение ЛС — процесс распространения ЛС по органам и тканям после того, как они поступят в системный кровоток.
Отсеки распределения:
1. Внеклеточное пространство (плазма, межклеточная жидкость)
2. Клетки (цитоплазма, мембрана органелл)
3. Жировая и костная ткань (депонирование ЛС)
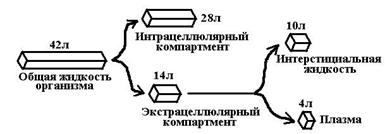
[ Vd=3-4 л, то все лекарство распределено в крови;
[ Vd= 4-14 л, то все лекарство распределено во внеклеточной жидкости;
[ Vd=14-42 л, то все лекарство приблизительно равномерно распределено в организме;
[ Vd>42 л, то все лекарство находится преимущественно во внеклеточном пространстве.
Молекулярные лиганды ЛС:
А) специфические и неспецифические рецепторы
Б) белки крови (альбумин, гликопротеин) и тканей
В) полисахариды соединительной ткани
Г) нуклеопротеиды (ДНК, РНК)
· Природа ЛС — чем меньше размеры молекулы и липофильнее ЛС, тем быстрее и равномернее его распределение.
· Размер органов – чем больше размер органа, тем больше лекарственного средства может поступить в него без существенного изменения градиента концентраций
· Кровоток в органе — в хорошо перфузируемых тканях (мозг, сердце, почки) терапевтическая концентрация вещества создается значительно раньше, чем в тканях плохо перфузируемых (жировая, костная)
· Наличие гистогематических барьеров – ЛС легко проникают в ткани с плохо выраженным ГГБ
· Связывание лекарства с белками плазмы — чем больше связанная фракция ЛС, тем хуже его распределение в ткани, т. к. покидать капилляр могут лишь свободные молекулы.
· Депонирование лекарства в тканях — связывание ЛС с белками тканей способствует его накоплению в них, т. к. снижается концентрация свободного ЛС в периваскулярном пространстве и постоянно поддерживается высокий градиент концентраций между кровью и тканями.
Количественной характеристикой распределения лекарства является кажущийся объем распределения (Vd).
Кажущийся объем распределения Vd – это гипотетический объем жидкости, в котором может распределиться вся введенная доза лекарства, чтобы создалась концентрация, равная концентрации в плазме крови.
Vd равен отношению введенной дозы (общего количества лекарства в организме) к его концентрации в плазме крови:
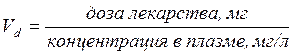
Чем больше кажущийся объем распределения, тем большая часть лекарств распределяется в ткани.
Источник
Основные фармакокинетические параметры
Фармакокинетика — раздел клинической фармакологии, изучающий пути введения, биотрансформацию, связь с белками крови, распределение и выведение лекарственных средств (ЛС).
Один из основных показателей, определяющих фармакологический эффект, — концентрация ЛС в области рецептора, однако в условиях целостного организма установить её невозможно. Экспериментально доказано, что в большинстве случаев имеется корреляция между концентрацией препарата в крови и его содержанием в других биологических жидкостях и тканях.
Поэтому для определения фармакокинетических параметров ЛС изучают его содержание в крови. Чтобы получить соответствующие представления о поступлении препарата в кровь и выведении его из организма, определяют содержание ЛС в плазме крови в течение длительного времени, используя методы жидкостной или газожидкостной хроматографии, радиоиммунный и иммуноферментный анализы, спектрофотометрический метод. На основании полученных данных строят график (фармакокинетическую кривую), отмечая на оси абсцисс время исследования, а на оси ординат — концентрацию ЛС в плазме крови.
В связи со сложностью описания деталей процесса распределения ЛС во всех органах и тканях, организм условно представляют в виде одной или нескольких изолированных проницаемой мембраной частей (камер), в которых Л С распределяется. Этот вид моделирования называют камерным. За центральную камеру обычно принимают кровь и хорошо кровоснабжаемые органы (сердце, лёгкие, печень, почки, эндокринные железы), за периферическую — менее интенсивно кровоснабжаемые органы и ткани (мышцы, кожу, жировую ткань). В этих камерах ЛС распределяется с разной скоростью: быстрее — в центральной, медленнее — в периферической. К наиболее простым относят однокамерную модель, когда предполагают, что после введения препарата его концентрация убывает по моноэкспоненциальному закону. В соответствии с законами линейной кинетики скорость изменения количества препарата в камере пропорциональна его количеству в этой камере.
Кажущийся объём распределения (Vd) — гипотетический объём жидкости организма, необходимый для равномерного распределения всего количества ЛС (введённой дозы) в концентрации, аналогичной таковой в плазме крови. Этот показатель измеряют в л/кг. При внутривенном введении объём распределения равен отношению дозы ЛС к его начальной концентрации в крови.
• Высокие значения объёма распределения свидетельствуют о том, что ЛС активно проникает в биологические жидкости и ткани. При этом, если ЛС активно связывается, например, жировой тканью, его концентрация в крови может практически мгновенно стать очень низкой, а объём распределения достигнет нескольких сотен литров, превысив реальный объём жидкостей организма. Поэтому этот показатель и называют кажущимся объёмом распределения.
• Объём распределения зависит от различных факторов.
— Физико-химические свойства ЛС (молекулярная масса, степень ионизации и полярности, растворимость в воде и жирах) влияют на его прохождение через мембраны.
— Физиологические факторы (возраст, пол, общее количество жировой ткани в организме). Например, у пожилых людей и ново рождённых Vd снижен.
— Патологические состояния, особенно заболевания печени, почек, сердечно-сосудистой системы (ССС).
Максимальная концентрация (Сmax) и время наступления максимальной концентрации (Тmax). При поступлении ЛС в системный кровоток (в случае внесосудистого введения) его концентрация постепенно возрастает, достигая значения (Сmax) в момент Тmax, а затем начинает снижаться.
• Если процесс абсорбции имеет линейный характер (скорость процесса прямо пропорциональна количеству ЛС в системе), скорость этого процесса характеризуется константой абсорбции (kabs), измеряемой в часах и рассчитывается через период полувсасывания (Т1/2abs) — время, в течение которого всасывается 1/2 введённой дозы препарата.
Биодоступность (F) — часть дозы Л С (в %), достигшая системного кровотока после вне-сосудистого введения (в этом случае не всё количество препарата достигает системного кровотока).
• Абсолютную биодоступность определяют соотношением значений площади под кинетической кривой (area under curve, AUC) при вне-сосудистом и внутривенном введениях препарата.
— В рамках однокамерной модели при внутривенном введении площадь под кинетической кривой определяется отношением начальной концентрации в крови (Со) к константе элиминации (кеl)
— AUC прямо пропорциональна однократной дозе ЛС, введённой внутривенно (в/в), и обратно пропорциональна общему клиренсу препарата. Она связана с величиной объёма распределения:
где Vd — объём распределения, кеl — константа элиминации, D — доза, AUC — площадь под кинетической кривой.
• Биоэквивалентность (относительная биодоступность) — соотношение количества ЛС, поступившего в системное кровообращение при применении его в различных лекарственных формах или лекарственных препаратах, выпускаемых различными фирмами. Если сравниваемые ЛС аналогичны (действующее вещество, доза, лекарственная t форма), но изготовлены разными производителями, их называют дженериками, и в этом случае необходимо исследование их биоэкви— валентности. Два лекарственных препарата биоэквивалентны, если они обеспечивают одинаковую биодоступность ЛС.
Константа скорости элиминации (кеl) — процент снижения концентрации вещества в крови в единицу времени (отражает долю препарата, выводимую из организма за единицу времени). Элиминация складывается из процессов биотрансформации и экскреции. Константа скорости элиминации характеризует элиминацию в рамках однокамерной модели при линейном характере процесса выведения. Период полувыведения (Т1/2) — время, необходимое для снижения концентрации препарата в крови на 50% в результате элиминации. В рамках линейной модели Т1/2 рассчитывают по формуле:
• Практически за один Т 1 / 2 из организма выводится 50% ЛС, за два периода — 75%, за 3 периода — приблизительно 90% и т.д.
• Зависимость между Т1/2 и кеl важна для подбора режима дозирования и особенно для определения интервала между дозами.
Клиренс (CI) — объём плазмы или крови, полностью освобождающийся от ЛС в единицу времени. Этот показатель количественно характеризует выведение препарата и выражается в мл/мин или л/ч. В рамках линейной модели клиренс рассчитывают по формуле:
где Сl — клиренс, Vd — объём распределения, Ке1 — константа скорости элиминации, D — доза, AUC — площадь под кинетической кривой.
• Общий клиренс представляет собой сумму почечного и печёночного клиренсов (так как эти органы служат основными путями выведения ЛС). (Другие пути выведения или внепечёночный метаболизм при расчёте общего клиренса обычно не учитывают.)
— Печёночный клиренс характеризует биотрансформацию ЛС в печени (метаболический клиренс) и выведение с жёлчью (жёлчный клиренс).
— Почечный клиренс отражает выведение препарата с мочой. На пример, почечный клиренс циметидина приблизительно составляет 600 мл/мин, метаболический — 200 мл/мин, жёлчный — 10 мл/мин, поэтому общий клиренс равен 810 мл/мин.
• Основные физиологические факторы, определяющие клиренс, — функциональное состояние основных физиологических систем организма, объём притекающей крови и скорость кровотока в органе. Печёночный клиренс зависит от скорости печёночного кровотока или функциональной способности метаболизирующих ферментов. Например, клиренс лидокаина, интенсивно метаболизируемого печёночными ферментами, зависит прежде всего от скорости его доставки к печени (т.е. от объёма притекающей крови и скорости кровотока), поэтому, например, при застойной сердечной недостаточности он снижен. Клиренс же фенотиазинов зависит в основном от активности метаболизирующих ферментов, поэтому при поражении гепатоцитов клиренс препаратов этой группы резко снижается, вследствие чего концентрация их в крови значительно возрастает.
Равновесная (или стационарная) концентрация (Css) — концентрация, достигнутая при состоянии, когда в каждом интервале между приёмом очередных доз количество всасывающегося ЛС равно количеству элиминируемого [т.е. при стационарном (steady state), или равновесном, состоянии]. Т.е. если ЛС вводят в постоянной дозе через фиксированные интервалы времени, продолжительность которых меньше времени элиминации, его концентрация в крови возрастает, а затем колеблется в пределах средней величины между максимальными и минимальными значениями.
• При достижении С проявляется в полном объёме клинический эффект ЛС. Чем меньше Т1/2 ЛС, тем скорее достигается Си и тем выражение будут её колебания. Например, Т1/2 новокаинамида равен 2— 3 ч, и при назначении через каждые 6 ч его Css характеризуется большим разбросом значений. Поэтому для предупреждения и уменьшения колебаний Css в крови всё большее распространение получают лекарственные формы с замедленным высвобождением активного вещества.
В клинической практике фармакокинетические параметры используют, в частности, для расчёта назначаемых доз препаратов.
• Для расчёта нагрузочной дозы, требуемой для достижения необходимой эффективной концентрации ЛС в крови, используют объём распределения:
где Dнагр — нагрузочная доза, VD — объём распределения, С — концентрация ЛС в плазме крови.
• Для расчёта поддерживающей дозы, т.е. дозы, необходимой для поддержания нужной концентрации ЛС в крови, используют значение клиренса:
где Dnoд — поддерживающая доза, Сl — общий клиренс, Сss — равновесная концентрация.
К основным фармакокинетическим процессам относят всасывание, метаболизм (биотрансформацию), распределение и выведение ЛС.
Источник