- Канцероматоз легких народные средства
- Рак легкого — не приговор
- Почему возникает рак легкого?
- Что должно насторожить?
- Ранние признаки рака легкого
- Стадии рака легкого
- Как лечат рак легкого?
- Как получить лечение?
- Можно ли вылечиться от рака легкого?
- Канцероматоз брюшины: кому и зачем нужны циторедуктивная операция и HIPEC
- При каких опухолях чаще всего развивается канцероматоз брюшины?
- Какие симптомы могут указать на перитонеальный канцероматоз?
- Как диагностируют канцероматоз брюшины?
- Почему канцероматоз брюшины сложно лечить?
- Что такое циторедуктивная операция и HIPEC?
- Кому может подойти такой метод лечения?
- Кому циторедуктивная операция и HIPEC не подходят?
Канцероматоз легких народные средства
Рак легкого — не приговор
19 октября 2020
Из всех заболеваний бронхолегочного древа самым редким можно считать рак трахеи, на который приходится 0,1-0,2% всех онкологических недугов.
Рак легкого — это не только медицинская, но и социальная проблема. В нашей стране ежегодно этим видом рака заболевают около 60 тыс. человек. В структуре смертности от онкологических заболеваний этот недуг занимает первое место. В 2018 г. на рак лёгкого пришлось 15% всех случаев смерти от онкологических заболеваний.
Почему возникает рак легкого?
Причина многих онкологических заболеваний — мутации в ДНК. Где, когда и почему возникает поломка, ведущая к возникновению раковой опухоли, зависит от ряда причин.
Что должно насторожить?
Коварство рака легкого и трахеи состоит в том, что ранние формы этих заболеваний не имеют клинических проявлений. Нередко пациенты длительно лечатся от других болезней у врачей других специальностей.
Ранние признаки рака легкого
Первые симптомы рака легкого часто не связаны с дыхательной системой. К ним относятся:
- Cубфебрильная температура
- Cлабость и усталость сразу после пробуждения
- Кожный зуд с развитием дерматита и появлением наростов на коже
- Слабость мышц и повышенная отечность
- Нарушение работы центральной нервной системы: головокружение (вплоть до обморока), нарушение координации движений или потеря чувствительности
- Специфические симптомы (кашель с «ржавой» мокротой, одышка, кровохарканье, боль) чаще возникают при распространенной форме заболевания
Стадии рака легкого
I стадия — опухоль меньше 3 см, метастазы отсутствуют, симптомов нет.
II стадия — опухоль до 6 см, находится в границах сегмента легкого или бронха.
Единичные метастазы в отдельных лимфоузлах (ограничены грудной клеткой на стороне поражения). Симптомы более выражены, появляется кровохарканье, боль, слабость, потеря аппетита.опухоль меньше 3 см, метастазы отсутствуют, симптомов нет.
III стадия — опухоль превышает 6 см, проникает в другие части легкого или соседние бронхи. Средостенные лимфатические узлы могут быть поражены метастазами.
IV стадия — опухоль дает метастазы в другие органы.
Как лечат рак легкого?
Выбор метода лечения во многом зависит от распространенности онкологического процесса.
Пациентам с ранними формами рака легкого, которым противопоказано хирургическое лечение, назначается лучевая терапия (стереотаксическая радиохирургия).
В НМИЦ онкологии им. Н.Н. Петрова успешно проводится уникальная операция: бронхопластическая лобэктомия — удаление части легкого (вместо традиционной операции — полного удаления органа).
Такое вмешательство позволяет сохранить качество жизни пациента. На сегодняшний день заведующим хирургическим торакальным отделением НМИЦ онкологии им. Н.Н. Петрова Евгением Левченко проведено более 300 бронхопластических лобэктомий. Это самый большой опыт «в одних руках» во всем мире.
Если опухоль большая или обнаружены метастазы, назначается лекарственная терапия.
Точечно воздействовать на клетки, которые несут генетические нарушения, не затрагивая другие, позволяет таргетная терапия, благодаря которой достигается высокая эффективность и низкая токсичность (а значит, хорошая переносимость) лечения. Если в эпоху химиотерапии 50% пациентов с распространенным раком легкого умирали в течение года после постановки диагноза, сегодня благодаря современному лечению эти больные стали жить в 3-4 раза дольше.
Еще одна прорывная технология в лечении рака легкого — иммунотерапия, которая блокирует механизм уклонения опухоли от надзора собственной иммунной системы и активизирует противоопухолевый иммунитет. Благодаря этому иммунитет распознает и самостоятельно уничтожает опухоль. Применение иммунной терапии позволяет надеяться на выздоровление даже пациентам с запущенной стадией рака легкого.
Как получить лечение?
Если вы заметили у себя настораживающие симптомы, обратитесь к участковому терапевту или врачу общей практики.
После осмотра и опроса в случае необходимости врач выдаст вам направление в онкологический диспансер, ЦАОП.
После осмотра онколог онкодиспансера или ЦАОП, если возникло подозрение на злокачественное новообразование, должен организовать ваше полное дообследование и взятие биопсии опухоли.
Если диагноз «рак» подтвердился, следует немедленно приступить к лечению: оно может быть амбулаторным или стационарным и включать в себя хирургическое вмешательство, медикаментозную и лучевую терапию.
Лечение может проходить по месту жительства или — в случае невозможности лечения по месту жительства — в федеральном центре (если потребуется лечение там, вам выдадут направление).
Помните: лечение (в том числе современные дорогостоящие препараты для иммунотерапии и таргетной терапии) предоставляется по ОМС бесплатно. Никаких доплат требовать не могут, если это происходит, обращайтесь к страховому представителю в компанию, выдавшую полис ОМС.
Сроки оказания онкологической помощи определены Приказом Минздрава № 915н «Об утверждении Порядка оказания медицинской помощи населению по профилю „онкология»», они должны строго соблюдаться:
- Через 5 дней — пациент, обратившийся к терапевту с подозрением на онкологическое заболевание, должен оказаться на приеме у онколога.
- В течение 1 рабочего дня онколог должен взять биопсию. Если это невозможно в силу ресурсов медицинской организации, врач должен немедленно направить пациента в ту медицинскую организацию, где это можно осуществить.
- В течение 15 рабочих дней гистолог должен рассмотреть полученный материал и дать заключение.
- В течение 15 рабочих дней после получения результата биопсии (если диагноз подтвердился) пациент должен пройти консилиум врачей (для планирования лечения) в онкодиспансере и быть госпитализирован.
При необходимости проведения операции предшествующая хирургическому вмешательству предоперационная химиотерапия или предоперационная лучевая терапия проводятся в сроки, установленные клиническими рекомендациями Минздрава России для каждого вида опухоли. После них выполняется операция.
Вопрос обеспечения лекарственными препаратами находится под пристальнейшим контролем Минздрава России.
Можно ли вылечиться от рака легкого?
Да, и таких случаев в копилке врачей немало. В НМИЦ онкологии им. Н.Н. Петрова часто вспоминают шахтера, который всю жизнь проработал за Полярным кругом: в Воркуте. После выхода на пенсию он переехал в Кировскую область и… заболел. Сначала врачи поставили диагноз «бронхит», затем — «астма», потом — «рак легкого». Младшая дочь посоветовала пройти обследование в Санкт-Петербурге, где они попали к Евгению Владимировичу Левченко. Хирург предложил сделать операцию по своей методике, сохраняя часть легкого.
Благодаря этому удалось добиться длительной ремиссии. В планах у 65-летнего пациента снова вернуться к спорту, в родном городе его уже ждет сборная ветеранов.
Муж привез ее в клинику уже в тяжелом состоянии. Дышать самостоятельно она уже не могла. Диагноз — «рак легкого 4-й стадии, осложненный тромбоэмболией» — не внушал оптимизма. Состояние было настолько тяжелым, что родные готовились к худшему. Брать биопсию в такой ситуации было нельзя: пациентка могла погибнуть от кровопотери. Генетическое исследование плазмы крови показало, что у пациентки болезнь вызвала особая мутация, против которой есть специализированный таргетный препарат.
Женщина быстро пошла на поправку. Сейчас она живет обычной жизнью. Все, что требуется для поддержания ее состояния, — это просто принимать таблетки.
Уроженец Дербента, врач-стоматолог — с молодости курил крепкие дорогие сигареты (на момент поступления в клинику стаж курения составлял 32 года).
«Я наивно полагал, что вред бывает только от дешевых папирос», — вспоминает он.
В феврале 2014 года его стали мучить ночные боли в руке. Местные врачи решили, что это профессиональное заболевание (как известно, руки стоматологов постоянно испытывают большую нагрузку), и назначили сначала физиопроцедуры с гормональным препаратом, а потом — инъекции другого гормонального препарата непосредственно в руку.
Поскольку эффекта так и не последовало, пациента решили «дообследовать». Рентгеновский снимок показал отсутствие в лучевой кости 6-сантиметрового фрагмента. Окончательный диагноз был поставлен в НМИЦ онкологии им. Н.Н. Блохина: оказалось, что это не саркома, как предполагалось ранее, а метастатический рак легкого 4-й стадии. Метастаз размером 10х15 см блокировал работу сустава и разрушил лучевую кость правой руки.
Пациенту была удалена верхняя доля правого лёгкого, ампутирована рука, 4 курса химиотерапии также не дали результата. В начале 2015 года он стал одним из первых пациентов, кто принял участие в клиническом исследовании нового иммуноонкологического препарата, которое проводилось в НМИЦ онкологии им. Н.Н. Блохина. Результат превзошел все ожидания: пациент быстро пошел на поправку, и с тех пор болезнь ни разу не напомнила о себе.
После операции пациент обратился за консультацией в НМИЦ онкологии им. Н.Н. Блохина. После молекулярно-генетического тестирования была выявлена редкая генетическая мутация, которая и стала причиной заболевания. При ней самым эффективным вариантом лечения является таргетная терапия.
После назначения препарата у пациента уменьшилась одышка, пропал кашель. Сегодня, спустя 5 лет после начала лечения, признаков опухолевого процесса у пациента нет.
Для лечения пациентов дневных и круглосуточных стационаров в 2020 году выделено 120 миллиардов рублей и запланировано выделить в 2021 году 140 миллиардов рублей.
Источник
Канцероматоз брюшины: кому и зачем нужны циторедуктивная операция и HIPEC
Злокачественные опухоли могут метастазировать — распространяться на другие ткани и органы. Если первичная опухоль расположена в брюшной полости, она может распространиться по брюшине — это состояние называется перитонеальным канцероматозом. Такой вариант течения болезни значительно ухудшает прогноз — в среднем, в зависимости от вида опухоли и полученного лечения продолжительность жизни человека составляет от полугода до двух лет. Долгое время пациентам с канцероматозом брюшины могли предложить только паллиативную помощь, но появились и другие методы.
Рассказываем о циторедуктивной операции и гипертермической внутрибрюшинной химиотерапии (HIPEC), которые могут продлить жизнь людям с таким диагнозом.
Этот текст мы написали вместе с Онкоцентром «СМ-Клиника».
Что такое перитонеальный канцероматоз?
Брюшина — оболочка, выстилающая стенки брюшной полости, таза и поверхность внутренних органов — печени, матки, яичников, селезенки, кишечника. Любой патологический процесс, затрагивающий брюшную полость, может распространяться по брюшине за счет движения жидкости и клеток в этом пространстве. Например, эпителиальные опухоли яичников возникают из эпителия маточных труб, который сообщается с брюшиной. Из-за роста опухоли злокачественные клетки «отслаиваются» и могут свободно плавать в перитонеальной жидкости. Как правило, эти клетки имплантируются в область таза и другие части брюшины.
Канцероматоз выглядит как множество опухолевых узлов, покрывающих брюшину. Размер и количество узлов могут быть различными.
При каких опухолях чаще всего развивается канцероматоз брюшины?
Перитонеальный канцероматоз у женщин чаще всего развивается при раке яичников, а у мужчин — при раке толстой кишки и желудка. Например, при раке желудка опухолевые узлы на брюшине возникают у 60% пациентов.
В более редких случаях канцероматоз брюшины может быть самостоятельным заболеванием. Иногда расположение первичной опухоли установить не получается.
Какие симптомы могут указать на перитонеальный канцероматоз?
У этого состояния неспецифические признаки. Среди них:
— увеличение объема живота из-за скопления жидкости в брюшной полости — асцит
— тошнота, вздутие живота
— запор или диарея
— необъяснимая потеря веса
Злокачественный (то есть вызванный опухолью) асцит, в свою очередь, может вызывать другие симптомы, среди которых:
Перитонеальный канцероматоз может вызывать кишечную непроходимость. В этом случае продвижение содержимого желудка и кишечника через ЖКТ затруднено или отсутствует. Злокачественная кишечная непроходимость чаще встречается у пациентов с раком яичников и колоректальным раком.
Как диагностируют канцероматоз брюшины?
Заподозрить перитонеальный канцероматоз можно с помощью УЗИ, КТ и МРТ брюшной полости и малого таза.
В частности, КТ брюшной полости позволяет приблизительно оценить, насколько опухоль распространена. МРТ будет эффективнее для осмотра малого таза и позволит врачу оценить степень поражения находящихся там органов, например матки, мочевого пузыря.
Однако эти методы позволяют обнаружить только крупные очаги — опухолевые узлы до 5 мм редко отчетливо видны во время УЗИ, КТ и МРТ. Наибольшей точностью обладает лапароскопия: через прокол врач вводит в брюшную полость камеру, осматривает брюшину и, если необходимо, проводит биопсию — забирает часть опухоли на исследование.
Почему канцероматоз брюшины сложно лечить?
«Традиционные» методы лечения онкологических заболеваний — лучевая терапия, операция — не эффективны в случае с канцероматозом брюшины. Облучать такую большую область слишком опасно. Не все опухолевые очаги можно удалить хирургическим путем — метастазы могут быть очень маленького размера, незаметными для врача, или располагаться в труднодоступном месте. Оставшиеся опухолевые клетки спровоцируют рецидив заболевания.
Стандарты лечения канцероматоза брюшной полости включают системную химиотерапию, облегчение симптомов. В последние годы в списке методов появились циторедуктивная операция и HIPEC — гипертермическая внутрибрюшинная химиотерапия.
Что такое циторедуктивная операция и HIPEC?
Циторедуктивная операция подразумевает удаление всех видимых опухолевых очагов на брюшине. Гипертермическая внутрибрюшинная химиотерапия (HIPEC) — завершающий этап операции, который нужен, чтобы убить максимальное количество оставшихся микроскопических опухолевых клеток, снизив вероятность рецидива.
Для этого брюшную полость пациента промывают нагретым до 42°C градусов раствором химиопрепаратов. В брюшную полость устанавливают катетеры, через которые в организм пациента попадает раствор. Такой способ введения позволяет охватить все отделы брюшной полости. Для отслеживания температуры в брюшную полость помещают датчики.
Местное, а не системное (внутривенное) применение цитостатиков позволяет увеличить дозу препаратов и при этом избежать побочных явлений. Высокая температура в сочетании высокими дозами химиотерапии усиливают противоопухолевый эффект.
Спустя примерно час–полтора раствор удаляют из брюшной полости, промывают ее физраствором и зашивают. В общей сложности такое вмешательство занимает 8–10 часов.
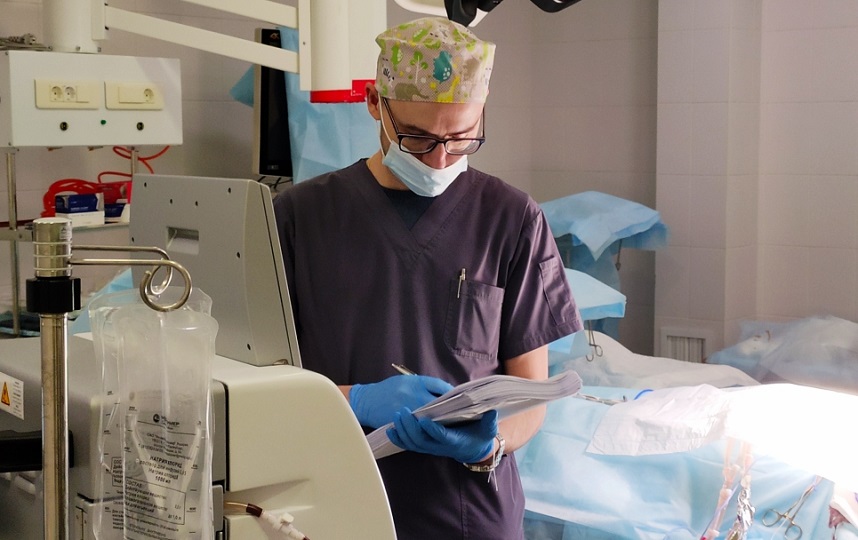 |
Техник наблюдает за процессом HIPEC-терапии
Кому может подойти такой метод лечения?
Отдельные исследования и мета-анализы демонстрируют эффективность этого метода — циторедуктивная операция в сочетании с гипертермической внутрибрюшинной химиотерапией увеличивает продолжительность жизни пациентов с перитонеальным канцероматозом. Например, в этом исследовании приняли участие пациентки с III стадией эпителиального рака яичников. Авторы приходят к выводу, что добавление гипертермической внутрибрюшинной химиотерапии к циторедуктивной операции увеличивает период без прогрессирования заболевания, общую продолжительность жизни и не повышает количество побочных эффектов по сравнению с циторедуктивной операцией.
Эта лечебная опция считается оптимальным вариантом лечения пациентов с опухолями аппендикса и псевдомиксомами брюшины.
Предполагается также, что профилактическое применение HIPEC может снизить риск развития канцероматоза брюшины в будущем. Не так давно появились данные о положительных результатах профилактического применения HIPEC при раке ободочной кишки, желудка и поджелудочной железы.
Кому циторедуктивная операция и HIPEC не подходят?
Необходимость таких вмешательств определяется исходя из истории болезни, тщательного обследования и общего состояния пациента. Циторедуктивную операцию в сочетании с HIPEC могут не провести, если:
— метастазы вышли за пределы брюшины
— заболевание прогрессирует несмотря на проведенную ранее химиотерапию
— есть кишечная непроходимость, вызванная опухолью
— общее состояние пациента тяжелое
— есть высокая опухолевая нагрузка — опухолевые импланты покрывают значительную часть толстой и тонкой кишки
В целом, исследования, оценивающие эффективность метода, как правило, основаны на результатах нерандомизированных испытаний.
Безопасность процедуры пока изучается. Например, авторы этого исследования пришли к выводу, что циторедуктивная операция в сочетании с HIPEC безопасна и чаще даже безопаснее в сравнении с другими широко распространенными онкологическими процедурами, в частности, операцией Уиппла (способ лечения рака поджелудочной железы — прим. ред.). Однако и сами авторы, и их коллеги отмечают, что у исследования есть недостатки, прежде всего, касающиеся выбора пациентов. У людей с раком поджелудочной железы в большинстве случаев нет других альтернатив, кроме операции Уиппла, а пациенту с перитонеальным канцероматозом можно предложить несколько вариантов: паллиативную терапию, циторедуктивную операцию без HIPEC, — чтобы выбрать оптимальный в конкретном случае способ лечения.
Кроме того, не существует единых протоколов, регламентирующих такое лечение: во время HIPEC могут использоваться различные химиопрепараты, температура, время промывания брюшной полости.
Таким образом, окончательное решение о выборе стратегии лечения пациент и врач должны принять, взвесив все «за» и «против».
Проконсультировать по вопросам назначения циторедуктивной операции в сочетании с HIPEC смогут специалисты Онкоцентра «СМ-Клиника». Врачи Онкоцентра оказывают различные виды помощи пациентам с онкологическими заболеваниями, в том числе проводят циторедуктивные операции с последующей процедурой HIPEC.
Источник



