Ингаляции эфирными маслами в профилактике и комплексной терапии острых респираторных заболеваний у детей
Опубликовано в журнале:
«Практика педиатра», март-апрель, 2013, с. 54-58 Е.А. Азова, профессор, д. м. н.; В.А. Воробьева, профессор, д. м. н.; О.Б. Овсянникова, профессор, д. м. н.; Н.А. Азов, доцент, к. м. н.; И.В. Сладкова,
ГБОУ ВПО «Нижегородская государственная медицинская академия» Минздрава РФ, Институт последипломного образования, факультет повышения квалификации врачей;
А.Г. Куликов, профессор, д. м. н., ГБОУ ВПО «РАМПО», кафедра физиотерапии;
Л.А. Митрошина, к. м. н.; О.В. Белоцерковская, МЛПУ «Детская городская поликлиника № 8», г. Нижний Новгород.
Значительная распространенность острых респираторных заболеваний, их неблагоприятное воздействие на состояние ведущих систем организма, недостаточная эффективность методов профилактики и реабилитации определяют важность медицинских аспектов данной проблемы, их социальную значимость [1, 2].
Одним из эффективных методов профилактики простудных заболеваний является ингаляция эфирными маслами, так как эфирные масла обладают ярко выраженными антисептическими, противовирусными, бактерицидными и противовоспалительными свойствами [7– 10]. Ингаляционный метод введения эфирных масел, например при рините, имеет ряд достоинств: безопасность и удобство метода, что позволяет использовать его у детей всех возрастных групп; максимально физиологичное введение лекарственного вещества – вместе со вдыхаемым воздухом; прямое действие на слизистую оболочку органов дыхания, купирование застойных и воспалительных реакций; смягчающее действие микрочастиц масла на слизистые оболочки; возможность избежать раздражения слизистой оболочки и мацерации кожных покровов, развивающихся при длительном интраназальном применении лекарственных средств [4]. В педиатрии наиболее удобны и безопасны пассивные ингаляции [5]. Цель проведенного нами исследования – совершенствование профилактики и комплексной терапии ОРЗ у детей в амбулаторных условиях. Нами была использована комбинация эфирных масел, воздействующих на слизистую оболочку верхних дыхательных путей и обладающих различными взаимодополняющими свойствами (табл.).
Таблица. Состав масла «Дыши» (процентное соотношение в 10 мл)
| Состав | Содержание в 10 мл | Действие |
| Масло мятное (без ментола) | 35,45% | Болеутоляющий, дезодорирующий, тонизирующий и легкий антисептический эффект |
| Масло эвкалиптовое | 35,45% | Один из сильнейших антисептиков в группе эфирных масел, широко используется в составе различных ингаляций, применяемых при респираторных инфекциях верхних дыхательных путей; оказывает иммуностимулирующее действие |
| Масло каепутовое | 18,50% | Обладает высокой гермицидной активностью по отношению к S. аureus, противовоспалительной активностью и тонизирующим эффектом |
| Левоментол | 4,10% | Антибактериальное, противовоспалительное, болеутоляющее действие |
| Масло винтергриновое | 3,70% | Противовоспалительный и тонизирующий эффект |
| Масло можжевеловое | 2,70% | Противомикробное действие |
| Масло гвоздичное | 0,10% | Антисептическое, противовоспалительное и болеутоляющее действие |
Материалы и методы исследования
Проведено открытое сравнительное исследование для оценки эффективности масла «Дыши» в комплексной терапии ОРЗ у детей в возрасте 3–14 лет в амбулаторно-поликлинических условиях. Под нашим наблюдением находилось 45 больных острыми респираторными заболеваниям, имеющих в анамнезе рецидивирующее течение ОРЗ. В основную группу вошло 30 детей, получивших в дополнение к стандартной терапии масло «Дыши», контрольная группа состояла из 15 пациентов, получивших только стандартную терапию. Стандартная терапия включала противовирусные, антибактериальные препараты, симптоматические лекарственные средства [6].
Методы исследования: клинический осмотр педиатра; осмотр лор-врача, включающий ринофарингоотоскопию, цитоскопию мазка со слизистой носа; общий анализ крови; изучение данных анамнеза заболевания; оценку качества жизни по данным анкетирования.
Предварительно проводился аллерготест на переносимость данной композиции эфирных масел. С помощью ватного тампона наносили 1 каплю масла «Дыши» на кожу с внутренней стороны предплечья, завязывали это место на 30 минут. Если появлялась гиперемия, сыпь, зуд, то данный ребенок исключался из основной группы.
Масло «Дыши» применялось путем проведения пассивных ингаляций по следующей схеме: 2–3 капли масла (на салфетку) 3 раза в день начиная с первых признаков ОРЗ. Продолжали ингаляции маслом «Дыши» на протяжении 30 дней, так как предыдущие ОРЗ, как правило, имели рецидивирующий характер течения.
Результаты исследования
У всех больных при клиническом осмотре отмечались жалобы на повышение температуры, заложенность в носу, слизистые или слизисто-гнойные выделения из носа, першение, сухость и боль в горле, сухой или влажный кашель, головную боль, потерю аппетита, плохое самочувствие и т. д. При риноскопии отмечалась гиперемия слизистой носа, гипертрофия нижней и верхней носовых раковин, ринорея, слизистые или гнойные выделения. При фарингоскопии – слизистая оболочка зева ярко гиперемирована, отмечались отек и гиперемия гранул и боковых валиков глотки, стекание слизистых или гнойных выделений носоглотки по задней стенке глотки.
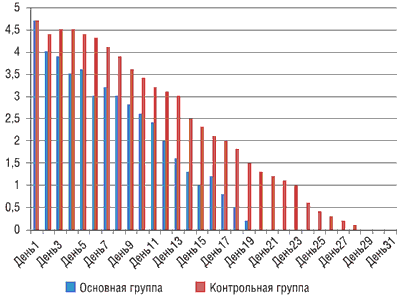
В течение 30 дней ежедневно оценивалось состояние носового дыхания (по 5-балльной шкале, где 0 – симптом заложенности носа отсутствует, 5 – симптом заложенности носа выражен максимально). Состояние носового дыхания представлено на рис. 1.
Рисунок 1. Динамика балльной оценки заложенность носа у детей в основной и контрольной группах (по оси OY – выраженность симптома в баллах)
На фоне ингаляций маслом «Дыши» происходило значительное понижение заложенности носа уже к 3-му дню ингаляций по сравнению с контрольной группой, где данный симптом понижается только к 7-му дню заболевания. Отмечалось улучшение риноскопической и фарингоскопической картины в основной группе у всех 30 детей (100%) уже на 3-и сутки после ингаляций маслом «Дыши», в то время как в контрольной группе аналогичная картина наблюдалась только у 3 из 15 (20%) детей.
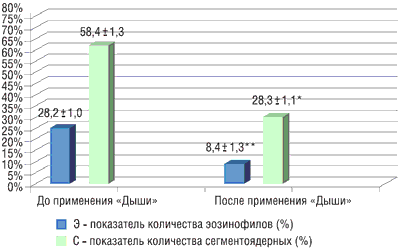
Повышенный уровень эозинофилов в назальном секрете наблюдался у 83% детей. Это позволяет с большой уверенностью говорить об аллергическом фоне организма ребенка [2]. У всех детей (100%) отмечался повышенный уровень сегментоядерных нейтрофилов, что свидетельствует о бактериальном воспалении в полости носа. У 28 детей (94%) после применения «Дыши» достоверно снизились показатели аллергического и бактериального воспаления в полости носа. Отмечено статистически значимое снижение среднего содержания сегментоядерных нейтрофилов (с 58,4 ± 1,3% до 28,3 ± 1,1%, р = 0,000) и эозинофилов (с 28,2 ± 1,0 до 8,4 ± 1,3%, р = 0,001) в назальном секрете до и после применения «Дыши» (рис. 2).
Рисунок 2. Соотношение сегментоядерных нейтрофилов и эозинофилов в назальном секрете до и после применения «Дыши» (**р = 0,000; *р = 0,001)
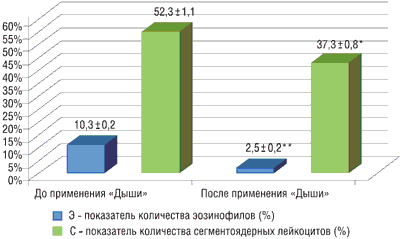
В крови уровень эозинофилов и сегментоядерных нейтрофилов также был повышен. Установлено, что у 24 детей основной группы (80%), которые получали ингаляции маслом «Дыши», значительно снизились показатели аллергического и бактериального воспаления: средний уровень эозинофилов в крови достоверно снизился с 10,3 ± 0,2% до 2,5 ± 0,3% (р = 0,000), а сегментоядерных нейтрофилов – с 52,3 ± 1,1% до 37,3 ± 0,8% (р = 0,001) (рис. 3). В контрольной группе данные показатели практически не изменились.
Рисунок 3. Соотношение сегментоядерных лейкоцитов и эозинофилов в периферической крови до и после применения «Дыши» (*р = 0,001; **р = 0,000)
По результатам исследования сегментоядерных нейтрофилов, эозинофилов в назальном секрете, периферической крови можно говорить о снижении воспалительного процесса в организме детей, получавших ингаляции данной композицией эфирных масел, что доказывает высокую эффективность масла «Дыши» в комплексной терапии ОРЗ у детей.
На фоне приема «Дыши» достоверно снизились продолжительность заболевания и количество пропусков детьми детских дошкольных учреждений или школы по причине ОРЗ (5,2 ± 0,01 дня в основной группе и 8,5 ± 0,1 дня — в контрольной, р = 0,01). Применение масла «Дыши» позволило добиться уменьшения продолжительности острого респираторного заболевания в 1,6 раза. Клиническая эффективность применения «Дыши», по данным анкет, была оценена как отличная (81%) и хорошая (19%).
У детей, получивших «Дыши» на протяжении 30 дней, в том числе и у детей с аллергическими заболеваниями в анамнезе, не регистрировались побочные реакции и нежелательные эффекты при его применении.
Таким образом, масло «Дыши» может успешно применяться для профилактики и в комплексной терапии повторных респираторных заболеваний у детей в домашних и амбулаторных условиях. Важным является отсутствие ограничений по длительности курса применения эфирных масел. Кроме того, с помощью эфирных масел можно проводить как индивидуальную, так и коллективную профилактику.
Список литературы находится в редакции.
Источник
Медицинские интернет-конференции
Языки
Лекарственные растения, содержащие эфирные масла
Николаева М.А., Купцова О.А.
Лекарственные растения, содержащие эфирные масла
Николаева М., Купцова О.
Научный руководитель: к.ф.н., доцент Романтеева Ю.В.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра общей биологии, фармакогнозии и ботаники
Лекарственные растения, содержащие эфирные масла
Николаева М., Купцова О.
Лекарственные растения, содержащие эфирные масла
Николаева М., Купцова О.
Научный руководитель: к.ф.н., доцент Романтеева Ю.В.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра общей биологии, фармакогнозии и ботаники
Лекарственные растения, содержащие эфирные масла
Николаева М., Купцова О.
Научный руководитель: к.ф.н., доцент Романтеева Ю.В.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра общей биологии, фармакогнозии и ботаники
Актуальность выбранной темы заключается в том, что в качестве сырья для производства лекарственных средств широко применяются эфиромасличные растения, которых насчитывают около 2500 видов. Эфирные масла растений — источник биологически активных веществ, на основе которых возможно создание новых лекарственных средств.
Цель работы: Изучить лекарственные растения, которые являются источником эфирных масел и освоить методы фармакогностического анализа.
Объекты исследования купленное сырье фирмы–производителя ПКФ ООО «Фитофарм».
В ходе проведенного макроскопического анализа было установлено, что лекарственное растительное сырье (ЛРС) мелиссы лекарственной ПКФ ООО «Фитофарм», a также ЛРС душицы обыкновенной ПКФ ООО «Фитофарм» соответствует описанию, заявленному на упаковке.
На основе проведенного микроскопического анализа были обнаружены диагностические признаки ЛРС душицы обыкновенной: извилистые стенки клеткок эпидермиса, округлые эфирномасличные железки, и ЛРС мелиссы лекарственной: клетки эпидермиса c извилистыми стенками, устьица аномоцитного типа, железистые волоски.
На основе проведенного фитохимического анализа в исследуемых образцах сырья были обнаружены эфирные масла, флавоноиды, дубильные вещества.
Товароведческий анализ представленных объектов подтвердил соответствие упаковки и маркировки требованиям ГФ XI издания.
Источник
Какие эфирные масла лечебные
Последнее время арсенал фармацевтического рынка значительно расширился высокоэффективными лекарственными препаратами (ЛП) синтетического происхождения. Благодаря этому стали решаться проблемы социально значимых заболеваний сердечно-сосудистой и гепатобилиарной систем, различных инфекций. Но такие ЛП имеют целый ряд побочных эффектов, основные из которых токсичность и аллергические реакции. Симптоматическое применение природных биологически активных веществ позволяет снизить влияние побочных эффектов на организм синтетических ЛП. К числу наиболее традиционных объектов следует отнести эфирномасличные растения, которые на протяжении многих веков применялись не только как пряности и источники парфюмерной продукции, но и как лекарственные средства.
Эфирные масла (ЭМ) – летучие жидкие смеси органических веществ, вырабатываемые растениями и обусловливающие их запах. В состав эфирных масел входят углеводороды, спирты, сложные эфиры, кетоны, лактоны, ароматические компоненты и т.д. В настоящее время из эфирных масел выделено более 1000 соединений, что значительно расширило арсенал их использования [2]. ЭМ применяются часто в качестве вспомогательных веществ, как корригенты вкуса и запаха в производстве фармацевтических продуктов, но в качестве фармацевтических субстанций не так распространены, хотя исследования показали, что ЭМ обладают разнообразными фармакологическими свойствами [3; 4].
Цель исследования. Выявить перспективные эфирные масла для внедрения в медицинскую практику в качестве фармацевтической субстанции.
На первом этапе нами изучен состав лекарственных препаратов (ЛП) с эфирными маслами, представленных на отечественном фармацевтическом рынке (табл. 1).
В результате анализа выявлено, что в состав ЛП наиболее часто входят эфирные масла, основным компонентом которых являются монотерпены. Наиболее распространенными в составе лекарственных препаратов являются: масло эвкалипта, шалфея и мяты, содержащие в своем составе такие моноциклические монотерпены, как цинеол, ментол.
Мировой ассортимент основных эфиромасличных растений насчитывает порядка 30-40 видов. Важнейшими среди них являются виды следующих родов: Citrus Abies, Coriandrum, Juniperus, Rosa, Geranium и др., в состав которых входят не только моноциклические монотерпены, но и их предшественники ациклические монотерпены: гераниол, линалоол, цитронеллол и др. [8]. Это показывает актуальность исследований в данном направлении и возможность расширения ассортимента лекарственных средств с эфирными маслами.
Ассортимент лекарственных препаратов, содержащих эфирное масло
Класс соединений [6]
транс-анетол (84-93%), цис-анетол, метилхавикол, анисовый альдегид и др.
Доктор Тайсс Анисовое масло
эвгенол (более 70%), ацетат эвгенола (до 13%), кариофиллен и др.
тимол (до 50%), карвакрол, геранилацетат
коричный альдегид (не менее 80%), бензальдегид
линалоол (30-35%), мирцен, α- и β-оцимены
α-лимонен (до 90%), цитраль, геранилацетат и др.
Лимонные пастилки от кашля Доктор-МОМ
Стрепсилс, таблетки для рассасывания медово-лимонные
Ментол (до 90%), α- и β-пинен, дипентен, фелландрен, цинеол и др.
Доктор Тайсс Анги Септ
Стрепсилс, таблетки для рассасывания медово-лимонные
мирцен, цис- и транс-β-оцимены, дипентен, α- и γ-терпинены и др.
Розеол, гераниол, цитронеллол
α- и β-пинены (30%), камфен (20%), борнеол, цинеол, камфора
α- и β-пинены, кадинен, борнеол, борнилацетат
Туссамаг бальзам от простуды
Эвкабал Бальзам С
тимол (до 30%), карвакрол и др.
цинеола (около 15%), D-α-пинена, α- и β-туйона, D-борнеола и D-камфоры
моноциклические и бициклические монотерпены
анетол (50-60%), фенхон и др.
цинеол, D-пинен, камфен, фенхен, валериановый, масляный и капроновый альдегиды
Бронхикум бальзам с эвкалиптовым маслом
Доктор МОМ® Колд Раб
Доктор МОМ® Рабон
Санорин с маслом эвкалипта
Стрепсилс с ментолом и эвкалиптом
Туссамаг бальзам от простуды
Эвкабал Бальзам С
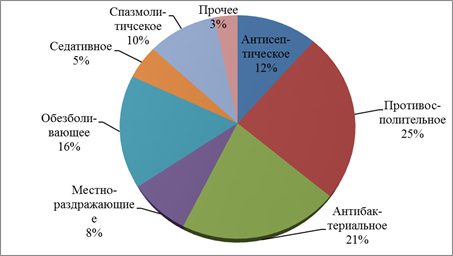
На следующем этапе нами изучено фармакологическое действие эфирных масел в составе ЛП (рис. 1). По основному проявляемому фармакологическому эффекту преобладают эфирные масла противовоспалительного 25% и антибактериального действия 21%, наиболее редко ЭФ используется в качестве седативных средств 8%.
В последние годы активно ведутся исследования по изучению специфической фармакологической активности эфирных масел можжевельника, чернушки посевной, розмарина и др. В Институте питания Республики Таджикистан изучены фармакологические свойства эфирного масла травы герани душистой и лимона. При этом установлено, что эфирное масло герани обладает желчегонным, противовоспалительным, гепатозащитным и спазмолитическим свойствами [1]. Исследования показали, что по эффективности гераниевое эфирное масло превосходит действие ЛП, таких как розанол, карсил, аллохол, холисал. Экспериментально показано, что эфирное масло лимона обладает выраженными гипогликемическими свойствами и снижает холестерин липопротеинов высокой плотности [1]. Выше сказанное показывает перспективность внедрения новых эфиромасличных растений в медицинскую практику.
Рис. 1. Распределение эфирных масел по фармакологическому действию.
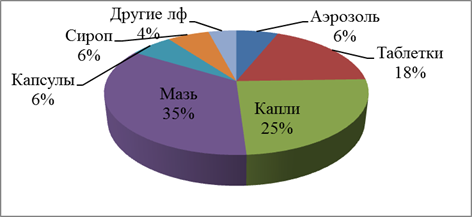
На следующем этапе работы изучены лекарственные формы эфирных масел, представленные на фармацевтическом рынке (рис. 2). Наиболее часто эфирные масла используются в мазях и каплях. Для расширения ассортимента лекарственных препаратов для перорального применения рационально использовать капсулы, в частности мягкие желатиновые капсулы, так как мягкие капсулы остаются одной из немногих ЛФ, способных сохранять и доставлять липофильные вещества в легкодоступной для организма форме – растворе.
Рис. 2. Лекарственные формы с эфирными маслами.
При использовании эфирного масла в качестве фармацевтической субстанции встает вопрос о стандартизации. До 1960-х гг. эфирные масла оценивали по таким классическим методам, как физические свойства (плотность, угол вращения поляризованного света, показатель преломления, температуры замерзания, плавления, кипения) и химические показатели (эфирное и кислотное число, эфирное число после ацетилирования). Стремительное развитие приборной и аналитической базы анализа органических соединений способствовало более детальному и тонкому анализу эфирных масел. Развитие хроматографических методов разделения и спектральных характеристик органических веществ, в том числе масс-спектрометрии, обеспечило возможность выделения и определения структуры природных соединений эфирных масел [5]. Это дает возможность для более точной стандартизации эфирных масел, содержащих в своем составе большое разнообразие соединений, обладающих биологической активностью.
Выводы
1. В качестве перспективных эфиромасличных растений для внедрения в медицинскую практику следует выделить траву герани душистой, кожуру плода лимона, плоды кориандра и можжевельника, семена чернушки посевной и др.
2. Актуальна разработка рациональных для перорального введения лекарственных форм эфирных масел, в частности мягких желатиновых капсул.
3. Для внедрения новых субстанций эфирных масел в медицинскую практику необходима стандартизация и разработка проекта фармакопейной статьи на субстанцию и лекарственную форму.
Рецензенты:
Олешко О.А., д.фарм.н., профессор кафедры фармацевтической технологии ГБОУ ВПО «ПГФА» Минздрава России, г. Пермь;
Белоногова В.Д., д.фарм.н., профессор, заведующая кафедрой фармакогнозии с курсом ботаники ГБОУ ВПО «ПГФА» Минздрава России, г. Пермь.
Источник