- Дисплазия шейки матки
- Дисплазия шейки матки, симптомы
- Что такое биопсия шейки матки?
- Лечение дисплазии шейки матки
- Медикаментозное лечение
- Основные условия для проведения радиоволновой терапии
- Основные показания к хирургическому лечению:
- Основные направления в лечении пациентов с дисплазией соединительной ткани
- Витамин С
- Витамин Р
- Витамин В6
- Витамин D
- Витамин Е
- Магний
- Марганец
- Кальций
- Селен
- 1-й курс
- 2-й курс
- 3-й курс
Дисплазия шейки матки
Поставленный диагноз «дисплазия шейки матки» — это сигнал женского организма, который требует внимания и помощи. Женский организм не в силах в одиночку преодолеть критические пороги заболевания. Женщины часто дисплазию шейку матки сравнивают с эрозией. Действительно, эрозию шейки матки и дисплазию шейки матки могут вызывать похожие этиологические факторы, но тактика ведения и лечения данных заболеваний принципиально разная.
Дисплазию шейки матки относят к предраковым состояниям эпителия шейки матки. Однако это не значит, что дисплазия шейки матки обязательно реализуется в рак. На вопрос можно ли вылечить дисплазию шейки матки, ответ очевиден: можно, если вовремя и правильно начать лечение!
Что же такое дисплазия шейки матки? Как образно и понятно объяснить диагноз простой женщине. Постараемся Вам помочь.
Представьте, что в норме эпителий, покрывающий шейку матки, имеет строгую слоистость. Слои эпителия располагаются строго последовательно. Нижний слой (базальный), затем идет парабазальный, промежуточный, поверхностный слои эпителия. Представьте свою шейку матки в виде салата « под — шубой».
Когда слои неправильно располагаются, возникает хаотический, диспластический процесс. В зависимости от выраженности изменений в эпителии шейки матки различают легкую, умеренную и тяжелую дисплазию шейки матки.
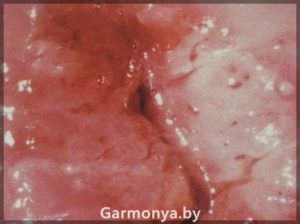
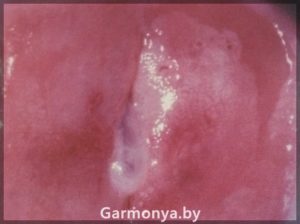
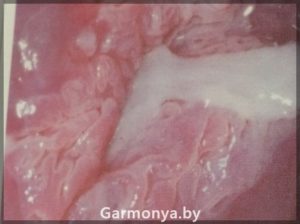
Дисплазию 1 степени ставят при выявлении полиморфных клеток с особыми (гиперхромными) ядрами и высоким ядерно-цитоплазматическим соотношением, а также при нарушении дифференцировки в нижней трети пласта многослойного плоского эпителия. Дифференцировка в верхних двух третьих эпителия происходит нормально.
Дисплазия шейки матки 2 степени характеризуется наличием клеточного атипизма и многочисленных митозов (делений клеток) в нижней половине эпителиального пласта. В верхней половине дифференцировка клеток не изменена.
Дисплазия шейки матки 3 степени характеризуется клеточным атипизмом в двух третях толщины эпителия..
Рак на месте или по латыне «cancer in situ» — состояние, когда все слои эпителия шейки матки поражаются полностью.
Среди причин, способствующих возникновению дисплазии шейки матки, различают экзогенные: (ВПГ, вирус простого герпеса и др. половые инфекции) и эндогенные факторы (хронические воспалительные заболевания органов малого таза и мочеполовых органов, нарушение гормонального гомеостаза, снижение иммунного ответа и др.) и смешанные факторы.
Исследования последних лет доказано, что в 50-80 % образцов умеренной и тяжелой дисплазии эпителия шейки матки обнаружен ВПЧ высокой степени онкогенного риска (преимущественно 16 и 18 типов).
Дисплазия шейки матки, симптомы
При дисплазии шейки матки как самостоятельном заболевании жалобы больных и симптоматика чаще отсутствуют. Боли внизу живота и кровянистые выделения из половых путей появляются только в особо запущенных случаях, когда заболевание развивалось на протяжении нескольких лет.
Дисплазия шейки матки может быть выявлена на обычном профилактическом осмотре. Надо отметить, что дисплазия шейки матки — это полностью предотвратимое заболевание для женщины, которая регулярно следит за своим здоровьем и выполняет обязательное цитологическое исследование на профилактическом визите у врача гинеколога или специально обученной медицинской сестры.
Если у женщины выявлены изменения в цитологии, указывающие на дисплазию 1 , 2 или 3 степени далее проводится углубленное обследование по протоколу лечения, утверждённому Министерством здравоохранения.
При сочетании дисплазии с фоновым заболеванием шейки матки больные могут предъявлять жалобы на бели, зуд наружных половых органов и т.д. В данной ситуации выполняется исключение половых инфекции, в том числе гонореи, ВПЧ, герпеса. Проводится противовоспалительное лечение с учетом диагностических находок.
С помощью специального прибора (кольпоскопа) уточняют характер данной болезни, выявляют наличие, распространенность и степень выраженности кольпоскопических проявлений дисплазии шейки матки с последующим забором материала из очага поражения для прицельного цитологического исследования. Цитология мазков позволяет установить степень выраженности дисплазии.
Для дальнейшего установления диагноза прицельно берут биопсию шейки, делают эндоцервикальный соскоб и их гистологически исследуют. Результаты исследования являются решающими в постановке диагноза дисплазии или рака шейки матки!
Что такое биопсия шейки матки?
Биопсия шейки матки – это инвазивный метод обследования шейки. С подозрительного участка шейки матки берется 1 или несколько участков ( кусочков) ткани шейки матки специальным инструментом. В медицинском центре Гармония биопсия шейки матки выполняется радиоволновым методом с помощью американского аппарата Сургитрон специальной радиоволновой петлей.
Манипуляция выполняется бескровно (используется два режима радиоволнового воздействия аппарата Сургитрон: разрез и коагуляция сосудов шейки матки) и безболезнено. Полученный материал помещается в специальную пробирку с формалином, фиксируется и далее передается для углубленного исследования в гистологическую лабораторию, где помещается в парафиновую среду. Далее парафиновые блоки исследуются врачом патоморфоологом под особым микроскопом. Врач патологоморфолог выносит окончательный диагноз.
Лечение дисплазии шейки матки
Лечение зависит от того, возникла дисплазия на основе предшествующих заболеваний шейки матки: цервицит, эрозия шейки матки, вирусное поражение шейки матки и т.д. или диагностировано впервые как самостоятельное заболевание.
Метод лечения определяют строго индивидуально, исходя из особенностей кольпоскопии, степени дисплазии: легкой, средней или тяжелой. Также лечение зависит от возраста больной и особенностей детородной функции, строения шейки локализации диспластического процесса, сопутствующих болезней. Однако радикальность вмешательства определяют по степени дисплазии.
Медикаментозное лечение
Чаще всего показано больным легкой дисплазией. При ее назначении используют два методологических подхода: выжидательную тактику и немедленную локальную деструкцию. В нашем медицинском центре мы используем радиоволновой метод лечения.
Выжидательная тактика основана на том, что у 30-60 % больных возможна спонтанная регрессия поражения шейки матки. Тогда необходимы постоянные цитологическое исследования в динамике (1-3 мес.), медикаментозное купирование воспалительного процесса, подавление пролиферативных изменений, регуляция менструального цикла. Если нет эффекта (регресса дисплазии) в течение 3 месяцев, следует изменить тактику лечения в сторону более радикальных мер.
Медикаментозное лечение показано также больным с легкой дисплазией назначают средства, подавляющие пролиферативную активность, обладающие противовирусным и иммуномодулирующим эффектом. Ретиноиды (предшественники и аналоги витамина А) подавляют пролиферацию, стимулируют киллеры и активность цитотоксических клеток. Подофиллин, трихлоруксусная кислота малоэффективны и токсичны. Они способны также подавлять патологические митозы с эффективностью 86 %. 5-Фторурацил применяют по методике лечения плоских папиллом или в форме мази (крема), которую наносят на поверхность шейки матки 2 раза в день на протяжении 2 нед. Интерферон стимулирует активность лимфоцитов, повышает уровень иммуноглобулинов, обладает антипролиферативной и антивирусной активностью. Его назначают в инъекциях, местно в виде геля или мази до 4 раз в сутки на протяжении 20 дней.
Второй методологический подход заключается в локальном удалении (деструкции) патологического очага или радикальной терапии.
Хирургическое устранение дисплазии независимо от метода разрушения патологической ткани должно быть достаточной глубины. Обычно крипты в цервикальном канале бывают глубиной до 7,8 мм, в среднем 3,4 мм. Поражение крипт тяжелой дисплазией и внутриэпителиальным раком бывает протяженностью до 5,2 мм (средняя глубина их проникновения по криптам − 3,2 мм). Поэтому при деструкции на глубину 3 мм полностью разрушается весь патологический очаг у 95 % больных, а на глубину 4 мм − у 99 %.
Криогенное воздействие − идеальное и оптимальное лечение легкой и умеренной дисплазии, особенно патологических очагов размером до 2,5−3 см. Криотерапия тяжелой дисплазии допускается, но не является методом выбора. Обычно используют большие температурные режимы при экспозиции 8−10 мин. Процедуру проводят в два этапа. Однако когда нужно промораживать более половины длины шейки матки и невозможен гистологический контроль после операции, от такой деструкции лучше отказаться.
В нашем медицинском центре Гармония мы используем современный метод лечения дисплазии шейки матки- радиоволновую терапию (РВТ).
РВТ показана больным легкой и умеренной дисплазией. Перед РВТ женщину полностью обследуют по регламентирующим протоколам. Исключают половые инфекции, сифилис, ВИЧ, гепатит С и В. Выполняют УЗИ органов малого таза, биопсию шейки матки, кюретаж цервикального канала, аспират из полости матки или РДВ. Шейку матки обрабатывают маркерами (раствором Люголя) для определения границ поражения.
Основные условия для проведения радиоволновой терапии
- нет данных (цитологической-эндоскопического скрининга), свидетельствующих о раке шейки матки;
- лечение должен проводить специалист, знающий основы кольпоскопии.
При дисплазии 3 степени вопрос лечения дисплазии решается совместно с онко-гинекологом. В последнее время достаточно часто проводят хирургическое лечение дисплазии. Ампутация шейки матки по Штурмдорфу показана больным, у которых дисплазия сочетается с элонгацией шейки при опущении матки.
Основные показания к хирургическому лечению:
- возраст больных старше 50 лет,
- отсутствие условий для конизации вследствие анатомических изменений,
- атрофии шейки,
- сглаживание сводов,
- тяжелая дисплазия на всем протяжении эндоцервикса;
- неэффективность предшествовавшего лечения либо невозможность иного лечения.
Согласно методическим рекомендациям белорусских онкогинекологов, целесообразно лечить дисплазии индивидуально в зависимости от клинической картины болезни и возраста женщины.
У женщин моложе 40 лет с умеренной дисплазией допустимо радиоволновое лечение шейки матки. Больным, у которых умеренная дисплазия сочетается с обширным эктропионом, деформацией шейки матки, а также старше 45 лет необходима диатермоэлектроэксцизия шейки матки либо операция типа операции Штурмдорфа, Эммета. Хирургическое вмешательство следует расширять до удаления шейки матки с телом матки у больных с сопутствующими умеренной дисплазии опухолями и опухолевидными образованиями матки и придатков (особенно у женщин в климактерический и менопаузальный периоды).
Дисплазия шейки матки может сочетаться с раком в начальных стадиях. Тогда в основном выполняют конусовидное иссечение или ампутацию шейки матки. Вследствие сглаженности влагалищных сводов, атрофических изменений полового аппарата у женщин старше 45-50 лет невозможно выполнить органосохраняющие вмешательства, поэтому операцию следует расширить до простой гистерэктомии (удаление шейки матки и тела матки).
Наблюдение за оперированными пациентками проводят акушеры-гинекологи общей лечебной сети путем контрольных осмотров с кольпоскопическим и цитологическим исследованиями.
Больную легкой дисплазией достаточно осмотреть 2 раза в году. Женщине с умеренной дисплазией контрольные осмотры необходимы каждые 3 месяца, а с тяжелой дисплазией − не реже 1 раза в месяц. Оперированных снимают с диспансерного учета при получении трех отрицательных результатов кольпоскопического и цитологического исследований, но не ранее чем через 2 года. Если после специального лечения вновь выявляют признаки дисплазии, женщину нужно направить к онкогинекологу для углубленного обследования и лечения в онкологическом учреждении.
Информация, расположенная на сайте носит строго информационный характер и не может быть использована самостоятельно.
Получить квалифицированную помощь можно у наших врачей гинекологов, прошедших специальную подготовку по патологии шейки матки. Запись по контактным телефонам или на сайте.
Источник
Основные направления в лечении пациентов с дисплазией соединительной ткани
Рассмотрены возможности медикаментозного воздействия на систему соединительной ткани с позиций влияния различных медикаментозных препаратов, макро-, микроэлементов, витаминов и биостимуляторов на обменные процессы в соединительной ткани с целью укрепления
Possibilities of drug effect on connecting tissue system accounting for different preparation’, macronutrients’, trace elements’, vitamins’ and biostimulant’s effects on metabolic process in connecting tissue to fixation of components of connecting tissue has been analyzed.
Проявления дисплазии соединительной ткани (ДСТ) на сегодняшний день знакомы почти каждому врачу: терапевту, педиатру, кардиологу, неврологу, гинекологу и многим другим специалистам. Практически на всех научных форумах, какой бы направленности они ни были, есть секции, посвященные данной проблеме. Однако не стихают дискуссии не только по вопросам классификации и диагностики, но и лечению пациентов с соединительнотканной дисплазией. Несмотря на выход новых национальных рекомендаций в 2012 году по лечению и ведению данной категории пациентов, имеется печальная статистика о применении их в реальной клинической практике [1]. Согласно данным Омского центра «Дисплазии соединительной ткани» в 23,4% случаев пациентам диагностируется диагноз ДСТ и не проводится лечение, в 66,3% случаев лечащий врач назначает только препараты магния, в 10,3% лечащий врач проводит полное комплексное лечение пациента с ДСТ. Все эти данные получены на первичных приемах из амбулаторных карт пациентов, направленных на консультацию для верификации диагноза и диспансерного наблюдения в Омском центре «Дисплазии соединительной ткани».
Согласно определению, разработанному Омской школой во главе с профессором В. М. Яковлевым: «Дисплазия соединительной ткани — это генетически детерминированное состояние, характеризующееся дефектами волокнистых структур и основного вещества соединительной ткани, приводящее к нарушению формообразования органов и систем, имеющее прогредиентное течение, определяющее особенности ассоциированной патологии, а также фармакокинетики и фармакодинамики лекарств» [2].
Однако генная терапия наследственных заболеваний человека пока остается проблемной. Результаты этой этиотропной терапии остаются весьма скромными. В основном в литературе указывается на пробные методики лечения болезней с установленными и конкретным генным дефектами (наследственные заболевания или дифференцированные формы ДСТ). Стратегия лечения пациентов с генетически детерминированной патологией (недифференцированная ДСТ) при большом разнообразии генетического дефекта сводится к коррекции метаболизма соединительной ткани, лежащего в основе патогенеза данного состояния. При этом не ставятся задачи повышения синтеза коллагена или предупреждение деградации белков, так как стратегия лечения должна строиться на выравнивании двух этих процессов.
Медикаментозная коррекция не решает проблемы комплексного многоуровневого воздействия на систему соединительной ткани и поэтому не может быть признана единственно возможной. Однако применение медикаментозного воздействия на систему соединительной ткани предпринято с позиций влияния различных медикаментозных препаратов, макро-, микроэлементов, витаминов, биостимуляторов на обменные процессы в соединительной ткани, направленных на укрепление компонентов соединительной ткани, и может применяться как фундамент в программах лечения.
Согласно литературным данным у подавляющего большинства пациентов с ДСТ имеет место снижение уровня большинства макро- и микроколлагеноспецифических биоэлементов. Наиболее часто встречается дефицит кремния (100%), селена (95,6%), калия (83,5%); кальция (64,1%); меди (58,7%); марганца (53,8%), магния (47,8%). Все они принимают активное участие в минерализации костной ткани, синтезе и созревании коллагена [3]. В связи с этим показаны продукты, обогащенные веществами, участвующими в метаболизме соединительной ткани: витаминами С, Е, В6, D, Р (флавоноиды), макро- и микроэлементами (магний, медь, марганец, цинк, кальций, калий, селен) [4, 5].
Витамин С
Свежие овощи, фрукты, черноплодная рябина, черная смородина, шиповник, сладкий красный перец, горох, клубника, капуста (кочанная, брюссельская, брокколи), хвоя, мандарины, апельсины, грейпфрут, помидоры, зелень петрушки, укропа и пр.
Витамин Р
Листья чая, листья руты пахучей, цитрусовые, плоды шиповника, рябины черноплодной, цветки гречихи, софоры, трава горца птичьего, листья подорожника большого, трава володушки многожильчатой, астрагала шерстистоцветкового, листья боярышника кроваво-красного, каштана обыкновенного, дуба, плоды черники обыкновенной, калины обыкновенной, земляники лесной, малины обыкновенной.
Витамин В6
Хлеб из муки грубого помола, зерна злаков, бобовые, гречневая и овсяная крупы, бананы, капуста, картофель, мясо, печень, почки, домашняя птица, молоко, творог, сыр, рыба, дрожжи.
Витамин D
Печень тунца, трески, палтуса, кита, сельдь, лосось, сардины, цельное молоко, желтки яйца.
Витамин Е
Зародыши злаковых культур, зеленые органы овощей, кукурузное, оливковое, виноградное, льняное, подсолнечное и другие растительные масла, многие овощи и фрукты, печень, мясо, рыба, сливочное масло, молоко; плоды облепихи крушевидной, рябины черноплодной, смородины черной, ежевики сизой, масло плодов ореха грецкого.
Магний
Палтус, семена тыквы, ячмень, гречка, йогурт, бобовые, шпинат, свежая зелень, нерафинированные крупы.
Печень, почки, мозги, морепродукты, гречневая крупа, миндаль, репа, авокадо, шпинат, перец сладкий красный, пшеничные зародыши, пшеничные отруби, пшенная, ячневая крупа, морковь, огурцы, томаты, редис, свекла, капуста, бобовые, земляника лесная, смородина черная, шоколад, какао, кофе, цитрусовые, крыжовник, грибы, яблоки.
Марганец
Пророщенная пшеница, орехи фундук, мука пшеничная, хлеб из муки цельного помола, какао-бобы, миндаль, хлеб ржаной, крупа гречневая, фасоль.
Кальций
Молоко пастеризованное, сметана, кефир, творог, йогурт, молоко сгущенное, сыр, брынза, плавленый сыр, рыба, петрушка, кунжут, миндаль, фасоль, абрикосы сушеные.
Маковое семя, семена подсолнуха, семя льна, соевая мука, соя, бразильский орех, чечевица сухая, арахис, грецкий орех, миндаль, орех кешью, лесной орех, белый гриб, хрен, фисташки, крапива.
Селен
Морская и каменная соль, почки (свиные, говяжьи и телячьи), печень, сердце, яйца, морская рыба, крабы, омары, лангусты, креветки, пшеничные отруби, проросшие зерна пшеницы, зерна кукурузы, помидоры, пивные дрожжи, грибы, чеснок, черный хлеб, другие продукты из муки грубого помола.
Однако назначением диетотерапии скомпенсировать дефицит микроэлементов сложно, кроме этого из всего списка микроэлементов есть наиболее значимые для стабилизации и укрепления структуры соединительной ткани. Безусловно, основой терапии пациентов с ДСТ является назначение препаратов. содержащих магний, т. к. для структуры соединительной ткани крайне важна роль магния, который является одним из основных биоэлементов, обеспечивающих физиологический метаболизм соединительной ткани. При дефиците магния — а это весьма частое явление у лиц с ДСТ — белковый синтез соединительной ткани замедляется, активность матричных металлопротеиназ увеличивается и внеклеточный матрикс прогрессивно деградирует, так как структурная поддержка ткани (в частности, коллагеновые волокна) разрушается быстрее, чем синтезируется [6].
На основе собственных многолетних клинических наблюдении был сделан вывод о безопасности и эффективности препаратов магния (Магнерот и Магне В6) в плане уменьшения вегетативной дисрегуляции и клинических проявлений ДСТ (нормализация частоты сердечных сокращений, артериального давления, снижение эпизодов нарушения ритма и т. д.), было установлено позитивное влияние на физическую работоспособность и целесообразность их применения на подготовительном этапе перед занятиями лечебной физкультурой, особенно у пациентов с ДСТ, имеющих изначально низкую толерантность к физическим нагрузкам [7, 8].
Опираясь на литературные и собственные данные о благоприятном влиянии магния на укрепление соединительной ткани, пациентам с ДСТ в качестве первого курса терапии рекомендовано назначение одного из вариантов препаратов (Магнерот или Магне В6), содержащих магний, продолжительностью курса не менее 4–6 нед.
Но не только магний имеет ключевое значение для поддержания метаболизма соединительной ткани, ионы меди являются интегральной частью активного центра лизилоксидазы — фермента, обеспечивающего химическую модификацию коллагена и эластина соединительной ткани.
Дефицит меди приводит к нарушению коллагена и эластина, что способствует формированию аномалий развития сердечно-сосудистой системы и скелета. Нарушение метаболизма при недостаточности меди приводит к различным патологическим синдромам, нередко имеющим генетическую природу (синдром Марфана, синдром Элерса–Данло и др.). У лиц с недифференцированной ДСТ дефицит меди часто проявляется сопровождающейся повышенной растяжимостью кожи, гиперэластозом, гипермобильностью суставов.
С целью стабилизации коллагена и эластина пациентам с ДСТ необходимо назначать 1% раствор сульфата меди — 10 капель на прием 3 раза в день продолжительностью до 4 недель.
Цинк необходим для функционирования многих металлоферментов, регулирующих ремоделирование коллагена в соединительной и костной тканях. Цинк активирует ферменты (матриксные металлопротеиназы), которые способствуют образованию фагоцитов и усиливают активность макрофагов, вследствие чего фибробласты поступают в пораженную область, восполняя дефицит гиалуроновой кислоты, которая относится к гликозамингликанам, формирующим аморфное вещество соединительной ткани. Таким образом, назначение препаратов цинка при лечении пациентов с ДСТ не менее важно, как и препаратов, содержащих магний и медь.
Положительное влияние на синтез коллагена и образование поперечных сшивок в его макромолекуле оказывает и аскорбиновая кислота, при ведении пациентов с ДСТ при отсутствии оксалатурии и семейного анамнеза по мочекаменной патологии возможно назначение аскорбиновой кислоты в виде коктейлей с молоком, йогуртом; доза — не более 1 г в день в зависимости от возраста.
Назначение микроэлементов это основа медикаментозной терапии в лечении пациентов с ДСТ с целью стимуляции коллагенообразования. Для достижения успеха в лечении пациентов с ДСТ целесообразно проводить комплексную метаболическую терапию [5]:
1) коррекция нарушений синтеза и катаболизма гликозаминогликанов (хондроитина сульфат);
2) стабилизация минерального обмена (витамин D2 и его активные формы, препараты кальция);
3) коррекция уровня свободных аминокислот крови (метионин, глутаминовая кислота, глицин);
4) улучшение биоэнергетического состояния организма (Мексикор, Милдронат, Лецитин, Лимонтар).
За назначением данных групп препаратов и схем лечения стоит большое количество клинических исследований с достоверными положительными результатами, позволяющими улучшить качество жизни пациентов с ДСТ и остановить прогредиентность течения данного состояния. В этой связи мы рекомендуем коллегам не ограничиваться только назначением препаратов магния, а проводить курсами метаболическую терапию 1–2 раза в год, в зависимости от состояния больного; продолжительность курса — до 4 месяцев. Примером терапии может послужить схема лечения, применяемая в Омском центре «Дисплазии соединительной ткани»:
1-й курс
Препарат Магне В6 в ампулах: взрослым рекомендуется принимать 3–4 ампулы в сутки. Детям старше 1 года (масса тела более 10 кг) суточная доза составляет 10–30 мг/кг и равняется 1–4 ампулам. Суточную дозу следует разделить на 2–3 приема, принимать во время еды, запивая стаканом воды. Раствор в ампулах растворяют в 1/2 стакана воды для приема 2–3 раза в день во время еды. В таблетках: взрослым рекомендуется принимать по 6–8 табл./сут; детям старше 6 лет (массой тела более 20 кг) — 4–6 табл./сут.
Магне В6 форте взрослым назначают 3–4 табл./сут, разделенные на 2–3 приема. Детям в возрасте старше 6 лет (с массой тела около 20 кг) назначают в дозе 10–30 мг/кг/сут (0,4–1,2 ммоль/кг/сут), т. е. 2–4 таб./сут, разделенные на 2–3 приема.
Магнерот назначают по 2 табл. 3 раза в день в течение 7 дней, затем — по 1 табл. 2–3 раза в сутки ежедневно. Продолжительность курса — не менее 4–6 нед. При необходимости Магнерот можно применять длительное время. При ночных судорогах икроножных мышц рекомендуется принимать по 2–3 табл. вечером.
Аскорбиновая кислота (при отсутствии оксалатурии и семейного анамнеза мочекаменной болезни) — до 0,6 г в день — 4 недели.
Милдронат — взрослым 5 мл раствора внутривенно на аутокрови № 10, далее по 250 мг 2 раза в день — 4–6 недель.
2-й курс
Цинкит — по 1 таблетке 2 раза в день — 1,5 месяца.
Мексикор — 100 мг 2% раствора внутривенно № 10, затем по 1 капсуле 3 раза в день –3 месяца.
3-й курс
Сульфат меди — 1% раствор, 10 капель на прием 3 раза в день — 4 недели.
Кальций Сандоз Форте — 500 мг в сутки 1–2 месяца, или Кальцемин Адванс — 1 таблетка 2 раза в сутки до 4 месяцев (индивидуально).
На фоне указанных курсов рекомендуется применение лимфотропных трав (корень шиповника, трава манжетки, кровохлебки) в виде отваров — 2–3 раза в день — с заменой состава сбора каждые 2 недели.
Главное помнить, что ведущим компонентом терапии должны быть немедикаментозные воздействия, направленные на улучшения гемодинамики (лечебная физкультура, дозированные нагрузки, аэробный режим). Однако нередко существенным фактором, ограничивающим достижение целевого уровня физических нагрузок у пациентов с ДСТ, оказывается плохая субъективная переносимость тренировок (обилие астенических, вегетативных жалоб, эпизоды гипотонии), что снижает приверженность пациентов к этому виду реабилитационных мероприятий. Так, по нашим наблюдениям до 63% пациентов имеют низкую толерантность к физической нагрузке по данным велоэргометрии, большинство из этих пациентов отказываются от продолжения курса лечебной физкультуры [9]. В основе низкой толерантности к физической нагрузке этиологическим фактором выступает гипокинетический тип гемодинамики у пациентов с ДСТ. А. Темниковой предложена методика патогенетической коррекции гипокинетического типа гемодинамики с помощью венотонического препарата — диосмина (Детралекс 500 мг), нормализующего структуру венозного притока у лиц с низкой толерантностью к физическим нагрузкам. После приема препарата по 2 таблетки в два приема в течение 4 недель у 100% пациентов отмечалось улучшение самочувствия, снижение утомляемости, увеличение работоспособности, в 62% случаях — уменьшение проявлений вегетативной дисфункции (синусовой тахикардии и дыхательной аритмии) с отчетливой тенденцией к увеличению ударного и минутного объемов правого и левого желудочков [10].
В связи с этим представляется единственно верным применение в комплексе с лечебной физкультурой препаратов метаболического действия для качественного лечения пациентов с дисплазией соединительной ткани. Не стоит забывать, что помимо базисной метаболической терапии, приведенной в данной статье, необходимо подходить индивидуально к каждому пациенту и, учитывая синдромное течение недифференцированной ДСТ, проводить активное лечение и профилактику ведущего синдрома на фоне базисной терапии.
Наибольшего внимания заслуживают аритмический и сосудистый синдром, в связи с повышенным риском внезапной смерти у данных пациентов. Согласно литературным данным β-адреноблокаторы предотвращают риск внезапной смерти у пациентов с ДСТ, способствуя устранению тахикардии, кроме того, данная группа препаратов имеет положительное влияние на диаметр аорты, особенно это выражено при диаметре аорты более 4 см. Патогенетически это происходит за счет уменьшения выброса в аорту и соответственно снижения нагрузки на стенки восходящего отдела, тем самым корригируя сопутствующую гемодинамическую артериальную гипертензию [11]. Применение β-адреноблокаторов нередко приводит к ухудшению самочувствия, так как большинство пациентов с ДСТ имеют нормальное или пониженное артериальное давление. Пациенты жалуются на усиление головокружения, слабость, снижение работоспособности, что приводит к отказу от лечения как самим пациентом, так и лечащим врачом. По нашим данным подбор β-адреноблокаторов из-за системной гипотонии следует подбирать методом титрования как при сердечной недостаточности. Согласно полученным нами данным при назначении β-адреноблокаторов (бисопролол) в начальной дозе 1,25 мг/сут с дальнейшим увеличением дозы до 2,5 мг/сут через 2 недели и дальнейшей титрации до достижения уровня частоты сердечных сокращений 59–69 ударов в минуту, отмечалось улучшение самочувствия и насосной функции сердца, снижение активации симпатического отдела нервной системы и тревожности [12]. Возможно также применение и других β-адреноблокаторов, таких как пропранолол в дозе от 40 до 200 мг в сутки или длительно действующих β-адреноблокаторов, например, атенолола в дозе от 25 до 150 мг/сутки или метопролола 50–200 мг в сутки.
Аневризма и дилатация грудной аорты являлись основной причиной ранней смерти пациентов с синдромом Марфана до 1970 г. За последние 30 лет продолжительность жизни пациентов с синдромом Марфана увеличилась прежде всего за счет своевременной диагностики жизнеугрожающих состояний и совершенствования тактики ведения пациентов в целом. Тем не менее, следует обратить внимание, что в значительном числе случаев наличие аневризмы аорты констатируется впервые только при секционном исследовании: в 95% случаев первым симптомом оказывается смерть, в то время как симптомы-предвестники разрыва или диссекции аневризмы аорты регистрируются только в 5% случаев. Если при синдроме Марфана существует статистика о распространенности дилатации и аневризме грудной аорты, то точная частота формирования данных изменений грудной аорты при недифференцированной форме ДСТ не известна. Накапливаются данные о большем в сравнении с общей популяцией диаметре аорты у пациентов с деформациями грудной клетки, а также у пациентов с пролапсом митрального клапана без признаков синдромной формы ДСТ. В последние годы появились работы, демонстрирующие перспективы применения ингибиторов ангиотензинпревращающего фермента (иАПФ) и блокаторов рецепторов ангиотензина II при расширении аорты у пациентов с синдромом Марфана [13, 14]. Таким образом, на сегодняшний день у врачей имеется достаточный арсенал средств для борьбы с прогрессированием ДСТ и предотвращения развития осложнений.
Литература
- Наследственные нарушения соединительной ткани. Российские рекомендации. М., 2012. 49 c.
- Яковлев В. М., Нечаева Г. И. Кардиореспираторные синдромы при дисплазии соединительной ткани. Омск: Изд-во ОГМА, 1994. 217 с.
- Кадурина Т. И., Аббакумова Л. Н. Принципы реабилитации больных с дисплазией соединительной ткани // Лечащий Врач. 2010. № 4. С. 28–31.
- Нечаева Г. И., Конев В. П., Друк И. В. и др. Выявление и тактика ведения пациентов с недифференцированной дисплазией соединительной ткани. Методические рекомендации для врачей. Под ред. акад. А. И. Мартынова. М.: РГ ПРЕ100, 2011. 52 c.
- Мартынов А. И., Яковлев В. М., Нечаева Г. И. и др. Диагностика и тактика ведения пациентов с дисплазией соединительной ткани в условиях первичной медико-санитарной помощи. Методические рекомендации для врачей. Омск, 2013. 133 c.
- Громова О. А. Магний и пиридоксин: основы знаний. М.: РСЦ Институт микроэлементов, Юнеско, 2006. 176 с.
- Нечаева Г. И., Яковлев В. М., Друк И. В., Тихонова О. В. Нарушения ритма сердца при недифференцированной дисплазии соединительной ткани // Лечащий Врач. 2008. № 6. C. 2–7.
- Нечаева Г. И. и др. Комплексная реабилитация больных с дисплазией соединительной ткани в условиях многопрофильного клинического учреждения. Омск, 2001. С. 39–44.
- Дубилей Г. С., Борисенко И. А., Гусев Д. А., Мазурова Л. Э. Комплексный подход к вопросу восстановительного лечения пациентов с дисплазией соединительной ткани / Дисплазия соединительной ткани: Материалы симпозиума, Омск, 1 ноября 2002. С. 160–162.
- Темникова Е. А. Медикаментозная коррекция нарушений гемодинамики при дисплазиях соединительной ткани: автореф. дис. … канд. мед. наук. Томск, 2001. 18 с.
- Shores J., Berger K. R., Murphy E. A., Pyerit R. E. Progression of aortic root dilatation and the benefit of long-term beta-adrenergic blockade in Marfan’s syndrome // N Engl J Med. 1994; 330: 1384–1385.
- Нечаева Г. И., Дрокина О. В. Возможности применения бисогаммы для контроля частоты сердечных сокращений у пациентов молодого возраста с дисплазией соединительной ткани // Кардиология. 2014. № 5. С. 14–18.
- Ahimastos A. A. et al. Effect of Perindopril on Large Artery Stiffness and Aortic Root Diameter in Patients With Marfan Syndrome // JAMA. 2007. № 298 (13). P. 1539–1547.
- Groenink M., den Hartog A. W., Franken R. et al. Losartan reduces aortic dilatation rate in adults with Marfan syndrome: a randomized controlled trial // Eur. Heart. J. 2013. Vol. 34. P. 3491–3500.
Г. И. Нечаева 1 , доктор медицинских наук, профессор
О. В. Дрокина
И. В. Друк, кандидат медицинских наук
М. В. Вершинина, кандидат медицинских наук
Е. А. Лялюкова, кандидат медицинских наук
И. В. Колменкова
ГБОУ ВПО ОмГМА МЗ РФ, Омск
Источник