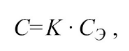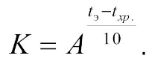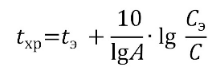- Учебная деятельность
- Учебная деятельность
- Архив семинаров в 2020 году
- Архив семинаров в 2019 году
- Архив семинаров в 2018 году
- Архив семинаров в 2017 году
- Обучение
- Обучение и GMP консалтинг
- Темы обучений:
- Сроки годности лекарственных средств (ОФС.1.1.0009.15)
- Основные термины и определения
- Общие положения
- Долгосрочные испытания стабильности лекарственных средств
- Испытания стабильности методом «ускоренного старения»
- Испытания стабильности методом экстраполяции
- Испытания стабильности методом крайних вариантов
- Испытания стабильности матричным методом
- Исследование влияния упаковки на стабильность лекарственного средства
- Исследования стабильности лекарственных препаратов после восстановления или разведения
- Стресс-исследования и фотостабильность
Учебная деятельность
Учебная деятельность
Реализуемые образовательные программы
На кафедре осуществляется подготовка слушателей по следующим образовательным программам дополнительного профессионального образования (повышение квалификации):
1.Мониторинг движения лекарственных препаратов в медицинских учреждениях.
Общая трудоемкость-36 часов
Программа рассчитана на следующий контингент слушателей: провизоры, руководители аптечной организации или компании дистрибьютора лекарственных средств, заместители руководителя аптечной организации, а также иные лица, ответственные за оборот лекарственных препаратов в аптечной и медицинской организации.
2. Правила надлежащей практики доклинических, клинических испытаний, обеспечение производства и контроль качества лекарственных средств в соответствии с требованиями GxP.
Общая трудоемкость – 432 часа
Программа рассчитана на следующий контингент слушателей: руководители, заместители руководителей, специалисты учреждения здравоохранения фармацевтических компаний и предприятий; врачи всех специальностей, провизоры, специалисты в области контроля качества лекарств, разработчики лекарственных препаратов, сотрудники отделов продвижения и маркетинга;
3. Поиск, доклинические и клинические исследования лекарственных средств («Good Clinical Practice» — GCP).
Общая трудоемкость – 144 часа
Программа рассчитана на следующий контингент слушателей: руководители, заместители руководителей, специалисты учреждения здравоохранения и фармацевтических компаний; врачи всех специальностей, провизоры, специалисты в области контроля качества лекарств, разработчики лекарственных препаратов, сотрудники отделов продвижения и маркетинга;
3. Деятельность Уполномоченного лица на фармацевтических предприятиях.
Общая трудоемкость – 144 часа
Программа рассчитана на следующий контингент слушателей: руководители, заместители руководителей, специалисты фармацевтических компаний и предприятий ; врачи всех специальностей, провизоры, специалисты в области контроля качества лекарств, разработчики лекарственных препаратов, сотрудники отделов продвижения и маркетинга;
4. Доклинические, токсикологические исследования лекарственных средств («Good Laboratory Practice» -GLP).
Общая трудоемкость – 144 часа
Программа рассчитана на следующий контингент слушателей: руководители, заместители руководителей, специалисты учреждения здравоохранения и фармацевтических компаний и предприятий; врачи всех специальностей, провизоры, специалисты в области контроля качества лекарств, разработчики лекарственных препаратов, сотрудники отделов продвижения и маркетинга»
5. Доказательная фитотерапия. Общая трудоемкость – 144 часа Программа рассчитана на следующий контингент слушателей: руководители, заместители руководителей, специалисты учреждения здравоохранения и фармацевтических компаний и предприятий; врачи всех специальностей, провизоры,специалисты в области контроля качества лекарств, разработчики лекарственных препаратов, сотрудники отделов продвижения и маркетинга»
6. Внедрение системы менеджмента качества в клиническую практику. Общая трудоемкость – 144 часа Программа рассчитана на руководителей, заместителей медицинских учреждений, для специалистов медицинского менеджмента, аудиторов и врачей клинических специальностей.
Слушателям, успешно освоившим учебный план программы (GxP, GCP, GМP, GLP , МДЛП, НАП, СМК.) в полном объеме и прошедшим итоговую аттестацию выдается УДОСТОВЕРЕНИЕ о повышении квалификации государственного образца.
На кафедре разработаны программы семинаров(в объеме до 36 часов), на внебюджетной основе для специалистов в сфере обращения лекарственных средств: GxP, GCP, GМP, GLP, доказательная фитотерапия. Внедрение системы менеджмента качества в клиническую практику, Мониторинг движениея лекарственных препаратов, Надлежащая аптечная практика, Аудит клинических исследований.
Слушателям, принимавшим участие в семинарах, выдается «УДОСТОВЕРЕНИЕ» Первый МГМУ им И.М. Сеченова.
Прием документов, предоставляемых специалистом, проводится на кафедре за месяц до начала обучения.
Обучение специалистов по программе «Доклинические, токсикологические исследования лекарственных средств» («Good Laboratory Practice» — GLP) Московская область г. Пущино

Обучение специалистов по программе «Поиск, доклинические и клинические исследования лекарственных средств» («Good Clinical Practice» — GCP) г. Санкт-Петербург
Источник
Архив семинаров в 2020 году
1.Современные методы газовой и высокоэффективной жидкостной хроматографии. Приборное обеспечение.
Дата проведения 29.01-30.01
Программа семинара
2. Микробиологический мониторинг. Правила работы с микроорганизмами 3 и 4 группы.
Дата проведения 19.02-20.02
Программа семинара
3. Технологические аспекты разработки мягких лекарственных форм (суппозитории, гели, мази, кремы, пасты)
Дата проведения 26.02-27.02
Архив семинаров в 2019 году
Архив семинаров в 2018 году
1.Современные методы газовой и высокоэффективной жидкостной хроматографии.Приборное обеспечение
Дата проведения: 24.01-25.01
Программа семинара
2. Изучение стабильности (Современные подходы к изучению стабильности лекарственных средств. Теория и практики.)
Дата проведения: 14.02-15.02
Программа семинара
3. Микробиологический мониторинг. Правила работы с микроорганизмами 3 и 4 группы.
Дата проведения: 26.02-27.02
Программа семинара
4. Обеспечения качества фармацевтического производства (Аудит. Подготовка к проведению аудита. Организация внутреннего и внешнего аудита.)
Дата проведенитя: 28.03-29.03
Программа семинара
5. Фармацевтическая разработка.
Дата проведения: 24.04-25.04
Программа семинара
6. Фармацевтический инжиниринг. Организация производства по правилам GMP. Технологическое оборудование. Валидация (квалификация) производственного оборудования.
Дата проведения: 18.04-19.04
Программа семинара
7. Фармацевтическая разработка (III модуль — использование практического опыта и навыков на завершающем этапе).
Дата проведения: 24.04-25.04
8. Обеспечение качества фармацевтического производства (теория и практики). Управление рисками по качеству. Методология и научный подход.
Дата проведения: 20.06-21.06 Программа семинара
9. Организация лаборатории по GLP. Обеспечение качества. Аудит качества. Аудит поставщиков.
10. Методология GxP: производство, лаборатория, склад. Фармацевтическая логистика.
11. Микробиологический мониторинг. Правила работы с микроорганизмами 3 и 4 группы.
Дата проведения: 17.10-18.10
Программа семинара
12. Фармацевтическая разработка.
Дата проведения: 20.06-21.06
13.Обеспечение качества фармацевтического производства. Валидация компьютерных систем.
Дата проведения: 24.10-25.10
14. Гармонизация требований к разработке инновационных лекарственных препаратов
( Риск — ориентированный подход к управлению системой документации. Целостность данных (data integrity).
Дата проведения: 14.11
Программа семинара
15. I Международная конференция «Гармонизация подходов к фармацевтической разработке».
Дата проведения: 28.11.18
Программа конференции
16. Изучение стабильности (Современные подходы к изучению стабильности лекарственных препаратов. Теория и практики).
Дата проведения: 12.12-13.12
Программа семинара
17. Обеспечение качества фармацевтического производства. (Аудит. Подготовка к проведению аудита. Организация внутреннего и внешнего аудита).
Дата проведения: 19.12-20.12
Программа семинара
Архив семинаров в 2017 году
1.Современные методы газовой и высокоэффективной жидкостной хроматографии.Приборное обеспечение
Дата проведения: 25.01-26.01
Программа семинара
Источник
Обучение
Обучение и GMP консалтинг
Центр фармацевтического образования, технологического консультирования и аудитов качества предприятий.
FAVEA Group имеет 25-летний опыт внедрения стандартов GMP, как на российских, так и на зарубежных производственных площадках. За годы нашей работы мы спроектировали и построили «под ключ» более 50 фармацевтических производств, в том числе производства иммунобиологических, гормональных и цитостатических лекарственных препаратов с использованием трансфера технологий. Реализованные нами объекты имеют заключения о соответствии GMP EU, GMP Евразийского Экономического Союза и Приказу Минпромторга РФ № 916 от 14.06.2013 г., выданные по результатам аудитов со стороны соответствующих организаций.
С целью поддержки наших уважаемых Заказчиков мы проводим техническое и технологическое консультирование, аудит производственных площадок, а также обучение специалистов фармацевтических производств.
FAVEA Group предоставляет следующий спектр услуг:
- Техническая и технологическая оценка проектов с точки зрения возможности их реализации
- Анализ, оценка производственного портфеля и совместимости планируемых к выпуску препаратов, включая анализ токсикологических групп OEB/OHC
- Анализ и оценка рисков для перекрестной контаминации, квалификации и валидации
- Анализ стратегии и подходов к проведению валидации на предприятии (Validation Master Plan)
- Экспертиза проектов с точки зрения соответствия требованиям GxP (Design qualification)
- Аудит действующих производственных предприятий, аудит поставщика с выдачей рекомендаций по проведению модернизации в соответствии с нормами GMP
- Аудит действующих предприятий с оценкой производственной эффективности, а также возможностей увеличения производственных мощностей
- Обучение персонала предприятий по тематике надлежащих практик GxP (более 300 тем): корпоративные и открытые семинары, вебинары, электронное обучение E-learning
- Консультирование по организации производства, квалификации и валидации в соответствии с действующим законодательством
- Оказание содействия по вопросам трансфера фармацевтических технологий
Темы обучений:
Законодательство по регулированию лекарственных средств
Источник
Сроки годности лекарственных средств (ОФС.1.1.0009.15)
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Сроки годности лекарственных средств (ОФС.1.1.0009.15)
ОБЩАЯ ФАРМАКОПЕЙНАЯ СТАТЬЯ
Взамен ГФ ХII, ч.1, ОФС 42-0075-07
Требования данной статьи распространяются на методы определения стабильности лекарственных средств промышленного производства, которые лежат в основе установления их сроков годности.
Основные термины и определения
Срок годности – период времени, в течение которого лекарственное средство полностью отвечает всем требованиям нормативной документации, в соответствии с которой оно было произведено и хранилось.
Стабильность — способность лекарственного средства сохранять химические, физические, микробиологические, биофармацевтические и фармакологические свойства в определенных границах на протяжении срока годности.
Долгосрочные испытания стабильности – испытания, проводимые в соответствии с заявленными в нормативной документации условиями хранения лекарственного средства с целью установления или подтверждения срока годности.
Испытания стабильности методом «ускоренного старения» – испытания, проводимые при повышенной температуре с целью установления или подтверждения срока годности лекарственного средства.
Стресс-исследования – испытания стабильности в стресс-условиях, проводимые с целью исследования вынужденного процесса разложения (установления продуктов и механизмов разложения) лекарственного средства.
Матричный метод исследования стабильности (matrixing) – метод исследования, при котором в определенный момент времени исследуется лишь подгруппа из общего числа образцов всех комбинаций факторов, подлежащих изучению.
Метод крайних вариантов (bracketing) – метод изучения стабильности, при котором во всех временных точках по полному протоколу тестируют только образцы с крайними вариантами факторов.
Экстраполяция − способ получения информации о будущих данных на основании имеющихся.
Дата производства лекарственных препаратов – дата выполнения первой производственной операции, связанной со смешиванием фармацевтической субстанции с другими компонентами. Для фармацевтических субстанций датой производства считается начальная дата операции по фасовке и упаковке.
Дата выпуска – дата поступления или разрешения поступления лекарственного средства в обращение.
Общие положения
Срок годности лекарственного средства устанавливается экспериментально при хранении в течение определенного времени в условиях и упаковке, регламентируемых нормативной документацией, и по мере накопления данных он может быть изменен как в сторону увеличения, так и в сторону уменьшения.
В основу определения сроков годности положено изучение стабильности лекарственного средства с использованием химических и физико-химических методов анализа, указанных в общих фармакопейных статьях, а также, в случае необходимости, других специальных методов исследований, например, биологических методов анализа, фармакологических испытаний.
Срок годности лекарственных препаратов устанавливают независимо от сроков годности фармацевтических субстанций. Однако для лекарственных препаратов, произведенных путем фасовки фармацевтических субстанций, следует учитывать, что стабильность лекарственных препаратов может зависеть от остаточного срока годности используемой фармацевтической субстанции.
Под остаточным сроком годности подразумевается период времени, оставшийся до окончания установленного срока годности лекарственного средства.
Также необходимо учитывать и оценивать влияние на стабильность лекарственных препаратов фактора длительного хранения нерасфасованной и промежуточной продукции до передачи с одного производственного участка на другой или на участок упаковки.
Первоначальный срок годности лекарственного средства определяет производитель (разработчик) лекарственного средства при подготовке проекта нормативной документации.
После регистрации лекарственного средства и начала промышленного выпуска производитель (разработчик) обязан продолжить работы по изучению стабильности лекарственного средства с целью подтверждения или уточнения его срока годности.
Для лекарственных препаратов не рекомендуется устанавливать сроки годности более 5 лет, даже если результаты изучения стабильности позволяют это сделать.
Изменение сроков годности лекарственных средств или условий хранения утверждается в установленном порядке на основе данных, подтверждающих обоснованность заявленных изменений.
Отсчет срока годности промышленной серии лекарственного средства проводят от даты выдачи разрешения на ее реализацию (даты выпуска). При нормальных обстоятельствах период до даты выдачи такого разрешения не должен превышать 30 суток от даты производства.
Если разрешение на реализацию серии лекарственного средства выдано по истечении установленных 30 суток от даты производства, то началом отчета срока годности лекарственного средства следует считать дату производства.
Данный подход не применим для иммунобиологических лекарственных препаратов, таких как вакцины, сыворотки, анатоксины и аллергены, для лекарственных препаратов, полученных из крови и плазмы крови человека и животных, а также для лекарственных препаратов, полученных с использованием биотехнологических процессов и методов.
На основании изучения свойств лекарственного средства устанавливают оптимальные требования к первичной и вторичной упаковке и условиям хранения.
После установления оптимальных требований к первичной и вторичной упаковке и условиям хранения производитель (разработчик) лекарственного средства экспериментально определяет сроки годности лекарственного средства, осуществляя его хранение в рекомендованной упаковке и в указанных условиях с целью обнаружения скрытых факторов, которые могут повлиять на устойчивость лекарственного средства при хранении. Для этого от каждой из не менее чем 3 серий образца лекарственного средства, специально произведенных по условиям лабораторного или опытно-промышленного регламента, отбирают и упаковывают часть из них в количестве, достаточном для исследования стабильности лекарственного средства.
При изучении стабильности лекарственных средств, расфасованных в крупногабаритную первичную упаковку (фляги, бутыли, железные бочки, жестяные барабаны, пакеты полимерные, мешки бумажные трех- и четырехслойные и т.д.), допускается использование аналогичной упаковки меньшей емкости, достаточной для моделирования условий оригинальной упаковки.
Перед началом испытания проводят анализ лекарственного средства по всем показателям, предусмотренным проектом нормативной документации. Испытания по показателям, которые не изменяются в процессе хранения, а также испытания по показателям, изменения которых в процессе хранения не происходят в сторону ухудшения качества лекарственного средства, допускается не включать в протоколы исследования стабильности лекарственного средства.
На основании полученных результатов производитель (разработчик), изучающий стабильность лекарственного средства, определяет срок годности с указанием вида упаковки, требуемых условий хранения и транспортирования и вносит эти данные в проект нормативной документации.
При исследовании стабильности лекарственного препарата одновременно с изучением стабильности действующего и вспомогательного веществ оценивают их совместимость.
Дизайн программы испытаний на стабильность должен учитывать климатические условия в той области, где планируется использование лекарственных средств.
В табл. 1 приведены средние значения температуры и влажности, установленные в соответствующих климатических зонах.
Таблица 1. Средние значения температуры и влажности в климатических зонах
| Наименование климатической зоны | Температура, ° С | Относительная влажность, % |
| Зона I – умеренный климат | 21 | 45 |
| Зона II – субтропический климат с возможной высокой влажностью | 25 | 60 |
| Зона III – жаркий и сухой климат | 30 | 35 |
| Зона IVА – жаркий и влажный климат | 30 | 65 |
| Зона IVБ – жаркий и очень влажный климат | 30 | 75 |
Примечание. Климатические зоны — разделение планеты на 4 зоны, основанное на преобладающих годовых климатических условиях.
Рекомендуется проводить изучение стабильности лекарственных препаратов, произведенных из разных серий фармацевтической субстанции.
Для некоторых лекарственных препаратов в таких лекарственных формах, как растворы, суспензии, эмульсии и др., при необходимости проводят исследования по изучению влияния на их стабильность отрицательных температур (циклы замораживания и оттаивания).
Долгосрочные испытания стабильности лекарственных средств
Долгосрочные испытания должны проводиться в рекомендованной для данного лекарственного средства первичной и вторичной упаковке при постоянной верхней (наиболее высокой) температуре установленного режима хранения в течение всего заявленного срока годности.
В ряде случаев могут требоваться дополнительные испытания при нижней температуре установленного режима хранения (например, для мягких лекарственных форм, для которых возможны изменения их физико-химического состояния при пониженных температурах).
Образцы лекарственных средств, находящиеся на изучении стабильности, подлежат проверке по показателям качества нормативной документации в следующие сроки:
- в течение первого года хранения – через каждые 3 мес;
- в течение второго и третьего года хранения – через каждые 6 мес;
- после третьего года хранения – через каждые 12 мес.
Испытания стабильности методом «ускоренного старения»
Метод «ускоренного старения» преимущественно используется для определения сроков годности фармацевтических субстанций, представляющих собой вещества с установленным химическим строением, и лекарственных препаратов, содержащих эти вещества в качестве действующих.
Не рекомендуется использовать этот метод определения для лекарственного растительного сырья, лекарственных растительных препаратов, гомеопатических лекарственных средств, термолабильных фармацевтических субстанций и лекарственных препаратов, иммунобиологических лекарственных препаратов, препаратов крови и др.
Срок годности, установленный с помощью метода «ускоренного старения», не должен превышать 3 лет для антибиотиков, полученных микробиологическим или полусинтетическим путем, и их лекарственных форм – 2 лет. Метод не применим для увеличения ранее установленного срока годности лекарственного средства свыше 3 лет.
Метод «ускоренного старения» заключается в выдерживании испытуемого лекарственного средства при температурах и влажности, превышающих температуру и влажность его хранения в процессе обращения.
В данной ОФС приводятся рекомендации по изучению сроков годности лекарственных средств методом «ускоренного старения» с использованием измененного температурного режима. При повышенных температурах, как правило, ускоряются протекающие в лекарственных средствах физико-химические процессы, приводящие со временем к нежелательным изменениям качества. Таким образом, при повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается в сравнении со сроком годности при температуре хранения. Это позволяет значительно сократить время, необходимое для установления срока годности.
По результатам, полученным в процессе «ускоренного старения» лекарственного средства, можно решить также обратную задачу, т.е. установить температуру хранения, обеспечивающую какой-либо заданный срок годности.
Срок годности (С) при температуре хранения (tхр). связан с экспериментальным сроком годности (СЭ) при повышенной температуре экспериментального хранения (tэ) следующей зависимостью:
где коэффициент соответствия (К)
Температурный коэффициент скорости химической реакции (A) принят равным 2,5.
Примечания
- Приведенная зависимость основана на правиле Вант-Гоффа о 2-4-кратном росте скоростей химических реакций при увеличении температуры на 10°С.
- В отдельных случаях возможно использование экспериментально определенных уточненных значений коэффициента A, а также прогнозирования сроков годности на основании более строгих зависимостей, например уравнения Аррениуса.
В табл. 2 приведены значения коэффициентов соответствия K для различных значений разности температур экспериментального и обычного хранения при A = 2,5.
Таблица 2. Значения коэффициентов соответствия (K) в зависимости от температурного интервала
| № | (tэ—tхр), о С | K |
| 1 | 10 | 2,5 |
| 2 | 15 | 4,0 |
| 3 | 20 | 6,3 |
| 4 | 25 | 9,9 |
| 5 | 30 | 15,6 |
| 6 | 35 | 24,7 |
Примечание. Условные обозначения: К ‑ коэффициент соответствия; tэ ‑ температура экспериментального хранения; tхр ‑ температура обычного хранения.
Для опытов по «ускоренному старению» лекарственных средств должны использоваться термостаты, термошкафы, климатические камеры или другие устройства, позволяющие автоматически поддерживать заданную температуру экспериментального хранения tэ в течение всего опыта с точностью ±2 °С.
Наиболее высокая температура экспериментального хранения должна обеспечивать получение результатов, необходимых для оценки сроков годности, в кратчайшие промежутки времени. Однако эта температура не должна превышать пределов, за которыми происходят изменения агрегатного состояния лекарственного средства или разрушение упаковочного материала.
Рекомендуются следующие предельные температуры экспериментального хранения:
| — для индивидуальных веществ | + 60 °С |
| — для парентеральных растворов в стеклянной упаковке, таблеток, капсул | + 60 °С |
| — для парентеральных растворов в полимерной упаковке, мазей, линиментов | + 40 °С |
| — для суппозиториев и аэрозолей: | + 30 °С |
Воздействие света на испытуемые образцы должно быть исключено.
Не рекомендуется установление срока годности методом «ускоренного старения» для эмульсий.
Определение сроков годности методом «ускоренного старения» должно проводиться не менее чем на 3 сериях лекарственного средства.
Температура экспериментального хранения (tэ) должна превышать температуру хранения (tхр) не менее чем на 10 °C.
Наблюдение за качеством изучаемых образцов лекарственного средства должно проводиться по показателям, предусмотренным нормативной документацией, с учетом общих положений настоящей статьи.
Показатели качества лекарственного средства в процессе «ускоренного старения» определяют через промежутки времени, эквивалентные 6 месяцам хранения при условиях хранения, указанных в проекте нормативной документации.
Количество образцов лекарственного средства, предназначенных для экспериментального хранения, должно быть достаточным для проведения исследований, предусмотренных планом эксперимента.
Началом экспериментального хранения считается момент помещения лекарственного средства в термостатирующее устройство, а концом – либо момент, когда истекает экспериментальный срок хранения, соответствующий не менее чем двухлетнему сроку годности, либо момент, когда показатели качества лекарственного средства перестают удовлетворять требованиям нормативной документации.
Сроки экспериментального хранения при различных температурах представлены в табл. 3.
Таблица 3. Сроки экспериментального хранения в зависимости от температурного интервала
| № | Срок годности | Сроки экспериментального хранения, сут | |
| 1 | 2 года | 10 | 292 |
| 15 | 182 | ||
| 20 | 116 | ||
| 25 | 74 | ||
| 30 | 47 | ||
| 35 | 30 | ||
| 2 | 3 года | 10 | 438 |
| 15 | 274 | ||
| 20 | 174 | ||
| 25 | 111 | ||
| 30 | 71 | ||
| 35 | 45 | ||
| 3 | 4 года* | 10 | 584 |
| 15 | 365 | ||
| 20 | 232 | ||
| 25 | 148 | ||
| 30 | 94 | ||
| 35 | 60 | ||
| 4 | 5 лет* | 10 | 730 |
| 15 | 457 | ||
| 20 | 290 | ||
| 25 | 185 | ||
| 30 | 117 | ||
| 35 | 74 |
Примечание
* — в случае подтверждения срока годности, равного ранее утвержденному.
Условные обозначения: tэ — температура экспериментального хранения; tхр — температура обычного хранения.
Для вычисления срока годности экспериментальный срок годности, выраженный в сутках (или часах), умножают на коэффициент соответствия K (см. табл. 1).
Если промежуток времени Со между датой производства/изготовления лекарственного средства и началом его экспериментального хранения превышает 30 сут (но не более 90 сут), и оно в это время хранилось в обычных условиях, расчет срока годности С проводят по уравнению:
Если сроки годности, установленные на различных сериях лекарственных средств, отличаются друг от друга, за срок годности принимают минимальное из полученных значений.
При необходимости температуру tхр, позволяющую обеспечить заданный срок годности С, рассчитывают по формуле:
Данные, полученные с использованием метода «ускоренного старения», должны быть подкреплены обязательствами предприятия (разработчика) по продолжению изучения стабильности в условиях долгосрочных испытаний в течение всего заявленного срока годности.
Испытания стабильности методом экстраполяции
При достаточном обосновании допускается экстраполяция данных, полученных по результатам долгосрочного хранения.
Экстраполяцию проводят с помощью статистической обработки данных. Если полученные результаты свидетельствуют о незначительной деградации и малой вариации, статистический анализ может не проводиться.
Методом экстраполяции предлагаемый срок годности может быть увеличен не более чем в 2 раза, но не более чем на 12 мес, по сравнению с долгосрочными испытаниями.
Данные, полученные с использованием метода экстраполяции, должны быть подкреплены обязательствами предприятия (разработчика) по продолжению изучения стабильности в условиях долгосрочных испытаний в течение всего заявленного срока годности.
Испытания стабильности методом крайних вариантов
При изучении стабильности лекарственных средств допускается проведение исследования методом крайних вариантов.
При использовании метода крайних вариантов во всех временных точках по полному протоколу тестируют только образцы с крайними (предельными) вариантами факторов (например, дозировки, размер упаковки (тары) и (или) номинальный объем). Такой протокол предполагает, что стабильность любых промежуточных вариантов соответствует стабильности исследуемых крайних вариантов.
Исследование крайних вариантов допускают в отношении нескольких дозировок с пропорциональным составом; в случае одного и того же вида упаковки, если при прочих равных условиях имеются различия в размере упаковки или номинальном объеме лекарственного препарата.
Испытания стабильности матричным методом
При использовании матричного метода в определенный момент времени исследуется лишь подгруппа из общего числа образцов всех комбинаций факторов, подлежащих изучению. В очередной момент времени проводят исследование другой подгруппы образцов всех комбинаций факторов. К различным факторам одного и того же лекарственного препарата относят, например, совокупность различных серий, различных дозировок, различных размеров одной и той же укупорочной системы упаковки и, в ряде случаев, различных укупорочных систем упаковки.
Применение матричного метода допускают в отношении нескольких дозировок, идентичных или близких по составам.
Исследование влияния упаковки на стабильность лекарственного средства
Изменения качества лекарственного препарата могут быть вызваны взаимодействием лекарственного средства и системы упаковки, включающей укупорочные средства. Если для жидких лекарственных препаратов (кроме тех, что находятся в запаянных ампулах) нельзя исключить отсутствие взаимодействия, то в испытания на стабильность включают образцы в перевернутом или горизонтальном положениях (т.е. образцы, которые контактируют с укупорочным средством, например, пробкой), наряду с вертикально установленными образцами, для определения влияния материала укупорочного средства (пробки) на качество лекарственного препарата. Результаты экспериментальных исследований должны фиксировать все сочетания различных систем упаковки (укупорки), анализируемых лекарственных средств.
Для лекарственных средств в многодозовой упаковке, кроме стандартных данных, необходимых для традиционной упаковки одноразового использования (например, флакона), заявитель должен провести испытания, подтверждающие способность упаковки выдержать условия повторного открывания/закрывания и при этом сохранить качество и эффективность лекарственного средства на протяжении всего срока применения.
К основным факторам, оказывающим влияние на лекарственный препарат после вскрытия упаковки, относятся микробное загрязнение и физико-химическая деградация.
В исследование стабильности лекарственных препаратов после вскрытия первичной упаковки следует включать не менее 2 серий; при этом, по крайней мере, одна серия должна быть с истекающим сроком годности.
Проверку показателей на соответствие требованиям нормативной документации осуществляют в первую временную точку, как минимум одну промежуточную, а также в последнюю временную точку предлагаемого срока годности вскрытого лекарственного препарата.
Анализ лекарственного препарата проводят по всем показателям нормативной документации, которые могут меняться в процессе хранения (за исключением показателей, изменения по которым в процессе хранения не могут происходить в сторону ухудшения качества), и обязательно должны включать контроль на микробиологическую чистоту или стерильность.
Исследования стабильности лекарственных препаратов после восстановления или разведения
Если предполагается возможность хранения восстановленного твердого лекарственного препарата или разведенного концентрированного лекарственного препарата в течение определенного периода времени, должны проводиться исследования стабильности приготовленного таким образом препарата.
Цель изучения стабильности восстановленных препаратов – определить срок, в течение которого после восстановления или разведения лекарственного препарата его качество продолжит соответствовать требованиям нормативной документации, и лекарственный препарат может применяться по назначению.
Изучению стабильности подлежат восстановленные лекарственные препараты, приготовленные с использованием всех возможных для растворения/разведения лекарственных препаратов растворителей, указанных в инструкции по медицинскому применению.
Условия хранения восстановленного лекарственного препарата могут отличаться от условий хранения исходного лекарственного препарата.
Для подтверждения стабильности восстановленного лекарственного препарата допускается предоставлять данные, полученные для 2 серий, при этом, по крайней мере, одна серия должна быть с истекающим сроком годности.
Проверку показателей на соответствие требованиям нормативной документации рекомендуется осуществлять в первую и последнюю временные точки предлагаемого срока годности восстановленного лекарственного препарата.
Анализ лекарственного препарата проводят по всем показателям, которые могут меняться в процессе хранения, и обязательно должен включать контроль на стерильность или микробиологическую чистоту.
Стресс-исследования и фотостабильность
Помимо установления срока годности и выбора условий хранения изучение стабильности оригинальных лекарственных препаратов и фармацевтических субстанций проводится с целью установления наиболее вредного влияния внешних факторов (высокие или низкие температуры, влага, кислород и другие компоненты воздуха, свет и т.п.) в зависимости от времени и условий их воздействия.
Стресс-исследования допускается проводить на одной серии лекарственного средства.
Неотъемлемой частью стресс-исследований является исследование фотостабильности.
Объем исследований лекарственного средства должен определяться на основании наличия или отсутствия изменений, возникших в результате влияния света.
Условия хранения лекарственных средств, указанные в нормативной документации, должны соблюдаться на всех этапах обращения лекарственного средства.
Источник