Исследование иммунотоксического действия лекарственных веществ
Целью работы являлись доклинические исследования аллергенности и иммунотоксичности потенциального ЛС на основе пептидэргического нейро- и стресс-протектора для лечения нарушений мозгового кровообращения — «Лизаргам, спрей назальный дозированный» (далее препарат «Лизаргам»).
Проведенные ранее доклинические исследования специфической фармакологической активности препарата «Лизаргам» показали его высокую нейропротекторную эффективность in vivo [1]. Было показано, что данный препарат обладает антиишемической, антигипоксической, ноотропной и актопротекторной активностями [2].
Материалы и методы исследования
В исследовании использовали готовую лекарственную форму (ГЛФ) препарата «Лизаргам, спрей назальный дозированный 0,5% и 1,0%». Активный фармацевтический ингредиент — «D-лизаргам, ацетат» представляет собой синтетический тетрапептид последовательности Nα-ацетил-D-лизил-лизил-аргинил-аргинил-амид в виде ацетатной соли. Один флакон ГЛФ содержит 15 или 30 мг «D-лизаргам, ацетата» для 0,5% и 1,0% растворов соответственно, D-маннит — 30 мг и физиологический раствор (ФР) — 3,0 мл. Терапевтическую дозу препарата для человека (20 мкг/кг) высчитывали на основании данных по изучению специфической активности препарата «Лизаргам» на экспериментальных животных и коэффициента экстраполяции доз мышей и крыс на человека в соответствии с руководством Т.А. Гуськовой [3].
Основные правила содержания и ухода за животными в виварии соответствовали «Санитарно-эпидемиологическим требованиям к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)», утвержденным Постановлением Главного санитарного врача РФ от 29.08.2014 г., а также правилам, принятым Европейской конвенцией по защите позвоночных животных (Страсбург, 1986 г.). Объем работ и перечень процедур был одобрен биоэтической комиссией института. Доклинические исследования проводили на основе рекомендаций действующих методических документов 5.
Реакцию общей анафилаксии (анафилактический шок) проводили на морских свинках обоего пола (200-250 г, 5-6 недель), разделенных на 3 группы (по 5 самок и 5 самцов). Контрольная группа получала ФР — первая инъекция — подкожно (п/к), две последующие – внутримышечно (в/м) через день. Опытные группы 1 и 2 по той же схеме получали препарат «Лизаргам» в дозах 0,1 мг/кг и 1 мг/кг соответственно. Через 21 день всем животным внутрисердечно вводили разрешающую дозу препарата, которая составила суммарную сенсибилизирующую дозу для каждой группы соответственно. В контрольной группе вводили разрешающую дозу, рассчитанную для 2 группы. Учет интенсивности анафилактического шока проводили в индексах по Weigle [5].
Реакцию активной кожной анафилаксии проводили на белых беспородных мышах обоего пола (19–21 г, 9–10 недель), разделенных на 3 группы (по 5 самок и 5 самцов). В контрольной группе вводили ФР: первая инъекция — п/к, две последующие – в/м через день. Опытные группы 1 и 2 по той же схеме получали препарат «Лизаргам» в дозах 2,4 мг/кг и 5 мг/кг, соответственно. Через 21 день всем мышам вводили препарат «Лизаргам» внутрикожно (в/к) в двукратных разведениях в концентрациях, не вызывающих кожно-раздражающего действия. Через 20 минут вводили внутривенно (в/в) по 0,5 мл 1% раствора красителя синего Эванса. Через 30 мин. мышей умерщвляли и определяли размеры синего пятна на внутренней стороне кожи в месте введения.
Реакцию гиперчувствительности замедленного типа (ГЗТ) проводили на мышах-гибридах F1 (CBA x C57Bl/6) обоего пола (19–21 г, 9–10 недель), разделенных на 2 группы (по 10 самок и 10 самцов). Контрольную группу животных сенсибилизировали однократным в/к введением 60 мкл эмульсии полного адъюванта Фрейнда с раствором Хенкса 1:1. Опытной группе по той же схеме вводили 60 мкл эмульсии полного адъюванта Фрейнда, содержащей 100 мкг препарата. Через 5 суток после сенсибилизации всем животным в подушечку одной задней лапы вводили 40 мкл раствора Хенкса, содержащего 100 мкг препарата «Лизаргам», в контралатеральную лапу вводили ФР. Через 24 часа, после эвтаназии всех животных, обе лапы отрезали выше пяточного сустава и взвешивали. Индекс реакции подсчитывали в процентах прироста массы лапы, в которую вводили препарат (Мо), по отношению к массе контрольной лапы (Мк) по формуле [(Мо — Мк) / Мк ]*100.
Иммунотоксичность изучали на мышах-гибридах F1 (CBAxC57Bl6). Были изучены 2 дозы препарата: первая доза, 10-кратная терапевтическая для мышей, составила 2,4 мг/кг (одна терапевтическая доза для мыши составляет 0,24 мг/кг и получена из предполагаемой терапевтической дозы для человека, составляющей 0,02 мг/кг с учетом межвидового коэффициента пересчета 11,8); вторая доза — 5 мг/кг. Для определения числа антителообразующих клеток (АОК) к эритроцитам барана (ЭБ) в селезенке мыши были разделены на 3 группы (по 6 самок и 6 самцов). Контрольная группа ежедневно в течение 14 дней интраназально получала ФР. Опытные группы 1 и 2 по той же схеме получали препарат «Лизаргам» в дозах 2,4 мг/кг и 5 мг/кг соответственно. На 14-й день все мыши были иммунизированы внутрибрюшинной (в/б) инъекцией ЭБ в субоптимальной дозе 5х10 7 эритроцитов на животное. Подсчет числа АОК в селезенке мышей проводили на 5-е сутки после иммунизации. Реакцию ставили на предметных стеклах без поддерживающей среды по Cunningham [7]. По количеству зон гемолиза эритроцитов вокруг отдельных АОК, определяемых под микроскопом, подсчитывали число клеток-продуцентов антител в расчете на 10 6 спленоцитов.
Для постановки реакции ГЗТ против ЭБ мыши были разделены на 3 группы (по 10 самок и 10 самцов). Контрольная группа ежедневно в течение 14 дней интраназально (и/н) получала ФР. Опытные группы 1 и 2 по той же схеме получали препарат «Лизаргам» в дозах 2,4 мг/кг и 5 мг/кг соответственно. На 14-й день все мыши были сенсибилизированы однократно п/к введением раствора, содержащего 2х10 5 ЭБ. Для выявления гиперчувствительности на 5-е сутки после сенсибилизации всем мышам в подушечку задней лапы вводили 10 8 ЭБ в 0,05 мл ФР (разрешающая инъекция). В противоположную лапу вводили равный объём ФР. Через 24 часа проводили оценку реакции и подсчитывали индекс, как описано выше.
Для оценки фагоцитарной функции перитонеальных макрофагов (Мф) мышей разделяли на 3 группы (по 10 самок и 10 самцов). Контрольная группа ежедневно в течение 14 дней и/н получала ФР. Опытные группы 1 и 2 по той же схеме получали препарат «Лизаргам» в дозах 2,4 мг/кг и 5 мг/кг соответственно. На следующий день после последнего введения препарата всех мышей забивали и промывали брюшную полость культуральной средой для получения клеточной взвеси. Ставили реакцию фагоцитоза с опсонизированными дрожжами на чашках Петри по стандартной методике. Чашки фиксировали и окрашивали по Романовскому-Гимзе. Под микроскопом подсчитывали процент фагоцитировавших Мф – фагоцитарный индекс (ФИ), и среднее количество поглощенных дрожжей – фагоцитарное число (ФЧ) в условных единицах (у.е.).
Статистический анализ проводили с помощью программы Microsoft Excel-2007 (Microsoft Corporation). Результаты представляли в виде средних значений и ошибок среднего (М±m) или стандартных отклонений (М±σ). Сравнение показателей между группами проводили с помощью непарного Т-критерия Стьюдента с неравными отклонениями, а также по U-критерию Манна-Уитни. Отличия считали достоверными при р 6 спленоцитов), М±m
Источник
Исследование иммунотоксического действия лекарственных веществ
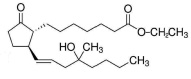
Исследуемое вещество 11-дезоксимизопростол (11-ДМП) – этиловый эфир (±)-11,15-дидезокси-16-метил-16-гидроксипростагландина E1 (рисунок), проявляющее утеротоническую активность.
Это соединение относится к ряду 11-дезоксипростагландинов и близко по химическому строению к мизопростолу. Будучи химически более стабильным и в 2 раза менее токсичным, оно превосходит мизопростол по утеротонической активности, что, наряду с синтетической доступностью и отсутствием побочных эффектов, делает его исключительно перспективным для внедрения в практику с целью замены мизопростола в гинекологических бинарных препаратах. Описаны синтез [5], противоязвенная и ряд других видов активности соединений 11-дезоксимизопростола [4, 8, 9].
Этиловый эфир (±)-11,15-дидезокси16-метил-16-гидроксипростагландина E1 (11-дезоксимизопростол)
Исходя из того, что 11-ДМП в настоящее время рассматривается как перспективное утеротоническое, иммуномодулирующее и противоязвенное средство, представляется целесообразным изучение и детализация механизмов его антиоксидантного действия, поскольку показано, что окислительный стресс может лежать в основе многих патологических процессов, а его устранение способствует коррекции нарушений [1]. Однако, прежде чем приступать к изучению специфической активности новых фармакологических субстанций, необходимо предварительно оценить их токсические свойства. Одним из обязательных этапов доклинических исследований новых лекарственных средств является изучение их влияния на функциональную активность иммунной системы лабораторных животных.
Под иммунотоксическим действием фармакологических средств понимают побочные, опасные для здоровья некомпенсированные нарушения в структуре и функции иммунной системы, которые могут привести к снижению резистентности организма к инфекции, повышению риска развития онкологических заболеваний, развитию аутоиммунных патологий [6].
Под аллергизирующими свойствами понимают способность того или иного вещества вызывать при введении в организм состояние повышенной чувствительности (гиперчувствительность, сенсибилизация) [2]. В основе патогенеза наиболее тяжелых аллергических осложнений, развивающихся по 1 типу гиперчувствительности, лежит активация Th2 хелперов и продукция цитокинов IL-4, IL-5 и IL-13, с последующим синтезом IgE-антител, имеющих высокое сродство к тучным клеткам и базофилам [3]. Антиген вступает во взаимодействие с фиксированными на тучных клетках IgE-антителами, что приводит к активации клеток и секреции медиаторов аллергии (гистамина, серотонина и др.). Согласно классификации P.G.H.Gell и P.R.A.Coombs имеется еще 4 типа гиперчувствительности, в основе которых лежат другие иммунопатологические механизмы [10].
Цель исследования: изучение иммунотоксических и аллергизирующих свойств лекарственного средства «11-дезоксимизопростол» при внутрижелудочном введении.
Материалы и методы исследования
Иммунотоксическое действие лекарственного средства 11-ДМП изучено на лабораторных животных. Исследование проведено в соответствии с «Методическими указаниями по оценке иммунотоксического действия фармакологических веществ» [6, 7]. Эксперименты выполнены на мышах-самках линии СВА 7–8-недельного возраста (масса тела 20–22 г), и белых морских свинках. Длительность карантина (акклиматизационного периода) для всех животных составляла четырнадцать (14) дней. В течение карантина проводили ежедневный осмотр каждого животного (поведение и общее состояние), дважды в день животных наблюдали в клетках (заболеваемость и смертность).
Животных распределяли по группам, используя при рандомизации в качестве основного критерия массу тела (отклонение значений массы тела в пределах группы не более 10 %). Количество животных в каждой экспериментальной группе – 15. Животные, не соответствующие критериям включения в исследование, исключены из исследования в течение карантина. Для оценки иммунотоксического действия 11-ДМП вводили животным внутрижелудочно в дозах 2, 10 и 20 мг/кг массы в форме суспензии в 1 %-м крахмальном геле. Рабочие разведения 11-ДМП готовили в день введения. Животные из группы негативного контроля получали 1 % крахмальный гель (плацебо).
Для оценки иммунотоксических свойств исследовали показатели неспецифического, специфического гуморального и клеточного иммунитета мышей, оценивали его влияние на массу лимфоидных органов и их клеточность. Аллергенные свойства 11-ДМП оценивали в методах анафилактического шока, непрямой реакции дегрануляции тучных клеток, реакции иммунных комплексов и конъюнктивальной пробы [6]. Для постановки конъюнктивальной пробы использованы белые морские свинки (самцы с массой тела 200–250 г., n = 30), разделенные в ходе эксперимента на две группы: опытную (n = 15) и контрольную (n = 15).
Результаты обрабатывались общепринятыми методами вариационной статистики и выражались в виде среднеарифметической (М) и её стандартной ошибки (m). Применялись критерии непараметрической статистики: Манна – Уитни (U). Обработка полученных данных производилась с использованием пакета прикладных программ Statistica 6.
Результаты исследования и их обсуждение
Лимфоидные органы (тимус и селезенка) экспериментальных животных взвешивали и определяли их массовые коэффициенты (индексы массы (ИМ)) и количество ядросодержащих клеток (клеточность). Результаты исследования представлены в табл. 1. Введение 11-ДМП не сопровождалось изменениями величины массовых коэффициентов и клеточности тимуса и селезенки у животных опытных групп.
Размеры и форма селезенки и тимуса у животных опытных групп не отличались от таковых в контрольной группе. Полученные данные позволяют заключить, что введение 11-ДМП в дозах 2, 10 и 20 мг/кг не привело к изменению массовых и клеточных параметров тимуса и селезенки.
Из данных, представленных в табл. 2, следует, что введение животным исследуемого препарата не повлияло на фагоцитарную активность макрофагов. Процент фагоцитирующих клеток значимо не изменялся в группах животных, которым вводили препарат. Таким образом, введение 11-ДМП экспериментальным животным не оказало влияния на изменение функциональной активности макрофагов.
Индексы массы (мг/10 г веса тела, М ± m) и клеточность (х10 6 , М ± m) тимуса и селезенки мышей при введении 11-ДМП
Источник
Исследование аллергизирующих свойств и иммунотоксического действия лекарственного препарата Гомеовокс
Полный текст:
Аннотация
Проведено исследование аллергизирующих свойств и иммунотоксического действия лекарственного препарата Гомеовокс. Гомеовокс – многокомпонентный гомеопатический препарат, который применяется при ларингитах различной этиологии.
Методы. Исследование аллергизирующих свойств и иммунотоксического действия лекарственного препарата Гомеовокс выполнено на 80 самцах морских свинок альбиносов и на 180 самцах мышей линий СВА, C57BL/6, гибридах F1(CBAхС57BL/6). При оценке иммунотоксичности Гомеовокс вводили мышам перорально 14 дней в дозах 100 мг/кг и 1 000 мг/кг, при изучении аллергенности Гомеовокса морским свинкам альбиносам препарат вводили также в дозах 100 мг/кг и 1 000 мг/кг согласно стандартным схемам иммунизации.
Результаты. 14-дневное пероральное введение Гомеовокса в дозах 100 мг/кг и 1 000 мг/кг мышам не вызывало значимых изменений основных показателей иммунного ответа по сравнению с контролем. При оценке аллергенности введение препарата Гомеовокс по стандартной схеме иммунизации в дозах 100 мг/кг и 1 000 мг/кг не вызывало у морских свинок альбиносов системной реакции анафилаксии и реакции активной кожной анафилаксии. После иммунизации морских свинок Гомеовоксом в тех же дозах в смеси с полным адъювантом Фрейнда у животных не выявлено аллергических реакций замедленного типа. Однократное введение препарата Гомеовокс перорально в дозе 1 000 мг/кг мышам линии CBA вызвало значимое уменьшение реакции воспаления на конканавалин А — на 58,4 %.
Заключение. Препарат Гомеовокс в диапазоне изученных доз не обладает иммунотоксическим действием и не вызывает аллергических реакций немедленного, замедленного типа и псевдоаллергических реакций.
Источник