Приложение 7. Производство лекарственных средств из растительного сырья
Производство лекарственных средств из растительного сырья
Лекарственные средства из растительного сырья имеют сложную природу и разнообразные характеристики, в связи с чем при их производстве особую роль играет контроль исходных материалов, условий хранения и переработки.
Исходными материалами при производстве лекарственных средств из растительного сырья*(1) могут быть необработанные растения, растительное сырье*(2) или промежуточные продукты. Растительное сырье должно иметь требуемое качество и сопровождаться документацией для производителя промежуточных продуктов и лекарственных средств из растительного сырья. Для того чтобы убедиться в однородности состава растительного сырья, может потребоваться более подробная информация о способе его получения (выращивания). Важными факторами, влияющими на качество растительного сырья, являются выбор семян; условия выращивания и сбора. Эти факторы могут оказать влияние на стабильность готового продукта. Рекомендации в отношении системы обеспечения качества при выращивании и заготовке растений приведены в руководстве НМРС*(3) «Руководство по выращиванию и сбору исходных материалов растительного происхождения (Guideline on Good Agricultural and Collection Practice for starting materials of herbal origin).
Данное приложение распространяется на все исходные материалы растительного происхождения: лекарственные растения, растительное сырье и промежуточные продукты из растительного сырья.
Иллюстрация применения настоящего стандарта (правил GMP) к производству лекарственных средств из растительного сырья приведена в таблице*.
Правила выращивания и сбора растений
Часть I стандарта
Выращивание, сбор и заготовка растений, морских водорослей, грибов и лишайников и сбор экссудатов (выделений)
Резка и сушка растений, водорослей, грибов, лишайников и экссудатов (выделений)(1)
Отжим из растений и перегонка(2)
Измельчение, переработка экссудатов, экстракция из растений, разделение на фракции, очистка, концентрация или ферментация субстанций из растительного сырья
Дальнейшая переработка в готовую продукцию, включая упаковывание готового лекарственного средства
Примечание — Классификация исходных материалов no GMP зависит от их использования производителем лекарственного средства. Материал может быть классифицирован как активная фармацевтическая субстанция, промежуточный или готовый продукт. Ответственность за классификацию несет производитель лекарственного средства.
(1) Производитель должен убедиться, что эти стадии соответствуют требованиям, установленным при государственной регистрации. Для стадий, выполняемых в полевых условиях (в соответствии с указанными выше требованиями), следует, при необходимости, руководствоваться Правилами выращивания и сбора растений (GACP). На последующих стадиях резки и сушки следует руководствоваться правилами GMP.
(2) Экстракцию из растений и дистилляцию, если они входят в перечень заготовительных операций для обеспечения соответствия продукции требованиям спецификаций, допускается проводить в полевых условиях. При этом растения должны быть выращены в соответствии с требованиями GACP. Это допускается в исключительных случаях и должно быть отражено в требованиях, установленных при государственной регистрации. Для операций, выполняемых в полевых условиях, должно быть обеспечено ведение документации, контроль и аттестация в соответствии с требованиями GMP. Контролирующие органы могут осуществлять надзор за этими операциями.
* Данная таблица детализирует таблицу 1 части II в отношении растительного сырья.
** Опубликованы Европейским Агентством по лекарственным средствам (ЕМЕА).
Помещения и оборудование
1 Растительное сырье следует хранить в отдельных зонах. Эти зоны должны быть защищены от проникания в них насекомых и животных, особенно грызунов. Следует предусмотреть меры против распространения животных и микроорганизмов, привносимых с растительным сырьем, для предотвращения ферментации или роста плесени, а также против перекрестного загрязнения. Карантинное хранение поступившего растительного сырья и допущенного к использованию должно быть организовано в различных выгороженных зонах.
2 Зоны хранения должны хорошо проветриваться. Порядок размещения упаковок не должен препятствовать свободной циркуляции воздуха.
3 Особое внимание следует уделять обслуживанию и чистоте складских зон, в которых может образовываться пыль.
4 Для хранения растений, экстрактов, настоек и другой продукции могут потребоваться особые условия по влажности, температуре и освещенности, которые необходимо обеспечить и контролировать.
5 При отборе проб, взвешивании, смешивании и других технологических операциях с растительным сырьем и промежуточным продуктом, сопровождающихся пылеобразованием, следует принимать особые меры по поддержанию чистоты, а также по предотвращению перекрестного загрязнения (удаление пыли, выделение специальных помещений и т.п.)
6 Используемое в технологическом процессе оборудование, фильтрующие материалы и пр. должны быть совместимы с растворами экстрактов, чтобы не допустить выделение и нежелательную абсорбцию веществ, которые могут оказать влияние на продукт.
Спецификации на исходные материалы
7 Производители лекарственных средств из растительного сырья должны убедиться в том, что они используют только исходные материалы растительного происхождения, соответствующие требованиям GMP и требованиям, установленным при государственной регистрации.
Следует в полном объеме вести документацию о проведении аудитов поставщиков исходных материалов растительного происхождения, выполненных производителем лекарственного средства или по его поручению. Контрольный анализ активных субстанций имеет исключительно важное значение в оценке качества исходных материалов. Производитель должен убедиться, что поставщики растительного сырья или промежуточной продукции из лекарственного сырья выполняют требования Правил выращивания и сбора растений (GACP).
8 Помимо данных, приведенных в настоящем стандарте (Часть I, раздел 4), в спецификации на растительное сырье и промежуточные продукты, используемые для производства лекарственных средств, следует включать:
— биноминальное наименование, принятое в ботанике с указанием, при необходимости, соответствующего классификатора (например, «Классификатор растений и животных» Карла Линнея); другую информацию, например, наименование культурного сорта растения и его хемотипическую разновидность;
— подробную информацию о происхождении растения (страна или местность, и при необходимости, культура, время и способ заготовки, использование пестицидов, возможность загрязнения радиоактивными веществами и т.д.);
— указание об использовании всего растения или только его части;
— данные о методе сушки, если используются высушенные растения;
— описание растения, а также данные его макро- и микроскопического исследований;
— результаты испытаний на подлинность, в т.ч. испытания на подлинность известных активных ингредиентов или маркеров. Следует провести специальные тесты, если возникает подозрение о фальсификации или подмене лекарственного сырья; для определения подлинности необходимо иметь соответствующие образцы сравнения;
— влажность растительного сырья, определенную в соответствии с нормативным документом*(4);
— по возможности, описание основных ингредиентов, обладающих установленной фармакологической активностью, или маркеров;
— методы определения содержания пестицидов и их допустимые концентрации в соответствии с нормативными документами или, при их отсутствии, аттестованным методом, если не предусмотрено иное*(5);
— испытания на загрязнение грибами и/или бактериями (в т.ч. афлатоксинами, другими микотоксинами и пест-инфестацинами) и предельные значения допустимого загрязнения;
— испытания на содержание токсичных металлов и других возможных посторонних примесей;
— испытания на включение инородных материалов;
— другие виды контроля в соответствии с нормативными документами*(6).
Любая обработка, обеспечивающая уменьшение загрязнений грибами, бактериями и пр., должна быть оформлена документально и включать в себя подробную информацию о процессе обработки, проводимых испытаниях и предельных значениях остаточного загрязнения.
9 Технологические инструкции должны содержать описание различных операций, проводимых с растительным сырьем (очистка, сушка, измельчение, просеивание и пр.), а также данные о времени и температуре сушки и методах, используемых для контроля размеров фрагментов или частиц. Они также должны содержать описание методов удаления посторонних материалов (например, просеивание и пр.).
10 Особое внимание следует обратить на наличие инструкций и протоколов, удостоверяющих, что каждая упаковка тщательно осмотрена на предмет определения фальсификации, подмены или присутствия посторонних веществ (частиц металла или стекла, остатков или экскрементов животных, камней, песка и т.д.) или следов гниения или разложения.
11 Технологические инструкции должны также содержать порядок или способ удаления посторонних веществ и методы очистки (отбора) растительных материалов до помещения растительного сырья на хранение или до начала производства.
12 Инструкции по приготовлению должны содержать подробное описание растворителей, времени и температуры экстракции, стадий концентрации и методов работы.
13 Так как необработанное лекарственное сырье получают из отдельных растений, оно является неоднородным. Отбор проб должен проводить специально обученный персонал с соблюдением особой предосторожности. Подлинность каждой серии продукции должна быть подтверждена отдельным документом.
14 Следует сохранять контрольные образцы растительного материала, особенно, если растительное сырье не описано в нормативных документах*(7). При изготовлении порошков следует сохранять образцы неразмолотого растительного материала.
15 Персонал, выполняющий контроль качества, должен иметь специальную подготовку и опыт работы с растительным сырьем, промежуточными продуктами или лекарственными средствами из растительного сырья для проведения испытаний поставляемого растительного сырья на подлинность и наличие примесей, выявления роста колоний грибов, заражения паразитами, неоднородности и т.п. в полученном сырье.
16 Подлинность и качество растительного сырья, промежуточных продуктов и лекарственных средств из растительного сырья должны контролироваться в соответствии с нормативной документацией*(8).
*(1) В данном приложении под лекарственным средством из растительного сырья понимаются и традиционные лекарственные средства из растительного сырья.
*(2) Термины даны по Директиве 2004/24/ЕС от 31 марта 2004 г., дополняющей Директиву 2001/83/ЕС о лекарственных средствах для использования человеком в отношении традиционных лекарственных средств из растительного сырья.
Растительное сырье (Herbal substances) — в основном, целое, разделенное и разрезанное растение, части растения, морских водорослей, грибов, лишайников в необработанной, обычно высушенной форме, но иногда и в свежем виде. Некоторые экссудаты (выделения) из растений, которые не прошли специальную обработку, также относятся к растительному сырью. В наименовании растительного сырья должны быть точно указаны используемая часть растения и ботаническое наименование по биноминальной системе.
Промежуточный продукт из растительного сырья (Herbal preparations) — продукт, полученный путем переработки растительного сырья, например, экстракцией, перегонкой, отжимом, разделением на фракции, очисткой, концентрацией или ферментацией. К промежуточным продуктам относятся измельченное или превращенное в порошок растительное сырье, настойки, экстракты, эфирные масла и вещества, выделенные в процессе переработки.
*(3) НМРС — комитет по лекарственным средствам из растительного сырья (Committee on Herbal Medicinal Products) Европейского агентства по лекарственным средствам (ЕМЕА — European Medicinal Agency).
*(4) В правилах GMP ЕС указано «в соответствии с Европейской Фармакопеей».
*(5) В правилах GMP ЕС указано «в соответствии с Европейской Фармакопеей».
*(6) В правилах GMP ЕС указано «в соответствии с общей или специальной статьей на растительное сырье Европейской Фармакопеи».
*(7) В правилах GMP ЕС указано «если оно не описано в Европейской Фармакопее и Фармакопее страны — члена ЕС.
*(8) В правилах GMP ЕС указано на необходимость соответствия Европейскому руководству по качеству и спецификациям на лекарственные средства из растительного сырья и традиционные лекарственные средства из растительного сырья и, при необходимости, Европейской Фармакопее.
Источник
Исходные сырье и материалы для производства медицинских и фармацевтических товаров
Современная медицина не может развиваться, не располагая новейшей медицинской техникой — аппаратурой и оборудованием. Конструкторы в содружестве с врачами продолжают работу по усовершенствованию медицинской техники, чтобы диагностика и лечение были более эффективными, а аппаратура, инструменты, оборудование — более надежными и удобными и мрактическом применении.
Качество медицинских изделий в значительной степени определяется свойствами тех исходных материалов, из которых они и изготовлены. При переработке в изделия материалы не только приобретают необходимую форму, но часто и новые свойства. По ному необходимо знать не только свойства исходных материалом, но так же методы и возможности их изменения в нужном направлении,
Материалы как исходное сырье для медицинских изделей должны удовлетворять следующим специфическим требованиям
— биологическая инертность и нетоксичность по отношению к тканям и средам организма, с которыми они соприкасаются;
— возможность асептической обработки без изменения свойств и формы;
Каждый материал обладает определенными механическими, химическими и технологическими свойствами. Они определяются ГОСТами.
К механическим свойствам материала относятся прочность, твердость, упругость, вязкость, пластичность, усталость.
Химические свойства определяются химическим составом материала, что влияет на его свойства и отношение к различным воздействиям.
Технологическими свойствами материалов обусловлены различные приемы их переработки в изделия, при которых возможны значительные изменения свойств.
Механические, химические и технологические свойства материалов тесно взаимосвязаны; от них зависит качество изделия.
Среди факторов, влияющих на качество товаров, важное место отводится качеству исходного сырья, материалов и комплектующих изделий и качеству технологических процессов в ходе производства.
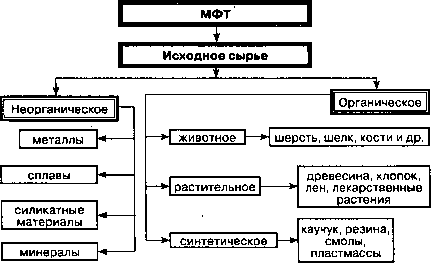
Под сырьем понимают различные вещества и материалы, используемые для производства готовых изделий. Эти вещества и материалы различаются по химическому составу и происхождению. Классификация исходного сырья для производства МФТ представлена на
Классификация основных видов исходного сырья для производства МФТ
Классификация основных видов исходного сырья для производства МФТ
По химическому составу вещества и материалы делят на неорганические и органические; по происхождению — на природные, искусственные и синтетические.
Из неорганических материалов широко применяются металлы и сплавы на их основе, силикатные материалы и минералы. Недостатком почти всех металлов и изделий из них является то, что они подвергаются коррозии и трудно поддаются обработке.
Силикатные материалы — это соединения кремнезема с другими оксидами. Они бывают природные и искусственные (cтекло, фарфор, фаянс).
К неорганическим сырьевым материалам относят так же различные минералы, в том числе драгоценные (алмаз и др.).
Органические вещества и материалы животного происхожде-ния — это различные белковые вещества: шерсть, кости и т.д. К материалам растительного происхождения относятся древесина, хлопок, лен, лекарственное растительное сырье. В число синтетических органических веществ и материалов входят каучук и резина на его основе, смолы для получения синтетических волокон (капрон, лавсан), пластмассы. В ходе технологического процесса получения изделия сырье и материал подвергаются механическим, термическим, физико-химическим и другим видам воздействий, в результате которых (формируется качество готовой продукции. При нарушении режимов технологических процессов могут появляться paзличные дефекты, снижающие качество продукции.
Сталь — это основной материал, широко применяемый для производства медицинских инструментов, оборудования и техники. Она обладает ценным комплексом механических, физико-химических и технологических свойств.
По химическому составу стали подразделяют на углеродистые и легированные.
Углеродистые стали, содержащие до 0,25% углерода, называют низкоуглеродистыми; от 0,25% до 0,6% — среднеуглеродистыми; более 0,6% — высокоуглеродистыми.
По назначению стали подразделяют на:
а) конструкционные (для деталей машин, приборов);
б) инструментальные (для инструментов);
в) специального назначения с особыми свойствами (нержавеющие, коррозионно-стойкие, жаростойкие, жаропрочные, износостойкие и др.).
Для изготовления медицинских инструментов используют разные марки углеродистых сталей: У7А — для изготовления ранорасши-рителей, пинцетов, корнцангов, зажимов; У8А — для изготовления пил, долот, щипцов костных, распаторов, троакаров; У10А — для изготовления ножей, ножниц; У12А — для изготовления глазных ножей (У — углеродистая сталь, 12 — содержание углерода, сотые доли процента: 0,12%, А — качественная сталь).
Для придания стали требуемых свойств в нее вводят различные элементы (хром, марганец, никель), такую сталь называют легированной.
Высоколегированная сталь содержит более 10% легирующих элементов. При добавлении 13—18% хрома получают нержавеющую сталь.
Нержавеющие стали выпускают двух классов:
1) закаливаемые или стали мартенситового класса 20X13; 30X13; 40X13 (40 — содержание углерода, X — хром, 13 — процентное содержание хрома). В производстве медицинских инструментов закаливаемые нержавеющие стали применяют для изготовления пинцетов, крючков, иглодержателей, зеркал, долот, щипцов, распаторов, ножниц;
2) незакаливаемые или стали аустенитового класса: 08Х18Н9; 12Х18Н10; 17Х18Н10Т (17 — содержание углерода, X — хром, 18 — процентное содержание хрома, Н — никель, 10 — процентное содержание никеля, Т — титан).
Из хромоникелевых сталей изготовляют зубные коронки, камеры стерилизаторов, корпусы кипятильников и др.
Из цветных металлов наиболее распространены в изготовлении медицинских инструментов и оборудования следующие:
1) медь и ее сплавы:
— с цинком: латунь: JI-62 (62% меди и 38% цинка), ЛС 59-1 (59% меди, 1% свинца, остальное — цинк) (катетеры, зонды, бужи, дилятаторы, арматура шприцев, головки игл инъекционных);
— с цинком, никелем и кобальтом: нейзильбер (трубки трахеотомические, канюли, глазные инструменты, зонды ушные и носовые);
2) алюминий и его сплав дюралюминий: с медью, марганцем, магнием, кремнием, железом; применяется в производстве деталей и медицинского оборудования;
3) благородные металлы — золото, серебро, платина; применяются для производства офтальмологических инструментов, зубных коронок в стоматологии, очковых оправ;
4) тантал и его сплавы применяются при изготовлении скобок для сшивающих аппаратов, проволок для сшивания костей;
5) виталиум — сплав сложного состава, предназначен для изготовления специальных гвоздей для соединения отломков костей.
В настоящее время для изготовления стержневого и лезвийного медицинского инструмента различного назначения применяются хромистые и хромоникелевые коррозионно-стойкие стали. С целью улучшения пластической деформации их легируют кремнием, молибденом, ванадием, марганцем. Защита металлических изделий от коррозии производится с помощью покрытия сплавами на основе никеля или титана.
Источник