Герпетический кератит
Содержание:
Герпетический кератит – заболевание, развивающееся в том случае, если на роговицу глаза попадает вирус герпеса. Чаще всего заболевание поражает маленьких детей, чей возраст еще не перешел отметку в 5 лет, но может встречаться и у взрослых пациентов. Лечение взрослых обычно затруднено тем, что у них развитие недуга связано с наличием других болезней.
Чтобы избежать осложнений, необходимо знать симптомы и причины патологии, а также представлять себе, как проходит лечение!
Виды болезни
Герпетический кератит глаза – недуг, у которого офтальмологи выделяют несколько разновидностей. В первую очередь разделение происходит на первичную и послепервичную патологию.
Первичное заболевание характерно для детей. Оно провоцируется незрелостью иммунитета, а поражает не только глаза, но и все тело в целом.
| Послепервичное отклонение развивается у детей старше двух лет, а также у взрослых пациентов. Основная причина кроется в снижении защитных сил организма. |
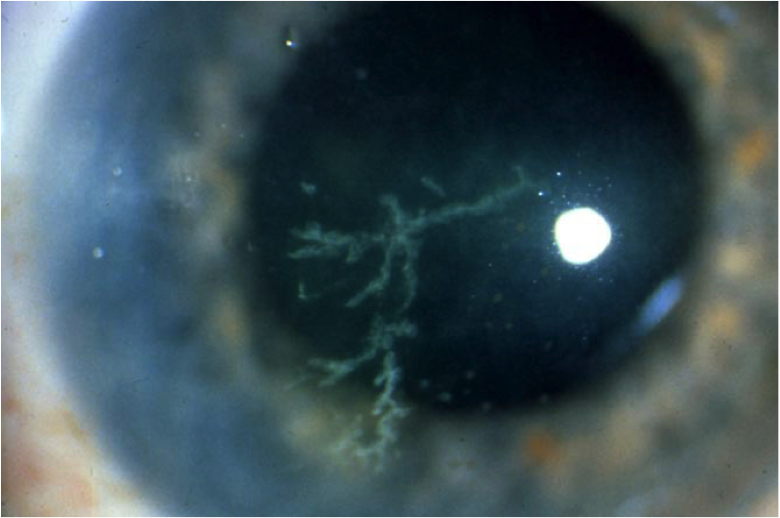
- древовидную форму, поражающую поверхностные слои, характеризующуюся образованием мелких пузырьков, которые после разрывов оставляют структуру, напоминающую дерево;
- дисковидный вариант, для которого характерно поражение глубоких слоев роговицы, сопровождающееся резким снижением зрения;
- метагерпетическая форма также сопровождается глубокими повреждениями стромы глаза, язвочки структурой похожи на реку;
- диффузный вариант напоминает дисковидный, но очаг поражения не обладает четко очерченными границами;
- кератоиридоциклит – разновидность, провоцирующая появление сильных болей из-за вовлечения в патологический процесс тройничного нерва.
Причины возникновения болезни
Основной фактор развития болезни – это наличие в организме вируса простого герпеса первого типа (ВПГ-1). Примерно в 70% случаях патоген поражает поверхностные слои глаза, 20% поражения приходится на компоненты стромы. Еще около 10% — это смешанная форма.
| В группе риска по этому заболеванию оказываются дети, а также подростки. |
У взрослых отклонение также диагностируется, но реже. Большую опасность для пациентов старшего возраста представляет вирус простого герпеса второго типа (ВПГ-2). Течение болезни в этом случае более продолжительное, строма поражается чаще с необратимыми изменениями.
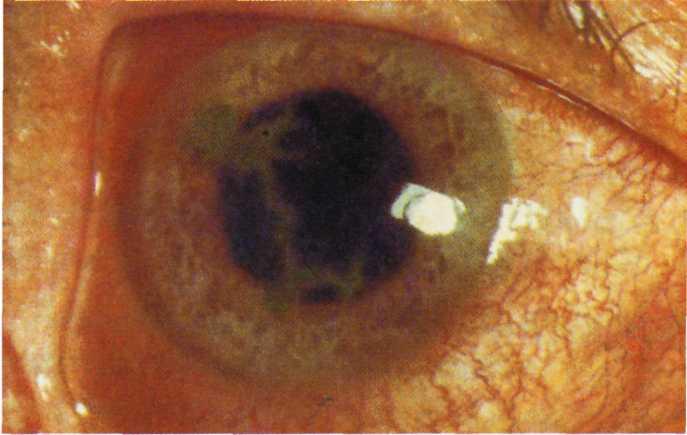
- частые стрессовые воздействия;
- переохлаждение или, напротив, перегрев организма;
- активное облучение ультрафиолетовым светом;
- заболевания эндокринной системы;
- инфекции иного происхождения, оттягивающие на себя силы иммунитета.
Установление причины активизации вируса – важный шаг в борьбе с герпетическим кератитом. Если понять, какой из факторов привел к снижению иммунитета, и устранить его, излечение произойдет быстрее.
Симптомы и развитие болезни
Кератит герпетического происхождения развивается постепенно. Сначала у пациента определяется бактериальная инфекция в легкой форме. Человек не обращается к врачу, так как может не обращать внимания на такие симптомы, как покраснение глаз без причины и слезотечение. По мере прогрессирования признаков появляются светочувствительность, отечность роговицы. Зрение снижается.
Первым признаком герпетического кератита является появление небольших пузырьков на роговицы. Со временем они лопаются, на их месте образуются язвочки. Зрение ухудшается. Если поражен один глаз, то только на нем. Если вовлечены оба органа, то с обеих сторон.
Люди нередко пытаются лечиться собственными силами, используя антибактериальные капли. Однако такое лечение не имеет эффекта, так как вирус не поддается воздействию антибактериальных средств. Симптомы быстро прогрессируют.
Первые эпизоды заболевания могут переноситься сравнительно легко. Связано это с тем, что болезнь не поражает глубокие слои роговой оболочки сразу. Однако при каждом следующем рецидиве состояние больного прогрессивно ухудшается.
Особенности диагностики
Герпетический кератит – заболевание, которое требует внимательной диагностики. Доктор может заподозрить недуг, ориентируясь на клиническую картину, однако перед началом лечения необходимо получить лабораторное подтверждение диагноза. Для этого:
- при подозрении на первичное заражение делают внутрикожную пробу с вакциной от ВПГ;
- выполняют соскоб и оценку клеток эпителия с роговой оболочки;
- делают анализ слезной жидкости;
- выполняют в кабинете офтальмолога измерение внутриглазного давления, используя для этого специальный прибор;
- при первичной форме проводят серологические тесты, показывающие титр антител к вирусным частицам;
- выполняют ПЦР – исследование, с помощью которого появляется возможность определить в биоматериале ДНК герпесного вируса, понять, какой штамм возбудителя спровоцировал заболевание.
Важным этапом диагностики считается определение того, насколько поражена роговица. Для этого пациенту в глаза закапывают специальное вещество, способное к безвредному временному окрашиванию элемента. В зависимости от степени прокрашивания разных участков делают выводы о том, насколько активна болезнь.
Консервативная терапия
Если развился герпетический кератит, лечение рекомендуется начинать как можно раньше. Терапия довольно сложная и долгая, так как вирус обладает способностью легко адаптироваться к противовирусным средствам. Задача осложняется еще и тем, что медикаменты часто имеют весомые противопоказания и ограничения для применения, что затрудняет их использование.
Лечение рекомендуется проводить в условиях стационара. Первый шаг – попытка использовать консервативные подходы, направленные на подавление инфекции.
Медикаменты

Применяют медикаменты в виде капель или масел. Это могут быть, например, Валацикловир или Ацикловир. На этом патогенетическая терапия заканчивается. Остальное лечение имеет чисто симптоматический характер.
Для уменьшения боли рекомендуют проводить обработку глаз с помощью Лидокаина. Препарат блокирует передачу импульсов, облегчая выраженность неприятных симптомов.
В качестве дополнительного лечения может быть рекомендована иммуностимулирующая терапия. Используются препараты на основе интерферона, способствующие выработке антител, уничтожению вирусных частиц.
Может назначаться Изопринозин – препарат, обладающий двойным воздействием. Он не только стимулирует иммунную систему, но и оказывает противовирусное действие в отношении герпеса. Изопринозин, в отличие от прочих лекарственных средств, выпускается только в таблетированной форме, а потому при использовании системно воздействует на организм пациента.
Электрофорез
Применение электрофореза носит в терапии герпетического кератита вспомогательный характер. Суть процедуры проста. На пораженную роговицу накладывается специальный тампон, пропитанный интерфероном. Время наложения в среднем составляет 5 минут. Под воздействием электрофореза препарат активнее усваивается клетками тела, лучше воздействует на организм.
Процедуру рекомендуется повторять до тех пор, пока на очагах поражения не сформируется свежий эпителиальный слой. После курса процедур удается избавиться от чувства раздражения роговицы, которое доставляет множество неудобств.
После курса процедур на месте очага воспаления разовьется небольшое помутнение. Как показывает практика, оно никак не влияет на зрение пациента.
Врачи заостряют внимание пациентов на том, что лечить кератит, вызванный вирусом герпеса, используя народные средства, категорически запрещено.
Неправильное лечение приведет к прогрессированию болезни, а та, в свою очередь, может стать причиной значительного снижения или утраты зрения. Народные средства не оказывают влияния на патогенный микроорганизм, помогая справляться только с симптомами. Для того, чтобы победить недуг, этого катастрофически недостаточно!
Оперативные вмешательства
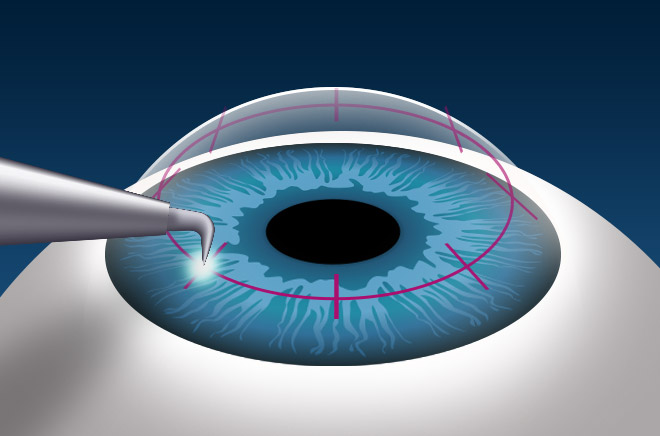
Соскабливание
Методика самая простая и распространенная. С помощью специального приспособления доктор аккуратно счищает эпителий, пораженный болезнью. Очищенные зоны обрабатываются с помощью раствора антисептика. Затем наблюдают за их заживлением.
Кератопластика
Сложная операция, которая является крайней мерой. Выполняется, если консервативная терапия с соскабливанием не возымели должного эффекта. В ходе операции удаляется пораженный участок роговицы, а на его место аккуратно подшивается донорская часть органа.
Перед кератопластикой больному необходимо пройти обследования, как перед полноценной хирургической операцией. Манипуляция выполняется только после того, как прошло обострение герпесного кератита. В период обострения вмешательство не делается, так как возможно поражение донорских тканей, их отторжение.
Оперативное решение проблемы – крайний вариант.
Применяется оно в том случае, если пациент запустил свое заболевание, и надежды скорректировать ситуацию с помощью консервативных методик нет.
Методы профилактики
Прогноз недуга во многом зависит от того, как быстро он был диагностирован, и как тщательно больной соблюдает рекомендации по лечению, полученные от офтальмолога. Ранние стадии кератита излечиваются с хорошим эффектом, вероятность их рецидива минимальна. Тяжелые формы требуют постоянного врачебного контроля, оперативной коррекции для сохранения способности видеть.
Гораздо проще, как отмечают офтальмологи, не лечить уже сформировавшуюся патологию, а избежать ее. Для этого рекомендуется соблюдать простые профилактические меры, не позволяющие инфекции активизироваться или попасть в организм. Среди них:
- избегание ситуаций, в которых есть вероятность получить травму глаза;
- использование специальных защитных очков, если работа человека связана с ремонтом, строительством, сваркой;
- тщательное соблюдение правил гигиены при использовании контактных линз, отказ от ношения чужих линз, которые могут быть инфицированы вирусом герпеса;
- соблюдение мер предосторожности при работе с веществами, способными оставить на роговице ожог;
- закалка организма, способствующая повышению иммунитета, не допускающая активизации патогена в организме;
- защита себя от перегреваний, переохлаждений, инфекций и других неприятных патологий, которые могут спровоцировать обострение герпеса.
Существует также вакцина, помогающая бороться с возбудителем инфекции. Вводить ее рекомендуется в период ранней осени, перед началом сильных холодов. Именно период холодов часто вызывает обострения. Перед вакцинацией пациенту рекомендуется пропить курс противовирусных средств.
Герпетический кератит – недуг, развивающийся медленно, но неуклонно. Если игнорировать его в течение длительного времени, можно столкнуться с весомыми неудобствами, а иногда даже потерять зрение частично или полностью. Своевременное обращение к доктору при появлении первых подозрительных симптомов поможет защититься от осложнений. Главное – выполнять рекомендации офтальмолога по лечению после того, как инфекция будет точно диагностирована!
Источник
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
- у 86,3% — хронические рецидивирующие заболевания респираторного тракта (хронический фарингит, хронический трахеит, хронический ларингит, хронический бронхит, хронические синуситы, повторные отиты);
- у 88,2% — хронические рецидивирующие заболевания урогенитального тракта смешанного генеза (цистит, уретрит, вульвовагинит, аднексит, сальпингоофорит, простатит);
- у 50–70% — астено-вегетативный и астено-депрессивный синдром, формирование синдрома хронической усталости;
- у 91,2% — дисбактериоз кишечной флоры, хронические воспалительные заболевания ЖКТ (хронический энтероколит, хронический гастродуоденит);
- у 25–30% — кожные псевдоаллергические реакции (кожный зуд, крапивница, дерматит).
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Наличие ВПГ-инфекции подтверждали на основании данных анамнеза, клиники, а также выявления дезоксирибонуклеиновой кислоты (ДНК) ВПГ методом полимеразной цепной реакции (ПЦР) в отделяемом из высыпаний. Исследование иммунного статуса включало определение основных субпопуляций лимфоцитов CD3 + , CD4 + , CD8 + , CD72 + , CD16 + , активационных маркеров лимфоцитов главного комплекса гистосовместимости — HLa-DR+, CD11b в периферической крови с помощью моноклональных антител. Также определяли содержание иммуноглобулинов (Ig) a, M, G, циркулирующих иммунных комплексов (ЦИК) в сыворотке крови. Функциональную активность нейтрофилов — продукцию активных форм кислорода, обеспечивающих бактерицидность, определяли по тесту с нитросиним тетразолием (НСТ-тест). Стимулированный НСТ-тест исследовали при инкубации in vitro с культурой Staphylococcus аureus. Интерфероновый статус оценивали по уровню сывороточного ИФН и продукции лейкоцитами ИФН a при стимуляции вирусом болезни Нью-Кастла и ИФН ( при стимуляции фитогемагглютинином. Количественное содержание цитокинов (ИФН α, ИФН γ, ФНО α, ИЛ-1β, ИЛ-2, ИЛ-4 ИЛ-6,) в плазме/сыворотке крови определяли методом иммуноферментного анализа (ИФА) с использованием тест-систем (ProCon, С.-Петербург, и Вектор-Бест, Новосибирск).
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
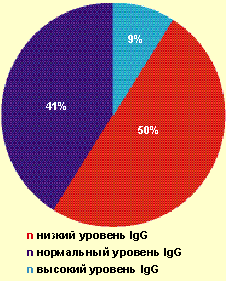 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
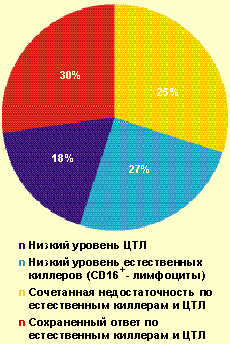 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
У больных с тяжелым течением ВПГ-инфекции при рецидиве число естественных киллеров было достоверно ниже нормы и в 2 раза ниже среднего показателя лиц с легким течением заболевания. Почти у половины больных ВПГ-инфекцией выявленные нарушения сочетались с дисиммуноглобулинемией и дефицитом продукции IgG. Уровень HLa-DR + лимфоцитов, отражающих продукцию ИЛ-2 и несущих рецептор DR + , необходимый для распознавания вирус-инфицированных клеток и других реакций иммунитета, был снижен у 39% больных ВПГ-инфекцией (его повышение отмечалось только у 17,4% больных).
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
При изучении интерферонового статуса пациентов в период обострения ВПГ-инфекции выявлены различия при легком и тяжелом течении болезни. Так, уровень сывороточного ИФН у пациентов с легким течением заболевания был повышен в 2 раза по сравнению с группой контроля (р
- Хахалин Л. Н. Вирусы простого герпеса у человека// Consilium Medicum. 1999. Т. 1. № 1. С. 5–18.
- Европейские стандарты диагностики и лечения заболеваний, передаваемых половым путем. М.: Медицинская литература, 2003. С. 102–110.
- Малашенкова И. К., Дидковский Н. А. Принципы иммунокорригирующей терапии вторичных иммунодефицитов, ассоциированных с хронической вирусно-бактериальной инфекцией// Русский медицинский журнал. 2002. Т. 10. № 21. С. 973–977.
- Малашенкова И. К., Дидковский Н. А., Танасова А. Н., Щепеткова И. Н., Левко А. А. Принципы терапии герпесвирусной инфекции// Доктор.Ру. 2004. № 4. С. 26–30.
- Малашенкова И. К., Дидковский Н. А., Левко А. А. К вопросу о роли индивидуального подбора иммунокорректоров// Фарматека. 2004. С. 118–122.
- Левко А. А. Значение индивидуального подбора иммунокорректоров в комплексной терапии хронического рецидивирующего простатита, вызванного урогенитальной инфекцией: автореф. дис. . канд. мед. наук. М., 2005.
- Шульженко А. Е., Викулов Г. Х., Тутушкина Т. В. Герпетические инфекции — настоящее и будущее// Трудный пациент. 2003. № 4. Т. 1. С. 6–15.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Источник


