Генетическое лекарственное средство что такое
Препарат Zolgensma был разработан швейцарской фармацевтической компанией Novartis. Он применяется одноразово и стоит 2 млн долларов. Врачи считают, что лекарство может дать начало массовому применению генной терапии: только за первые три месяца 2019 года было зарегистрировано 372 новых клинических испытания генно-терапевтических препаратов.
Для многих наследственных заболеваний нет эффективного лечения, существующие препараты помогают облегчить жизнь пациентов. Причиной таких заболеваний являются изменения генетического материала – мутации. В результате мутаций с гена синтезируется либо изменённый белок, который не может правильно выполнять свою функцию, либо белок не синтезируется вовсе. Для полного излечения пациентов необходимо исправить в их клетках мутации. Задачу немного упрощает тот факт, что для многих наследственных заболеваний неработающий белок оказывается критически важен только в одном месте организма. Поэтому достаточно исправить ген только в этом органе или ткани.
Генно-терапевтический подход к лечению наследственных заболеваний разрабатывается уже 40 лет. Основная технология генной терапии основана на замещении гена с мутацией правильно функционирующей копией этого гена. Но есть еще две стратегии: выключение неправильно работающего гена и введение нового гена, который поможет организму победить заболевание.
Надо подчеркнуть принципиальное отличие генной терапии от редактирования генома, которое сейчас тоже активно разрабатывается для лечения наследственных заболеваний. Генная терапия доставляет ген в клетки, чтобы компенсировать дефектный ген. Но при этом не происходит удаление дефектной ДНК из клеток. При редактировании генома происходит удаление или изменение дефектной ДНК в клетках пациента.
Для доставки генная терапия использует различные вирусы, которые транспортируют ген специфично в определённый орган. Вирусы — внутриклеточные паразиты, они встраивают свою генетическую информацию в ДНК клетки и таким образом заставляют клетку делать копии вирусной ДНК. Это оказалось очень полезным свойством для генной терапии. Перед использованием вирусы делают безвредными, чтобы они не могли вызывать заболевание, но могли доставить ген в клетки.
В зависимости от цели генная терапия бывает соматической и фетальной. В первом случае вирус с геном вводят в клетки тела, во втором – в эмбрион на ранней стадии развития. В результате фетальной генной терапии генетический материал попадает во все клетки и может быть передан детям.
В ходе клинических испытаний препарат Zolgensma показал хорошие результаты у пациентов со спинальной мышечной атрофией: из 21 пациентов 19 смогли начать двигать головой и самостоятельно сидеть.
Спинальная мышечная атрофия — наследственное заболевание, к развитию которого приводят мутации в гене SMN1. При этом заболевании из-за нарушения работы нервных клеток спинного мозга развивается слабость мышц и их атрофия. Дети теряют способность ходить, а по мере развития заболевания — самостоятельно дышать. Более 90% случаев заболевания заканчиваются смертью детей до 2-х лет.
Препараты генной терапии могут стать эффективным средством лечения многих наследственных заболеваний, для которых не существовало лечения до этого. Так, в ближайшее время ожидает одобрения международного регулятора еще один новый генно-терапевтический препарат для лечения талассемии и серповидноклеточной анемии. Оба этих заболевания связаны с мутациями, результатом которых является синтез неправильно работающего гемоглобина – белка, переносящего кислород в крови.
Прежде всего, препараты генной терапии разрабатываются для заболеваний, причиной которых является одна в мутация в одном гене. Таких болезней 10 000. В связи с большими затратами на разработку генно-терапевтических препаратов, они очень дорогие. Но постепенно отработка технологии позволит значительно снизить стоимость таких лекарств и сделать их доступными большинству пациентов.
Источник
ДНК как лекарство: клеточная и генная терапия меняют фармацевтику
Лекарства, полученные с помощью генной инженерии и клеточных технологий, вряд ли в ближайшие годы станут столь массовыми, что обгонят по продажам антибиотики и жаропонижающие. Но эти современные препараты незаменимы в лечении некоторых видов рака, редких наследственных заболеваний, терапии ВИЧ и других вирусных инфекций. А это большой рынок с потенциальным оборотом в десятки миллиардов долларов.
Стволовые клетки и генная инженерия
Генная терапия — общее название для технологий (а также соответствующих лекарств), которые используют изменение генов для достижения нужных медицинских эффектов. Например, в организм пациента могут доставить ген, кодирующий определенный белок. Когда нужная ДНК попадет в клетки, те смогут начать производство данного протеина, что будет иметь лечебное воздействие.
Другой вариант — отредактировать «дефектные» варианты генов, чтобы они начали работать правильно. Если у человека есть только одна мутантная версия гена, который вызывает заболевание, можно просто отрезать ее — и ДНК починит себя сама, скопировав генетическую информацию со своей второй «половинки». В случае, когда повреждены обе цепи ДНК, можно доставить в клетки донорскую последовательность.
Наконец, есть возможность с помощью специальных препаратов управлять экспрессией генов. Если активность определенного гена приводит к болезни, ее подавляют. И наоборот: в ситуации, когда заболевание возникает по причине «недоработки» какого-то гена, лекарство помогает его включить.
Что касается клеточной терапии, она в большинстве случаев представляет собой лечение стволовыми клетками. Они могут развиться в клетки любого типа, любого органа, если правильно управлять их ростом. И эту науку ученые освоили, но важно было еще и получить достаточный запас стволовых клеток. Проблему решил японский ученый Синья Яманака, который в 2006 году впервые смог получить индуцированные плюрипотентные стволовые клетки, то есть вернуть клетки взрослого человека в то состояние, когда из них может вырасти что угодно. Перед наукой открылись захватывающие перспективы: можно выращивать новые органы, восстанавливать поврежденные участки нервной системы, лечить заболевания крови — все это становится возможным с применением стволовых клеток.
На стыке клеточной и генной терапии находится технология модификации клеток. Сегодня ученые экспериментируют в основном с клетками иммунитета — Т-лимфоцитами. С помощью генетического редактирования их «учат» лучше распознавать вредителей (например, раковые клетки) и эффективно их уничтожать.
Генный рынок
В 2016 году рынок препаратов для генной терапии оценивался в $584 млн. А к 2023 году, по прогнозам аналитиков, глобальная выручка от продажи таких препаратов превысит $4,4 млрд — это более 30% роста ежегодно.
Среди лидеров рынка как традиционные фармацевтические гиганты (такие, как Novartis и GlaxoSmithKline), так и более специализированные компании (Spark Therapeutics, Bluebird bio, Amgen, Celgene).
Как следует из отчета Allied Market Research, подавляющее большинство препаратов генной терапии производится для больных с онкологическими патологиями. И в ближайшее время — как минимум до 2023 года — эта ниша сохранит свое первенство на рынке. Следом за лекарствами от рака идут средства генной терапии от редких заболеваний, сердечнососудистых болезней, неврологических расстройств, инфекций.
Лидеры рынка следуют за трендами и разрабатывают препараты для онкобольных. Например, в компании Amgen, которая возглавила топ-25 биотехнологических компаний в 2017 году с капитализацией в $129,1 млрд, из 37 препаратов в стадии клинических испытаний 20 относятся к лечению опухолей и заболеваний крови.
А компания Novartis стала первой, кому американское управление по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) разрешило запустить массовое производство клеточной терапии рака, основанной на генетической модификации. Это тот самый случай, когда фармкомпания производит лекарство из Т-лимфоцитов, превращая их в средство борьбы с онкологией, а именно с острым лимфобластным лейкозом.
Novartis уже начала получать первые деньги от продажи своего препарата под названием Kymriah. И немалые — каждый курс генной терапии рака стоит порядка $475 000. Вслед за этим FDA одобрило еще одно лекарство для лечения онкологии с подобным механизмом действия — Yescarta от компании Gilead Sciences (капитализация в 2017 году — $103 млрд); оно будет продаваться по цене в $373 000 за курс и помогать больным с неходжкинской лимфомой.
На продажах Kymriah фармгигант Novartis сможет зарабатывать порядка $300 млн в год. А Gilead Science аналитики пророчат выручку от препарата Yescarta в $250 млн за 2018 год.
Novartis хочет расширить спектр применения своего лекарства, чтобы его также можно было назначать пациентам с неходжкинской лимфомой — это позволит компании побороться за рынок, который оценивают примерно в $1 млрд. Но фармгиганту придется конкурировать не только с Gilead Sciences, которые уже предложили свое — и более дешевое — решение, но и с Bluebird Bio и Juno Therapeutics, разрабатывающими аналогичные продукты.
Прибыльность клеточной генной терапии аналитики пока затрудняются оценить. Но по их данным, стоимость производства подобных лекарств от рака должна составлять не менее $200 000 за курс.
По-настоящему революционные открытия, которые происходят на рынке генной терапии и грозят перевернуть фармацевтический рынок (как минимум в области лечения онкологии), привлекают в отрасль инвестиции: за последние пять лет компании-производители получили порядка $600 млн венчурного капитала на свои разработки.
Рыночные перспективы стволовых клеток
По прогнозу аналитиков из Grand View Research, рынок препаратов, основанных на стволовых клетках, к 2025 году достигнет $15,6 млрд. Сегодня самые перспективные сферы применения стволовых клеток — это лечение болезни Паркинсона и болезни Альцгеймера, а также повреждений спинного мозга, сахарного диабета первого типа, заболеваний крови и онкологии.
Но пока что даже топовые компании, занимающиеся стволовыми клетками, не могут похвастаться такими же масштабами, как их коллеги по генной терапии. Например, крупнейшая компания, которая торгуется на бирже NASDAQ — Sangamo Therapeutics, — имеет капитализацию всего в $2,1 млрд.
В данный момент Sangamo Therapeutics разрабатывает два вида терапии на основе собственных — аутологичных — стволовых клеток для лечения заболеваний крови. Если производитель добьется успеха, то с помощью этих препаратов можно будет лечить такие генетические болезни крови, как бета-талассемия и серповидноклеточная анемия.
Развитие рынка стволовых клеток тормозится тем, что лекарства на основе аутологичных клеток делать невыгодно, так как такое производство нельзя масштабировать: лекарство, созданное для одного пациента, нельзя применить для другого. В то же время может быть прибыльно производить препараты на основе чужих — аллогенных — стволовых клеток. Но на разработку таких средств требуется много времени: необходимо сделать их «незаметными» для иммунитета пациентов, чтобы снизить риск отторжения.
Что дальше?
По всем оценкам, рынок клеточной и генной терапии в ближайшие годы будет активно развиваться, и средний годовой рост продаж составит не менее 30%. Новые открытия в сфере генной терапии обещают 2200 клинических испытаний, которые проводятся по всему миру: ученые ищут средства от различных видов рака, редких генетических нарушений, болезни Паркинсона, ВИЧ и других болезней.
Впереди планеты всей, как всегда, США — около 55% исследований происходят именно там. Также разработками в сфере генной терапии занимаются в Европе, Канаде и Китае. Один препарат, созданный при участии генной инженерии, запустили и в России — это Неоваскулген, лекарство, призванное помочь при ишемии нижних конечностей.
Что же касается стволовых клеток, рост рынка ожидается в результате появления новых препаратов регенеративной медицины — сейчас многие из них находятся в стадии разработки. Большинство исследований проходят в США, но новые решения в области стволовых клеток также появляются в Сингапуре и Японии.
Источник
Генерики и оригинальные препараты: взгляд практического врача
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Всемирная Организация Здравоохранения (ВОЗ) в 2004 г. приняла резолюцию, провозгласившую радикальное увеличение безопасности лечения приоритетной задачей ВОЗ [1]. В этой резолюции особый акцент сделан на право больного знать все о своем заболевании, методах его лечения и на необходимости получения информированного согласия больного на лечение. В связи с этим следует учитывать, что информированное согласие предполагает заведомое разъяснение пациенту различий между «аналогами» лекарственных средств (ЛС). Однако только 60% врачей обнаруживают знакомство с такой постановкой вопроса [2].
Проблема генерических препаратов чрезвычайно актуальна для России. Во–первых, потому что в РФ – самая большая доля генериков на фармацевтическом рынке (78–95%) (рис. 1). Некоторые оригинальные ЛС имеют огромное количество генериков. Так, у Вольтарена – 120 генерических «копий», что само по себе противоречит международной практике. Обычно же на фармацевтическом рынке присутствует 4–5 генериков, качество которых скрупулезно проверено при регистрации препаратов.
Во–вторых, потому что генерики, производимые в РФ, в большинстве своем – низкого качества. Так, Сергей Иванов, первый заместитель Председателя Правительства РФ на встрече с членами Общественной палаты заявил: «Я не могу не упомянуть проблему фармакологической промышленности. Наряду с лесной и рыбной отраслями, я их отношу к самым криминализированным в экономике России. Ведь там и контрафакта полно, а даже если это не контрафакт, то качество все равно низкое. Здесь давно пора навести порядок» [3].
Так чем же генерический препарат отличается от оригинального?
Оригинальный лекарственный препарат – это впервые синтезированное, прошедшее полный цикл доклинических и клинических исследований ЛС, защищенное патентом на срок до 20 лет. Только по истечении срока действия патента возможно воспроизведение ЛС любой фармацевтической компанией: создается генерик. Таким образом, генерик должен появляться значительно позже оригинального препарата. Однако уже на этом этапе в РФ имеют место нарушения. Например, патент на оригинальный азитромицин истек только в 2007 г.(!!), а в РФ уже зарегистрировано не менее 14 генериков [4].
Термин «генерик» возник в 70–е годы XX века, когда считалось, что препараты–аналоги надо называть родовым (генерическим) именем, в отличие от оригинального ЛС, которое продавалось под специальным торговым наименованием. Смысл этого правила заключался в том, что оно облегчало распознавание оригинального ЛС среди препаратов–аналогов. В настоящее время генерики часто имеют собственные названия, что не позволяет различать генерики и оригинал. Например, оригинальный препарат диклофенака называется Вольтарен (Новартис), а генерики, которые теоретически должны называться родовым (генерическим) именем диклофенак, имеют самые разнообразные наименования.
В целом основными признаками генерика должны являться:
• отсутствие патентной защиты;
• сравнительно низкая цена;
• назначение и продажа под непатентованным наименованием (МНН);
• почти полное соответствие оригинальному продукту по составу (вспомогательные вещества могут быть иными);
• соответствие фармакопейным требованиям;
• производство в условиях GMP (надлежащая производственная практика).
Однако в РФ генерики сегодня это:
• сравнительно низкая цена – не всегда;
• назначение и продажа под непатентованным наименованием (МНН) – далеко не всегда;
• почти полное соответствие оригинальному продукту по составу (вспомогательные вещества могут быть иными) – большие проблемы;
• соответствие фармакопейным требованиям – не всегда;
• производство в условиях GMP – не всегда.
В законе РФ «О лекарственных средствах» (1998) введено определение понятия «воспроизведенные лекарственные средства», однако в нем упущен центральный элемент: не указано, что они являются копиями или аналогами оригинальных препаратов [1].
Согласно международному стандарту генерик – это лекарственный продукт с доказанной фармацевтической, биологической и терапевтической эквивалентностью с оригиналом.
Фармацевтическая эквивалентность
Фармацевтическая эквивалентность предполагает содержание одних и тех же активных субстанций в одинаковом количестве и в одинаковой лекарственной форме; соответствие требованиям одних и тех же или сходных стандартов [5]. «Фармацевтически альтернативными являются лекарства, содержащие одинаковый терапевтический компонент, представленный в виде различных солей, эфиров или комплексов, либо в различных дозах» [6].
К сожалению, в РФ отменен аналитический контроль генерических препаратов на этапе регистрации, он проводится только для новых отечественных ЛС [7].
Биологическая эквивалентность
«Биоэквивалентные лекарственные препараты – это фармацевтически эквивалентные или фармацевтически альтернативные препараты, обладающие сопоставимой биодоступностью, изученной в сходных экспериментальных условиях. Под биодоступностью понимается скорость и доля всасывания активного ингредиента или активного компонента лекарства, которое начинает действовать в точке приложения» [6].
В сущности, биоэквивалентность – это эквивалентность скорости и степени всасывания оригинала и генерика в одинаковых дозах по концентрации в жидкостях и тканях организма. Тест проводится с участием 18–24 здоровых добровольцев, которые однократно принимают 1 дозу изучаемого генерика (для пролонгированного препарата – 5 суток приема), затем после нескольких периодов полувыведения принимают аналогичную дозу оригинального препарата. При сравнении двух графиков фармакокинетики различия не должны превышать 20% (рис. 2). Исследование на биоэквивалентность обязательно проводится для всех генерических препаратов. Естественно, биоэквивалентность – это не гарантия, а предположение терапевтической эквивалентности и безопасности препарата [8].
Если генерик разрешен к применению в других странах, он регистрируется в РФ по упрощенной схеме (без определения биоэквивалентности). Только генерики новых производителей исследуются на биоэквивалентность. Из 1256 зарегистрированных в 2001 г. зарубежных препаратов только 22 прошли экспертизу на биоэквивалентность при регистрации в РФ. Таким образом, при регистрации зарубежных генериков в РФ мы полностью доверяем досье, представляемым фармацевтическими компаниями [2]. Такая «доверчивость» дорого обходится пациентам. Так, по мнению директора Государственного фармакологического центра МЗ Украины В.Т. Чумака – «…ни один из 150 имеющихся на рынке Украины препаратов диклофенака по своим фармакокинетическим свойствам не соответствует Вольтарену» [9].
Хорошо известен пример контрольной проверки биоэквивалентности генериков оригинальному кларитромицину. Работа C.N. Nightingale была представлена в 2000 г. на 5–й Конференции по макролидам, азалидам, стрептограминам, кетолидам и оксазолидинонам в Севилье [10]. Автор сравнил оригинальный препарат кларитромицина с 40 копиями в отношении биоэквивалентности, применив стандарты Американской фармакопеи. Исследование показало, что 70% генериков растворяются значительно медленнее оригинального препарата, что критично для их усвоения. 80% генериков отличаются от оригинала по количеству действующего начала в одной единице продукта. Количество примесей, не имеющих отношения к действующему началу, в большинстве образцов больше, чем в оригинале. В «лучшем» генерике их было 2%, в «худшем» – 32%.
Терапевтическая эквивалентность
«Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при введении пациентам в соответствии с указаниями в инструкции» [6].
Генерик терапевтически эквивалентен другому препарату, если он содержит ту же активную субстанцию и, по результатам клинических исследований, обладает такой же эффективностью и безопасностью, как и препарат сравнения, чья эффективность и безопасность установлены.
Надо отметить, что сравнительное исследование должно проводиться по определенным правилам (GCP – надлежащая клиническая практика) и должно быть:
• независимым;
• многоцентровым;
• рандомизированным;
• контролируемым;
• длительным (средняя продолжительность приема ЛС);
• с жесткими конечными точками (смерть, инфаркт, инсульт).
Такого рода исследования выполнены только для единичных генериков, применяемых в РФ. К сожалению, данные клинических исследований при регистрации в РФ обязательны только для новых оригинальных препаратов, эффективность и безопасность генериков остается без внимания [7].
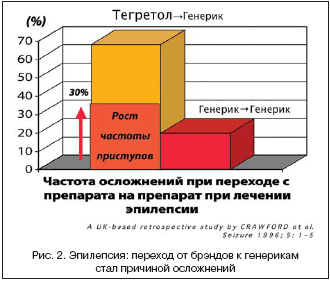
Отсутствие исследований на терапевтическую эквивалентность при регистрации генериков имеет многочисленные негативные последствия. Так, в хорошо известном исследовании противоэпилептических препаратов было показано, что переход с оригинального ЛС Тегретола на генерик приводил в 70% случаев к негативным последствиям, а в 30% случаев к значимому повышению частоты приступов [11].
По мнению профессора В.А. Насоновой, «…распространение в РФ огромного количества генериков диклофенака, не всегда обладающих основными качествами оригинального ЛС, стали заметно влиять на авторитет Вольтарена» [12].
Примером отсутствия терапевтической эквивалентности являются результаты сравнительного изучения антигипертензивной эффективности генериков эналаприла и оригинального ЛС – Ренитека. Продемонстрировано, что дозе Ренитека 12 мг, необходимой для достижения целевого АД, были эквивалентны различные дозы генериков [13].
Таким образом, особенностями генериков в РФ являются:
• появление многих генериков в России раньше соответствующих оригинальных ЛС;
• отсутствие данных о терапевтической эквивалентности с оригинальным ЛС;
• относительно высокие цены генериков;
• самая высокая доля генериков на фармацевтическом рынке.
Интересными являются сведения о том, из чего складывается стоимость оригинальных ЛС и генериков. 80% стоимости оригинального ЛС составляет стоимость исследований эффективности и безопасности препарата, а 20% стоимости – это стоимость синтеза лекарственного вещества. Вообще процесс создания оригинального ЛС очень длительный и дорогостоящий. Сначала создается молекула, потом она оценивается в исследованиях на клетках и тканях, затем на животных. После этого следуют три этапа клинических исследований на здоровых добровольцах и пациентах. После завершения клинических исследований ЛС проходит регистрацию.
Исследование оригинального ЛС продолжается и после регистрации. Проводятся с соблюдением правил GCP так называемые пострегистрационные исследования.
Известно, что только 1 из 5 000 молекул доходит до рынка в виде ЛС. Этот путь продолжается 12–15 лет и «стоит» от 800 млн. до 1 млрд. $. Прибыльными являются только 1–2 из вновь созданных ЛС.
Таким образом, преимуществами оригинальных ЛС являются:
• доказанная эффективность;
• доказанная безопасность;
• инновационность;
• воспроизводимость эффекта;
• жесткий контроль качества.
Процесс создания генерика происходит совершенно иначе. Отсутствуют три этапа клинических исследований, перед регистрацией проводится только исследование биоэквивалентности. 50% себестоимости составляет стоимость активной субстанции. Для того чтобы снизить стоимость, фармацевтические компании либо изменяют методы синтеза, либо ищут возможность приобретения наиболее дешевых субстанций. В целом приобретение активной субстанции у компаний, специализирующихся на ее производстве, является общепринятой практикой. Зачастую активная субстанция приобретается в странах, мало доступных для контроля: Китай, Индия, Вьетнам. Поставки субстанций происходят через большое количество посредников, сведения о месте производства обычно не публикуются и готовый продукт рекламируется, как изготовленный в высокоразвитой стране [1].
Качество наполнителей тоже имеет большое значение: любое изменение в составе вспомогательных веществ или оболочки могут существенно изменить качество препарата, его биодоступность, привести к токсическим или аллергическим явлениям. В том, что генерики отличаются от оригинала составом вспомогательных веществ, можно легко убедиться, изучив данные фармацевтических справочников.
Таким образом, источниками низкой стоимости генерических ЛС являются:
• отсутствие клинических исследований;
• отсутствие сравнительных исследований с оригиналом;
• отсутствие изучения профиля безопасности.
Могут ли генерики низкого качества повлиять на здоровье нации? Да, могут. Например, применение генерических антибиотиков приводит к хронизации заболеваний, резистентности бактерий, вирусов и грибов к антимикробным препаратам, росту инвалидизации и смертности [14].
Несоблюдение международных требований к генерикам в РФ влечет за собой огромные потери от «выгодной» цены вследствие затрат на повторные госпитализации, большие дозы ЛС и лечение побочных эффектов.
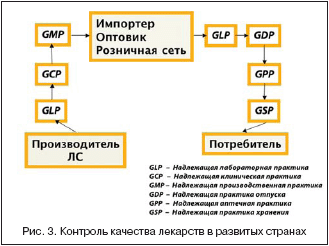
Как решается проблема генерических препаратов в развитых странах? Прежде всего это жесткий контроль качества на каждом этапе пути ЛС от производителя к пациенту (рис. 3). Кроме того, в развитых странах имеет место отрицательное отношение к биоэквивалентности, как к единственному способу оценки равнозначности лекарств. Для того чтобы считать генерик качественным, необходимо проведение клинических исследований на терапевтическую эквивалентность.
Очень важно то, что врач имеет полноценную информацию о том, какое ЛС является оригинальным препаратом, а также о качестве генерических препаратов. В США генерики разделены на группы «А» и «В». Код «А» присваивается генерикам, прошедшим клинические исследования на терапевтическую эквивалентность и имеющим отличия биоэквивалентности от оригинального ЛС не более 3–4%. Генерики с кодом «А» могут являться заменой оригинальному препарату по финансовым соображениям. Код «В» присваивается генерикам, не прошедшим клинические испытания на терапевтическую эквивалентность. Генерик с кодом «В» не может быть автоматической заменой оригинальному препарату или другому генерику с кодом «А». Сведения о статусе лекарственных препаратов – общедоступны и содержатся в справочнике «Orange Book». В аптеке провизор может отпустить больному препарат только с тем торговым названием, которое выписал врач [1,2,6].
Как решить проблему генериков в России? Конечно, наиболее кардинальным является изменение законодательства, приведение его в соответствие с законодательством цивилизованных стран. Пока этого не произошло, возможно оценивать качество генериков по некоторым весьма существенным критериям.
Во–первых, по мнению экспертов качество генерика вполне удовлетворительно, если ЛС зарегистрировано в странах с развитой контрольно–разрешительной системой, к которым относятся члены PIC–PI C/S – «Конвенции и схемы сотрудничества по фармацевтическим инспекциям» (старые члены Евросоюза, США, Япония, Канада, Австралия, Австрия, Швейцария, Норвегия, Венгрия, Чехия, Словакия, Сингапур) [1]. Важно именно место регистрации, а не производства ЛС.
Во–вторых, генерик имеет достойное качество, если компания–производитель доказала терапевтическую эквивалентность генерика оригинальному препарату в пострегистрационных рандомизированных контролируемых исследованиях [15].
В–третьих, должна быть уверенность, что при производстве генерика соблюдаются правила GMP [16].
Что делать врачу в России, если он хочет качественно лечить пациента? Скорее всего, назначать оригинальный препарат при наличии такой возможности или выбрать качественный генерик при невозможности назначить оригинальный препарат по финансовым соображениям.
Может ли практический врач в РФ заниматься оценкой качества генериков? Конечно нет, хотя многие врачи пытаются это делать. Однако это не входит в задачи практического врача, который просто должен иметь на рабочем столе источник достоверной информации о ЛС, в том числе о том, какой препарат является оригинальным, а какой генерическим, какой генерик относится к группе «А» и является качественным, а какой к группе «В» и не может быть заменой оригинальному ЛС и более качественному генерику. Тогда практический врач будет спокойно назначать то ЛС, которое считает нужным для данного больного. Кроме того, в этом случае врач должен иметь гарантию, что пациент в аптеке получит именно то ЛС (с тем торговым наименованием), которое выписано в рецепте. В нашей стране, к сожалению, нельзя допускать выписку рецептов по МНН, так как на фармацевтическом рынке присутствует огромное количество генерических ЛС очень различного качества. Врач же, как лицо юридически отвечающее за качество лечения пациента, должен быть уверен, что пациент получит именно то ЛС, которое он больному назначил.
Что делать пациенту в РФ? Начать задавать правильные вопросы врачу и государству, а также перестать экономить на здоровье. Хорошо известно, что население нашей страны на биологические добавки тратит в 10 раз больше средств, чем на лекарства [17].
Но, наверное, больше всего вопросов по поводу того, почему врач не имеет информации о том, какое торговое наименование соответствует оригинальному препарату, а какое генерическому. Почему в РФ отсутствует справочник ЛС, где это было бы указано? Ответственность за недостаточную информированность врача несет государство, которое должно обеспечивать все категории населения непредвзятой и доказательной информацией в отношении ЛС [18]. Полноценное лекарственное средство – это лекарственный продукт плюс полноценная информация о нем. Безусловно, наиболее простым решением проблемы с точки зрения практического врача был бы допуск на фармацевтический рынок РФ только качественных генерических ЛС.
Литература
1. Мешковский А.П. Место дженериков в лекарственном обеспечении. Фарматека. 2003; 3: 103–4.
2. Белоусов Ю.Б. Дженерики – мифы и реалии. Remedium. 2003;7–8: 4–9.
3. Иванов С. Выступление на встрече с членами Общественной палаты. Заседание, посвященное промышленности и инновациям. МГТУ имени Баумана. 2007; 18.05.
4. Панюшин Р. Оригинальные и дженериковые препараты: единство или борьба противопо¬ложностей? Фарм. вестник. 2003; 16: 23–25.
5. ЕМЕА, The rules governing medicinal products in the European Union Investigation of Bioavailability and Bioequivalence.1998; 3C: 231–244.
6. FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 23th Edition, 2003.
7. Материалы семинара «Совершенствование процесса регистрации и контроль качества лекарственных средств». Казахст. //Фармацевтический вестник. 16.10.2005.
8. Верткин А.Л., О.Б.Талибов О.Б. Генерики и эквивалентность – что стоит за терминами. Неотложная терапия. 2004; 1–2: 16–17.
9. Чумак В. Т. Оборот лекарственных средств в Украине. Проблемы и перспективы. Материалы І Международной конференции «Клинические испытания лекарственных средств в Украине». Киев, 2006, ноябрь.
10. Nightingale CH. A survey of the Quility of Generic Clarithromydn Product from 13 Countries. Clin Drug Invest 2000; 19: 293–05.
11. A UK–based retrospective study by CRAWFORD et al Seizure. 1996; 5: 1–5.
12. Насонова В.А. Особенности применения различных форм диклофенака натрия при болезнях мягких тканей плечевого пояса и боли в нижней части спины. Consilium medicum. 2006; 2 (8): 45–48.
13. Недогода С.В., Марченко И.В., Чаляби Т.А. Сравнительная антигипертензивная эффективность генериков ангиотензинпревращающего фермента эналаприла (ренитека, энапа, эднита, инворила, энваса и энама) и стоимость лечения у больных гипертонической болезнью. Артериальная гипертония. 2000; 1: 52–5.
14. Сущук Е.А. Симпозиум «Исследования по биоэквивалентности препаратов как основа для рационального использования генериков». Конгресс «Человек и лекарство», 3 апреля 2006 г.
15. The rules governing medicinal products in the European Union. Investigation of Bioavailability and Bioequivalence.1998; 3C: 231–244.
16. Марцевич С.Ю., Кутишенко Н.П., Дмитриева Н.А., Белолипецкая В.Г. Выбор лекарственного препарата в кардиологии: на что должен ориентироваться практический врач? Кардиоваскул. тер. и профилактика. 2004; 4: 77–82.
17. Гарматина Ю. Реклама против закона. //АиФ–Здоровье. 2004; 11, март: 2.
18. Рабочее совещание ВОЗ: Политика в области информации о ЛС в странах Европы и в Новых Независимых Государствах. Хиллеред. 1996; 27.03–2.04
Источник