Лекция 5 фармакодинамика
Фармакодинамика состоит из первичной и вторичной фармакологических реакций. Первичная фармакологическая реакция представляет собой взаимодействие с циторецепторами — биомакромолекулами, генетически детерминированными для взаимодействия с биологически активными веществами, включая лекарственные средства.
Взаимодействие с циторецепторами необходимо для развития вторичной фармакологической реакции в виде изменений метаболизма и функции клеток и органов. Нерецепторные механизмы действия встречаются редко. Отсутствуют циторецепторы для ингаляционных наркозных средств, плазмозаменителей, осмотических мочегонных препаратов, комплексонообразователей.
Одна и та же первичная фармакологическая реакция может приводить к различным вторичным изменениям (возбуждение -адренорецепторов норадреналином вызывает расширение зрачков и сужение сосудов). В основе вторичной фармакологической реакции иногда лежат различные первичные механизмы (спазм бронхов возникает при возбуждении М-холинорецепторов ацетилхолином или Ну-рецепторов гистамином).
Взаимодействие лекарственных средств с циторецепторами
Циторецепторы (греч. kytos — сосуд, клетка, лат. recipere — получать) созданы природой для эндогенных лигандов — гормонов, факторов роста, нейромедиаторов, аутакоидов. Они имеют структуру липо-протеинов, гликопротеинов. металлопротеинов. нуклеопротеинов. Реакция рецепторов на ксенобиотики обусловлена низкой специфичностью взаимодействия. Как правило, ксенобиотики обладают такой же стереохимической композицией, как и биологически активные вещества организма.
Концепция циторецепторов была предложена Паулем Эрлихом и Джоном Лэнгли в начале XX века. По мнению Эрлиха, функцию рецепторов выполняют молекулярные боковые цепи клеточной протоплазмы. способные воспринимать питательные вещества и токсины. Боковые цепи, циркулирующие в крови, образуют антитоксины (антитела). Рецепторами являются также «крайние образования» чувствительных клеток. Они превращают физическую или химическую энергию раздражения в возбуждение чувствительных нервов. Лэнгли установил, что кураре устраняет сокращение скелетных мышц, вызываемое никотином, но не изменяет возбуждающий эффект электрического тока.
В структуре циторецепторов присутствуют домен для связывания лигандов и эффекторный домен. Активные центры циторецепторов образованы функциональными группами аминокислот, фосфатидов, нуклеотидов, Сахаров.
Лекарственные средства устанавливают с циторецепторами непрочные физико-химические связи — вандерваальсовы, ионные, водородные, дипольные по принципу комплементарности (активные группы лекарств взаимодействуют с соответствующими группами активного центра циторецепторов).
Необратимые ковалентные связи с циторецепторами образуют немногие вещества — необратимые ингибиторы холинэстеразы, тяжелые металлы, цитостатики. Все они высокотоксичны.
По отношению к циторецепторам лекарственные средства обладают аффинитетом (лат. affinis — родственный) и внутренней активностью. Аффинитет (сродство) рассматривают как способность образовывать комплекс с циторецепторами. Внутренняя активность направлена на создание их активной стереоконформации. приводящей к появлению клеточного ответа. В зависимости от выраженности аффинитета и наличия внутренней активности лекарственные средства разделяют на 2 группы:
— агонисты (греч. agonistes — соперник, адоп — борьба), или миметики (греч. mimeonnai — подражать) — вещества с умеренным аффинитетом и высокой внутренней активностью: полные агонисты вызывают максимально возможный клеточный ответ, частичные (парциальные) агонисты — менее значительную клеточную реакцию;
— антагонисты (греч. antagonisma — соперничество, anti – против, agon — борьба), или блокаторы — вещества с высоким аффинитетом, но лишенные внутренней активности. Они экранируют циторецепторы от действия эндогенных лигандов и препятствуют развитию клеточного ответа, усиливая эффекты других, неблокированных циторецепторов. Вещества, блокирующие активные центры циторецепторов, являются конкурентными антагонистами. Возможно сочетание в фармакодинамике свойств агониста и антагониста, например, агонисты-антагонисты возбуждают одни циторе-цепторы и блокируют другие.
Циторецепторы возбуждаются только в начальный момент взаимодействия с лекарственными средствами. Для агонистов характерна высокая константа диссоциации комплекса «лекарство — циторецептор». Антагонисты, обладая высоким аффинитетом, более продолжительно связываются с циторецепторами, при этом в первый момент взаимодействия возможно появление эффекта возбуждения.
Лекарственные средства присоединяются также к аллостерическим центрам циторецепторов. что модифицирует структуру активных центров и изменяет их реакцию на лекарства или эндогенные лиганды. Пример аллостерических рецепторов — бензодиазепиновые рецепторы, повышающие аффинитет ГАМК-рецепторов типа А.
На мембране одной и той же клетки могут присутствовать циторецепторы с различным функциональным значением, поэтому клеточный ответ на возбуждение циторецепторов является алгебраической суммой вызываемых ими индивидуальных реакций.
Циторецепторы классифицируют на 4 типа (рис. 5.1):
• Рецепторы ионных каналов;
• Рецепторы, ассоциированные с G-белками;
Циторецепторы-протеинкиназы связаны с плазматической мембраной клеток. Они имеют внеклеточный домен для взаимодействия с лигандами и внутриклеточный каталитический домен — протеинкина-зу. Оба домена соединены внутримембранной цепью из гидрофобных аминокислот. Рецепторы-протеинкиназы фосфорилируют белки клеток — киназы, регуляторные и структурные белки. Чаще всего происходит фосфорилирование тирозина белков-мишеней. Примеры циторецепторов-протеинкиназ — рецепторы инсулина, лимфокинов, эпидермального и тромбоцитарного факторов роста.
Циторецепторы к предсердному (атриальному) натрийуретическо-му пептиду, ассоциированные с гуанилатциклазой, повышают продукцию цГМФ.
Циторецепторы ионных каналов, повышая проницаемость мембран для Na + , К + . Са 2+ и С/ — , обеспечивают мгновенный клеточный ответ. Примеры рецепторов ионных каналов:
• Рецепторы, вызывающие деполяризацию и возбуждение функции клеток, — Н-холинорецепторы. рецепторы глутаминовой и аспара-гиновой кислот (увеличивают проводимость для Na + , К + , Са 2+ )
• Рецепторы, вызывающие гиперполяризацию и торможение функции клеток, — ГАМКд-рецепторы и рецепторы глицина (увеличивают проводимость для С/-).
Циторецепторы, ассоциированные с G-белками, состоят из регуляторного домена для связывания лигандов, внутримембранного G-белка и эффекторной системы. G-белок передает информацию от регуляторного домена на эффекторную систему, используя энергию ГТФ. Эффекторная система представлена аденилатциклазой. фосфолипазами А, С и D, белками ионных каналов, транспортными белками. При возбуждении рецепторов образуются внутриклеточные биологически активные вещества — вторичные мессенджеры (англ. messenger— вестник, посредник).
Аденилатциклаза превращает АТФ во вторичный мессенджер цАМФ. Рецепторы могут как активировать, так и ингибировать аденилатциклазу.
Источник
ФУНКЦИОНАЛЬНЫЕ ИЗМЕНЕНИЯ, ВЫЗЫВАЕМЫЕ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ В ОРГАНИЗМЕ
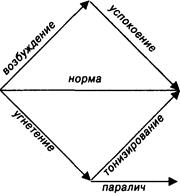
Успокоение— возврат возбужденной функции к норме: снижение температуры тела жаропонижающими средствами при лихорадке, уменьшение боли под влиянием анальгетиков.
Угнетение— снижение функции ниже нормы: положительное угнетение — утрата сознания, подавление рефлексов и снижение тонуса скелетных мышц при наркозе; отрицательное угнетение — торможение дыхательного центра при действии наркозных, снотворных средств, наркотических анальгетиков.
Тонизирование— возврат угнетенной функции к норме: улучшение деятельности дыхательного и сосудодвигательного центров при дыхательной недостаточности, коллапсе, шоке под влиянием камфоры, кофеина и других аналептиков; усиление сокращений декомпенсированного миокарда у больных, получающих сердечные гликозиды.
Паралич— прекращение функции: положительный паралич — обратимое устранение болевой чувствительности при действии сильных местных анестетиков, полное расслабление скелетной мускулатуры, вызываемое миорелаксантами; отрицательный паралич — необратимый паралич дыхательного центра после его возбуждения атропином и аналептиками в токсических дозах.
ЭФФЕКТЫ ПРИ ПОВТОРНОМ ПРИЕМЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Кумуляция
Кумуляция (лат. cumulatio — увеличение, скопление) — накопление в организме молекул лекарственных средств (материальная кумуляция) или их эффектов (функциональная кумуляция).
Материальная кумуляция возникает при приеме липофильных лекарственных средств, обладающих низким печеночным и/или почечным клиренсом и длительным периодом полуэлиминации. В клинике необходимо учитывать кумуляцию фенобарбитала, бромидов, сердечных гликозидов наперстянки (дигитоксин, целанид, дигоксин), антикоагулянтов непрямого действия.
Кумуляция имеет как положительное, так и отрицательное значение. Положительное значение связано с пролонгированием действия лекарственных средств, возможностью их редкого приема, например, больные тяжелой застойной сердечной недостаточностью могут не принимать сердечные гликозиды ночью. Отрицательное значение обусловлено опасностью интоксикации в результате суммирования дозы повторно введенного препарата с его количеством, сохранившемся от предыдущего назначения. Для того, чтобы исключить интоксикацию, необходимо принимать кумулирующие средства в поддерживающей дозе, равной количеству препарата, элиминируемому за сутки:
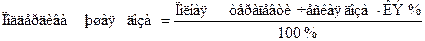 |
КЭ — коэффициент элиминации (часть дозы в процентах, элиминируемая за сутки).
Относительная материальная кумуляция развивается при заболеваниях печени и почек, а также у детей и пожилых людей. При патологии печени возможна кумуляция активных метаболитов лекарственных средств.
Примеры функциональной кумуляции — хронический алкоголизм при злоупотреблении спиртом этиловым; паралич центров продолговатого мозга при отравлении свинцом, возникающий после элиминации яда из организма.
Дата добавления: 2016-07-27 ; просмотров: 3195 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
ВИДЫ ФАРМАКОЛОГИЧЕСКОГО ДЕЙСТВИЯ ЛС (ЧАСТЬ 3)
Индивидуальная несовместимость организма с ЛС может быть врожденной (идиосинкразия) или приобретенной (сенсибилизация).
Идиосинкразия (греч. idios — своеобразный, synkrasis — смешение) — врожденная индивидуальная непереносимость ЛВ. Она обусловлена отсутствием или снижением активности ферментов, либо отсутствием систем обезвреживания веществ определенной химической группы.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Идиосинкразия возникает при первом приеме вещества (агента) и при этом иммунитет не развивается, антитела не образуются, не возникает реакции «АГ+АТ». Например, врожденная аномалия фермента псевдохолинэстеразы удлиняет миорелаксирующее действие суксаметония йодида (Дитилин). У ряда больных с наследственной недостаточностью фермента глюкозо–6–фосфатдегидрогеназы может возникать гемолиз эритроцитов при применении противомалярийного препарата «Примахин» или антибиотика «Хлорамфеникол».
Аллергические реакции являются одними из наиболее часто встречающихся отрицательных видов действия ЛС. Многие из них (антибиотики, сульфаниламиды, препараты инсулина и др.) при попадании в организм людей с повышенной чувствительностью приводят к образованию и накоплению специфических антител. При повторных введениях этих ЛС происходит их взаимодействие с антителами и в результате возникают аллергические реакции. Лекарственная аллергия обусловлена нарушением иммунологических свойств организма, это приобретенная повышенная чувствительность организма к лекарственным веществам. Она протекает в виде аллергических реакций по немедленному или замедленному типу. К аллергическим реакциям немедленного типа относятся крапивница, отек Квинке, поллинозы, бронхиальная астма, сывороточная болезнь, лекарственный анафилактический шок. Они возникают при повторных курсах терапии, через несколько минут (≈20–30 мин.) после приема лекарства. Из аллергических реакций немедленного типа наиболее опасным является анафилактический шок. Анафилактический шок — быстроразвивающаяся реакция организма на повторное введение лекарства при имеющейся повышенной чувствительности к данному лекарственному веществу. Симптомы: боль за грудиной, отек гортани, спазм бронхов и удушье, снижение АД и ослабление сердечной деятельности, возможна потеря сознания. Если вовремя не оказать помощь, может наступить гибель организма. Аллергические реакции немедленного типа могут вызвать антибактериальные препараты (в частности, введение антибиотиков пенициллинового ряда), НПВС, анестетики, введение сывороток, вакцин.
Аллергические реакции замедленного типа развиваются через 24–48 часов и более, после повторного введения лекарственного вещества, к которому имеется сенсибилизация организма. Сенсибилизацией (лат. sensibilis — чувствительный) называется иммунологически опосредованная повышенная чувствительность организма к экзогенным или эндогенным антигенам. К ним относятся: лекарственная аллергия, вызывающая цитотоксический эффект в виде дерматитов, васкулитов, флебитов, аллергические реакции на пробы Манту, Пирке.
К отрицательным видам действия ЛС относится также «синдром отмены» — абстиненция (лат. abstinentia — воздержание), физическое и психическое состояние пациента после внезапного или полного прекращения препаратозависимой терапии. Синдром отмены может наблюдаться после прекращения приема опиоидных наркотических анальгетиков (Морфин, Тримеперидин); гормональных препаратов (Инсулин, глюкокортикостероиды); антигипертензивного средства «Клофелин», адреноблокатора «Анаприлин» и некоторых психотропных средств.
Всесоюзная организация здравоохранения (ВОЗ) рассматривает все случаи неблагоприятных реакций на организм зарегистрированных ЛС. Согласно определению ВОЗ, побочное нежелательное действие — это непредвиденные вредные (губительные) эффекты, которые возникают при использовании доз лекарственного средства, рекомендованных для профилактики и лечения заболеваний. При однократном введении лекарства неблагоприятные реакции могут не развиваться, не проявляться и никак не выявляться. При длительном применении ЛС побочный нежелательный эффект может стать причиной различных осложнений, в т.ч. обострения наследственных заболеваний. Различают нежелательные реакции, связанные с применением ЛС, на:
- побочные (негативные) реакции;
- серьезные нежелательные реакции (приводящие к различным осложнениям, инвалидности, угрозе жизни человека или к летальному исходу);
- непредсказуемые нежелательные реакции;
- серьезные непредвиденные нежелательные реакции.
Нежелательные эффекты, возникающие при применении ЛС в дозах, превышающих терапевтические, называются токсическими, как правило, это связано с передозировкой того или иного лекарственного препарата.
Согласно международной классификации выделяют 4 типа отрицательных побочных эффектов или нежелательных реакций на ЛС.
Тип А — предсказуемые реакции организма на введенное лекарство. Как правило, это дозозависимые побочные реакции, возникающие в 75% случаев от всех нежелательных реакций и приблизительно наблюдаются более чем у 1 из 100 больных. Эти реакции связывают с лекарственным взаимодействием, абсолютной, относительной передозировкой, индивидуальными особенностями организма. Летальность пациентов невысокая.
Тип В — непредсказуемые реакции организма, как правило, нечастые и возникают только у чувствительных людей. Это — дозонезависимые реакции, в
25% случаев неизвестного генеза, иммунологические или неиммунологические (иммунопатии, энзимопатии, идиосинкразия, сенсибилизация, гиперчувствительность). Возникновение таких реакций — менее 1 на 1000 больных, высокая летальность.
Тип С — реакции организма, связанные с длительной терапией заболевания. Возникает синдром отмены, кумуляция, лекарственная зависимость, подавление выработки эндогенных веществ. Диагностика таких реакций затруднительна.
Тип D — тяжелые необратимые побочные эффекты на вводимое лекарство. Как правило, чаще всего наблюдаются отсроченные эффекты: мутагенность, канцерогенность и тератогенность. Предсказать такие реакции организма крайне трудно. В настоящее время все лекарства, которые регистрируются, проходят тестирование на вышеперечисленные необратимые побочные эффекты.
Одновременное использование нескольких ЛС с мало прогнозируемым результатом их совместного взаимодействия может привести к полипрагмазии (греч. poli, polys — многий, pragma — действие). У больных старше 60 лет нередко диагностируют одновременно несколько заболеваний. В норме врач назначает не более 3–5 лекарств. Использование 3–5 лекарств одновременно приводит к развитию нежелательных реакций у 4% пациентов. Применение 16–20 лекарств одновременно может вызвать развитие побочных нежелательных эффектов в 54% случаев.
Токсическое действие возникает также при абсолютной или относительной передозировке ЛС и проявляется в значительном, иногда обратимом нарушении функций отдельных органов или систем органов. Абсолютная передозировка бывает при повышении высших, суточных и курсовых доз, а относительная передозировка – при назначении средних (обычных) доз лицам с поражениями печени, почек, что сопровождается накоплением в организме применяемого действующего вещества, т.к. замедляется его инактивация и выделение из организма. Хорошо известно токсическое действие аминогликозидных антибиотиков (Стрептомицин, Канамицин) на слуховой нерв, когда поражается восьмая пара черепно-мозговых нервов и возникает ототоксический эффект. У больных наблюдается снижением слуха, шум, звон или заложенность в ушах, вплоть до глухоты.
Токсическое действие, кроме общего и местного, может обозначаться как ориентированное на определенные органы: нейро–, нефро–, гепато–, гемато– или кардиотоксический эффект и т.д.
При нейротоксическом эффекте повреждаются ткани нервной системы (ЦНС, периферическая нервная система). Примером нейротоксического действия является повреждающее действие ЦНС местным анестетиком «Новокаином» и близким к нему по химической структуре антиаритмическим препаратом 1А класса — «Новокаинамидом». При в/в введении возможно развитие головокружения, двигательного возбуждения или неприятные ощущения (чаще в конечностях), парестезии, которые проявляются онемением, покалыванием, жжением или эффектом «ползание мурашек». Антибиотик «Циклосерин», применяемый для лечения больных туберкулезом, может вызвать развитие психозов, галлюцинаций, псевдоэпилептических припадков.
Антибиотики из группы аминогликозидов вызывают нефротоксический эффект. Повреждение клубочкового аппарата или канальцевой системы нефрона почек могут возникать при применении полимиксинов и некоторых цефалоспоринов.
Гепатотоксическое действие — повреждение паренхимы печени и нарушение ее метаболической функции и др. Например, при применении Метациклина, Рифампицина.
Гематотоксическое действие (угнетение кроветворения) оказывают большинство цитостатиков, т.к. оказывают прямое угнетающее влияние на быстро размножающиеся ткани и в т.ч. на кроветворную систему (костный мозг). Это токсическое действие возникает только при резорбтивном применении хлорамфеникола (левомицетина). После местного применения препаратов, в состав которых входит левомицетин: 0,25% раствор левомицетина в глазных каплях, 1% глазной линимент, линимент синтомицина, содержащий рацемическую смесь (1 ч. хлорамфеникола + 1 ч. — его правовращающий изомер), комбинированная мазь «Левомиколь» и антибактериальный аэрозоль «Олазоль», таких побочных эффектов не возникает.
При назначении ЛС беременным женщинам возможно отрицательное действие на развивающийся плод. Эти отрицательные действия возникают при применении ЛС, проникающих через плацентарный барьер. Наиболее серьезными являются тератогенное и эмбриотоксическое действия.
Тератогенное действие (греч. teras — урод) проявляется врожденными уродствами, развившимися в результате влияния некоторых ЛС на организм плода (наиболее опасный период с 3 по 12 неделю беременности). Хорошо известна история применения в некоторых зарубежных странах успокаивающего и снотворного средства «Талидомид». У женщин, принимавших в первую треть беременности этот препарат, рождались дети, имевшие врожденные уродства (дефекты конечностей, их недоразвитие, пороки сердца, почек, нарушение функций желудочно–кишечного тракта и др. органов). Известны случаи уродств от применения некоторых гормональных препаратов, антибиотиков. Для предупреждения тератогенного действия рекомендуется воздерживаться от приема ЛС в первые три месяца беременности, особенно когда происходит закладка органов ребенка.
Эмбриотоксическое действие ЛС проявляется нарушением развития эмбриона, процессов имплантации (1–2 неделю беременности) и образования плаценты (3–6 неделю). В результате эмбриотоксического действия беременность или не развивается, или заканчивается самопроизвольным абортом.
Фетотоксическое действие связано с изменением функции органов и систем плода, а также обмена веществ в период с 9 по 38 неделю.
Мутагенное действие связано со стойким повреждением зародышевой клетки в период эмбриогенеза и ее генетического аппарата (до 12 недели беременности). Мутации могут проявляться в половых клетках, изменяя генотип потомства. Мутации в соматических клетках могут привести к развитию злокачественных образований (канцерогенному действию).
Безопасность ЛС должна изучаться на всех этапах продвижения препарата на фармацевтическом рынке (даже после тщательно проведенных доклинических и клинических испытаний). Одно только официальное разрешение на применение лекарства не является гарантией его безопасности для всех больных.
Источник


