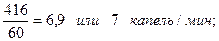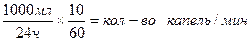- Раздел 4: СКОРОСТЬ ВНУТРИВЕННОГО ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
- Расчет скорости инфузии препарата через линеомат (скорость титрования)
- Вам также могут быть полезны:
- Об этом калькуляторе
- Формула
- Дополнительные сведения
- Краткие замечания по описанным препаратам
- Дофамин
- Парентеральное питание новорожденных
- Общая информация
- Краткое описание
- Автоматизация клиники: быстро и недорого!
- Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран 1 место — 800 RUB / 4500 KZT / 27 BYN в месяц
- Классификация
- Диагностика
Раздел 4: СКОРОСТЬ ВНУТРИВЕННОГО ВВЕДЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ



Цель: Научиться рассчитывать скорость внутривенного введения лекарственных средств.
Инфузионная система устроена таким образом, чтобы распределить 1мл раствора на определенное количество капель. Эти капли могут быть большими или очень маленькими в зависимости от изготовителя и типа капельницы.
Например
Капельница может дозировать:
60 капель/мл (микрокапельницы)
Назначая препарат внутривенно, врач указывает название раствора, его общий объем и продолжительность введения.
Например
Назначения врача: 1000 мл 5% раствора глюкозы внутривенно капельно в течение 24 ч.
Капельница дозирует 10 капель/мл.
Расчеты можно произвести двумя способами:
1) во-первых: подсчитать нужную скорость инфузии (в мл/ч).
1000 мл/ 24 ч = 41,6 мл/ч;
во-вторых: подсчитать скорость введения препарата в каплях в минуту, используя следующую формулу:
2) можно использовать другую формулу:
Врач может назначить препарат внутривенно капельно, указав скорость инфузии (в мл/ч) и ее продолжительность.
Например
Назначение врача: 5% раствор глюкозы внутривенно капельно со скоростью 125 мл/ч в течение следующих 8 ч.
Капельница дозирует 10 капель/мл.
Подсчитайте скорость введения препарата в каплях/мин:



125мл/1 ч × 10/60 = капель/мин
1250/60 = 20,83 или 21 капель/мин
Тестовый контроль
- Назначение врача:2000 мл 5% раствора глюкозы внутривенно капельно в течение 24 ч.
Капельница дозирует 10 капель/мл.
Подсчитайте скорость инфузии в каплях/мин.
- Назначение врача: 5% раствор глюкозы внутривенно капельно со скоростью 150 мл/ч в течение 10 ч.
Капельница дозирует 10 капель/мл.
Подсчитайте скорость инфузии в каплях/мин.
- Назначение врача: 2000 мл 5% раствора глюкозы внутривенно капельно в течение 24 ч.
Капельница дозирует 10 капель/мл.
Инфузия началась в 10 ч со скоростью 14 капель/мин. Сейчас 15 ч того же дня, в первом 1000-миллилитровом флаконе осталось 400 мл раствора.
Нужно отрегулировать скорость введения первых 1000 мл препарата или скорость инфузии в течение первых 12 ч до ____ капель/мин.
Источник
Расчет скорости инфузии препарата через линеомат (скорость титрования)
Вам также могут быть полезны:
Об этом калькуляторе
*Этот калькулятор позволяет расчитать скорость инфузии препарата через линеомат (скорость титрования в мл/час) при известном количестве препарата в милиграммах в известном объеме раствора. Также необходимо указать вес пациента и дозировку, определяемую либо в мкг*кг/мин, либо в мл/час.
Например, 4% раствор дофамина объемом 5 мл содержит 200 мг чистого вещества (4% — 40 мг, 40*5=200). Ампула препарата (5 мл) разведена физ. раствором до объема 20 мл. Соответственно, 200 мг — это количество препарата, а 20 мл — общий объем раствора. Вес пациента — 70 кг и используется почечная дозировка дофамина (2 мкг*кг/час). Таким образом, скорость введения составит 0,84 мл/час.
Скорость в мл/час автоматически пересчитывается в скорость в каплях в минуту при указании дозировки препарата в микрограммах на килограмм в минуту. При этом в рачет берется то, что в 1 милилитр содержит 20 капель.
Если скорость в каплях в минуту менее 1 капли в минуту, калькулятор предлагает выбрать меньшее разведение и перейти с капельного введения на введение с помощью линеомата.
Также калькулятор позволяет рассчитать скорость инфузии в мкг*кг/мин при известной дозировке препарата в мл/час.
Для того, чтобы использовать калькулятор при расчете доз препаратов, не зависящих от веса, в поле «Вес пациента» введите значение равное 1.
Формула
Скорость инфузии = масса тела пациента (кг) * доза препарата (мкг/кг*мин) / (количество препарата в инфузионном растворе (мг) * (1 000/общий объем инфузионного раствора))*60
Дополнительные сведения
| Препарат | Диапазон доз, (мкг/кг*мин) | Количество препарата в 1 мл стандартной формы выпуска, мг | Скорость, мл/час |
|---|---|---|---|
| Адреналин (гидрохлорид) | 0,05-0,4 | 1 (0.1% — 1,0) | 4.2 |
| Норадреналин (левонор) | 0,03-1 | 1 (0.1% — 1,0) | 2.5 |
| Дофамин | 1-20 | 200 (4% — 5,0) | 0.4 |
| Нитроглицерин | 10-400 мкг/мин | 20 (1% — 2,0) | 0.6 |
| Фенилэфрин (мезатон) | 0.3-2 | 10 (1% — 1,0) | 2.5 |
Краткие замечания по описанным препаратам
Дофамин
Если скорость инфузии > 20—30 мкг/кг/мин, дофамин целесообразно заменить другим сосудосуживающим средством (адреналин, норадреналин).
Действие на гемодинамику зависит от дозы:
- Низкая доза: 1—5 мкг/кг/мин, увеличивает почечный кровоток и диурез.
- Средняя доза: 5—15 мкг/кг/мин, увеличивает почечный кровоток, ЧСС, сократимость миокарда и сердечный выброс.
- Высокая доза: > 15 мкг/кг/мин, оказывает сосудосуживающее действие.
Источник
Парентеральное питание новорожденных
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2015
Общая информация
Краткое описание
Парентеральное питание – это вид искусственного питания или нутритивной поддержки, при котором все питательные вещества или определенная часть вводятся в организм внутривенно, минуя желудочно-кишечный тракт.
Название протокола: Парентеральное питание новорожденных
Код протокола:
Сокращения, используемые в протоколе:
Дата разработки протокола: 2015 год.
Категория пациентов: новорожденные.
Пользователи протокола: неонатологи, детские анестезиологи-реаниматологи, педиатры, диетологи пери — и неонатальных отделений.
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++или+), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
— 800 RUB / 4500 KZT / 27 BYN — 1 рабочее место в месяц
Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Перечень основных и дополнительных диагностических мероприятий
Оценка объема жидкости:
При назначении парентерального питания с нутритивными целями определяется необходимостью следующих процессов [5] (УД – А):
Оценка эффективности ПП согласно рекомендациям ВОЗ «Шкалы прироста массы тела у мальчиков и девочек (Fenton T.R., 2013)» (приложение 1).
В период транзиторной убыли массы тела концентрация натрия (Na+) в экстрацеллюлярной жидкости возрастает. Ограничение Na+ в этот период понижает риск некоторых заболеваний у новорожденных, но гипонатриемия ( Вес ребенка, грамм
Необходимо полное покрытие всех компонентов потребляемой энергии с помощью парентерального и энтерального питания. Только при наличии показаний к полному ПП все потребности необходимо обеспечивать парентеральным путем. В остальных случаях парентерально должно вводиться лишь то количество энергии, которое недополучено энтеральным путем. Наиболее высокая скорость роста характерна для наименее зрелых детей, поэтому необходимо как можно раньше обеспечить ребенка энергией для роста. В транзиторный период необходимо предпринимать усилия для минимизации потерь энергии (выхаживание в условиях термонейтральной зоны, ограничение испарения с кожи, охранительный режим). В 1-3-е сутки жизни обеспечьте поступление энергии, равной обмену покоя, 45-60 ккал/кг. Необходимо увеличивать калорийность ПП ежедневно на 10-15 ккал/кг с целью достижения калорийности 105 ккал/кг к 7-10-м суткам жизни.
При частичном ПП теми же темпами необходимо увеличивать суммарное поступление энергии с целью достижения калорийности 120 ккал/кг к 7-10-м суткам жизни. Отмену ПП необходимо проводить, только когда калорийность энтерального питания достигнет не менее 100 ккал/кг. После отмены ПП должен быть продолжен контроль антропометрических показателей, производите коррекцию питания.
При невозможности достижения оптимального физического развития при исключительно энтеральном питании должно быть продолжено парентеральное питание. Примерный расход энергии у недоношенных новорожденных представлен в табл. 2.
Таблица 2. Компоненты энергетического обмена у недоношенных детей
Жиры являются более энергоемким субстратом, чем углеводы. Белки у недоношенных детей также частично могут использоваться организмом для получения энергии. Избыток небелковых калорий вне зависимости от источника используется для синтеза жиров.
Белки – это важный источник пластического материала для синтеза новых белков, и энергетический субстрат, у детей с ЭНМТ и ОНМТ. 30% поступающих аминокислот может использоваться для целей синтеза новых белков в организме ребенка. При недостаточной обеспеченности небелковыми калориями (углеводами, жирами) доля белка, используемого для синтеза энергии, увеличивается, а на пластические цели используется меньшая доля, что нежелательно. Дотация аминокислот в дозе 3 г/кг в сутки в течение первых 24 часов после рождения у детей с ОНМТ и ЭНМТ безопасна и связана с лучшей прибавкой массы [5] (УД – А);.
Препараты альбумина, свежезамороженной плазмы и других компонентов крови не являются препаратами для парентерального питания. При назначении парентерального питания их не следует принимать в расчет в качестве источника белка.
Метаболический ацидоз не является противопоказанием к применению аминокислот. Необходимо помнить, что метаболический ацидоз в большинстве случаев является проявлением другого заболевания, не имея отношения к применению аминокислот у новорожденных.
Потребность в белке определяется количеством белка, исходя из количества, необходимого на синтез и ресинтез белка в организме (запасаемый белок), идущего на окисление как источник энергии и количества экскретируемого белка.
Оптимальное количество белка или аминокислот в питании определяется гестационным возрастом ребенка, так как композиционный состав тела меняется по мере роста плода.
У наименее зрелых плодов в норме скорость синтеза белка выше, чем у более зрелых, большую долю во вновь синтезированных тканях занимает белок. Поэтому чем меньше гестационный возраст, тем больше потребность в белке.
Оптимальное соотношение белка и небелковых калорий в питании плавное, меняется от 4 г/100 ккал и более у наименее зрелых недоношенных до 2,5 г/100 ккал у более зрелых. Это позволяет моделировать композицию массы тела, характерную для здорового плода.
Тактика дотации белков:
Стартовые дозы, темп увеличения и целевой уровень дотации белка в зависимости от гестационного возраста указаны в таблице 3.
У детей с массой тела при рождении менее 1500 г дотация парентерального белка должна оставаться неизменной до достижения объема энтерального питания 50 мл/кг в сутки.
1,2 г аминокислот из растворов для парентерального питания эквивалентен примерно 1 г белка. Для рутинного расчета принято округлять это значение до 1 г.
Обмен аминокислот у новорожденных имеет ряд особенностей, поэтому для проведения безопасного ПП следует использовать препараты белка, разработанные с учетом особенностей обмена аминокислот у новорожденных и разрешенные с рождения (0 месяцев). Препараты для ПП взрослых не должны применяться у новорожденных.
Дотация аминокислот может осуществляться как через периферическую вену, так и через центральный венозный катетер.
Контроль безопасности и эффективности дотации белка
На сегодняшний день не разработано эффективных тестов, позволяющих контролировать достаточность и безопасность парентерального введения белка. Оптимально использовать для этой цели показатель азотистого баланса, однако в практической медицине для интегральной оценки состояния белкового обмена используется мочевина.
Контроль уровня мочевины информативен в отношении безопасности применения аминокислот, начиная со 2-й недели жизни. Исследование следует проводить с периодичностью 1 раз в 7-10 дней. При этом низкий уровень мочевины ( Масса тела при рождении, грамм
* Белковая нагрузка не изменяется до достижения объема энтерального питания 50 мл/кг в сутки.
** точно не определена, потребность повышается при состояниях, сопровождающихся высоким катаболизмом (сепсис).
Потребность в углеводах рассчитывается на основе потребности в калориях и скорости утилизации глюкозы. В случае переносимости углеводной нагрузки (уровень глюкозы в крови не более 8 ммоль/л) углеводную нагрузку следует увеличивать ежедневно на 0,5-1 мг/кг в 1 мин, но не более 12 мг/кг в 1 мин. Тактика дотации углеводов 1 г глюкозы содержит 3,4 кал.
Тактика назначения представлена в таблице 3.
Контроль безопасности и эффективности дотации углеводов осуществляется путем мониторирования уровня глюкозы в крови.Гипогликемия — состояние, опасное для жизни, которое может привести к инвалидности.
Уровень глюкозы в крови составляет от 8 до 10 ммоль/л, углеводную нагрузку не следует увеличивать. Необходимо помнить, что гипергликемия часто является симптомом другого заболевания, которое следует исключить.
Уровень глюкозы в крови пациента остается Ион
7,5% КСl – 1,0 ммоль/л
10% КСl – 1,35 ммоль/л
Панангин КСl – 0,25 ммоль/л
10% NаCl – 1,5 ммоль/мл
0,66 мл 10% NаCl = 1 ммоль
Цинк.
Цинк участвует в обмене энергии, макронутриентов и нуклеиновых кислот. Быстрый темп роста глубоконедоношенных детей обусловливает их более высокую потребность в цинке по сравнению с доношенными новорожденными. Глубоконедоношенные дети и дети с высокими потерями цинка, обусловленными диареей, наличием стомы, тяжелыми заболеваниями кожи, требуют включения цинка сульфата в парентеральное питание.
Селен:
Селен является антиоксидантом и компонентом активной глутатионпероксидазы – фермента, защищающего ткани от повреждения активными формами кислорода.
Низкий уровень селена часто встречается у недоношенных детей, что способствует развитию у данной категории детей БЛД и ретинопатии недоношенных. Потребность в селене у недоношенных детей – 1-3 мг/кг в сутки (актуально при очень длительном парентеральном питании в течение нескольких месяцев).
В настоящее время в Казахстане не зарегистрированы препараты фосфора, цинка и селена для парентерального введения, что делает невозможным их использование у новорожденных в ОРИТ.
Источник