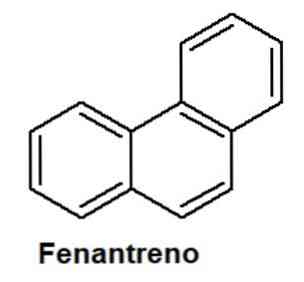
Фенантрен
| Фенантрен | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | фенантрен |
| Химическая формула | C14H10 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 178,23 г/моль |
| Термические свойства | |
| Температура плавления | 99 °C |
| Температура кипения | 340 °C |
| Классификация | |
| Рег. номер CAS | 85-01-8 |
| SMILES | c1ccc2c(c1)ccc3ccccc32 |
Содержание
Свойства
Блестящие бесцветные кристаллы. tпл 101 °C, tkип 340 °C. Не растворяется в воде, растворяется в органических растворителях. Растворы фенантрена флуоресцируют голубым цветом.
Нахождение фенантрена в природе
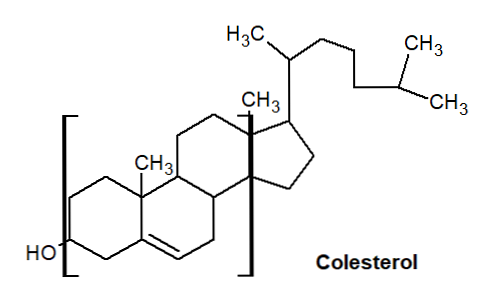
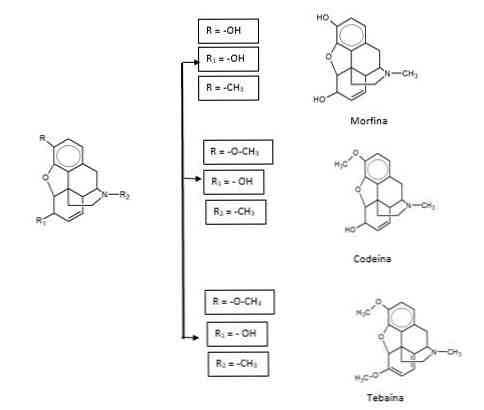
Содержится в каменноугольной смоле вместе со своим линейным изомером антраценом. Производные фенантрена широко распространены в живой природе (стероиды, алкалоиды группы морфина).
Применение
Фенантрен применяется при производстве красителей. Является стабилизатором взрывчатых веществ.
Влияние на здоровье
Имеется детальное исследование, направленное на выяснение механизмов, с помощью которых вещества, содержащиеся в сигаретном дыме, приводят к повреждениям структуры ДНК и (по мнению авторов) как следствие – к раку легких. Статья опубликована в журнале Chemical Research in Toxicology, одном из официальных изданий Американского Химического Общества (American Chemical Society).
Профессор Стивен С. Хехт (Stephen S. Hecht) и его коллеги, проводившие исследования, указывают, что ежедневно в мире от рака легких умирает 3000 человек, и в большинстве случаев причиной заболевания является курение. Также курение ассоциируется еще с 18 типами онкологических заболеваний.
Содержащиеся в сигаретном дыме полициклические ароматические углеводороды считаются главными виновниками рака легких, однако до настоящего времени было неясно, каким образом происходит повреждение ДНК в результате курения.
Исследователи добавили в сигареты меченый фенантрен и проследили его судьбу в организме 12 добровольцев. Обнаружилось, что, попав в кровь, фенантрен быстро превращается в токсичное вещество, разрушающее ДНК. Токсичное производное фенантрена появлялось в крови испытуемых всего 15-30 минут спустя после выкуривания сигареты. Такой быстрый эффект удивил даже исследователей – вдыхание сигаретного дыма было равноценно прямому введению фенантрена в кровь.
«Это исследование уникально, — говорит Хехт, — мы впервые показали, как курение напрямую влияет на метаболизм человека. Полученные нами результаты должны послужить предупреждением людям, которые хотят начать курить». [1]
Тем не менее, это исследование не доказывает, что именно фенантрен является фактором канцерогенеза табачного дыма: во-первых, механизм канцерогенеза через спонтанные химические повреждения ДНК никем не доказан, а во-вторых, при токсикологических испытаниях этого вещества на животных и при обследовании рабочих, контактирующих с ним, никаких данных о его канцерогенности не получено. У подопытных животных отмечены лишь лейкоцитоз и комплексная анемия, а у рабочих, занятых на его переработке — только лейкоцитоз.
Литература
Вредные вещества в промышленности. т.1 с. 136 — Л., «Химия», 1976.
Источник
Фенантрен Химическая структура, свойства и применение
фенантрена это углеводород (в его структуре углерод и водород), физико-химические свойства которого изучаются органической химией. Он относится к группе так называемых ароматических соединений, основной структурной единицей которых является бензол..
Ароматические соединения также включают конденсированные полициклические соединения, образованные несколькими ароматическими кольцами, которые имеют углерод-углеродную (С-С) связь. Фенантрен является одним из них, он имеет три конденсированных кольца в своей структуре. Он считается изомером антрацена, соединения, в котором три кольца конденсированы линейным образом..
Он был изолирован от антраценового масла из каменноугольной смолы. Его получают путем перегонки древесины, выбросов автотранспорта, разливов нефти и других источников..
Он попадает в окружающую среду через сигаретный дым и в стероидных молекулах образует ароматическую основу химической структуры, как показано в молекуле холестерина..
- 1 Химическая структура
- 2 Физические и химические свойства
- 3 использования
- 3.1 Фармакология
- 4 Влияние на здоровье
- 5 ссылок
Химическая структура
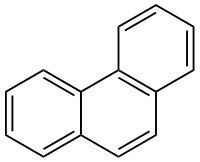
Фенантрен имеет химическую структуру, образованную тремя бензольными кольцами, слитыми вместе углерод-углеродной связью.
Это считается ароматической структурой, поскольку она соответствует закону Хюккле об ароматичности, который гласит: «Соединение является ароматическим, если оно имеет 4n + 2 пи (π) делокализованных и сопряженных (чередующихся) электронов с сигма-электронами (σ) простые ссылки.
При применении закона Хюккеля к структуре фенантрена и с учетом того, что n соответствует числу бензольных колец в структуре, оказывается, что 4n + 2 = 4 (3) +2 = 16 электронов π. Они рассматриваются как двойные связи в молекуле.
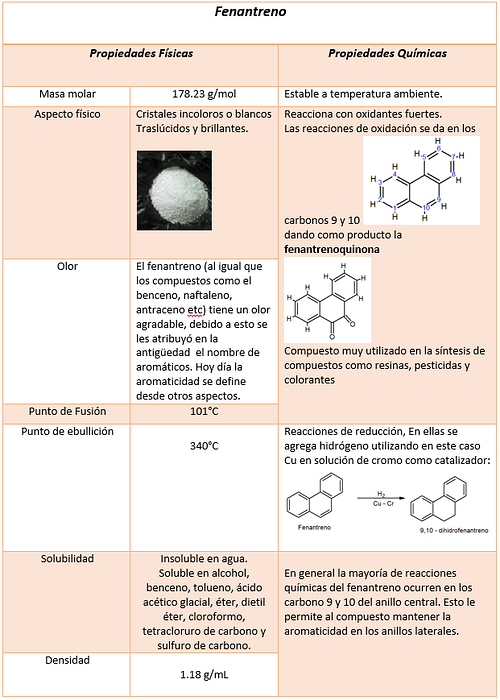
Физико-химические свойства
-Плотность 1180 кг / м3; 1,18 г / см3
-Температура плавления 489,15 К (216 ° С)
-Температура кипения 613,15 К (340 ° С)
Свойства соединения — это характеристики или качества, которые позволяют отличать его от других. Свойства, которые измеряются для соединения, это физические свойства и химические свойства..
Хотя фенантрен является изомерной формой антрацена, его свойства очень разные, что придает фенантрену большую химическую стабильность благодаря угловому положению одного из его ароматических колец..
приложений
фармакология
Опиоидные препараты могут быть природного происхождения или производными фенантрена. Среди них морфин, кодеин и тебаин.
Наиболее репрезентативные применения фенантрена получаются, когда он находится в окисленной форме; то есть как фенантренхинон. Таким образом, его можно использовать в качестве красителей, лекарств, смол, фунгицидов и для ингибирования полимеризации некоторых процессов. 9,10-бифенилдикарбоновая кислота используется для получения полиэфирной и алкидной смолы.
Влияние на здоровье
Не только фенантрен, но и все полициклические ароматические углеводороды, обычно известные как ПАУ, токсичны и вредны для здоровья. Они обнаруживаются в воде, на земле и в воздухе в результате сгорания, разливов нефти или как продукт реакций в промышленной сфере..
Токсичность возрастает по мере увеличения их цепей с конденсированными бензольными кольцами, хотя это не означает, что ПАУ с короткой цепью — нет..
Из бензола, который является фундаментальной структурной единицей этих соединений, уже известно его высокая токсичность и мутагенная активность у живых существ..
Нафталин, вызываемый против моли, используется в качестве средства борьбы с вредителями, которые нападают на ткани одежды. Антрацен — это микробицид, используемый в форме таблеток для противодействия запахам, вызываемым бактериями..
В случае фенантрена он накапливается в жировых тканях живых существ, создавая токсичность, когда человек подвергается воздействию загрязнителя в течение длительных периодов времени..
В дополнение к этим эффектам могут быть названы следующие:
— После длительных периодов воздействия фенантрена человек может кашлять, одышка, бронхит, раздражение дыхательных путей и раздражение кожи..
— При нагревании до разложения может вызвать раздражение кожи и дыхательных путей из-за выделения густого и удушающего дыма.
— Может реагировать с сильными окислителями.
— В случае пожара, связанного с этим соединением, его можно контролировать с помощью сухого диоксида углерода, галогенового огнетушителя или распыления воды.
— Хранить в прохладных местах, в герметичных контейнерах и вдали от окислителей..
— Необходимо носить средства индивидуальной защиты (MMP), закрытый ботинок, фартук с длинными рукавами и перчатки..
— По данным Национального института безопасности и гигиены труда, для работы с составом следует использовать полумаску, оснащенную противотуманными фильтрами и другим специальным фильтром для паров химических веществ..
— В случае раздражения глаз и / или кожи рекомендуется промыть большим количеством воды, снять загрязненную одежду или аксессуары и, в очень серьезных случаях, обратиться за медицинской помощью к пациенту..
Источник
ФЕНАНТРЕН
ФЕНАНТРЕН, мол. м. 178,2, бесцв. кристаллы; т. пл. 101 0 C, т. кип. 340 0 C; 
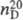
Ф енантрен по хим. св-вам аналогичен нафталину. Взаимод. с Cl 2 (в р-ре CS 2 или CCl 4 ) или Br 2 с образованием 9,10-дигалогенфенантренов. При натр, оба дигалогенфенантрена отщеп ляют HHaI, превращаясь в моногалогензамещенный фенантрен. Нитрование [HNO 3 , (CH 3 CO) 2 O и ледяная CH 3 COOH] приводит к смеси 9- (наиб, кол-во), 1-й 3-нитрофенантренов. Фенантрен легко сульфируется: в зависимости от т-ры в разл. соотношениях образуется смесь 2-, 3- и 9-фенантренсульфокислот с небольшой примесью 1-фенантренсульфокислоты. Взаимод. фенантрена с бензоилхлоридом в присут. AlCl 3 по р-ции Фриделя — Краф-тса приводит к смеси 1-, 2- и 3-бензоилфенантренов. В р-ции с малеиновым ангидридом образуется соед. ф-лы I:
Действием Na в амиловом спирте фенантрен восстанавливается до смеси 1,2,3,4-тетрагидрофенантрена (тетрантрена) и 9,10-ди-гидрофенантрена. Каталитич. гидрирование на смешанном катализаторе (CuO, Cr 2 O 3 и BaO) при 300-350 0 C приводит сначала к 1,2,3,4,5,6,7,8-октагидрофенантрену (октантрену), а затем к пергидрофенантрену. Окисление фенантрена соед. Сг(Ш) в ледяной CH 3 COOH приводит к фенантрен-9,10-хинону, оранжево-желтые кристаллы с т.пл. 208,5-210 0 C, дальнейшее окисление к-рого H 2 O 2 дает 2,2-дифеновую к-ту.
В природе встречаются многочисленные производные фенантрена, напр, алкалоиды группы морфина, нек-рые терпены.
Фенантрен обычно выделяют из ацетиленовой фракции кам.-уг. смолы. Синтезируют фенантрен фотоциклодегидрогенизацией стильбена или конденсацией о-нитробензальдегида с фенилуксусной к-той. Производные фенантрена обычно получают Пшорра синтезом.
Длит. контакт с фенантреном приводит к снижению содержания гемоглобина в крови и вызывает лейкоцитоз; ЛД 50 1,8-2,0 г/кг (мыши, перорально). ПДК 0,8 мг/м 3 .
Лит.: Клар Э., Полициклические углеводороды, пер. с англ., т. 1, M., 1971, с. 220-33; Общая органическая химия, пер. с англ., т. 1, M., 1981, с. 314-455; Ullmann’s Encyklopadie, 4 Aufl., Bd 14, Weinheim, 1977, S. 685-87.
Источник
Фенантрен синтезе лекарственных веществ
Изложенные выше принципы можно проиллюстрировать синтезом фенантрена из нафталина.
Используя подходы, описанные в предыдущем разделе, и планируя схему синтеза в обратном порядке (см. стр. 10), можно предположить, что удобнее всего исходить из нафталиноциклогексана.
Рассматривая далее стадию образования насыщенного кольца, необходимо иметь в виду, что при попытке нарастить целое кольцо в одну стадию могут встретиться значительные трудности (низкие выходы, сложное разделение продуктов реакции). Поэтому мы допускаем, что к нафталиновому ядру уже присоединена боковая цепь и что на свободном конце этой цепи имеется функциональная группа (для осуществления циклизации). Этим требованиям удовлетворяют две возможные структуры:
Отметим, что при циклизации обеих структур может быть получено нужное соединение
Из этих двух структур 

значительно ниже, чем скорость образования 

Впрочем, в этом случае выход требуемого изомера будет достаточно высоким, так как положение 


Теперь необходимо обсудить, какая функциональная группа должна быть на конце боковой цепи. Многие функциональные группы могут вступать в реакцию Фриделя — Крафтса. Для реакции циклизации можно использовать любую функциональную группу из ряда 

Рассмотрим далее присоединение боковой цепи к молекуле нафталина. Очевидно, необходим четырехуглеродный фрагмент с неразветвленной цепью углеродных атомов. Соответствующая молекула должна, по-видимому, содержать функциональные группы на обоих концах. В противном случае концевой атом углерода в боковой цепи полученного монозамещенного нафталина не будет содержать функциональной группы. Например:
Но в этом случае боковая цепь не может быть замкнута, и для получения подходящего для циклизации соединения потребуется дополнительная стадия
В связис этим лучше использовать легкодоступное бифункциональное соединение с четырехуглеродной цепью, такое, как янтарная кислота
В реакции Фриделя — Крафтса карбоновые кислоты выступают как реагенты менее электрофильные, чем
ангидриды. Следовательно, используем ангидрид янтарной кислоты.
И снова в этом синтезе возникает проблема изомеров. Известно, что нафталин реагирует с производными карбоновых кислот (как и с другими реагентами) как по 1-, так и по 



Теперь, чтобы получить боковую цепь подходящего типа, т. е. 
Далее следует стадия циклизации. Карбоновую кислоту можно превратить в галогенангидрид, а последний подвергнуть внутримолекулярной реакции Фриделя — Крафтса. Однако проще воспользоваться для циклизации имеющейся карбоксильной группой, т. е. осуществить вторую стадию синтеза (см. стр. 33):
Оставшуюся кетогруппу восстановим, как указано выше (стадия 4):
Полный синтез фенантрена теперь будет выглядеть так:
После того как студенты познакомились с общими методами, применяемыми для осуществления элементарных синтезов, необходимо привести некоторые общепринятые правила написания схем. Эти правила, большинство из которых уже применялось в этой главе, отличаются от требований по составлению уравнений реакций с коэффициентами.
Источник