- Новости
- Фармакокинетические исследования ЛС
- Биоаналитическая лаборатория «Клинфарм» совместно с клиническими и доклиническими базами планирует, организовывает и выполняет биоаналитическую часть:
- доклинических исследований фармакокинетики ЛС;
- клинических (I/IIa фазы) исследований фармакокинетики ЛС;
- “in vivo” исследований биоэквивалентности ЛС
- Регламент
- Фармакокинетические доклинические исследования препарата
- Новости
- Фармакокинетические исследования ЛС
- Биоаналитическая лаборатория «Клинфарм» совместно с клиническими и доклиническими базами планирует, организовывает и выполняет биоаналитическую часть:
- доклинических исследований фармакокинетики ЛС;
- клинических (I/IIa фазы) исследований фармакокинетики ЛС;
- “in vivo” исследований биоэквивалентности ЛС
- Фармакокинетические исследования лекарственных средств
Новости
тел./ факс
+380 (44) 390-73-72,
+380 (44) 390-73-71
Фармакокинетические исследования ЛС
Биоаналитическая лаборатория «Клинфарм» совместно с клиническими и доклиническими базами планирует, организовывает и выполняет биоаналитическую часть:
доклинических исследований фармакокинетики ЛС;
клинических (I/IIa фазы) исследований фармакокинетики ЛС;
“in vivo” исследований биоэквивалентности ЛС
1 Фармакокинетика — раздел фармакологии, изучающий пути поступления, распределения и метаболизм лекарственных веществ в организме, а также их выведение.
В фармакокинетике лекарственных препаратов выделяют четыре основных этапа:
- 1 этап — всасывание. Всасывание — это процесс проникновения лекарственного вещества через неповрежденные ткани организма в кровоток. Происходит со всех поверхностей человеческого тела, но особенно интенсивно из желудочно-кишечного тракта, из легких, с поверхности слизистых оболочек.
- 2 этап — распределение. Этот процесс зависит от сродства лекарства различным органам и тканям. Кроме того, в организме есть определенные барьеры, регулирующие проникновение веществ в органы и ткани. Особенно важными являются гематоэнцефалический (ГЭБ) и гематоплацентарный (ГПБ) барьеры. Для некоторых препаратов характерно также перераспределение. Эти лекарственные препараты, вначале накапливаясь в одной ткани, в последующем перемещаются в другой орган, являющийся мишенью для них.
- 3 этап — метаболизм (превращение). Это процесс, при котором активное лекарственное вещество подвергается превращениям и становится, как правило, биологически неактивным. Этот процесс идет во многих тканях, но в наибольшей степени — в печени.
- 4 этап — выведение. Основным органом выведения являются почки, однако лекарства могут выводиться и кишечником, легкими, потовыми и молочными железами.
- Элиминация — сумма всех процессов, связанных с метаболизмом и выведением лекарственного препарата, то есть прекращением его действия. Степень элиминации характеризуется периодом полужизни лекарственного вещества — это интервал времени, в течение которого концентрация активного лекарственного вещества в крови снижается в два раза.
2 Биоэквивалентность лекарственных средств
Биоэквивалентность – сравнительная оценка биодоступности двух препаратов.
Два лекарственных препарата биоэквивалентны, если они являются фармацевтически эквивалентными (содержат то же количество того же действующего вещества (тех же действующих веществ) в тех же лекарственных формах, которые соответствуют требованиям тех же или сравнимых стандартов) или фармацевтически альтернативными (содержат тот же активный компонент, но отличаются его химической формой (спирт, эфир и т. д.) или лекарственной формой, или силой действия) и если их биодоступности после введения в одной и той же молярной дозе сходны до такой степени, что действие этих препаратов в отношении эффективности и безопасности будет по сути одинаковым.
Изучение биоэквивалентности ЛС — один из видов клинических испытаний препаратов, цель которого – сравнительная оценка биодоступности двух препаратов для определения возможности их использования, как аналогичных.
См. Фармацевтическую энциклопедию и др.
Источник
Регламент
Фармакокинетические доклинические исследования препарата
Под фармакокинетикой подразумевают изучение пространственного и временного распространение лекарственных средств. Фармакокинетические исследования проводятся по двум основным причинам. Первая заключается в определении фармакокинетических параметров новых препаратов, которые могут быть полезны для пациентов. Этот процесс имеет важное значение для доклинических исследований лекарственных средств. Прежде чем приступить к клиническим исследованиям I и II фазы, необходимо понимание фармакокинетики в экспериментальных системах. Второй причиной для проведения фармакокинетических исследований является понимание дозозависимого эффекта.
Целью исследования фармакокинетики лекарственного средства является количественная характеристика процессов его всасывания, распределения и элиминации (метаболизм и экскреция).
В задачи фармакокинетических исследований лекарственных средств входит:
1. Обоснование выбора путей и методов его введения, выявление тканей, в которые наиболее интенсивно проникает и/или наиболее длительно удерживается то или иное фармакологическое средство, а также диагностирование путей элиминации.
2. Установление зависимости «концентрация-эффект», которая характеризуется меньшими видовыми различиями, чем зависимость «доза-эффект».
3. Изучение концентрации препарата в крови (плазме) с последующим выбором ориентировочной схемы дозирования.
4. Оптимизация лекарственной формы.
Точное описание фармакокинетики является жизненно важным для того, чтобы получить соответствующие выводы относительно поведения и полезности лекарственных средств.
Источник
Новости
тел./ факс
+380 (44) 390-73-72,
+380 (44) 390-73-71
Фармакокинетические исследования ЛС
Биоаналитическая лаборатория «Клинфарм» совместно с клиническими и доклиническими базами планирует, организовывает и выполняет биоаналитическую часть:
доклинических исследований фармакокинетики ЛС;
клинических (I/IIa фазы) исследований фармакокинетики ЛС;
“in vivo” исследований биоэквивалентности ЛС
1 Фармакокинетика — раздел фармакологии, изучающий пути поступления, распределения и метаболизм лекарственных веществ в организме, а также их выведение.
В фармакокинетике лекарственных препаратов выделяют четыре основных этапа:
- 1 этап — всасывание. Всасывание — это процесс проникновения лекарственного вещества через неповрежденные ткани организма в кровоток. Происходит со всех поверхностей человеческого тела, но особенно интенсивно из желудочно-кишечного тракта, из легких, с поверхности слизистых оболочек.
- 2 этап — распределение. Этот процесс зависит от сродства лекарства различным органам и тканям. Кроме того, в организме есть определенные барьеры, регулирующие проникновение веществ в органы и ткани. Особенно важными являются гематоэнцефалический (ГЭБ) и гематоплацентарный (ГПБ) барьеры. Для некоторых препаратов характерно также перераспределение. Эти лекарственные препараты, вначале накапливаясь в одной ткани, в последующем перемещаются в другой орган, являющийся мишенью для них.
- 3 этап — метаболизм (превращение). Это процесс, при котором активное лекарственное вещество подвергается превращениям и становится, как правило, биологически неактивным. Этот процесс идет во многих тканях, но в наибольшей степени — в печени.
- 4 этап — выведение. Основным органом выведения являются почки, однако лекарства могут выводиться и кишечником, легкими, потовыми и молочными железами.
- Элиминация — сумма всех процессов, связанных с метаболизмом и выведением лекарственного препарата, то есть прекращением его действия. Степень элиминации характеризуется периодом полужизни лекарственного вещества — это интервал времени, в течение которого концентрация активного лекарственного вещества в крови снижается в два раза.
2 Биоэквивалентность лекарственных средств
Биоэквивалентность – сравнительная оценка биодоступности двух препаратов.
Два лекарственных препарата биоэквивалентны, если они являются фармацевтически эквивалентными (содержат то же количество того же действующего вещества (тех же действующих веществ) в тех же лекарственных формах, которые соответствуют требованиям тех же или сравнимых стандартов) или фармацевтически альтернативными (содержат тот же активный компонент, но отличаются его химической формой (спирт, эфир и т. д.) или лекарственной формой, или силой действия) и если их биодоступности после введения в одной и той же молярной дозе сходны до такой степени, что действие этих препаратов в отношении эффективности и безопасности будет по сути одинаковым.
Изучение биоэквивалентности ЛС — один из видов клинических испытаний препаратов, цель которого – сравнительная оценка биодоступности двух препаратов для определения возможности их использования, как аналогичных.
См. Фармацевтическую энциклопедию и др.
Источник
Фармакокинетические исследования лекарственных средств
В 90-е годы снова началась эпидемия туберкулеза, и в настоящее время туберкулез представляет угрозу населению планеты не меньше, чем другие инфекционные заболевания. По данным Всемирной организации здравоохранения, жертвами туберкулеза ежегодно становятся около 1,7 миллионов. Происходит быстрое распространение его лекарственно-устойчивой формы [8, 9]. Процент больных туберкулезом детей составляет 12–35 % от общего числа. В Казахстане наиболее неблагополучна в этом отношении Павлодарская область, где отмечается самый высокий уровень заболеваемости детей [3].
Отсутствие детских противотуберкулезных лекарственных средств является глобальной проблемой, которая наиболее остро стоит в развивающихся станах. Во всем мире многие лекарственные средства для детей используются без соответствующих данных об их воздействии на организм ребенка и специального разрешения. Мировой фармацевтический рынок остро нуждается и в качественных, эффективных и безопасных противотуберкулезных лекарственных препаратах в специальных детских лекарственных формах [2].
В рамках решения этой проблемы на базе ООО «РОМАТ», Казахстан, разработан состав и технология детской лекарственной формы противотуберкулезного лекарственного средства РИЗЭФ-Д рифампицин/изониазид 60/30 мг, диспергируемые таблетки на основе молекулярно инкапсулированных действующих веществ с β-циклодекстрином. Очевидным преимуществом этой композиции стала установленная на этапе доклинических исследований уменьшенная более чем в 20 раз в сравнении с аналогами острая токсичность [3].
Создание любых дженериков предполагает проведение фармакокинетических исследований и оценку биоэквивалентности, являющуюся основным видом медико-биологического контроля дженериков [5].
Поэтому целью настоящего исследования явилось изучение фармакокинетики и относительной биодоступности лекарственного препарата РИЗЭФ-Д 60/30, таблетки диспергируемые (ТОО «Павлодарский фармацевтический завод», Республика Казахстан) в сравнении с препаратом рифампицин 60/изониазид 30 таблетки диспергируемые (Маклеодс Фармасьютикалс Лтд, Индия).
Материалы и методы исследования
Тестируемый лекарственный препарат производства ТОО «Павлодарский фармацевтический завод», Республика Казахстан, содержит комбинацию двух противотуберкулезных средств – рифампицина 60 мг и изониазида 30 мг.
В качестве препарата сравнения выбран аналог, не зарегистрированный в Республике Казахстан – таблетки рифампицин 60/изониазид 30, производства Маклеодс Фармасьютикалс Лтд, Индия, так как на фармацевтическом рынке Казахстана отсутствует аналог тестируемому лекарственному препарату по лекарственной форме и дозировке.
Исследования проводились на кроликах-самцах породы Шиншилла массой тела – 3,23 ± 0,39 кг, полученных из питомника ТОО НПП «Антиген» (г. Алматы).
Животным с помощью зонда внутрь вводили 1 таблетку лекарственного препарата РИЗЭФ-Д 60/30 таблетки диспергируемые или 1 таблетку лекарственного препарата рифампицин 60/изониазид 30 таблетки диспергируемые. Промежуточный период составил 7 дней, по истечении которого указанные лекарственные препараты вводили в обратном порядке.
Образцы крови (около 1,0 мл) отбирали из краевой ушной вены с помощью игл и переносили в центрифужные пробирки, предварительно обработанные гепарином. Взятие образцов крови для последующего определения содержания препарата в плазме крови осуществлялось в дискретные интервалы времени: через 0; 0,5; 1,0; 2,0; 3,0; 4,0; 6,0; 8,0; 12,0 и 24,0 часа после перорального введения препаратов. Образцы крови отстаивались в течение 15 минут в условиях комнатной температуры. После центрифугирования (3000 об/мин в течение 10 минут) отбирали плазму крови, которая хранилась при температуре –30° С в морозильной камере «Premium».
Для количественного определения рифампицина в плазме крови использовали хроматографический метод [4]. Анализ проводили на жидкостном хроматографе «Agilent 1100» с УФ-детектором и компьютером с соответствующим пакетом программ для обсчета хроматограмм. Условия хроматографирования: аналитическая колонка – «Zorbax Bonus-RP», Agilent (150´4,6 мм; 5 мкм); подвижная фаза 0,01 М раствор аммония фосфата двузамещенного – ацетонитрил (50:50), профильтрованная через мембранный фильтр с размером пор 0,45 мкм и дегазированная на ультразвуковой бане; скорость потока элюента – 1,0 мл/мин; детектирование при длине волны 215 нм; температура колонки + 35 °С.
Для экстракции рифампицина из плазмы крови в экстракционную пробирку, содержащую 1 мл плазмы крови, добавляли 5,0 мл смеси пентан:дихлорметан (1:1), встряхивали на шейкере и центрифугировали при 4000 об/мин в течение 10 минут. Супернатант переносили в выпарительную колбу. Органическую фракцию выпаривали досуха на роторном испарителе в токе азота. Сухой остаток растворяли в 250 мкл подвижной фазы и по 50 мкл аликвоты вводили в петлю инжектора.
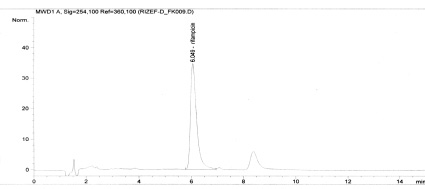
Процент извлечения рифампицина из плазмы крови составил в среднем 83,9 ± 7,5 %. Количественное определение рифампицина проводили методом абсолютной калибровки. Установлено, что в диапазоне концентраций 5–40 мкг/мл калибровочная кривая линейна. Стандартная кривая рифампицина описывалась уравнением y = 34,033x – 85,17 (R2 = 0,9997), где y – площадь хроматографического пика рифампицина; х – концентрация в мкг/мл (рис. 1–3). Минимальная обнаруживаемая концентрация составила 25 нг/мл. Относительная ошибка метода для концентрации 5 мкг/мл не превышала 29,76 %.
Рис. 1. Хроматограмма стандартного раствора рифампицина 20 мкг/мл
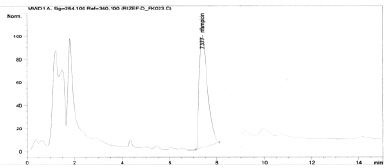
Рис. 2. Хроматограмма стандартного раствора рифампицина в плазме крови in vitro
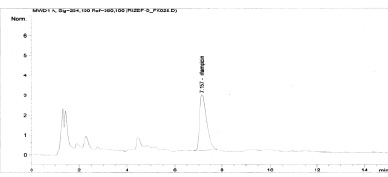
Рис. 3. Хроматограмма плазмы крови кролика через 0,5 ч после введения препарата РИЗЭФ-Д 60/30
Полученные данные предварительно были подвергнуты математической статистической обработке с помощью программы «Excel». Расчет фармакокинетических параметров анализируемых препаратов был проведен с использованием программы «ANOVA».
Результаты исследования и их обсуждение
На рис. 1 представлена хроматограмма стандартного раствора рифампицина с концентрацией 20 мкг/мл, на рис. 2 – хроматограмма плазмы крови кролика in vitro с концентрацией 40 мкг/мл, на рис. 3 – хроматограмма плазмы кролика через 0,5 часа после введения препарата РИЗЭФ-Д 60/30. Из хроматограмм видно, что время удерживания пика рифампицина лежит в пределах от 5,8 до 7,4 мин.
С целью оценки биологической доступности исследуемых лекарственных форм были определены концентрации рифампицина в сыворотке крови кроликов при применении препаратов, рассчитаны основные фармакокинетические параметры, позволяющие количественно охарактеризовать относительную биодоступность (f), величины площадей под фармакокинетическими кривыми зависимости «концентрация ‒ время» (AUC0-360), время достижения максимальной концентрации (Тmax) и значения максимальных концентраций (Сmax) [1, 6, 7].
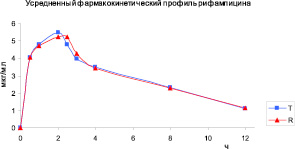
На рис. 4 представлен усредненный фармакокинетический профиль рифампицина после введения тестируемого и референс-препаратов.
Профили концентраций рифампицина тестируемого и референс-препаратов схожи. Фармакокинетические кривые рифампицина показывают, что исследуемое соединение определяется на протяжении 12 часов после однократного введения животным и испытуемого лекарственного препарата, и препарата сравнения.
В табл. 1 представлены фармакокинетические параметры рифампицина у кроликов после введения исследуемых лекарственных препаратов.
Рис. 4. Усредненный фармакокинетический профиль рифампицина в плазме крови кроликов после однократного перорального введения лекарственных препаратов
Индивидуальные и средние значения фармакокинетических параметров рифампицина тестируемого (Т) и референс-препаратов (R)
Источник