- Евросовет рекомендовал разрешить въезд привитым одобренными вакцинами туристам
- Европейский регулятор обновил список побочных эффектов вакцин от COVID-19
- Европейское агентство по лекарственным препаратам одобренные вакцины от коронавируса
- Препарат против Covid-19: зачем нужно лекарство, если есть вакцина? Эксперты говорят о двойном ударе по вирусу
- В ЕС одобрили применение вакцины Pfizer от коронавируса
- Какие вакцины от коронавируса используют в мире
Евросовет рекомендовал разрешить въезд привитым одобренными вакцинами туристам
Совет ЕС обновил рекомендации о въезде иностранных туристов в европейские страны в условиях пандемии коронавируса. Об этом говорится на сайте ведомства.
Согласно новой версии документа, основанием для въезда без дополнительных ограничений может быть прохождение полного курса вакцинации не позднее чем за две недели до поездки. При этом прививка должна быть сделана препаратом, одобренным Европейским лекарственным агентством (EMA) или Всемирной организацией здравоохранения (ВОЗ).
На сегодняшний день EMA одобрены вакцины компаний Pfizer/BioNTech, Moderna, AstraZeneca и Johnson & Johnson, ВОЗ — все перечисленные и китайская вакцина от Sinopharm. Разработанные в России препараты «Спутник V», «ЭпиВакКорона» и «КовиВак» в число одобренных на данный момент не входят. РФПИ сообщил, что подал заявление о регистрации препарата «Спутник V» в Евросоюзе в конце января, 4 марта Европейское агентство лекарственных средств (EMA) начало процедуру последовательной экспертизы регистрационного досье (rolling review) российской вакцины.
В соответствии с новыми рекомендациями страны ЕС также могут впускать туристов из государств, в которых число заражений коронавирусом за последние две недели не превышает 75 на 100 000 населения. При этом документ предусматривает механизм «экстренного торможения» — запрета на въезд из стран и регионов, где происходит резкий всплеск заболеваемости, в том числе из-за распространения новых штаммов COVID-19.
Рекомендация Евросовета не является юридически обязывающим документом, решения об открытии границ будут принимать правительства стран — участниц ЕС.
Накануне глава СВР России Сергей Нарышкин заявил, что EMA намеренно «тянет» с регистрацией российской вакцины от коронавируса, следуя «сигналами, которые поступают из высоких кабинетов ЕС». «Почему это происходит? В этом есть только лишь причины политического характера или еще присутствует экономический фактор? Не знаю, пусть в этом разбираются сами граждане европейских стран и правоохранительные органы, но мы понимаем, что это просто аморально», — сказал Нарышкин.
Источник
Европейский регулятор обновил список побочных эффектов вакцин от COVID-19
Европейское агентство по лекарственным средствам (EMA) опубликовало предварительные итоги исследований побочных эффектов вакцин от коронавируса. Проверку проходили четыре препарата, одобренные для применения в ЕС, — вакцины компаний Pfizer/BioNTech, Moderna, AstraZeneca и Johnson & Johnson. В числе побочных эффектов эксперты назвали заболевания сердца.
Исследованием занимался Комитет по безопасности EMA. В пресс-релизе упоминаются четыре вакцины: Comirnaty (от Pfizer/BioNTech), Spikevax (Moderna), Vaxzevria (AstraZeneca) и Janssen (Johnson & Johnson). Среди возможных побочных эффектов ЕМА называет:
- миокардит (воспаление сердечной мышцы) и перикардит (воспаление ткани, окружающей сердце) — эти побочные эффекты возможны от применения вакцин Comirnaty и Spikevax, но «в очень редких случаях» (в ЕС после 177 млн доз вакцины Pfizer/BioNTech было выявлено 145 случаев миокардита, 138 случаев перикардита; после 20 млн доз Moderna — по 19 случаев обоих заболеваний сердца);
- синдром капиллярной утечки (повышенная проницаемость капилляров, при которой плазма из сосудов может протечь в окружающие ткани) — от вакцины Janssen (этот побочных эффект выявили у трех привитых, двое умерли; по всему миру было получено более 18 млн вакцины);
- синдром Гийена—Барре (СГБ, аутоиммунное заболевание, вызывающее воспаление нервных окончаний, приводит к мышечной слабости и онемениям) — от вакцины Moderna (ЕМА пишет, что «нельзя исключить» возможную связь СГБ с вакцинацией);
- комбинация тромбоза (образование тромбов в сосудах) и тромбоцитопении (заболевание, при котором снижается уровень тромбоцитов или нарушается их выработка) — от вакцины Janssen (также встречается «очень редко»).
ЕМА одобрило применение вакцины Pfizer/BioNTech в декабре 2020 года, вакцины Moderna — в марте 2021 года. Всемирная организация здравоохранения (ВОЗ) разрешила применение вакцины Pfizer/BioNTech в декабре 2020 года, вакцины Moderna — в мае 2021 года. Американские врачи жаловались, что препарат Moderna может вызывать кожные воспаления и высыпания. В числе побочных эффектов вакцины Pfizer называли лихорадку и недомогания.
Как ВОЗ одобрила применение прививки против COVID-19 у подростков, читайте в материале “Ъ” «Вакцинации сбавляют возраст».
Источник
Европейское агентство по лекарственным препаратам одобренные вакцины от коронавируса
Еврокомиссия подписала рамочное соглашение о совместном приобретении препарата Covid-19. Покупать его будут у фармацевтической компании Eli Lilly. 18 стран ЕС приняли участие в совместной закупке 220 000 доз для лечения. В препарате используются так называемые моноклональные антитела.
Этот препарат используется для лечения пациентов с Covid, которым не нужно специального кислородного питания. Но он важен для пациентов, которые подвержены риску развития тяжелой формы коронавирусной болезни. Моноклональные антитела производятся в лаборатории и предназначены для нейтрализации вируса после заражения.
Европейское агентство по лекарственным средствам (EMA) в настоящее время рассматривает возможность утверждения «коктейля» из антител. Вопрос о том, входит ли Германия в число 18 стран-участниц, изначально оставался открытым. Комиссия ЕС уже подписала контракты на другие препараты.
Комиссия подписала рамочный договор о совместных закупках с фармацевтической компанией Eli Lilly на поставку препарата для лечения пациентов с коронавирусом с помощью моноклональных антител. Это новая разработка — в первом кейсе препаратов. Планируется появление пяти терапевтических средств.
Препарат против Covid-19: зачем нужно лекарство, если есть вакцина? Эксперты говорят о двойном ударе по вирусу
Стелла Кириакидес, комиссар по вопросам здравоохранения и безопасности пищевых продуктов, считает, что это хорошее решение. По ее словам, более 73% взрослого населения ЕС в настоящее время полностью вакцинировано. И этот показатель будет продолжать расти. Но вакцины не могут превратиться в единственный ответ на COVID-19. «Люди по-прежнему продолжают инфицироваться и болеть. Нам необходимо продолжать нашу работу по профилактике заболеваний с помощью вакцин и в то же время гарантировать, что мы сможем лечить болезнь с помощью терапевтических средств».
Эксперты говорят, что вакцинация — самый сильный ответ на вызов в виде коронавирусной пандемии. Но терапевтические средства помогают спасать жизни, ускоряют время восстановления. Также они сокращают продолжительность госпитализации и снижают давление на систему здравоохранения. А самое важное — в том, что они помогают восстановить силы пациенту, чтобы он быстро вернулся к нормальной жизни без сложного реабилитационного периода.
Источник
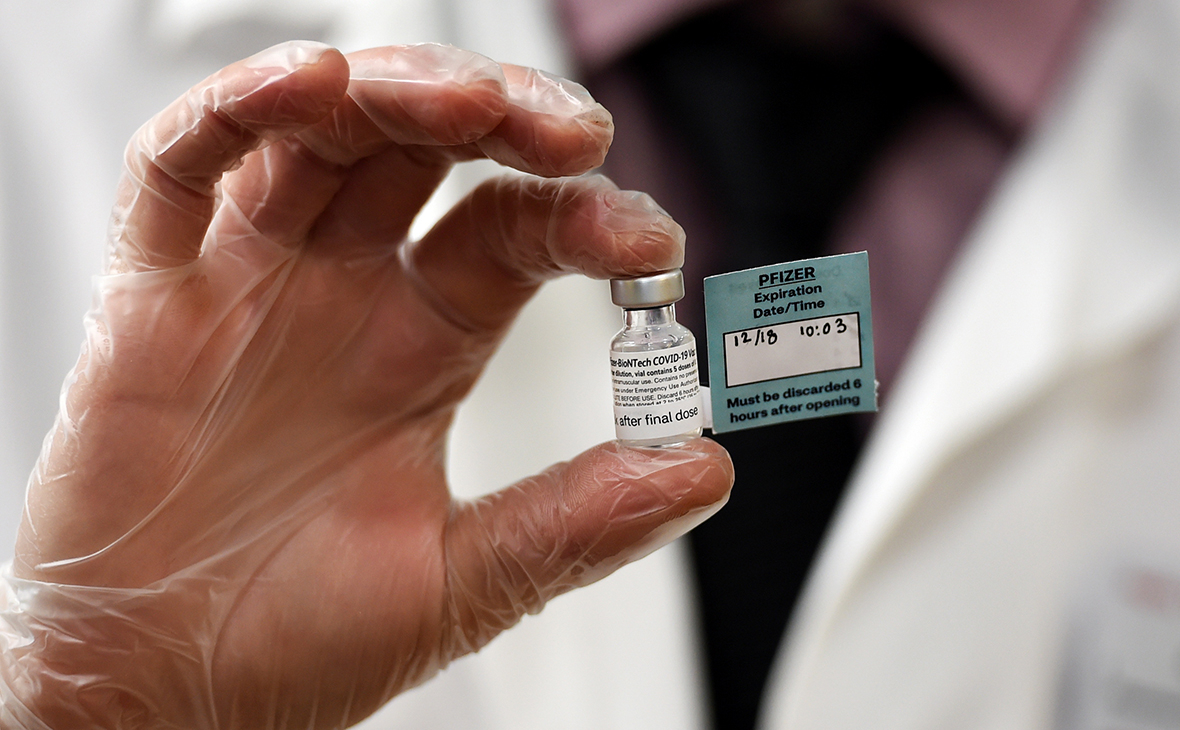
В ЕС одобрили применение вакцины Pfizer от коронавируса
Европейское агентство по лекарственным препаратам (EMA) одобрило применение на территории Евросоюза вакцины от коронавируса, разработанной американской Pfizer и немецкой BioNTech. Об этом говорится в сообщении регулятора.
Как заявили в EMA, препарат Comirnaty (BNT162b2) рекомендовано использовать для предотвращения заболевания COVID-19 у лиц старше 16 лет.
«Мы можем заверить граждан ЕС в безопасности и эффективности этой вакцины, а также в том, что она соответствует необходимым стандартам качества», — заявила исполнительный директор EMA Эмер Кук. Она добавила, что регулятор продолжит сбор и анализ данных о безопасности и эффективности препарата.
По словам главы Еврокомиссии Урсулы фон дер Ляйен, ЕК примет окончательное решение об использовании препарата к вечеру понедельника, 21 декабря.
В середине декабря вакцину разрешили использовать в США, в начале месяца — в Великобритании и Канаде.
Препарат BNT162b2 вводится двумя дозами с промежутком в три недели. По данным разработчиков, его эффективность достигает 95%. В Pfizer сообщили, что вакцина показывала высокую эффективность во всех группах добровольцев независимо от пола, возраста или расы. 17 декабря в США у медработницы зафиксировали сильную аллергическую реакцию после прививки, аналогичные случаи произошли в Великобритании. В Pfizer начали проверку.
Вакцина требует специальных транспортировки и хранения. Вплоть до разморозки она должна храниться при очень низкой температуре — не выше минус 70 градусов по Цельсию. Как отмечал Bloomberg, такие условия требуют создания дорогостоящей охлаждающей инфраструктуры, что может стать препятствием для продажи препарата даже в богатые страны.
Помимо BioNTech и Pfizer Евросоюз заключил контракты еще с пятью производителями: AstraZeneca, Sanofi-GSK, Johnson & Johnson, CureVac и Moderna. По словам фон дер Ляйен, вакцинация в ЕС начнется 27–29 декабря.
Источник
Какие вакцины от коронавируса используют в мире
В России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК
«Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре.
Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб.
5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран
Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря
Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцин вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз.
18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства
Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%.
У препарата есть два преимущества: его можно хранить при той же температуре, которую позволяет создать обычный холодильник, а его стоимость составляет $4–5. Вводится два раза с интервалом в 4–12 недель.
Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко.
В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах.
В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca.
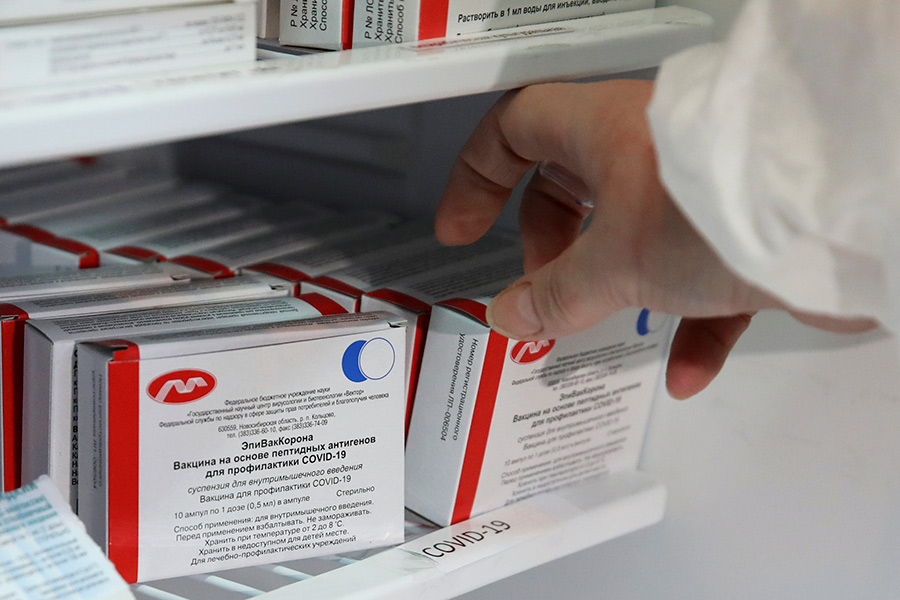
Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний.
Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб.
Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной»
Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая.
Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно.
Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac
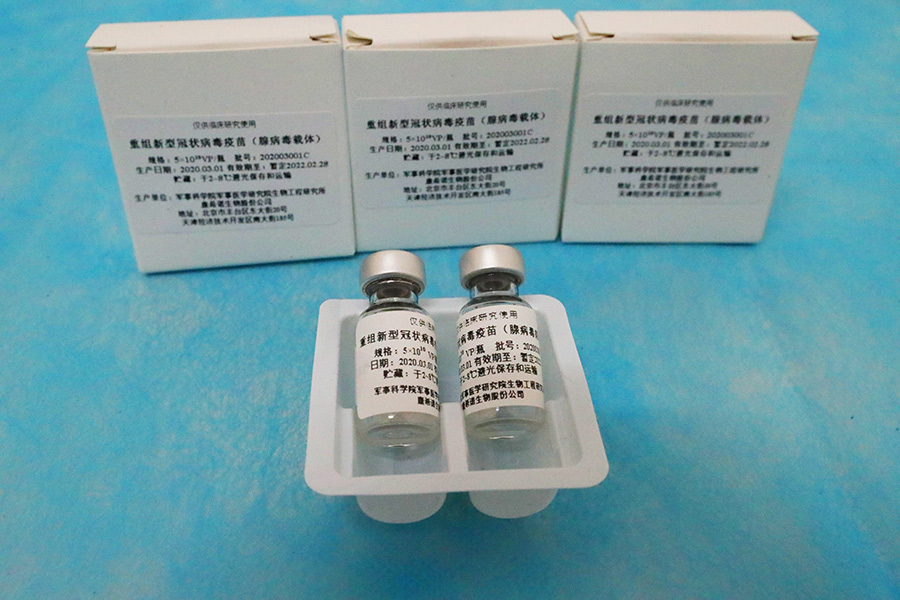
Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия.
В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России.
Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года
Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели.
30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине.
В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования
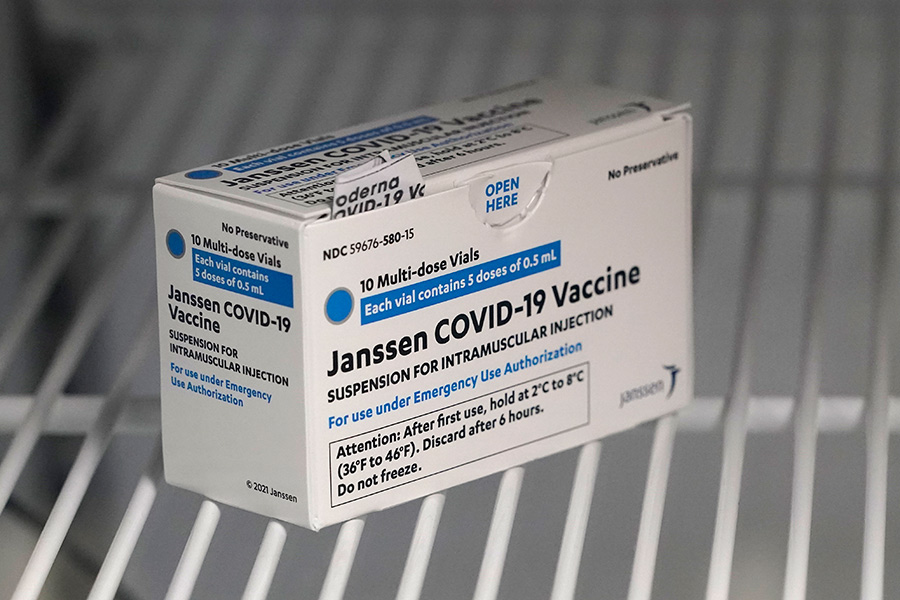
Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ.
В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%.
Вакцина Janssen хранится при температуре -20 градусов по Цельсию. Но у нее есть особенность — на протяжении трех месяцев она может находиться в условиях от 2 до 8 градусов по Цельсию. Главное преимущество — однодозное введение.
Источник