- Иностранная пресса о России и не только
- Лиза Барнеу | Le Monde
- Что говорится о вакцинах от Covid-19 в документах, похищенных у Европейского агентства лекарственных средств
- Европейское агентство лекарственных средств вакцины от covid
- Препарат против Covid-19: зачем нужно лекарство, если есть вакцина? Эксперты говорят о двойном ударе по вирусу
- Какие вакцины от коронавируса используют в мире
Иностранная пресса о России и не только
|
 |
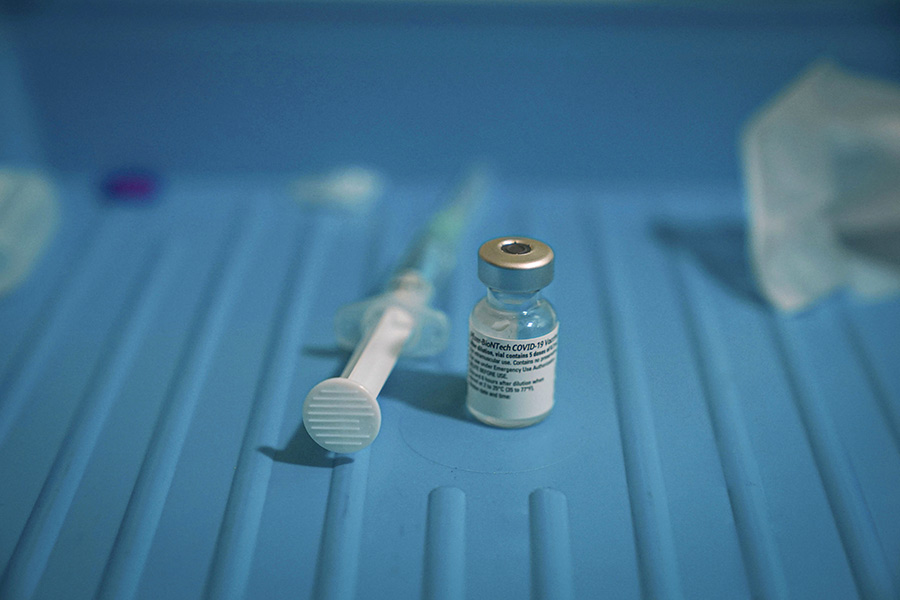
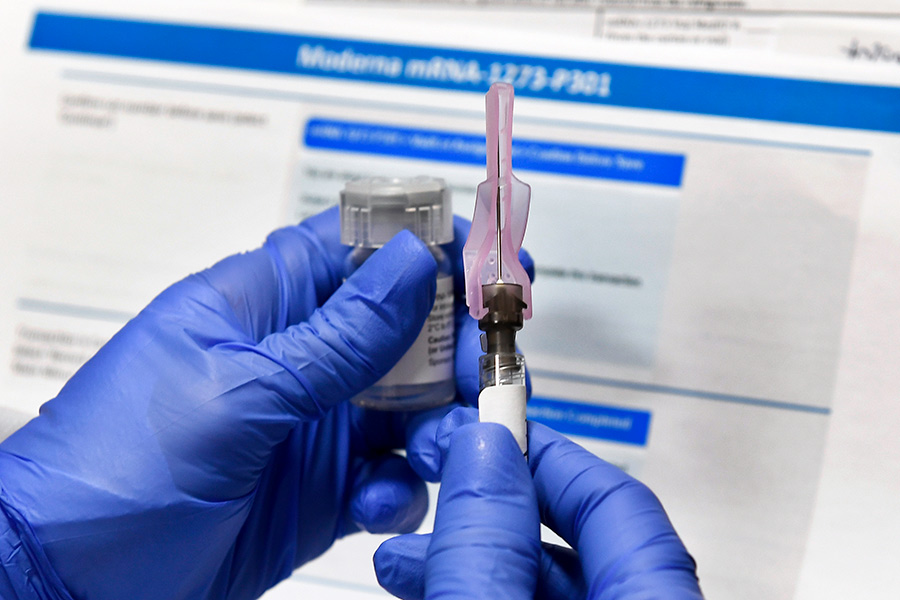
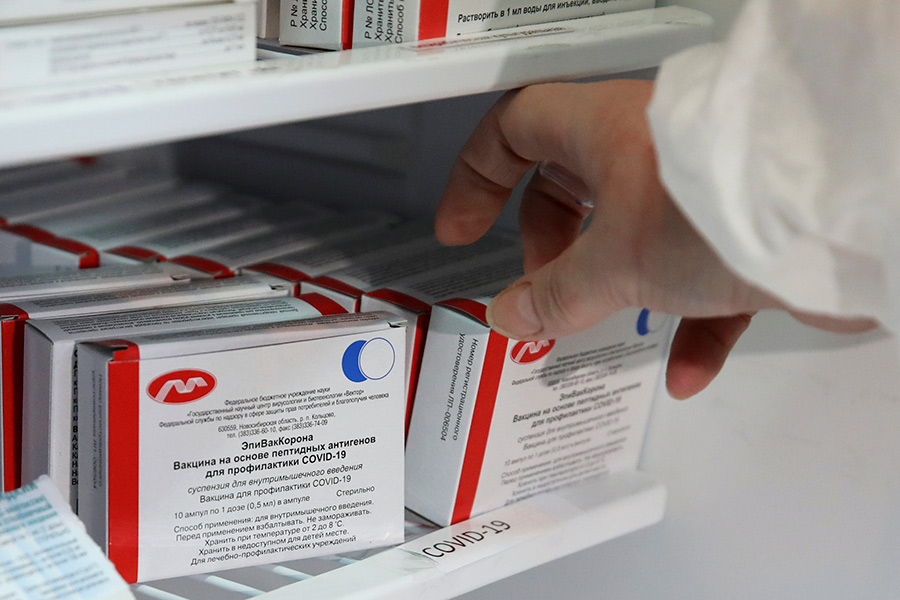
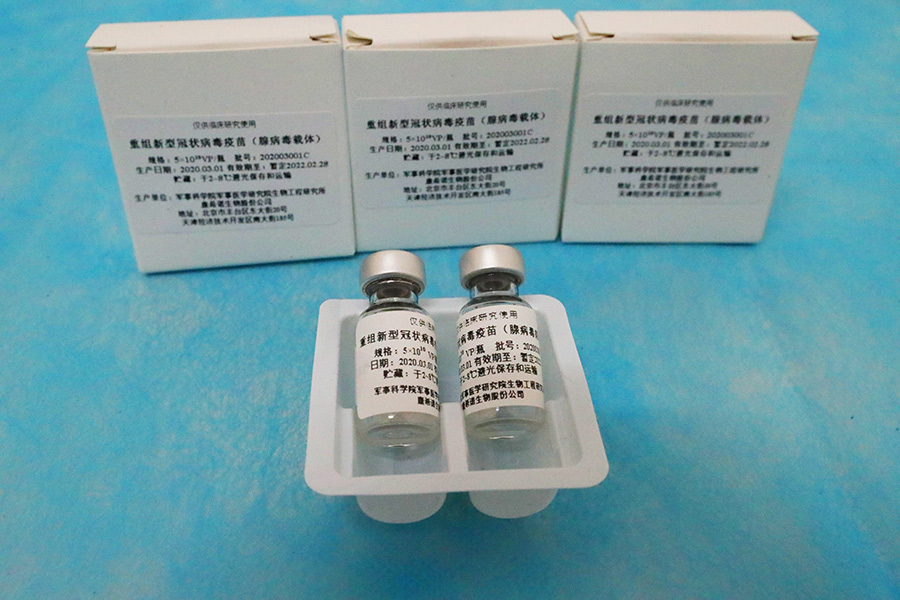
Лиза Барнеу | Le MondeЧто говорится о вакцинах от Covid-19 в документах, похищенных у Европейского агентства лекарственных средств«Украденные данные, которые затем были опубликованы в даркнете, свидетельствуют о давлении, которому подвергалось Европейское агентство лекарственных средств, чтобы как можно скорее одобрить вакцину Pfizer-BioNTech», — пишет Le Monde в статье, опубликованной в выходные. «Конфиденциальные документы, украденные с серверов Европейского агентства лекарственных средств (EMA) 9 декабря 2020 года, снова появились в даркнете. Le Monde удалось найти некоторые из них, и европейская команда журналистов тщательно их просмотрела. Набор включает около 20 наименований, в основном, это досье для оценки вакцины Pfizer-BioNTech. Он также включает в себя 19 электронных писем, которыми с 10 по 25 ноября обменивались различные должностные лица агентства, некоторые из которых якобы подверглись «манипуляциям» со стороны хакеров, как предупреждает EMA в заявлении, сделанном в пятницу, 15 января. Однако в беседе с Le Monde агентство признало, что «просочившиеся электронные письма действительно отражают возникшие проблемы и дискуссии». «Среди электронных писем есть такие, которые выглядят должным образом, на них видны даты и получатели, поэтому априори менее вероятно, что они стали предметом манипуляций, пять писем позволяют нам указать на давление, с которым столкнулось агентство, чтобы одобрить первую вакцину от Covid-19 как можно быстрее. В беседе от 12 ноября официальный представитель EMA указывает, например, на дискуссию с комиссаром ЕС по здравоохранению Стеллой Кириакидес. Она настаивала на том, «чтобы все государства-члены ЕС получили вакцину одновременно», и подчеркивала важность того, чтобы не «заставлять» их применять национальные процедуры, так как это может привести к задержкам в процессе официального утверждения препарата. Согласно директиве ЕС, в случае эпидемии, государства могут использовать препараты, не разрешенные EMA», — говорится в статье. «(. ) В центре внимания других документов, украденных в декабре 2020 года и не подозреваемых в манипуляциях со стороны EMA, находятся некоторые «проблемы». И, в частности, проблемы с вакциной Pfizer-BioNTech. Таким образом, мы обнаруживаем, что в ноябре европейское агентство сформулировало три «основных возражения» против этой вакцины: отдельные производственные площадки еще не были одобрены; данные о коммерческих партиях вакцин по-прежнему отсутствовали; и, самое важное, имеющиеся данные выявили качественные различия между коммерческими партиями и партиями, использованными в клинических испытаниях. Именно по этому последнему пункту исследователи, занимающиеся оценкой качества вакцины, проявили наибольшую озабоченность», — передает автор статьи Лиза Барнеу. «На самом деле, чтобы перейти от клинической стадии к коммерческой, производителям пришлось изменить свои производственные процессы, они также инвестировали средства в новые производственные линии и новые фабрики. Такими изменениями можно объяснить различия в точном составе вакцин, в частности, снижение уровня целостности РНК. Это ключевой элемент этой вакцины, которая после введения в клетки позволяет производить спайк-белок вируса и таким образом научить иммунную систему распознавать этот патоген и нейтрализовать его. Целостность вакцины, используемой в клинических испытаниях, составляла от 69% до 81% РНК, то ексть это была полная цепочка для формирования спайк-белка. Зато данные о партиях, произведенных на этих новых производственных линиях, показывали более низкий процент, в среднем 59%, — указывает журналистка. — Некоторые партии даже опустились до 51% и 52%. Это стало «камнем преткновения», — заявило EMA 23 ноября. «Возникает вопрос, способна ли более низкая доля РНК повлиять не только на эффективность вакцинации, но и на ее безопасность, потому что более низкий уровень целостности РНК может означать более количество примесей, особенно в виде усеченных РНК. «В этих продуктах мы часто имели дело с немного более короткими или немного более длинными РНК. Мы фильтруем их по размеру молекулы, но эту фильтрацию сложно проводить в больших масштабах», — комментирует Стив Пасколо, исследователь университетской больницы Цюриха, который работал над РНК-вакцинами в течение двадцати лет (став соучредителем CureVac в 2000 году, он покинул эту компанию, и теперь у него есть общие проекты с BioNTech). Очевидно, что эти усеченные РНК больше не могут способствовать формированию спайк-белка. Однако данные, предоставленные производителем в EMA, показывают, что уже при уровне РНК в 62% белок по-прежнему производится в нужном количестве. «В начальных испытаниях BioNTech у них возникал иммунный ответ всего с одним микрограммом РНК», — отмечает Стив Пасколо. В вакцине предполагается 30 мкг, так что у них есть запас». «(. ) Был получен снимок экрана с изображением электронного письма, полученного 30 ноября между EMA и производителями: «Эти проблемы считаются критическими, особенно в контексте новизны этого типа продуктов и ограниченного опыта. поэтому ожидается более строгая стратегия контроля». Однако из одного из последних доступных докладов мы узнаем, что корректировка производственных процессов позволяет восстановить уровень целостности до 75%, что сопоставимо с партиями, использовавшимися в клинических испытаниях», — пишет Le Monde. «Три дня спустя, 3 декабря, газета The Wall Street Journal опубликовала статью о проблеме с производством вакцины Pfizer. «Некоторые из первых партий сырья не соответствовали стандартам. Мы решили проблему, но у нас не хватило времени, чтобы осуществить поставки, запланированные на этот год», — объясняет «человек, принимавший непосредственное участие в разработке вакцины Pfizer». «(. ) В ответ на запрос EMA подтвердило, что проблема качества была впоследствии решена: «Компания смогла решить эти проблемы и предоставить информацию и данные, необходимые для того, чтобы позволить EMA перейти к положительному решению по этой вакцине». Агентство также указывает, что текущие технические требования в отношении уровня РНК «считаются научно обоснованными и приемлемыми». Например, маловероятно, отмечает агентство, что эти усеченные молекулы РНК могут способствовать формированию белка или пептида и, таким образом, вызывать нежелательные эффекты. «Несмотря на срочность, в ЕС всегда существовал консенсус о том, чтобы не ставить под угрозу высокие стандарты качества и основывать любые рекомендации на силе научных доказательств, безопасности, качества и эффективности вакцины», — настаивает EMA. «(. ) Остается узнать, кто мог стоять за этой кибератакой. Украденные данные появились на Rutor: «Ru» означает Россия (Russie) и «tor» — это браузер для анонимного просмотра веб-страниц. Что могло бы подтвердить идею о российском или русофильском хакере, пользующемся поддержкой государства. «Такая хакерская тактика с кражей данных с последующей утечкой уже практикуется российскими агентами (достаточно вспомнить Guccifer 2.0 или дело Всемирного антидопингового агентства)», — поясняет Жан-Мишель Доан, специалист по киберпреступности в Sekoia, компании, занимающейся информационной безопасностью. Трудно исключить и промышленный кибершпионаж, тем более, что, по всей видимости, была сделана подборка документов, специально нацеленных на Pfizer. Об этом свидетельствует и название этого файла: «Доказательство большого мошенничества с данными о вакцинах Pfizer (. )!» А как насчет группы антипрививочников, стремящихся дискредитировать вакцины? «Маловероятно, что хакер-антипрививочник опубликует данные на малоизвестном сайте, специализирующемся на взломах», — комментирует Жан-Мишель Доан. «Независимо от интерпретации этих документов, факты таковы: вакцина Pfizer-BioNTech была окончательно одобрена 21 декабря 2020 года со стороны EMA, через три недели после Великобритании и через две недели после США, это показывает, что Европейскому агентству, тем не менее, потребовалось некоторое время, чтобы решить возникшую проблему качества, прежде чем дать свое разрешение», — резюмирует Le Monde. Источник Европейское агентство лекарственных средств вакцины от covidЕврокомиссия подписала рамочное соглашение о совместном приобретении препарата Covid-19. Покупать его будут у фармацевтической компании Eli Lilly. 18 стран ЕС приняли участие в совместной закупке 220 000 доз для лечения. В препарате используются так называемые моноклональные антитела. Этот препарат используется для лечения пациентов с Covid, которым не нужно специального кислородного питания. Но он важен для пациентов, которые подвержены риску развития тяжелой формы коронавирусной болезни. Моноклональные антитела производятся в лаборатории и предназначены для нейтрализации вируса после заражения. Европейское агентство по лекарственным средствам (EMA) в настоящее время рассматривает возможность утверждения «коктейля» из антител. Вопрос о том, входит ли Германия в число 18 стран-участниц, изначально оставался открытым. Комиссия ЕС уже подписала контракты на другие препараты. Комиссия подписала рамочный договор о совместных закупках с фармацевтической компанией Eli Lilly на поставку препарата для лечения пациентов с коронавирусом с помощью моноклональных антител. Это новая разработка — в первом кейсе препаратов. Планируется появление пяти терапевтических средств. Препарат против Covid-19: зачем нужно лекарство, если есть вакцина? Эксперты говорят о двойном ударе по вирусуСтелла Кириакидес, комиссар по вопросам здравоохранения и безопасности пищевых продуктов, считает, что это хорошее решение. По ее словам, более 73% взрослого населения ЕС в настоящее время полностью вакцинировано. И этот показатель будет продолжать расти. Но вакцины не могут превратиться в единственный ответ на COVID-19. «Люди по-прежнему продолжают инфицироваться и болеть. Нам необходимо продолжать нашу работу по профилактике заболеваний с помощью вакцин и в то же время гарантировать, что мы сможем лечить болезнь с помощью терапевтических средств». Эксперты говорят, что вакцинация — самый сильный ответ на вызов в виде коронавирусной пандемии. Но терапевтические средства помогают спасать жизни, ускоряют время восстановления. Также они сокращают продолжительность госпитализации и снижают давление на систему здравоохранения. А самое важное — в том, что они помогают восстановить силы пациенту, чтобы он быстро вернулся к нормальной жизни без сложного реабилитационного периода. Источник Какие вакцины от коронавируса используют в миреВ России массовая вакцинация от COVID-19 началась 18 января. В мире на конец марта прививают население уже в 141 стране. Какие вакцины используют — в обзоре РБК «Спутник V», разработанная Центром эпидемиологии и микробиологии имени Н.Ф. Гамалеи, получила госрегистрацию Минздрава в августе. Вакцину зарегистрировали после второй фазы испытаний, а третий финальный этап стартовал в сентябре. Эффективность «Спутника V» разработчики оценили выше, чем в 95%. Эти данные были получены при исследовании добровольцев, получивших две инъекции препарата. «Спутник V» разработан в двух видах: замороженном (жидкая «Гам-КОВИД-Вак» хранится при температуре не выше минус 18 °С) и лиофилизированном (порошок «Гам-КОВИД-Вак-Лио» хранится при температуре от плюс 2 до 8 °С). Препарат вводится двукратно с интервалом в три недели. В ФАС заявили, что стоимость инъекции «Спутником V» не превысит 1 тыс. руб. 5 декабря Москва стала первым российским регионом, начавшим масштабную вакцинацию «Спутником V», а с 18 января началась массовая вакцинация во всей России. Первой среди зарубежных стран, зарегистрировавших российский препарат, стала Белоруссия. Такое же решение приняли власти Аргентины, Венесуэлы и некоторых других стран Немецкая компания BioNtech разработала вакцину совместно с американской Pfizer. На третьей фазе клинических испытаний препарат показал эффективность на уровне 95%. У вакцины есть обязательное условие использования: ее нужно хранить при температуре не выше минус 70 градусов Цельсия, а после разморозки она пригодна в течение пяти дней. Разработка Pfizer-BioNTech вводится в два приема с промежутком в три недели. Великобритания стала первой страной, одобрившей применение Pfizer и BioNTech, за ней последовали Канада, США и страны Европы и Ближнего Востока. Массовая вакцинация в США и Канаде началась 14 декабря, а в европейских странах — 27 декабря Эффективность вакцины американской фармацевтической компании Moderna составила 94,5%, а при тяжелых случаях заболевания — 100%. Вакцин вводят в два приема с интервалом в четыре недели. Препарат можно до 30 дней хранить при 2–8 градусах Цельсия. В этом году Moderna планирует выпустить 600 млн доз. 18 декабря США одобрили использование Moderna и заказали 200 млн доз с возможностью покупки еще 300 млн. Следом разрешение на использование она получила в Канаде, Израиле, Великобритании и Швейцарии. 6 января Европейский регулятор одобрил препарат американского производства Вакцина, разработанная британской компанией AstraZeneca вместе с Оксфордским университетом, показала эффективность на уровне 70%, а при одном из способов введения (сначала вводят половину дозы, а через месяц — полную) — 90%. У препарата есть два преимущества: его можно хранить при той же температуре, которую позволяет создать обычный холодильник, а его стоимость составляет $4–5. Вводится два раза с интервалом в 4–12 недель. Великобритания первой в мире разрешила использовать AstraZeneca и заказала 100 млн доз. Препарат получил разрешение на использование в Индии, Аргентине, Доминиканской Республике, Сальвадоре, Мексике и Марокко. В марте 2021 года вокруг препарата AstraZeneca разразился скандал. Более 15 стран Европы, в том числе Германия, Франция, Испания, и некоторые страны Азии и Африки частично или полностью отказались от препарата. Такое решение власти приняли на фоне сообщений об образовании тромбов у привившихся и смертельных исходах. В самой компании указывают на отсутствие доказательств, что к смерти пациентов привела именно вакцинация. 18 марта вышло заключение Европейского агентства лекарственных средств (EMA) о том, что AstraZeneca не увеличивает риски по образованию тромбов. ВОЗ также продолжает рекомендовать использование препарата. После этих заявлений европейские страны, кроме некоторых скандинавских, возобновили иммунизацию AstraZeneca. Пептидная вакцина новосибирского научного центра «Вектор» «ЭпиВакКорона» получила регистрационное удостоверение в октябре 2020 года. Она, как и «Спутник V», была зарегистрирована после двух стадий клинических испытаний. Вакцину вводят двукратно внутримышечно с интервалом в две-три недели. Препарат можно хранить при температуре от 2 до 8 градусов выше нуля. В Роспотребнадзоре отмечают, что вакцина подходит для пожилых и людей с хроническими заболеваниями. В центре «Вектор» заявили, что стоимость препарата будет эквивалента стоимости «Спутника V», то есть около 1 тыс. руб. Глава Роспотребнадзора Анна Попова сообщала, что «ЭпиВакКорона» поступила в гражданский оборот в пяти городах — Москве, Санкт-Петербурге, Ростове-на-Дону, Туле и Новосибирске. После завершения пострегистрационных клинических испытаний в 2021 году может начаться массовая вакцинация «ЭпиВакКороной» Инактивированная вакцина CoronaVac, разработанная китайской Sinovac Biotech, хранится в холодильнике при плюс 2–8 градусах Цельсия. В Sinovac заявили, что обеспечат производство 300 млн доз в год. Для иммунизации требуется две дозы, а это означает, что CoronaVac смогут привиться 150 млн человек — чуть больше десятой части населения Китая. Данные об эффективности вакцины от Sinovac разнятся. Последние испытания в Бразилии показали 50,4% эффективности, а в Индонезии и Турции — 65,3% и 91,5% соответственно. Вакцина была одобрена для экстренного применения в группах высокого риска в Китае с июля. Использование этой вакцины 13 января разрешили власти Турции. Несколько азиатских стран — Сингапур, Малайзия и Филиппины, а также Бразилия и Украина подписали соглашения о закупках CoronaVac Еще одна китайская вакцина Ad5-nCoV («Конвидеция»), на основе человеческого аденовируса типа 5, разработана фармкомпанией CanSino Biologics. Преимуществом этого препарата является однократное введение, а также возможность хранения при температуре от плюс 2 до плюс 8 градусов Цельсия. В ноябре 2020 года были поданы документы в Минздрав России для регистрации вакцины. В декабре Минздрав выдал разрешение на проведение третьего международного этапа клинического исследования Ad5-nCov. В случае, если вакцина покажет высокую эффективность и безопасность, CanSino Biologics с российским «Петроваксом» организуют ее производство в России. Согласно промежуточным результатам третьей фазы клинических испытаний в России, Ad5-nCoV показала эффективность в 92,5%. Окончательные результаты исследования появятся в середине 2021 года Другую китайскую инактивированную вакцину разработала China National Biotec Group (CNBG) (подразделение Sinopharm). Она не требует отрицательной температуры хранения и вводится двумя дозами с интервалом в две недели. 30 декабря Sinopharm объявила, что на третьем этапе испытаний препарат показал эффективность на 79%. Однако Объединенные Арабские Эмираты, которые одобрили вакцину Sinopharm в этом месяце, заявили, что эффективность вакцины составила 86%. Кроме Китая и ОАЭ вакцина Sinopharm проходит клинические испытания в Бахрейне, Иордании, Перу и Аргентине. В Китае препарат Sinopharm с июля используется в рамках программы по экстренному вакцинированию, а 31 декабря Государственное управление по лекарственным средствам Китая одобрило препарат для широкого использования Вакцину Janssen американской корпорации Johnson & Johnson 11 марта одобрил ЕС. Чуть раньше экстренное применение препарата разрешило Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Препарат также включен в список для экстренного применения ВОЗ. В ходе клинических испытаний с участием 44 тыс. человек из США, Южной Африки и стран Латинской Америки препарат показал эффективность в 67%. Вакцина Janssen хранится при температуре -20 градусов по Цельсию. Но у нее есть особенность — на протяжении трех месяцев она может находиться в условиях от 2 до 8 градусов по Цельсию. Главное преимущество — однодозное введение. Источник |