- Как убрать возрастные пигментные пятна
- Возрастные пигментные пятна
- Старческое лентиго
- Себорейный кератоз
- Как убрать возрастные пигментные пятна на лице
- Почему ретиноиды
- Как работают ретиноиды
- Правила применения ретиноидов
- Осветляющая сыворотка «Брайтинг» DermaQuest
- Обновляющий крем с Ретинальдегидом DermaQuest
- Клинический случай нефропатии обусловленной приемом репешка обыкновенного (agrimonia eupatoria)
Как убрать возрастные пигментные пятна
Почему к 55-60 годам на коже появляются пигментные пятна и какими они бывают? Опасны ли они, и как избавиться от возрастных пигментных пятен? Здесь подробный разбор ответов на эти вопросы и разбор основных средств для борьбы с пигментными пятнами.
При появлении пигментных пятен на коже, возникает масса вопросов и волнений, связанных не только с внешней непривлекательностью, но и опасения о возможности их перерождения в недоброкачественные образования. Бежать к врачу, к косметологу или есть средства, которые уберут пигментацию при самостоятельном применении? Ответы читайте ниже.
Возрастные пигментные пятна
После 55 – 60 лет на лице часто появляются непривлекательные пятна, которые у многих вызывают огорчения и опасения.
- Придают неухоженный вид
- Акцентируют возраст
- Вызывают онко-настороженность или боязнь развития рака
Возрастная пигментация бывает 2-х видов: себорейный кератоз и старческое лентиго.
Старческое лентиго
Возникает в период гормональных возрастных изменений, причина – снижение вырабатываемых организмом половых гормонов.
Клиническая картина: плоские коричневые пятна с размытыми границами, что говорит о достаточной глубине их залегания. Размер пятен может быть разным и достигает до 1 см в диамерте.
Себорейный кератоз
Образуется на участках с повышенным количеством сальных желез, т.е. на себорейных зонах.
Клиническая картина: пятна коричневого и темно-коричневого цвета, отличительные особенности — возвышаются над поверхностью кожи, сами пятна имеют жирную поверхность, покрыты роговыми чешуйками.
Высыпания имеют характерную локализацию — это себорейные участки кожи — спина, грудь и лицо (преимущественно Т-зона).
Пятна доброкачественные, но необходимо проявлять онко-настороженность, до 20% вероятности их озлокачествления.
Как убрать возрастные пигментные пятна на лице
Себорейный кератоз
Из-за существующей вероятности озлокачествления необходима консультация онколога или дерматолога-онколога о возможности удаления образований.
Способ коррекции – хирургическое удаление.
Старческое лентиго
Коррекция возможна путем назначения косметических препаратов – схема терапии соответствует классическому избавлению от пигментации и включает в себя 3 пункта:
- Отшелушивающие средства
- Осветляющие препараты
- Антиоксиданты
Профилактикой повторного появления лентиго является регулярное нанесение на кожу солнцезащитных средств с SPF и препаратов с антиоксидантами, т.к. присутствует несостоятельность собственной антиоксидантной системы защиты кожи.
После консультации дерматолога назначаются осветляющие препараты и предпочтительными признаны ретиноиды.
Почему ретиноиды
Для эффективного осветления кожи от возрастных пигментных пятен необходимы все те же три группы средств: осветляющие субстанции – снижающие выработку меланина, антиоксиданты – снижают количество свободных радикалов, провоцирующих гиперпродукцию меланина и отшелушивающие – ускоряют клеточное обновление и удаляют окрашенные клетки с поверхности кожи.
ВАЖНО! Ретиноиды участвуют в активации генов, ответственных за подавление роста опухоли.
Поэтому некоторые ретиноиды применяются как местный вспомогательный препарат при терапии кожных проявлений онкозаболеваний. Таким образом, применение ретиноидов – это профилактика перерождения возрастных новообразований.
Как работают ретиноиды
Ретиноиды – группа субстанций-производных витамина А, используемая дерматологами и косметологами по ряду показаний. Благодаря физиологическому воздействию на кожу, эффективно омолаживают, устраняют акне и осветляют кожу.
- Ингибируют тирозиназу
- Тормозят транспорт пигмента в коже — процесс передачи меланина внутрь пигментных клеток меланоцитов
- Нормализуют клеточное обновление и стимулируют своевременное отшелушивание с поверхности кожи пигментированных роговых чешуек.
- Активируют кератогенез – появление на поверхности кожи клеток с нормальным, генетически запрограммированным количеством пигмента, т.е. нормально окрашенных.
- Работают проводниками для других активных ингредиентов, обеспечивая их глубокое проникновение.
Зная принципы работы и правила применения, позволяют добиться истинной коррекции имеющихся проблем с кожей.
Правила применения ретиноидов
ВАЖНО! Грубая ошибка косметолога, если он избегает назначения ретиноидов из-за опасений побочных эффектов: покраснение, эритема, сухость и шелушения. Этих симптомов легко избежать, если соблюдать рекомендации:
Использовать косметические препараты с ретинолом профессиональных брендов
Есть соблазн приобрести в аптеке недорогое средство с ретиноидами? Важно знать отличия:
В аптечных формах используются синтетические аналоги ретинола , более агрессивные по работе на кожу, с большей долей вероятности провоцирующие ретиноевый дерматит;
Профессиональные косметические препараты содержат натуральные формы ретинола , мягкого по работе, при этом оказывающие все необходимые функции на кожу;
В состав профессиональной косметики с ретинолом вводятся ингредиенты осветляющего действия для усиления результативности, а также успокаивающего и восстанавливающего эффекта – для комфорта применения
Придерживаться рекомендуемым схемам применения
Каждый препарат имеет собственную схему использования, с которой необходимо ознакомиться до начала применения. Разница в в чатоте нанесения средства связана с процентным содержанием и формой ретинола.
- Наносить локально на пигментные пятна
Если нет дополнительных показаний к применению ретинола, достаточно наносить средство только на область пигментных пятен.
- Использовать только на ночь
Ретиноиды наносятся на кожу только вечером- единое правило для всех средств с ретинолом! Однократного нанесения достаточно, важно не забыть утром нанести на кожу солнцезащитный крем с SPF, т.к повышается ретиноиды истончают роговый слой и повышают уязвимость кожи к воздействию ультрафиолета и прочих лучей.
Однако, регулярное применение минерального SPF сводит все угрозы со стороны солнца к нулю и делает применение ретинола совершенно безопасным!
Работа ретиноидов физиологична, поэтому результат применения виден не моментально. Стойкий видимый эффект ожидайте примерно по второму месяцу от начала использования. Однако, спешим порадовать — результат благодаря постепенному физиологичному воздействию ретинола, стойкий и выраженный. Полностью избавиться от пигментных пятен возможно за 6 – 8 месяцев применения.
Осветляющая сыворотка «Брайтинг» DermaQuest
Разработана сециально для комплексной борьбы с пигентными пятнами — содержит 2% ретинола, обогащена Стволовыми клетками лилии белоснежной и Бакучиолом.
- Высокая рабочая концентрация ретинола 2% эффективно нормализует работу меланоцитов, одновременно эффективно восстанавливая повреждения и омолаживая кожу.
- Богатый комплекс отбеливающий ингредиентов разнонаправленного действия:
- Стволовые клетки Лилии белоснежной,
- Бакучиол (имитатор Витамина А), дополнительно повышает эффективность препарата,
- Гексилрезорцинол — безопасный аналог гидрохинона, превышает его активность в 4 раза
- Растительные экстракты осветляющего действия
- Содержит антиоксиданты – Витамин С в современной форме, Витамин Е, экстракт зеленого чая – восстановление защитных механизмов кожи;
Осветляющая сыворотка «Брайтинг» работает против всех видов пигментации, в том числе глубокой, застойной и давно существующей.
Применение по специальной схеме:
В 1-ю неделю наносят – 1 раз, во 2-ю — 2 раза, в 3-ю — 3 раза в неделю, в 4-ю и последующие 4 раза в неделю.
Обновляющий крем с Ретинальдегидом DermaQuest
Уникальный крем с Ретинолом в особой современной форме — ретинальдегид, находка для обладателей тонкой, чувствительной кожи.
Преимущества крема:
- Содержит ретинол для чувствительной кожи – ретинальдегид, что позволило произвожителю вклюяить его в группу средств для деликатной кожи.
- Назначают при любой проблеме, когда необходим ретинол: фотостарение, возрастные изменения, акне и пигментация;
- Состав усилен имитатором Витамина А – Бакучиол – повышение эффективности ретинальдегида;
- Содержит антиоксиданты и увлажняющие комплексы – мощная профилактика воспаления и раздражения кожи, сохранность ее барьеров;
- Используется ежедневно, 1 раз в день вечером.
Обновляющий крем с ретинальдегидом DermaQuest — полноценный вечений крем, не требующий использования каких-либо дополнительных питательных кремов на ночь.
Обновляющий крем с Ретинальдегидом удобен для первого знакомства с ретиноидами, для комфортного старта терапии и адаптации кожи к ретиноидам, а также в случае чувствительной и раздраженной кожи.
Применение:
Крем наносить ежедневно вечером на чистую кожу, длительность применения не ограничена.
Источник
Клинический случай нефропатии обусловленной приемом репешка обыкновенного (agrimonia eupatoria)
Батюшин М.М. 1 , Садовничая Н.А. 1 , Руденко Л.И. 1 , Повилайтите П.Э. 2
1 Кафедра внутренних болезней с основами физиотерапии №2, Нефрологическое отделение ГБОУ ВПО РостГМУ Минздрава России, г.Ростов-на-Дону
2 Ростовское областное патологоанатомическое бюро Министерства здравоохранения Ростовской области, г.Ростов-на-Дону
Адрес: 344022, г. Ростов-на-Дону, пер. Нахичеванский, 29, тел. (863)2014423 Эл.почта: batjushin-m@rambler.ru, sadovnichaya@list.ru, nephr-roon@rambler.ru
За прошедшее десятилетие отмечен значительный рост популярности «нетрадиционной медицины». Это объясняется такими факторами, как неудовлетворенность методами и эффективностью ранее проводимого лечения, бесконтрольным использованием информации о неблагоприятных побочных действиях фармацевтических препаратов, ростом цен на фармакопейные лекарственные средства и низким уровнем общей культуры населения. В отношении использования сбора лекарственных растений в литературе имеются указания на ограничения их применения, так как их прием при определенных заболеваниях может вызывать нежелательные побочные эффекты. В Европе, США и Канаде постоянно увеличивается доля населения, регулярно использующего фитотерапевтические средства и биологически активные добавки, в странах Азии и Африки более 30% всех случаев острого почечного повреждения развивается как осложнение лечения растительными препаратами [1, 2]. По данным исследования импортированных патентованных азиатских аюрведических растительных продуктов в Калифорнии, было установлено, что 32% из них содержали не декларированные фармацевтические средства и тяжелые металлы (свинец, ртуть, кадмий, мышьяк). Среди не декларированных веществ наиболее часто встречаются: эфедрин, хлорфениламин, колхицин, метилтестостерон, глюкокортикостероиды, нестероидные противовоспалительные препараты [3, 4, 5, 6, 7, 8]. Сегодня в Европе зарегистрировано более 100 препаратов, содержащих растительные флавоноиды. Они обладают антиоксидантной активностью и применяются в основном в лечении нарушений периферического кровообращения.
Потенциальное значение этой проблемы чрезвычайно велико, в частности остается неясной степень взаимодействия фармацевтического препарата с травами и растительными продуктами [9, 10]. Неконтролируемый прием лекарственных трав может превышать потенциальный положительный эффект, особенно среди лиц с заболеваниями почек [11, 12, 13, 14], что связано с непосредственным воздействием растительных препаратов на клетки канальцев и их активной реабсорбцией с достижением высокой концентрации в мозговом слое. Результатом такого воздействия на почки является острое канальцевое повреждение, папиллярный некроз, острый и хронический интерстициальный нефрит, синдром Фанкони, нефролитиаз, артериальная гипертензия, рабдомиолиз [15, 16].
К фитотоксинам, обладающим прямым нефротропным действием относят аристохолиевую кислоту, сапонины, метилсалицилат, флавоноиды, ореллаин, алкалоиды эфедры, охратоксин [17]. На территории России наиболее часто с целью лечения и профилактики заболеваний почек применяются такие лекарственные травы как: пижма, барбарис, берѐза, бессмертник песчаный, брусника, бузина, календула, кукуруза (рыльца), можжевельник, толокнянка, хвощ, шиповник, репешок обыкновенный (Argimonia Eupatoria), а также марена красильная грузинская (Rubia tinctorum var. iberica), дикорастущая трава.
Репешок обыкновенный (Argimonia Eupatoria) – многолетнее травянистое растение, широко распространенное в европейской части России, на территории Западной и Восточной Сибири, Дальнего Востока [18]. В народной и традиционной медицине все части растения применяются при широком спектре заболеваний в качестве желчегонного, противовоспалительного, антиаритмического, гипогликемического, антигельминтного, анальгетического, гемостатического, антигипертонического, антитоксического и антиканцерогенного средства. В европейских странах некоторые виды Agrimonia являются официальными лекарственными растениями и используются в практической медицине как вяжущее, противовоспалительное средство [19]. При проведении биохимического анализа структуры растения в надземной части A.Eupatoria обнаружены вещества фенольной природы (филавоноиды, дубильные вещества, кумарины, изокумарины, оксикоричные кислоты), тритерпеноиды, эфирное масло, полисахариды и др., а в подземных органах растения обнаружены медь, цинк, железо, ванадий, никель, хром, титан, марганец, стронций, цирконий, серебро [20].
Токсические эффекты А. Eupatoria в большей степени связаны не со специфическими токсикантами, а с наличием в нем большого количества гликозидов кумарина и его метаболитами. В 1994 г. на основании углубленного анализа токсикологических исследований экспертами Европейского Совета сделаны рекомендации о снижении допустимого уровня содержания кумарина в продуктах питания до 0,5 мг/кг вследствие его канцерогенного и мутагенного действия.
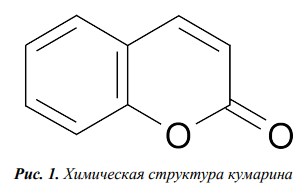
КУМАРИН (2-хроменон) имеет молекулярную массу 146,14 и представляет собой бесцветные кристаллы с запахом свежего сена и горьким вкусом (рисунок 1).
Рис. 1. Химическая структура кумарина
Сообщения о гепатотоксических эффектах для человека, развивающихся вследствие приема кумарин-содержащих лекарственных препаратов, часто противоречивые, вызвали значительный интерес исследователей к изучению его метаболизма и механизма токсического действия [20, 21].
Современные представления о метаболизме кумарина предполагают наличие двух основных путей трансформации данного соединения в организме млекопитающих. Первый этап трансформации кумарина реализуется по двум направлениям: в результате 7-гидроксилирования кумарина образуется малотоксичный 7-гидроксикумарин, элиминирующийся из организма млекопитающих с мочой; в процессе 3-гидроксилирования образуется 3-гидроксикумарин, промежуточным метаболитом в данном процессе является токсичный 3,4-эпоксид, подвергающийся дальнейшей трансформации с образованием о-гидроксифенилальдегида, окисляющегося до о-гидроксиэтанола и о-гидроксифенилуксусной кислоты. Рядом авторов было показано, что доминирование одного из двух направлений метаболизма кумарина в организме обусловливает межвидовые различия в проявлении гепатотоксических свойств данного соединения [22, 23]. Риск осложнений при приеме кумарина возрастает при сочетанном приеме НПВС, антикоагулянтов прямого и непрямого действия.
В экспериментальных работах [24, 25] установлено, что кумарин при однократном введении в больших дозах крысам вызывает центрилобуллярный некроз гепатоцитов. Это свидетельствует о том, что метаболизм кумарина [3-l4C] в данном случае проходил с образованием более токсичных метаболитов. Исследования in vitro показали, что химически активные [3-l4C]-кумариновые метаболиты, образующиеся при участии цитохром P450-зависимых энзимов, способны ковалентно связывать микросомальные протеины [26]. Было сделано предположение, что токсическим метаболитом в данном случае может выступать 3,4-эпоксид.
Нами представлен случай нефротоксического действия алкалоидов кумарина и его метаболитов при употреблении отваров и настоев Репешка обыкновенного.
Пациентка А. 43 лет, поступила в нефрологическое отделение клиники РостГМУ с жалобами на легкую ноющую боль в поясничной области с обеих сторон, усиливающуюся при физической нагрузке, пастозность голеней и стоп, периодически повышающееся артериальное давление до 220/140 мм рт. ст., не связанное с психоэмоциональными и/или физическими нагрузками, сопровождающееся головной болью и головокружением. Из анамнеза известно, что в 1990 году в течение всего периода первой беременности выявлялась протеинурия до 3,3 г/л, не сопровождающаяся отечным синдромом и артериальной гипертензией, в течение 5 лет после родов протеинурия сохранялась на уровне 0,5-1,0 г/л. В 1995 г. впервые зарегистрирован высокий уровень артериального давления (АД) – 150/100 мм рт. ст. Антигипертензивную терапию не получала, однако с 1999 г. артериальная гипертензия приобрела злокачественный характер, с повышением уровня системного АД до 200/120 мм рт. ст., по поводу чего в 2000 году проходила обследование в стационаре, где был поставлен диагноз гипертонической болезни II стадии, 3 степени, риск 3 (высокий), тогда же была подобрана антигипертензивная терапия, позволявшая контролировать АД на уровне 130-150/80-90 мм рт. ст., но пациентка данные рекомендации не соблюдала, а самостоятельно приобрела фитопрепарат (Репешок обыкновенный), отвар и настои которого, принимала более полугода непрерывно по несколько раз в сутки. В 2001 году, во время прохождения планового медицинского осмотра выявлен нефросклероз справа, дальнейшего наблюдения и лечения не проходила. В 2008 году при выполнении ультразвукового исследования почек выявлен конкремент правой сморщенной почки, по данным реносцинтиграфии функция правой почки отсутствует.
Помимо приема фитопрепаратов постоянно использует дипиридамол в дозе 75 мг/сутки, эналаприл 10 мг/сутки с 2001 года, в 2011 году уровень протеинурии составил 0,044 г/л, уровень артериального давления до 240/140 мм ртутного столба.
По данным клинико-лабораторного обследования в нефрологическом отделении клиники РостГМУ со стороны ОАК на себя обращали внимание ускорение СОЭ до 32 мм/час, признаки анемии легкой степени тяжести (эритроцитов 2,52х1012/л, гемоглобин 100 г/л), снижение количества тромбоцитов (75х103 /л), со стороны свертывающей системы крови по данным коагулограммы выявлены признаки гипокогуляции, характеризующиеся снижением АПТВ до 20 сек., протромбиновое время 10 сек., МНО 0,5, тромбиновое время 6 сек., фибриноген 1,98 г/л, со стороны биохимических показателей крови отмечалась гиперхолестеринемия до 10,79 мМ/л, гиперазотемия (креатинин крови 129 мкМ/л, мочевина 14,9 мМ/л), уровень АСТ достигал 68 Ед/л, АЛТ – 51 Ед/л. В ОАМ – протеинурия, характерная для нефритического синдрома (до 0,4 г/л). Снижение концентрационной функции почек, проявляющееся снижением СКФ до 45,5 мл/мин (по формуле MDRD), изостенурией (по данным пробы Фольгарда). Суточная протеинурия не превышала 0,495 г/сутки, по данным суточной экскреции солей с мочой отмечается высокая экскреция кальция до 9,73 мМ/сутки, и мочевой кислоты до 9,13 мМ/сутки. За все время наблюдения состояние пациентки оставалось стабильным, уровень АД в пределах 130-140/70-80 мм рт. ст., суточный диурез около 1500-1700 мл. По данным УЗИ почек отмечаются диффузные изменения паренхимы почек, уменьшение размеров, микролит правой почки.
Таким образом, клиническая картина болезни соответствовала аутоиммунному заболеванию почек, на что указывали наличие протеинурии, мочевой синдром, характеризующийся микрогематурией, снижением азотвыделительной функции почек, наличием артериальной гипертензии, тем не менее, нельзя было исключить наличие хронического повреждения канальцевого эпителия, преимущественно в проксимальных отделах, с нарушением реабсорбции, без формирования клиники острого канальцевого некроза, что позволило заподозрить наличие специфического патологического процесса, связанного с токсическим влиянием метаболита кумарина на канальцевый эпителий почек. Следует также учесть наличие процесса нефросклероза в правой почке, вероятно, обусловленного мочекаменной болезнью в анамнезе.
Пациентке была выполнена пункционная нефробиопсия левой почки с последующим морфологическим исследованием биоптата с целью верификации патологического процесса и определения тактики терапии. В результате получены следующие данные.
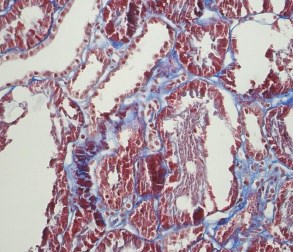
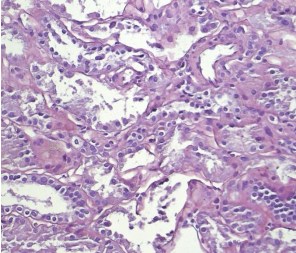
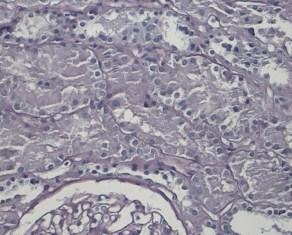
Светооптически 1 из 9 клубочков склерозирован полностью, остальные гипертрофированы. В одном клубочке выраженная интракапиллярная гиперклеточность и пролиферация базальных мембран. Остальные клубочки не имеют признаков выраженных пролиферативных изменений, за исключением сегментарного расширения парамезангиальных зон. Сегментарного склероза капиллярных пучков не наблюдается. В интерстиции слабый диффузный и мелкоочаговый фиброз. Резко выраженная гидропическая дистрофия эпителия канальцев вплоть до вакуолизации (рисунки 2, 3, 4).
Рис. 2. Х20 массон1 – резко выраженные дистрофические изменения эпителия канальцев, его слущивание
Рис. 3. Х20 ШИК – резко выраженные повреждения эпителия канальцев – слущивание фрагментов цитоплазмы и целых клеток в просвет канальцев
Рис. 4. Х20 ШИК – расширение и гиперклеточность мезангиальных зон
Окраска на амилоид отрицательна. Иммуноморфологически: IgA в клубочках: отрицательно, в канальцах: отрицательно, IgG в клубочках: отрицательно, в канальцах: отрицательно, IgM в клубочках: единичное редкое пунктирное, в канальцах: единичные цилиндры, C3 комплимент: единичные зерна в клубочках и в капсуле, а также зернистое в стенках артериол, C1q комплимент: отрицательно. Каппа: отрицательно в клубочках, единичные очаги в интерстиции. Лямбда: отрицательно в клубочках, единичные очаги в интерстиции. Электронномикроскопически: толщина и структура базальных мембран в пределах нормы, депозитов не обнаружено. Имеются протяженные очаги распластывания малых отростков подоцитов, пролиферация мезангиальных клеток отсутствует. Результаты были интерпретированы как очаговое распластывание малых отростков подоцитов, а также тубулопатия неясного генеза. Особое внимание в клинической картине на себя обращало постепенное нарастание протеинурии, артериальной гипертензии на фоне снижения фильтрационной функции почек и канальцевой дисфункции. Подобная двойственность клинических проявлений препятствовала пониманию сути патологического процесса в почках, и не позволяла в полной мере проводить медикаментозную терапию, отвечающую патогенетическим и этиологическим принципам. Указание в анамнезе на длительный прием фитопрепаратов позволило предположить токсическое воздействие метаболитов кумарина на функциональное состояние почек, однако в доступной литературе нет прямых указаний на прямое нефротоксическое действие кумарина. Исследователи ограничивают область токсических влияний кумарина и его метаболитов на функцию печени и гемостаза. Действительно, в рассматриваемом клиническом примере отмечаются как нарушения гемостаза, характеризующиеся гипокоагуляцией, так и печеночная дисфункция. Однако по данным нефробиопсии отмечаются признаки токсического процесса на уровне канальцев почки, характеризующегося резко выраженной гидропической дистрофией эпителия канальцев вплоть до вакуолизации, слабым диффузным и мелкоочаговым фиброзом интерстиция. Эти изменения соотносятся с изменениями клубочков, характеризующимися выраженной интракапиллярной гиперклеточностью и пролиферацией базальных мембран, сегментарным расширением парамезангиальных зон, наличием очагов распластывания малых отростков подоцитов.
Таким образом, впервые в литературе описан случай прямого нефротоксического воздействия кумарина и его метаболитов. Повреждение канальцевого эпителия почек метаболитами кумарина обуславливается во многом изначальным повреждением гломерулярной базальной мембраны, а также дисморфизмом подоцитов, что обуславливает повышенную готовность канальцевого эпителия к повреждению на фоне усиления процессов реабсорбции в связи с дефектами гломерулярной базальной мембраны и подоцитов. В свою очередь, низкая молекулярная масса кумарина и его метаболитов позволяет свободно проникать через гломерулярный фильтр, что, в условиях повреждения базальной мембраны и подоцитов, приводит к критическому повышению его в первичной моче и обуславливает токсическое действие на уровне канальцев почки.
Литература
1. Ермоленко, В.М. Острая почечная недостаточность / В.М. Ермоленко, А.Ю. Николаев – М.: Гэотар-Медиа, 2010. – 400 с.
2. Angell, M. Alternative medicine – the risks of untested and unregulated remedies / M. Angell, J.P. Kassirer // N. Engl. J. Med. – 1998. – V.339. – P.839-841.
3. Fugh-Berman, A. Herb-drug interactions / A. Fugh-Berman // Lancet. – 2000. – V.355. – P.134-138.
4. Recent patterns of medication use in the ambulatory adult population of the United States: the Spone survey / D.W. Kaufman, J.P. Kelly, L. Rosenberg et al. // JAMA. – 2002. –V.287. – P.337-344.
5. Screening methods for drugs and heavy metals in Chinese patent medicines / A. Au, R. Ko, F. Boo et al. // Bull. Environ. Contam. Toxicol. – 2000. – V.5. – P.112-119.
6. Chopra, A. Ayurvedic medicine: core concept, therapeutic principles, and current relevance/ A. Chopra, V. Doiphode. // Med. Clin. North. Am. – 2002. – V.86. – P.75-89.
7. Ernst, E. Heavy metals in traditional Indian remedies / E. Ernst // Eur. J. Clin. Pharmacol. – 2002. – V.57. – P.891-896.
8. The use and safety of non-allopathic Indian medicines / N. Gogtay, H. Bhatt, S. Dalvi, N. Kshirsagar // Drug Saf. – 2002. – V.25. – P.1005-1019.
9. Indian herbal remedies for diabetes as a cause of lead poisoning / R.W. Keen, A.C. Deacon, H.T. Delves et al. // Postgraduate Medical Journal. – 1994. – V.70. – P.113-114.
10. Ko, R.J. Adulterants in Asian patent medicines / R.J. Ko // N. Engl. J. Med. – 1998. – V.339. – P.847.
11. Arlt, V. Aristolochic acid as a probable human cancer hazard in herbal remedies: a review / V. Arlt, M. Stiborova, H. Schmeiser // Mutagenesis. – 2002. – V.17. – P.265-277.
12. Trends in alternative medicine use in the United States, 1990-1997: results of a follow-up national survey / D.M. Eisenberg, R.B. Davis, S.L. Ettner et al. // JAMA. – 1998. – V.280. – P.1569-1575.
13. Ernst, E. Adulteration of Chinese herbal medicines with synthetic drugs: a systematic review / E. Ernst // J. Intern. Med. – 2002. – V.252. – P.107-113.
14. Foote, J. Medicinal herb use and the renal patient / J. Foote, B. Cohen // J. of Renal Nutrition. – 1998. – V.8. – P.40-42.
15. International Agency for Research on Cancer (IARC). Some traditional herbal medicines, some mycotoxins, nafhtalene and styrene. In IARC Monographs on the Evaluation of Carcinogenic Risks of Chemicals to Humans. Lyon. France: IARC, 2002. – Р.82.
16. Herbs and the kidney/ C. Isnard Bagnis, G. Deray, A. Baumelou et al. // Am. J. Kidney Dis. – 2004. – V.44. – №1. – P.1-11.
17. Morris L. Side-effects of coumarin / L. Morris, P.D. Welsby // Postgrad. Med. J. – 1995. – №71. – P.701-702.
18. British Herbal Pharmacopoeia. – 1996. – 212 p.
19. Advances in research on chemical constituents and pharmacological activities of Agrimonia pilosa / G. Hong, Y.H. Dai, P.X. Liu et al.// Pharm. Care and Research. – 2008. – V.8. – № 5. – P.362-366.
20. Карташова, Г.С. Содержание дубильных веществ в Agrimonia pilosa Ledeb. / Г.С. Карташова, И.В. Гравель, Е.Г. Таран // Растительные ресурсы. – 1991. – Т.27. – №1. – С.139-143.
21. Wei, Y. Isolation of hyperoside and luteolin-glucoside from agrimonia pilosa ledeb using stepwise elution by high-speed countercurrent chromatography / Y. Wei, Y. Ito // J. of Liquid Chromatography and Related Technologies. – 2007. – V.30. – №9-10. – P.1465–1473.
22. Separation and determination of flavonoids in Agrimonia pilosa Ledeb. by capillary electrophoresis with electrochemical detection / X. Xu, X. Qi, W. Wang, G. Chen // J. of Separation Science. – 2005. – V.28. – №7. – P.647-652.
23. Analysis of the volatile components of Agrimonla Pilosa Ledeb by gas chromatography-mass spectrometry / Y.W. Li, L.F. Huang, C. Liang et al. // J. of Central South University (Science and Technology). – 2007. – V.38. – №3. – P. 502-506.
24. Фитохимическое исследование растений флоры Сибири / Д.Л. Макарова, В.В. Величко, Н.Е. Ким и др.// Фармация. – 2008. – №3. – С.19-22.
25. 500 важнейших лекарственных растений / В.К. Лавренов, Г.В. Лавренова. – М., 2003. – 510 с. 26. Comparative metabolism and kinetics of coumarin in mice and rats / S.L. Born, A.M. Api, R.A. Ford et al. // Food Chem. Toxicol. – 2003. – №41. – P.247-258.
Статья опубликована в журнале «Вестник урологии». Номер №3/2013 стр. 30-39
Источник