Доклинические исследования токсичности лекарственных средств
Профилактика и лечение сосудистых заболеваний головного мозга является в настоящее время важной и актуальной задачей во всем мире. Инсульт – это серьезная проблема общественного здравоохранения, поскольку ежегодно около 15 миллионов человек во всем мире переносят инсульт [1; 2]. В нашей стране инсульт поражает более 450 000 человек в год, заболеваемость и смертность от острых нарушений мозгового кровообращения находится на 2-м месте среди других заболеваний. Для того чтобы избежать высокой смертности и инвалидности, необходимо раннее выявление и адекватное лечение инсульта, а также обязательное проведение реабилитационных мероприятий, которые препятствуют возникновению рецидива. Одним из компонентов реабилитации является медикаментозная терапия с использованием церебропротекторных, ноотропных и стресс-протекторных препаратов. Одним из перспективных направлений создания новых препаратов, обладающих церебропротекторным действием, является разработка инновационных соединений на основе пептидных биорегуляторов.
Новое потенциальное лекарственное средство (ЛС) на основе пептидэргического нейро- и стресс-протектора Nα-ацетил-D-лизил-лизил-аргинил-аргинил-амид является кандидатным препаратом для лечения нарушений мозгового кровообращения. Проведенные ранее доклинические исследования специфической фармакологической активности потенциального ЛС показали его высокую нейропротекторную эффективность in vivo [3]. Было показано, что данное потенциальное ЛС обладает антиишемической, антигипоксической, ноотропной и актопротекторной активностями [4]. Выявлено, что Nα-ацетил-D-лизил-лизил-аргинил-аргинил-амид, являющий активным фармакологическим ингредиентом потенциального ЛС, оказывает интегральное нейропротекторное действие, нормализует уровень провоспалительных цитокинов IL-1β и TNF-α, а также повышает содержание противовоспалительного интерлейкина-4 в головном мозге. Защитное действие пептида при церебральной ишемии характеризуется также нейротрофическим компонентом.
Целью данной работы являлись доклинические исследования острой и хронической токсичности потенциального ЛС «Лизаргам» на основе пептидэргического нейро- и стресс-протектора для лечения нарушений мозгового кровообращения.
Материалы и методы исследования
Исследуемое потенциальное ЛС «Лизаргам, спрей назальный дозированный 0,5% и 1,0%» (далее потенциальное ЛС «Лизаргам»), один флакон потенциального ЛС содержит активный фармацевтический ингредиент («D-лизаргам, ацетат») – 15 (0,5%) или 30 (1,0%) мг; физиологический раствор (ФР) — 3,0 мл; D-маннит — 30 мг. «D-лизаргам, ацетат» представляет собой синтетический тетрапептид последовательности Nα-ацетил-D-лизил-лизил-аргинил-аргинил-амид в виде ацетатной соли. Терапевтическая доза потенциального ЛС у человека составляет 20 мкг/кг. Эта доза рассчитывалась исходя из данных по изучению специфической активности потенциального ЛС на экспериментальных животных и коэффициента экстраполяции доз мышей и крыс на человека в соответствии с руководством Т.А. Гуськовой [9].
Доклинические исследования были выполнены на основе рекомендаций действующих методических документов 6. Животные поступили из питомника РАМН «Рапполово» Ленинградской области. Основные правила содержания и ухода соответствовали правилам, принятым Европейской конвенцией по защите позвоночных животных (Страсбург, 1986 г.). Объем работ и перечень процедур был одобрен биоэтической комиссией института. Исследования проводили на 3 видах животных: белых беспородных крысах обоего пола (масса 180-200 грамм, возраст 9–10 недель), белых беспородных мышах обоего пола (19–21 г, 9–10 недель) и на кроликах породы шиншилла обоего пола (2-2,5 кг, 2-3 месяца).
Острая токсичность потенциального ЛС была изучена на мышах, крысах и кроликах. Период наблюдения после введения возрастающих доз составил 14 дней, для достижения высоких доз потенциальное ЛС вводили многократно в течение 10 часов. Эксперименты были проведены при интраназальном (и/н) и внутривенном (в/в) введении потенциального ЛС по одинаковым схемам. Мыши и крысы были случайным образом разделены на группы (по 5 самок и 5 самцов). В опытных группах мышам и крысам и/н вводили потенциальное ЛС в дозах 2, 20, 50 мг/кг; в/в — в дозах 20, 200, 500 мг/кг. И/н потенциальное ЛС вводилось животным при помощи автоматической одноканальной пипетки 10-100 мкл с соответствующим наконечником, введение осуществлялось в каждый носовой ход. В/в введение производилось в соответствии с требованиями [6], в максимальной дозе 500 мг/кг (50 мл/кг) каждой крысе вводили не более 2 мл за раз с интервалом 2 часа в течение 10 часов. Кролики были случайным образом разделены на группы (по 3 самки и по 3 самца в каждой). Кроликам в опытной группе потенциальное ЛС вводили и/н в дозе 25 мг/кг, в/в — в дозе 400 мг/кг. В контрольных группах животным по тем же схемам вводили ФР.
Во всех экспериментах проводили наблюдение за лабораторными животными в течение 14 суток после введения потенциального ЛС. Проводили клинический осмотр (ежедневно) до начала эксперимента (фоновые значения), а также выполняли взвешивание на 2, 7 и 14-й день после введения. У крыс и кроликов измеряли частоту сердечных сокращений (ЧСС) и частоту дыхательных движений (ЧДД). На 14-е сутки все животные были подвергнуты эвтаназии и патоморфологическому исследованию.
Оценка местнораздражающего действия была проведена на 3 кроликах-самцах. На слизистую оболочку правого глаза наносили 0,1 мл 1% потенциального ЛС, на слизистую оболочку левого глаза — 0,1 мл ФР. Наблюдение проводили в течение 24 часов с момента нанесения потенциального ЛС.
Испытания на пирогенность были проведены на кроликах-самцах и соответствовали требованиям ГФ XIII, ОФС 1.2.4.0005.15 [8]. Потенциальное ЛС вводили в ушную вену в объеме 0,2 мл/кг. Температуру измеряли 2 раза до начала исследования и каждые 30 минут в течение 3 часов после введения потенциального ЛС.
Хроническая токсичность потенциального ЛС была изучена на крысах, случайным образом разделенных на 4 группы (по 15 самок и 15 самцов в каждой). Потенциальное ЛС вводили и/н ежедневно, в течение 90 дней в 3 дозах: 1 мг/кг (50-кратная терапевтическая доза для человека, минимально возможная для экспериментального введения крысам), 3 и 5 мг/кг. Хроническая токсичность потенциального ЛС была также изучена на кроликах, самцах и самках, которые были случайным образом разделены на группы (по 3 самки и 3 самца в каждой). Потенциальное ЛС вводили и/н ежедневно, в течение 90 дней в 3 дозах: терапевтической дозе для кролика — 0,06 мг/кг (доза рассчитана путем умножения терапевтической дозы для человека на коэффициент пересчета по площади поверхности тела кролика 3,2); 3 мг/кг и максимальной — 5 мг/кг (более чем в 250 раз превышающей терапевтическую дозу для человека). Крысам и кроликам в контрольных группах по той же схеме вводили ФР.
Клинический осмотр животных выполняли ежедневно, в течение эксперимента регистрировали интегральные показатели состояния организма всех животных, а также патоморфологическое и патогистологическое исследования по окончании эксперимента. Физиологические исследования проводили до начала исследования, а также на 30-й и на 90-й день после начала введения потенциального ЛС.
Офтальмологическое исследование проводили на тех же сроках, оценивая состояние слизистых оболочек, наличие правильных роговичных рефлексов и измеряя величину зрачка и ширину глазной щели. Для лабораторных исследований собирали образцы крови и костный мозг.
Клинический анализ крови выполняли на автоматическом гематологическом анализаторе Abacus Junior vet5 (Diatron, Венгрия) и на мазках крови, окрашенных по Романовскому-Гимзе. Биохимические показатели в сыворотках крови (аланинаминотрансфераза (АлАТ), аспартатаминотранфераза (АсАТ), билирубин, глюкоза, креатинин, мочевина, общий белок, холестерин, щелочная фосфатаза) оценивали на полуавтоматическом биохимическом анализаторе Chem-7 (Erba, Чехия). Исследование мочи выполняли на экспресс-анализаторе мочи DocUReader (ANALYTICON Biotechnologies AG, Германия). Кроме того, проводили микроскопический анализ миелограммы на мазках смывов костного мозга и подсчет количества клеток костного мозга. Все тесты выполнялись по стандартным протоколам и инструкциям производителей наборов.
На основании результатов эксперимента по изучению хронической токсичности рассчитывали расчетный безопасный курс (РБК) и индекс безопасности (ИБ) потенциального ЛС при клиническом применении в соответствии с инструкцией Т.А. Гуськовой [9].
Патоморфологическое исследование после завершения экспериментов включало в себя некропсию, макроскопическое исследование и взвешивание внутренних органов. Также рассчитывали отношение массы органа к массе тела.
Патогистологическое исследование было выполнено с использованием образцов тканей, полученных от животных, которым вводили потенциальное ЛС в максимальной дозе, а также образцов тканей от животных контрольных групп. Материал фиксировали в 10%-ном формалине, обезвоживали, заключали в парафин и изготовляли гистологические срезы, которые окрашивали гематоксилином и эозином («Биовитрум», Россия). Препараты изучали в световом микроскопе DMLB (Leica Microsystems AG, Германия).
Статистический анализ проводили с помощью программы Microsoft Excel 2007 (Microsoft Corporation). Подсчитывали средние значения и ошибки среднего (М±m). Сравнение показателей между группами проводили с помощью непарного Т-критерия Стьюдента с неравными отклонениями, а также по U-критерию Манна-Уитни. Отличия считали достоверными при р 5) потенциальное ЛС «Лизаргам, спрей назальный» относится к III классу малотоксичных лекарственных препаратов.
- Изучение хронической токсичности на кроликах
Ежедневный клинический осмотр кроликов всех экспериментальных групп не выявил каких-либо значимых различий между группами, гибели подопытных животных не наблюдалось. Измерение массы тела показало, что данный параметр равномерно увеличивался на протяжении всего срока исследования как в контрольной, так и во всех опытных группах. Анализ показателей массы тела, потребления корма и воды, а также физиологических параметров (ЧДД, ЭКГ и ЧСС и АД) показал, что достоверные различия между всеми экспериментальными группами отсутствуют. Офтальмологическое исследование не выявило различий между экспериментальными группами, получавшими потенциальное ЛС или ФР.
Представленные в таблице 6 данные подтверждают, что ежедневное и/н введение потенциального ЛС в дозах 0,06-5 мг/кг в течение 30 и 90 дней не оказывало значительного влияния на количественный и качественный состав периферической крови кроликов. Также не было выявлено влияния потенциального ЛС на состояние красного костного мозга, биохимический состав крови, мочи и функциональную активность почек.
Оценка влияния ежедневного интраназального введения потенциального лекарственного средства «Лизаргам» на показатели периферической крови кроликов-самцов
Источник
Доклинические исследования токсичности лекарственных средств
В последнее время наблюдается увеличение числа сосудистых заболеваний и цереброваскулярных нарушений центральной нервной системы. В лечении данных патологий важная роль принадлежит церебропротекторным, ноотропным и стресс-протекторным препаратам.
В данной работе приведены результаты исследований репродуктивной токсичности и эмбриотоксического действия, а также оценки возможного мутагенного и канцерогенного действия потенциального ЛС для лечения нарушений мозгового кровообращения — «Лизаргам, спрей назальный дозированный» (далее препарат «Лизаргам»).
Исследования показали, что активный фармакологический ингредиент препарата «Лизаргам» (Nα-ацетил-D-лизил-лизил-аргинил-аргинил-амид) обладает нейропротекторным действием [1]. Введение препарата нормализует уровни цитокинов в головном мозге, а также обладает антиапоптотическим действием, поскольку может ограничивать развитие апоптоза в головном мозге после воздействия оксида углерода. Защитное действие исследуемого пептида характеризуется также нейротрофическим компонентом. Таким образом, препарат «Лизаргам» обладает высокой нейропротекторной эффективностью in vivo.
Материалы и методы исследования
В данной работе использовали готовую лекарственную форму (ГЛФ) «Лизаргам, спрей назальный дозированный 0,5% и 1,0%». Подробная характеристика ГЛФ приведена нами ранее [2]. Терапевтическую дозу препарата для человека (20 мкг/кг) высчитывали в соответствии с руководством Т.А. Гуськовой [2; 3].
Животные содержались в виварии согласно санитарно-эпидемиологическим требованиям от 29.08.2014 г., условия соответствовали Европейской конвенции по защите позвоночных животных (Страсбург, 1986 г.). Эксперименты проводились с разрешения биоэтической комиссии института. В качестве контроля во всех экспериментах использовали физиологический раствор (стерильный 0,9% раствор хлорида натрия, ФР).
Оценку репродуктивной токсичности (генеративной функции) проводили на белых беспородных крысах обоего пола (180-200 г, 9-10 недель) [4; 5]. Препарат «Лизаргам» вводили самкам (n=20) ежедневно интраназально (и/н) в дозе 5 мг/кг (максимальная доза, использованная в эксперименте по изучению хронической токсичности) в течение 15 дней (3 эстральных цикла). Самцам препарат вводили (n=10) и/н в дозе 5 мг/кг в течение всего периода сперматогенеза (48 дней). После введения препарата самок помещали с самцами на 2 эстральных цикла (10 дней). Взвешивание крыс проводили до начала эксперимента (фоновые значения), после завершения введения препарата и перед эвтаназией (самки). Забой и морфологическое исследование репродуктивной системы самок проводили на 20-й день после оплодотворения. Состояние внутренних органов и костной системы плодов исследовали по методу Вильсона или по модифицированному методу Даусона [4].
Исследование эмбриотоксического действия препарата проводили в 2 этапа [4; 6; 7]. Спаривание виргинных самок осуществляли с интактными самцами. На первом этапе препарат и/н вводили двум опытным группам самок по 15 особей с 1-го по 19-й день беременности: в 1-й группе — в дозе 1 мг/кг (10-кратная предполагаемая терапевтическая доза для человека с учетом коэффициента пересчета на площадь поверхности тела крыс, равного 6); во 2-й группе — в дозе 5 мг/кг. В контрольной группе самкам (n=15) в эти сроки вводили ФР. Вскрытие самок проводили после эвтаназии на 20-й день беременности, при этом определяли показатели репродуктивной системы самок и состояния плодов.
На втором этапе препарат вводили и/н одной группе самок (n=15) в дозе 5 мг/кг с 1 по 21-й день беременности, в контрольной группе самкам (n=15) в эти же сроки вводили ФР. На 4, 7, 14 и 21-й дни после рождения у 8 крысят из каждого помета проводили оценку физического развития неполовозрелого потомства. На 2-6-й дни изучали скорость созревания сенсорно-двигательных рефлексов крысят, а на 30-й день — эмоционально-двигательное поведение по методу «открытое поле».
При изучении генотоксичности руководствовались рекомендациями действующих методических документов [4; 8]. Мутагенные свойства препарата «Лизаргам» изучали in vitro с использованием чашечного метода учета мутаций в тесте Эймса.
Мутагенность и риск канцерогенного действия препарата «Лизаргам» изучали in vivo в 2 сериях экспериментов на белых беспородных мышах и мышах-гибридах F1(CBA x С57В1) обоего пола. Проводили оценку хромосомных аберраций в клетках красного костного мозга (ККМ). В первой серии экспериментов были сформированы три группы по 5 самцов. В 1-й (опытной) группе «Лизаргам» вводили однократно и/н в дозе 6 мг/кг; во 2-й группе (негативный контроль) — по той же схеме вводили ФР; в 3-й группе (позитивный контроль) в те же сроки однократно, внутрибрюшинно (в/б) вводили циклофосфамид в дозе 20 мг/кг. Во второй серии экспериментов в двух группах (опытная и контрольная) было по 5 самцов и по 5 самок. В опытной группе препарат вводили и/н в дозе 6 мг/кг ежедневно 5 дней. Через 24 часа после введения «Лизаргама» после эвтаназии у мышей получали ККМ для исследований.
Проводили изучение индукции доминантных летальных мутаций в зародышевых клетках мышей (CBA x С57В1). В опытной и контрольной группах было по 15 самцов. В опытной группе «Лизаргам» вводили и/н в дозе 6 мг/кг однократно. К каждому самцу подсаживали по 3 интактных виргинных самки, затем заменяли новыми через 7 дней. На 15-17-й день беременности после эвтаназии самок вскрывали. Уровень постимплантационных потерь (А) подсчитывали по формуле:
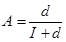
Статистическую обработку проводили в программе Microsoft Excel-2007. Полученные данные представляли в виде средних значении и ошибок среднего (M±m). Различия между группами оценивали с помощью Т-критерия Стьюдента, а также теста Манна-Уитни.
Результаты исследования и их обсуждение
1. Оценка репродуктивной токсичности
1.1. Генеративная функция
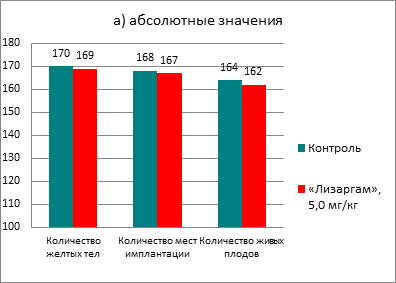
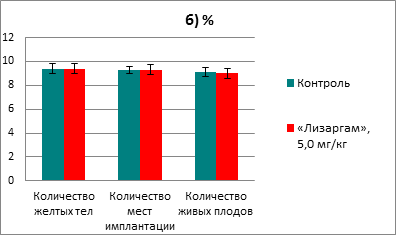
После введения препарата ни в одной из групп не наблюдалось гибели крыс. Не происходило снижение прироста массы тела, а также не было выявлено изменений в поведении животных. При изучении репродуктивной системы у самок не было обнаружено никаких патологических изменений. В каждой из групп было по 18 беременных самок, при этом индекс фертильности составил 90% и в опытной, и в контрольной группе. Результаты оценки параметров репродуктивной системы самок приведены на рисунке 1.
Количество резорбций не отличалось в контрольной и опытной группах (всего 4 и 5; 0,22±0,13% и 0,28±0,19% соответственно). Предимплантационная гибель составила в контрольной — 1,02±0,70, в опытной группе — 1,12±0,79, а постимплантационная — 2,36±1,40 и 2,40±1,67 соответственно. Таким образом, показатели предимплантационной и постимплантационной потерь также были близкими в обеих группах. При исследовании состояния плодов в обеих группах не было выявлено значительных различий. Так, средний вес составил в контрольной группе 3,15±0,04 г, а в опытной группе — 3,12±0,03 г, краниокаудальный размер плодов был в среднем 34,09±0,12 и 34,12±0,13 мм соответственно. При внешнем обследовании 164 плодов в контрольной и 162 в опытной группе не было выявлено никаких аномалий развития. При изучении развития внутренних органов у 82 плодов в контрольной и 81 в опытной группе, а также состояния костного скелета также не обнаружено патологий развития. Число центров оссификации метакарпальных (справа 3,66±0,07; слева 3,59±0,05) или метатарзальных (справа 3,63±0,09; слева 3,57±0,05) в контрольной группе значительно не различалось от таковых в опытной группе (метакарпальных — справа 3,64±0,06; слева 3,60±0,05 или метатарзальных — справа 3,67±0,05; слева 3,54±0,06).
Рис. 1. Влияние препарата «Лизаргам» на параметры репродуктивной системы самок крыс
1.2. Изучение возможного эмбриотоксического действия
На первом этапе проводили оценку возможного действия препарата в пренатальный период развития. При и/н введении препарата самкам в дозах 1 и 5 мг/кг в течение 19 дней в репродуктивной системе самок не было обнаружено патологических изменений. Также не было выявлено нарушений в состоянии плодов.
На втором этапе изучали возможное постнатальное действие препарата. Результаты показали, что после введения препарата крысам не было обнаружено патологических изменений в развитии их потомства. Оценка количественных показателей, параметров физического развития, сроков формирования сенсорно-двигательных рефлексов и эмоционально-двигательного поведения неполовозрелого потомства самок крыс, получавших «Лизаргам», не выявила различий между контрольными и опытными группами (таблицы 1-3, рисунки 2, 3).
Количественные показатели потомства, рожденного от самок крыс, получавших препарат «Лизаргам»
Источник