- Борьба с лекарственной устойчивостью: порядок действий
- Устойчивость к антибиотикам – что это?
- Алена Герасимова (Dalles) Разработчик сайта, редактор
- Откуда возникает устойчивость к антибиотикам?
- Классификация антибиотиков
- Что такое устойчивость к антибиотикам?
- Почему антибиотик может быть неэффективным?
- Материалы конгрессов и конференций
- IX РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
- МНОЖЕСТВЕННАЯ ЛЕКАРСТВЕННАЯ УСТОЙЧИВОСТЬ ОПУХОЛИ И МЕХАНИЗМ-СПЕЦИФИЧЕСКАЯ ХИМИОТЕРАПИЯ: ПРОТИВОРЕЧИЕ?
Борьба с лекарственной устойчивостью: порядок действий
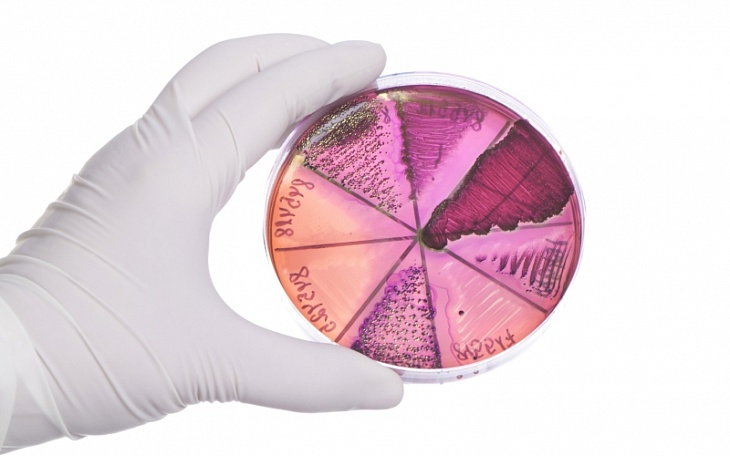
Своевременная диагностика антибиотикорезистентности — важнейшая задача современного мира: лекарственно устойчивые микроорганизмы убивают как минимум 25000 человек ежегодно только в Евросоюзе. При инфекционном заболевании необходимо прежде всего выявить инфекционный агент и показать, какой антибиотик будет против него эффективным, затем выявить механизмы резистентности и определить, какие меры позволят контролировать распространение инфекции. (См. предложенную авторами заявления схему классификации инфекций: порядок вопросов, которые должен ставить клиницист, и пути получения ответов.)
На современном этапе лекарственную устойчивость можно выявить с помощью секвенирования ДНК — это метод быстрый, довольно точный и сравнительно простой методически. Однако могут быть и ошибки, связанные с появлением до сих пор не известного гена устойчивости. По сути, генотипирование — суррогат, а точный ответ об устойчивости дают только методы, связанные с культивированием, но они не везде доступны и отнимают много времени. Поэтому, отмечают авторы, важно ускорить методы фенотипического тестирования (один из вариантов с использованием MALDI-TOF см. в нашей новости). Время до результата (TTR, time to result) — это один из самых важных факторов: задержка адекватного лечения антибиотиками при тяжелых инфекциях увеличивает смертность.
Большинство клинических микробиологов не готовы принять системы, которые не идентифицируют микроорганизмы, а только определяют лекарственную устойчивость: врачам трудно принимать решения о терапии без точной информации о видовой принадлежности. В этом плане также перспективна спектрометрия MALDI-TOF — она дает информацию и о виде.
Особая группа проблем связана с государственным регулированием медицинских услуг. В каждой стране существуют свои правила и процедуры регистрации, поэтому разработчикам трудно удовлетворить всем требованиям одновременно. Здесь необходимы коммуникация между представителями государств и стандартизация требований. Кроме того, процедуры регуляции зачастую занимают много времени и оказываются слишком дорогостоящими для среднего и малого бизнеса.
Сейчас, как заявляет Европейский центр по предотвращению и контролю заболеваний, от трети до половины антимикробных препаратов назначается без необходимости, что способствует росту лекарственной устойчивости. Важная задача — просвещение населения и медработников, сокращение безответственного использования антибиотиков. Но тут тоже необходимы быстрые тесты, поскольку как пациенты, так и врачи склоняются к тому, чтобы начать прием антибиотиков как можно скорее.
Еще одна задача — сбор и представление информации о резистентных штаммах и эффективности антибиотиков. Хотелось бы предоставлять ее в режиме реального времени и для максимального количества образцов, тогда у больного будет больше шансов своевременно получить эффективное лечение.
Возможно, самая большая проблема на сегодняшний день — высокая стоимость современных быстрых диагностических тестов, которая не компенсируется их преимуществами и мешает им выйти на рынок.
Авторы перечислили основные барьеры для разработки и внедрения усовершенствованных систем тестирования на антимикробную чувствительность и предложили способы их преодоления. Кроме того, они представили общую схему разработки и внедрения диагностического продукта, от бизнес-предложения и изучения вопросов интеллектуальной собственности до коммерциализации, с комментариями к каждому этапу. «Несмотря на то, что малые и средние предприятия могут предлагать инновационные и гибкие подходы, крупным компаниям по диагностике, с необходимой критической массой и финансовой поддержкой, намного проще накопить опыт в области клинического развития, регуляторных аспектов и коммуникации и провести обширные (а значит, дорогостоящие) клинические исследования. Это важный барьер для проникновения на рынок новых продуктов, разработанных небольшими компаниями. Поэтому некоторые небольшие компании преуспели, наладив партнерские отношения с более крупными компаниями на заключительных этапах разработки. Следовательно, необходимы новые пути финансирования доклинических исследований и спонсорства для покрытия расходов, связанных с более формальными этапами развития», — говорится в заявлении.
Источник
Устойчивость к антибиотикам – что это?
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/06/ustojchivost-k-antibiotikam-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/06/ustojchivost-k-antibiotikam.jpg» title=»Устойчивость к антибиотикам — что это?»>
Алена Герасимова (Dalles) Разработчик сайта, редактор
- Запись опубликована: 27.06.2020
- Время чтения: 1 mins read
Устойчивость к антибиотикам – это термин, означающий потерю способности антибиотика уничтожать бактерии. Устойчивость к антибиотикам развивается под влиянием постоянных изменений (мутаций), которым подвергаются микроорганизмы.
Приобретенная устойчивость к антибиотикам возникает, когда, несмотря на использование антибиотика, бактерии продолжают размножаться, что требует применения нового антибиотика, более сильного, чем принимаемый ранее.
Откуда возникает устойчивость к антибиотикам?
Некоторые ученые называют изобретение антибиотиков величайшим открытием 20-го века. Они правы в этом, так как использование пенициллина положило конец многим инфекционным заболеваниям, которые являлись причиной высокой смертности в Европе. Сегодня антибиотики широко используются в борьбе с различными видами бактерий. К сожалению, доступность таких препаратов со временем превратилась в недостаток, спровоцировавший феномен, который называется устойчивостью к антибиотикам.
Антибиотиками злоупотребляют не только в ситуациях, когда нет показаний, например, принимая их при вирусных инфекциях или в легких случаях, не требующих антибиотикотерапии, но и неправильно выбирая препараты. Создание последующих поколений антибиотиков со все более широким спектром активности побуждает штаммы бактерий приобретать устойчивость к новым лекарствам и, таким образом, образуется замкнутый круг.
Классификация антибиотиков
Антибиотики – это группа антибактериальных препаратов, предназначенных для уничтожения или остановки размножения бактерий. Изначально антибиотики получали только естественным путем, сегодня существует огромное количество бактериостатиков, синтезированных в лабораториях (химиотерапевтические препараты). Из-за частой аллергии на пенициллин и устойчивости многочисленных бактериальных штаммов к его воздействию были разработаны различные группы антибиотиков без пенициллина.
Есть несколько категорий, по которым можно классифицировать антибиотики. Первая делит их на натуральные и синтетические. Основным критерием разделения является химическая структура антибиотиков, основанная на их механизме действия против бактерий.
- бета-лактамные антибиотики (пенициллины, цефалоспорины, карбапенемы, монобактамы);
- пептидные антибиотики;
- аминогликозиды;
- тетрациклин;
- макролиды.
Макролиды, тетрациклины, карбапенемы, цефалоспорины 3-го, 4-го и 5-го поколений и некоторые пенициллины обладают очень широким спектром действия. Они борются с так называемыми грамположительными и грамотрицательными бактериями, а также нетипичными микроорганизмами.
Разделение бактерий в соответствии с методом Грама основано на структуре бактериальной клеточной стенки и результирующем цвете, в который бактериальная клетка окрашивает при просмотре под микроскопом.
Цефалоспорины второго поколения, монобактамы и аминогликозиды ингибируют (подавляют) пролиферацию главным образом грамотрицательных бактерий, а цефалоспорины первого поколения предотвращают синтез грамположительных клеток.
Что такое устойчивость к антибиотикам?
Представьте себе ситуацию, когда программист борется с хакером. Чем более совершенную антивирусную программу создаст ИТ-специалист, тем более сложные вирусы будет создавать хакер. После каждого нового вируса, который проник в систему и не был обнаружен и удален существующей антивирусной программой, ИТ-специалист должен подготовить улучшенный алгоритм. Когда на рынке появляется последняя антивирусная программа, хакеры уже начинают работать над другим вирусом, устойчивым к этой программе.
Устойчивость к антибиотикам – аналогичное явление, только оно возникает, когда бактерии приобретают устойчивость. Чем лучше и эффективнее антибиотик представлен на рынке, тем больше бактерий сосредоточено на изменении своих свойств, нейтрализующих свойства нового препарата. Так возникает устойчивость к антибиотикам.
С этой целью бактерии могут изменять свой генетический материал таким образом, что устойчивость к новому антибиотику становится их постоянной характеристикой, передаваемой будущим поколениям. Если с последующей серией лекарств, созданных учеными, бактерии приобретают устойчивость к воздействиям, то мутации в бактериальной ДНК накапливаются и образуют бактериальные штаммы, устойчивые практически к большинству антибиотиков. Этот процесс является основой бактериальной устойчивости к антибиотикам.
Устойчивость к антибиотикам
Почему антибиотик может быть неэффективным?
Помимо описанного явления устойчивости бактерий к действию антибиотика, существует несколько причин, которые снижают эффективность препарата.
- Антибиотикотерапия неэффективна в борьбе с вирусами. Вирусные инфекции часто дают сходные с бактериальными заболеваниями симптомы. В случае сомнений причины болезни основанием для диагноза должно стать проведение лабораторных анализов, исключающих или подтверждающих бактериальную инфекцию. При вирусной этиологии антибиотики не помогут, так как они не борются с вирусами.
- Антибиотики широкого спектра действия снижают иммунитет . При бактериальном происхождении инфекции следует использовать соответствующий антибиотик. Но чаще всего врачи назначают антибиотики широкого спектра действия, например, амоксициллин, то есть те, которые борются с большинством бактерий. Эти препараты, в дополнение к несомненным преимуществам, имеют огромный недостаток – они также уничтожают здоровую бактериальную флору и, следовательно, ослабляют иммунитет.
- Разные бактерии лечатся разными антибиотиками . Несмотря на широкий спектр антибактериальной активности, вещество, содержащееся в антибиотике, может быть неэффективно в отношении возбудителя, вызвавшего инфекцию. Это частая ситуация при инфекциях, вызванных нетипичными бактериями или устойчивыми к определенной группе антибиотиков.
Чтобы исключить подобные ошибки и получить максимальный эффект от лечения антибиотиками, перед назначением препаратов врач должен направить пациента на анализы. После того как специалист убедится, что имеет дело с бактериями, ему потребуются результаты антибиотикограммы, показывающей, как конкретный возбудитель реагирует на разные препараты.
Только после получения результата чувствительности бактерий к антибиотикам врач должен рекомендовать конкретное лекарство.
Источник
Материалы конгрессов и конференций
IX РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
МНОЖЕСТВЕННАЯ ЛЕКАРСТВЕННАЯ УСТОЙЧИВОСТЬ ОПУХОЛИ И МЕХАНИЗМ-СПЕЦИФИЧЕСКАЯ ХИМИОТЕРАПИЯ: ПРОТИВОРЕЧИЕ?
А.А. Штиль
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Несмотря на достижения современной фармакологии, эффективность химиотерапии опухолей остается недостаточной. Это связано с важнейшей особенностью живых систем (в т.ч. опухолевых клеток) – способностью адаптироваться к изменениям внешней среды. Одно из проявлений такой пластичности – развитие в опухолевых клетках устойчивости к лекарственным препаратам. Множественная лекарственная устойчивость (МЛУ) злокачественных новообразований — сохранение клетками жизнеспособности в ответ на воздействие ряда лекарственных веществ — одна из основных причин прогрессирования болезни: опухоль нечувствительна к химиотерапии независимо от комбинации применяемых лекарств. Не будет преувеличением сказать, что МЛУ — наиболее подробно исследованный (и исследуемый) вид лекарственной устойчивости.
Основной механизм МЛУ — пониженное накопление препаратов в клетке, обусловленное активным выведением веществ в межклеточную среду [7]. Такой транспорт осуществляется белком плазматической мембраны Р гликопротеином (Pgp), кодируемым геном MDR1 (multidrug resistance 1) [6]. Этот механизм обеспечивает долговременное выживание клеток в присутствии веществ, различных по структуре и биологическому действию. Антрациклиновые антибиотики (адриамицин, даунорубицин), винкаалкалоиды (винкристин, винбластин), таксаны (таксол, таксотер), митоксантрон, ингибиторы топоизомераз (этопозид) — вот неполный перечень групп противоопухолевых препаратов, устойчивость к которым обусловлена Pgp-опосредованным транспортом. Увеличение количества иРНК MDR1 и Pgp часто служит фактором устойчивости многих типов опухолей к лечению [4, 9, 11, 15, 16, 20].
Рассмотрим два аспекта проблемы преодоления МЛУ: 1) срочное становление резистентности в ответ на действие противоопухолевых препаратов и 2) расширение роли Pgp за пределы транспортной функции и представление об этом белке как “универсальном” факторе выживания клетки. Анализ этих вопросов позволяет критически оценить подход к терапии новообразований, основанный на воздействии на конкретный механизм в опухолевой клетке.
МЛУ формируется в ответ на воздействие химиопрепаратов. Как клетка накапливает иРНК MDR1 и белок Pgp? Правомерно предположить, что устойчивые клетки несут несколько копий гена MDR1 (амплификация гена). Однако такой механизм не выявлен в опухолях человека. Следовательно, этот ген должен активироваться в ответ на внеклеточные сигналы. Действительно, однократного кратковременного (несколько часов) воздействия лекарств на культивируемые клетки достаточно, чтобы накопились иРНК MDR1 и функционирующий Pgp. Активация МЛУ подтверждена и в клинической ситуации, например, при интраоперационной перфузии адриамицином легких у больных с метастазами фибросаркомы [2]. МЛУ может развиваться в клетках различного тканевого происхождения в ответ на действие многих химиопрепаратов. В активации МЛУ участвуют многочисленные механизмы проведения внутриклеточных сигналов. Важно, что эти механизмы не уникальны для регуляции данного гена, а обеспечивают другие защитные реакции клетки на стресс.
Регуляция гена MDR1 (а значит и МЛУ) осуществляется на многих уровнях; возможны “обходы” сигналов, если тот или иной механизм не функционирует. Такая взаимозаменяемость механизмов надежно обеспечивает развитие МЛУ при действии лекарств.
Итак, МЛУ “с готовностью” развивается в клетках, переживших воздействие химиопрепаратов. Более того, активация гена MDR1 возрастает с увеличением концентрации токсина [5]. Поэтому применение высокодозных режимов лечения (оправданное потребностью повысить его эффективность) может вести к развитию МЛУ в выживших клетках. Снижение доз (с целью избежать развития МЛУ) заведомо неэффективно; концентрации же лекарств, требуемые для полной элиминации опухоли, могут оказаться выше допустимых для больного, что определяет предел эскалации доз.
МЛУ — компонент многофакторной защиты клетки. Казалось бы, один механизм устойчивости (даже обеспечивающий резистентность к нескольким веществам) не способен сильно ограничить возможности противоопухолевой терапии. Однако МЛУ оказывается не единственным фенотипом устойчивости, а Pgp — не только молекулярный транспортер. Исследования последних лет показывают, что Pgp может защищать клетку и помимо транспортной роли. Накапливаются свидетельства того, что Pgp может препятствовать гибели клетки, сопровождающейся активацией каспаз — протеолитических ферментов, вызывающих деградацию важнейших клеточных структур в ответ на действие токсинов [12]. Так Pgp выступает как один из механизмов анти-апоптоза.
Кроме того, Pgp — не единственный фактор защиты. Опухолевые клетки, пройдя отбор в организме на способность “ускользать” от контроля пролиферации и дифференцировки, накапливают механизмы, способствующие выживанию. Классические примеры — химерная тирозинкиназа Bcr-Abl в клетках острого лимфобластного лейкоза, хронического миелоидного лейкоза, стромальных опухолей желудочно-кишечного тракта, нарушения структуры и функции р53, рецепторов семейства фактора некроза опухоли и др. Это не удивительно: выдержали отбор те опухолевые клетки, в которых имеются (до лечения) молекулярные детерминанты выживаемости. Если в процессе химиотерапии в таких клетках накопится Pgp, то их резистентность будет действительно многофакторной. Таким образом, способность быстро приобретать МЛУ проявляется в уже устойчивых клетках. Как преодолеть эту плейотропную резистентность?
Механизм-специфическая химиотерапия и МЛУ. Возможно ли преодоление резистентности воздействием на конкретный механизм? Представляется дискутабельным доминирующее в современной литературе стремление к непременной идентификации клеточных мишеней в надежде на создание конкретного для отдельной опухоли (или, шире, клинической ситуации) подхода к лечению (mechanism-based therapy). Это стремление продиктовано необходимостью добиться максимального противоопухолевого эффекта при возможно меньшей обще резорбтивной токсичности. Мишенями направленной терапии служат нарушения, чаще встречаемые в опухолях (но не всегда специфичные для новообразований), чем в интактных клетках. Такие нарушения могут быть обусловлены изменениями структуры генов (например, инактивация функции р53 за счет мутаций или делеций гена) и/или эпигенетической дизрегуляцией экспрессии онкогенов и антионкогенов. Несомненно, детальное изучение механизмов выживания и смерти опухолевых клеток плодотворно и для фундаментальной биологии, и для практической онкологии. Уже сегодня в клинике применяются препараты-антагонисты конкретных механизмов регуляции пролиферации, в частности, ингибитор эпидермального фактора роста ZD1839 (Иресса) и блокатор тирозинкиназы Bcr-Abl STI-571 (Гливек). Однако безупречен ли подход к терапии опухолей, основанный на взаимодействии препарата с одной клеточной мишенью? Всегда ли целесообразно уменьшать обще резорбтивный эффект химиотерапии за счет прицельной манипуляции с конкретной структурой опухолевой клетки? Не послужит ли такая индивидуализация лечения сужению терапевтического спектра и снижению эффективности препарата?
Во-первых, специфичность взаимодействия малых молекул — а именно они составляют подавляющее большинство современных средств противоопухолевой терапии — с биологическими структурами относительна. Например, ингибиторы того или иного семейства протеинкиназ реагируют и с другими киназами. Ингибирование фермента предполагает взаимодействие малой молекулы с участком (участками) молекулы энзима, существенным для ее активности, в частности, с каталитическим сайтом или сайтом связывания АТФ. Однако структура этих районов редко бывает уникальной для конкретного фермента. Кроме того, проникновение в клетку чужеродного химического соединения вызовет ряд общих стрессорных реакций. Эти реакции (а они неизбежны как ответ на раздражитель!) в клетке налагаются на эффект взаимодействия потенциального модулятора с его основной мишенью. Еще более проблематична оценка эффекта ингибитора на уровне организма.
Второе возражение связано с биологической гетерогенностью опухоли. Экспрессия того или иного механизма может широко варьировать между участками опухоли. Поэтому неодинаковой будет и чувствительность к лечебному препарату отдельных клеток или клеток в разных зонах новообразования. Если так, то применение узко специфического агента предоставит селективное преимущество в выживании клеткам, в которых механизм-мишень экспрессирован слабее. Но тогда остаточная опухоль будет резистентна к препарату из-за отсутствия его мишени в клетках, т.е. эффект лечения оказывается заведомо неполным. Предположение же о том, что мишень, против которой действует препарат, есть единственный или главный фактор злокачественности в данной опухоли, может оказаться неправомерным. Ведь основные черты злокачественной трансформации — неконтролируемая пролиферация, способность к выживанию и делению без контакта с адгезивным субстратом, инвазия, метастазирование — обеспечиваются многочисленными механизмами, и блокирование одного фактора приведет к смене фенотипов резидуальной опухоли, но не обязательно к ее исчезновению. Как быть в случаях рецидивов опухоли в результате развития устойчивости, например, к STI571, благодаря выживанию клеток с мутацией в киназном домене Bcr-Abl [24]? А ведь МЛУ может развиваться быстро в ответ на воздействие многих веществ (см. выше); тогда рецидивная опухоль окажется резистентной и к STI571, и к ряду других препаратов.
Наконец, третье, важнейшее возражение, возвращает нас к поставленной в начале статьи проблеме необычайной пластичности опухолевой клетки как биологической системы. Функции клетки, нарушенные при злокачественном росте — пролиферация, смена фаз клеточного цикла и др. — регулируются чрезвычайно “надежно”. Мы представили это многообразие регуляторных механизмов на примере становления МЛУ; и преодоление этого фенотипа путем обхода механизмов устойчивости также обосновано сложностью (многочисленностью, взаимозаменяемостью) процессов, обеспечивающих выживание клеток. В ряде ситуаций удается блокировать приобретение клетками Pgp-опосредованной МЛУ, воздействуя на конкретный механизм [5, 12, 27]. Однако всегда остается возможность ускользания опухолевой клетки от терапевтических воздействий. Такая возможность может возрастать при прогрессии опухоли. Важнейшая особенность онкологического заболевания — именно развертывание каскадов регуляции клетки. “Вооружаясь” таким образом, клетка и получает способность ускользать от систем биологического контроля.
Приведенные соображения не умаляют значимости терапии опухолей, ориентированной на конкретный механизм. Однако постоянная возможность (или угроза) “ускользания” опухоли заставляет критически оценить стремление этой стратегии к универсальности. Многофакторная устойчивость — результат постоянного ускользания, приобретения опухолью новых возможностей надежного регулирования функций, важных для ее выживания; эта способность злокачественных клеток предполагает, что оптимизация противоопухолевой терапии может быть достигнута сочетанием механизм-специфических воздействий с активацией путей гибели, сохраняющих функцию при формировании резистентности.
Одним из таких путей является нарушение целостности плазматической мембраны. Некроз не нарушен в Pgp-экспрессирующих клетках с МЛУ [13, 25, 26]. При некрозе быстро произойдут повреждения практически любых субклеточных структур, в отличие от апоптотических каскадов, сопровождающихся последовательным расщеплением субстратов и строгой специфичностью взаимодействия протеаз с мишенями [29]. Блокирование одного или нескольких звеньев апоптотических каскадов прервет передачу сигналов на нижележащие механизмы, результатом чего станет ускользание клетки от гибели и, в итоге, формирование устойчивости. Такая возможность не исключена при формировании многофакторной резистентности, в том числе Pgp-опосредованной МЛУ. Еще и по этой причине для борьбы с МЛУ желательно, чтобы механизмы смерти были множественными и включали активацию каспаз и других протеаз (лизосомальных, протеосомальных, ядерных), путей потенцирования сигнала (митохондриальный путь) и нарушения проницаемости мембран. Таким образом, терапевтическими мишенями выступают не только отдельные молекулы, но и надмолекулярные комплексы (органеллы, плазматическая мембрана).
МЛУ — не единственный фенотип устойчивости клеток к ксенобиотикам, а Pgp — не единственный механизм, обеспечивающий выживание в присутствии токсинов. Сегодня не представляется возможным предсказать, совокупность каких факторов резистентности (транспорт веществ через плазматическую мембрану, внутриклеточный катаболизм токсинов, антиоксидантная защита и др.) определит неэффективность конкретного лечебного режима в отношении конкретной опухоли. Блокирование отдельного “специфического” механизма может оказаться заведомо недостаточным. Чем больше механизмов смерти удастся активировать в резистентных клетках, чем менее зависима такая стратегия от динамичного “молекулярного профиля” опухоли, тем надежнее конечный результат — преодоление многофакторной резистентности.
1. Трунова С.А. Инициация вхождения в митоз и проблема избыточности функций митотических циклинов // XIV Всероссийский симпозиум “Структура и функции клеточного ядра”. Санкт-Петербург, 15-17 октября 2002 г.: Цитология. — 2002. — Т. 44. С. 910.
2. Abolhoda A., Wilson A.E., Ross H. et al. Rapid activation of MDR1 gene expression in human metastatic sarcoma after in vivo exposure to doxorubicin. // Clin. Cancer Res. — 1999. — Vol. 5. — P. 3352-3356.
3. Ambudkar S.V., Dey S., Hrycyna C.A. et al. Biochemical, cellular, and pharmacological aspects of the multidrug transporter // Annu. Rev. Pharmacol. Toxicol. — 1999. — Vol. 39. — P. 361-398.
4. Arceci R.J. Clinical significance of P-glycoprotein in multidrug resistance malignancies // Blood. 1993. — Vol. 81. — P. 2215-2222.
5. Chaudhary P.M., Roninson I.B. Induction of multidrug resistance in human cells by transient exposure to different chemotherapeutic drugs // J. Natl. Cancer Inst. — 1993. — Vol. 85. — P. 632-639.
6. Chen C.-J., Chin J.E., Ueda K. et al. Internal duplication and homology with bacterial transport proteins in the mdr1 (P-glycoprotein) gene from multidrug-resistant human cells // Cell. — 1986. — Vol. 47. — P. 381-389.
7. Dano K. Active outward transport of daunorubicin in resistant Ehrlich ascites tumor cells // Biochim. Biophys. Acta. — 1973. — Vol. 323. — P. 466-483.
8. Fang B., Roth J.A. Tumor-suppressing gene therapy // Cancer Biol. Ther. 2003. — Vol. 2. — P. S115-S121.
9. Goldstein L.J., Galski H., Fojo A. et al. Expression of a multidrug resistance gene in human cancers // J.Natl. Cancer Inst. 1989. — Vol. 81. — P. 116-124.
10. de Graaf D., Sharma R.C., Mechetner E.B. et al. P-glycoprotein confers methotrexate resistance in 3T6 cells with deficient carrier-mediated methotrexate uptake // Proc.Natl. Acad. Sci. USA. — 1996. — Vol. 93. — P. 1238-1242.
11. Hegewisch-Becker S., Hossfeld D.K. The MDR phenotype in hematologic malignancies: prognostic relevance and future perspectives // Ann. Hematol. 1996. — Vol. 72. — P. 105-117.
12. Johnstone R.W., Cretney E., Smyth M.J. P-glycoprotein protects leukemia cells against caspase-dependent, but not caspase-independent, cell death // Blood. 1999. — Vol. 93. — P. 1075-1085.
13. Johnstone R.W., Taiinton K.M., Rueffli A.A. et al. P-glycoprotein does not protect cells against cytolysis induced by pore-forming proteins // J.Biol. Chem. 2001. — Vol. 276 — P. 16667-16673.
14. Juliano R., Ling V. A surface glycoprotein modulating drug permeability in Chinese hamster ovary cell mutants // Biochim. Biophys. Acta. — 1976. — Vol. 455. — P. 152-162.
15. Leith C.P., Kopecky K.L., Godwin J. et al. Acute myeloid leukemia in the elderly: assessment of multidrug resistance (MDR1) and cytogenetics distinguishes biologic subgroups with remarkably distinct responses to standard chemotherapy. A Southwest Oncology Group study // Blood. 1997. — Vol. 89. — P. 3323-3329.
16. Marie J.P. Drug resistance in hematologic malignancies // Curr. Opin. Oncol. 2001. — Vol. 13. — P. 463-469.
17. O’Dwyer M.E., Mauro M.J., Druker B.J. STI571 as a targeted therapy for CML // Cancer Invest. 2003. — Vol. 21. — P. 429-438.
18. Ogretmen B., Hannun Y.A. Updates on functions of ceramide in chemotherapy-induced cell death and in multidrug resistance // Drug Resist. Updat. 2001. — Vol. 4. — P. 368-377.
19. Pallares-Trujillo J., Lopez-Soriano F., Argiles J.M. Lipids: A key role in multidrug resistance? // Int.J.Oncol. — 2000. — Vol. 16. — P.783-798.
20. del Poeta G., Stasi R., Aronica G. et al. Clinical relevance of P-glycoprotein expression in de novo acute myeloid leukemia // Blood. 1996. — Vol. 87. — P. 1997-2004.
21. Reddy A., Kaelin W.G.Jr. Using cancer genetics to guide the selection of anticancer drug targets // Curr. Opin. Pharmacol. — 2002. — Vol. 2. — P. 366-373.
22. Russello S.V., Shore S.K. Src in human carcinogenesis // Front Biosci. 2003. — Vol. 8. — P.1068-1073.
23. Sattler M., Scheijen B., Weisberg E., Griffin J.D. // Adv. Exp. Med. Biol. 2003. — Vol. 532. — P.121-140.
24. Shah N.P., Sawyers C.L. Mechanisms of resistance to STI571 in Philadelphia chromosome-associated leukemias // Oncogene. — 2003. — Vol. 22. — P. 7389-7395.
25. Shtil A., Turner J., Durfee J. et al. Cytokine-based tumor cell vaccine is equally effective against parental and isogenic multidrug-resistant myeloma cells: the role of cytotoxic T-lymphocytes // Blood. — 1999. — Vol. 93. — P. 1831-1837.
26. Shtil A., Turner J., Dalton W., Yu H. Alternative pathways of cell death to circumvent pleiotropic resistance in myeloma cells: role of cytotoxic T-lymphocytes // Leukemia and Lymphoma. — 2000. Vol. 38. — P. 59-70.
27. Shtil A.A. Emergence of multidrug resistance in leukemia cells during chemotherapy: mechanisms and prevention. // J.Hematother. Stem Cell Res. — 2002. — Vol. 11. — P. 231-241.
28. Tamura K, Fukuoka M. Molecular target-based cancer therapy: tyrosine kinase inhibitors. // Int. J. Clin. Oncol. 2003. — Vol. 8. — P. 207-211.
29. Thornberry N.A., Lazebnik Y. Caspases: enemies within. //Science. — 1998. — Vol. 281(5381). — P.1312-1316.
30. Warmuth M., Damoiseaux R., Liu Y. et al. SRC family kinases: potential targets for the treatment of human cancer and leukemia. // Curr. Pharm. Des. 2003. — Vol. 9. — P. 2043-2059.
Источник


