- Что такое период полувыведения лекарственного вещества
- Что такое период полувыведения лекарственного вещества
- Новости синтона
- Подпишитесь на нашу рассылку!
- Руководство по психофармакотерапии
- Список сокращений.
- Предисловие к изданию на русском языке.
- Глава 1. Введение в психофармакологию.
- Перед началом лечения.
- Применение психофармакотерапии.
- Прекращение психофармакотерапии.
- Прочие вопросы психофармакологии.
- Глава 2. Антипсихотические препараты.
Что такое период полувыведения лекарственного вещества
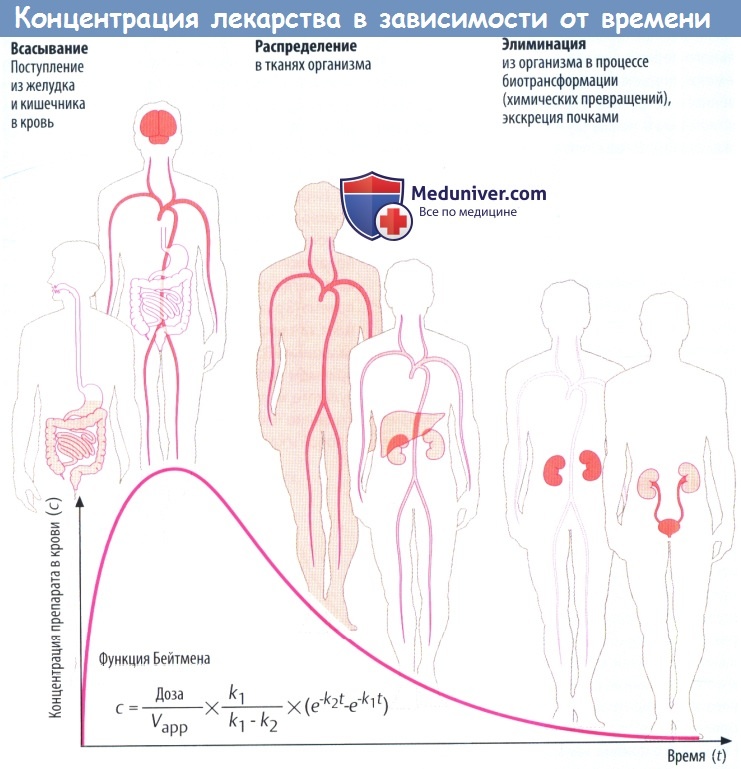
Такие процессы, как всасывание и выведение, обладают экспоненциальными характеристиками. В отношении всасывания это следует из простого факта: количество препарата, перемещающегося за единицу времени, зависит от разности концентраций (градиента) на границе двух тканей (закон Фика).
В процессе всасывания из пищеварительного тракта содержимое кишечника и кровь представляют собой ткани с изначально высокой и низкой концентрациями соответственно. При выведении лекарственного вещества через почки экскреция часто зависит от скорости клубочковой фильтрации, т. е. от количества препарата, попавшего в первичную мочу.
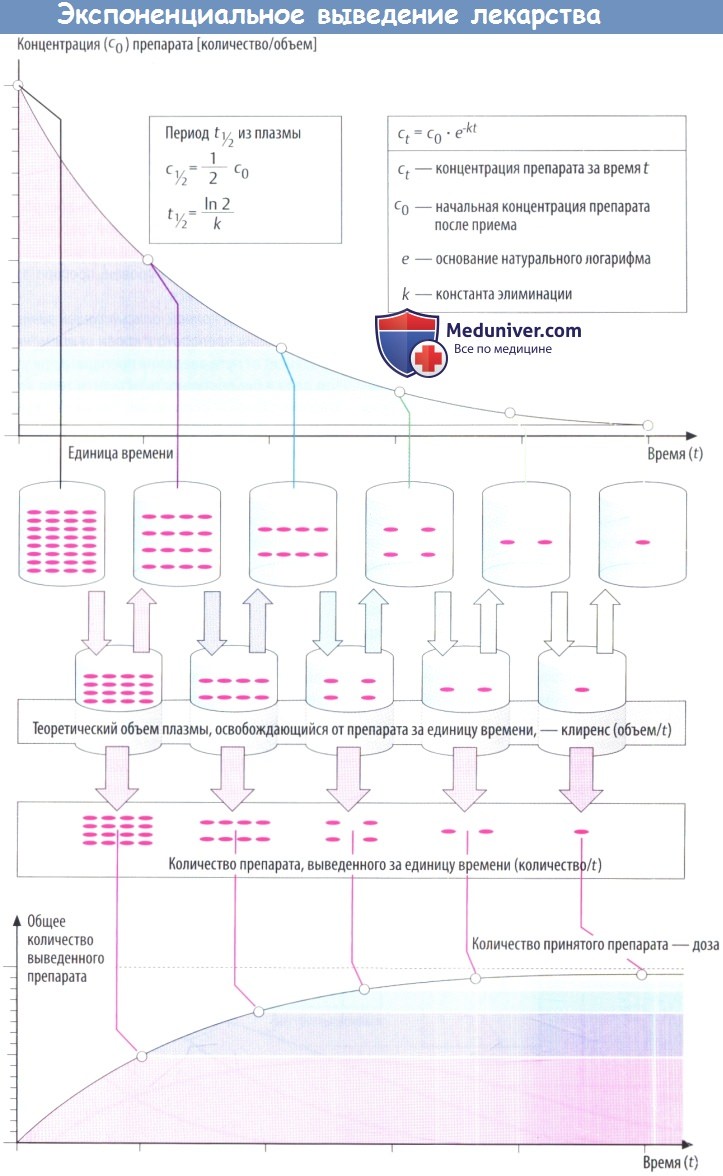
По мере снижения концентрации в крови количество лекарственного вещества, экскретируемого через почки за единицу времени, уменьшается. В результате происходит экспоненциальное снижение, показанное на рисунке ниже. Время экспоненциальногоснижения — постоянный интервал, в течение которого концентрация снижается в 2 раза.
Этот интервал представляет собой период полувыведения (t1/2) и связан с константой скорости элиминации (k) уравнением: t1/2 = (ln2)/k. Эти два параметра вместе с исходной концентрацией (с0) описывают скорость реакции первого порядка (экспоненциальную).
Поскольку эта скорость постоянная, она дает возможность вычислить объем плазмы, освобожденной от лекарственного вещества, учитывая, что оставшееся количество не распределено равномерно в общем объеме плазмы (условие, невозможное в реальности). Теоретический объем плазмы, освобождающейся от лекарственного вещества за единицу времени, называется клиренсом.
В зависимости от того, снижается концентрация в плазме в результате экскреции с мочой либо в результате разрушения в процессе метаболизма, клиренс называют почечным или печеночным. Почечный и печеночный клиренсы суммируются, образуя общий клиренс (Cltot) в случае, если препараты выводятся в неизмененном виде через почки и подвергаются биотрансформации в печени.
Cltot представляет собой сумму всех процессов, участвующих в выведении; он связан с периодом полувыведения (t1/2) и объемом распределения препарата (Vapp) формулой:
Чем меньше объем распределения и чем больше общий клиренс, тем короче период полувыведения.
Для препаратов, выводимых почками в неизмененном виде, t1/2 можно вычислить на основании кумулятивной экскреции с мочой; итоговое общее количество выведенного препарата соответствует количеству всосавшегося препарата.
Печеночная элиминация происходит по экспоненте, т. к. ферменты, катализирующие реакции метаболизма, действуют в квазилинейной области своей кривой активности концентрации; следовательно, количество вещества, подвергшегося метаболизму за единицу времени, уменьшается параллельно снижению концентрации в крови.
Самое известное исключение из экспоненциального закона — выведение алкоголя (этанола), которое происходит по линейному закону (кинетика нулевого порядка), во всяком случае, при концентрации в крови менее 0,02%. Это происходит потому, что лимитирующий скорость фермент алкогольдегидрогеназа достигает полунасыщения при очень низких концентрациях вещества — примерно 80 мг/л (0,008%).
Таким образом, при концентрации этанола в крови на уровне примерно 0,02% скорость реакции выходит на плато, при концентрациях выше этого уровня количество лекарственного вещества, выведенного за единицу времени, остается постоянным.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Что такое период полувыведения лекарственного вещества
В распределении анестетика важную роль играет также связывание с белками плазмы, наибольшее значение из которых имеют альбумины. Связанная с белками часть препарата образует депо и находится в равновесии с растворенной в плазме частью, но лишь растворенная часть препарата (не связанная с белками плазмы) распределяется в тканях и оказывает фармакологическое действие. Различные прераты при одновременном введении вместе конкурируют за места связывания с белками плазмы.
В результате концентрация свободной фракции отдельных препаратов в плазме может возрасти, что проявляется признаками передозировки. Аналогичный эффект может вызвать уменьшение белково-связывающей емкости плазмы при заболеваниях печени и почек, а также алиментарной белковой недостаточности. В этих случаях дозу анестетика можно уменьшить. Еше большее практическое значение имеет зависимость связывания препарата с белками плазмы от скорости его введения.
При быстром введение препарата свободная его фракция (т.е. экологически активная часть) увеличиваются. Во избежание острой передозировки внутривенные анестетики вводят можно и с учетом достигаемого эффекта.|
Элиминация. Внутривенные анестетики подвергаются биотрансформации. Отчасти метаболизируются или инактивируются в печени и выводятся с желчью, почками (гепаторенальный клиренс). Лишь небольшая часть препаратов выдится из организма в неизмененном виде. Метаболизация с участием фермнтов более длительный процесс, чем вывод через легкие. Поэтому время элиминации даже современных внутривенных аанестетиков короткого действия больше ингаляционных анестетиков.
Период полувыведення. При системном применении фармакологических препаратов различают три объема (пространства, камеры) распределения: 1. Плазма крови, составляющая 4 объема тела (центральный объем).
2. Интерстициальное пространство (15%).
3. Внутриклеточный объем (40%). Поскольку эндотелий большинства органов содержит межклеточные поры или фенестрирован, то проникновение веществ через него происходит относительно беспрепятственно и зависит только от размера молекул. В связи с этим представляется привлекательной концепция, согласной которой интерстициальное пространство и плазма с точки зрения фармакокинетики рассматриваются как единое (внеклеточное) пространство.
Для активного проникновения внутривенного анестетика решающее значение имеет скорость, с которой анестетик диффундирует из центрального объема (плазма крови) в более глубокие пространства головного мозга. Математически этот процесс можно описать уравнением, рассчитав равновесный период полувыведения 11/2 keO. Он позволяет судить о начале действия препарата. Время, в течение которого происходит начальное распределение препарата по всему организму, обозначают как период полураспределения (tl/2a).
После завершения распределения между концентрациями препарата в отдельных пространствах устанавливается устойчивое равновесие (steady state). Дальнейшая динамика концентрации определяется в первую очередь процессом элиминации анестетика (клиренс плазмы). Время, необходимое для уменьшения концентрации вещества в плазме до половины исходного уровня, называют периодом полувыведения (tl/2p). Снижение концентрации, как правило, описывается логарифмической зависимостью.
Период полувыведения вещества не следует отождествлять с длительностью его действия (см. выше)! Чтобы рассчитать элиминацию при непрерывном поступлении препарата (ТВА, ИУЦК), основываются на контекстно-чувствительном периоде полувыведения. Под контекстно-чувствительным периодом полувыведения понимают время, за которое концентрация анестетика в плазме крови после прекращения внутривенной его инфузии уменьшается на 50%. Элиминационный период полувыведения анестетика определяют исходя из его плазменного клиренса и объема распределения. Этот период тем короче, чем больше клиренс и чем меньше объем распределения.
Источник
Новости синтона
Новое на сайте
Подпишитесь
на нашу рассылку!
Руководство по психофармакотерапии
Список сокращений.
DSM — руководство по диагностике и статистике психических заболеваний
FDA — управление по контролю за лекарственными средствами и пищевыми продуктами
АДГ — антидиуретичеcкий гормон
ГТР — генерализованное тревожное расстройство
ЗНС — злокачественный нейролептический синдром
ИМАО — ингибитор моноаминооксидазы
КГС-3β — 3β-киназа гликогенсинтазы
НПВП — нестероидные противовоспалительные препараты
OAK — общий анализ крови
ОКР — обсессивно-компульсивное расстройство
ПТСР — посттравматическое стрессовое расстройство
СГФ — скорость гломерулярной фильтрации
СИОЗС — селективные ингибиторы обратного захвата серотонина
СНВГ — синдром нарушения внимания с гиперактивностью
ТСГ — тиреоид-стимулирующий гормон
ТЦА — трициклические антидепрессанты
ЭПС — экстрапирамидные симптомы
Предисловие к изданию на русском языке.
Предлагаемая вниманию читателей работа по сути является третьим, после уже устаревшего справочного руководства Е. Шейдера «Психиатрия» (Москва, Практика, 1998) и блестящей книги Ф. Яничак, Дж. Дэвис, Ш. Прескорн, Ф. Айд мл. «Принципы и практика психофармакотерапии» (Киев, Ника-Центр, 1999), изданием на русском языке книги американских авторов, посвященной вопросам клинического применения современных психофармакологических препаратов.
В отличие от последней книги, которая больше посвящена методологии, тщательному анализу и систематизации научных доказательств эффективности психофармакотерапии, настоящее руководство имеет большую практическую направленность и фактически представляет собой справочное пособие по применению различных классов применяемых в психиатрии лекарственных препаратов (антипсихотиков, антидепрессантов, нормотимиков, анксиолитиков, психостимуляторов и некоторых других средств). При этом в каждой главе систематически и в сравнительном аспекте по отдельным препаратам излагаются основные фармакологические данные (механизм действия, фармакокинетика), показания к применению и методика применения, особенности использования в пожилом возрасте, при беременности и лактации, побочные эффекты, лекарственные взаимодействия, передозировка и другие полезные в повседневной клинической практике сведения. Информация представлена в достаточно сжатом и наглядном виде, но с учетом современных методов доказательной медицины. В первую очередь приводятся те методы лечения и препараты, эффективность которых была доказана мета-анализом нескольких рандомизированных контролируемых исследований. Затем последовательно излагаются и другие методы терапии, не получившие столь весомой доказательной базы, в том числе новые (экспериментальные) и старые, но хорошо зарекомендовавшие себя на практике, лекарственные средства. Это позволило авторам кратко информировать врача о практически всех имеющихся в настоящее время в его распоряжении возможностях фармакотерапии тех или иных психических расстройств, оставляя за ним право выбора в соответствии с надежностью приведенных доказательств.
Как и все американские издания, книга отличается крайним прагматизмом с приоритетом количественной оценки, часто в ущерб качественной, и не всегда опирается на клиническую дифференциацию показаний и другие принципы клинического подхода к психофармакотерапии, характерные для европейской и отечественной психиатрии. Используемая авторами диагностическая система (DSM-IV-TR) основана на операциональных критериях, не ориентированных на дифференцирование отдельных клинических синдромов и оттенков состояния, что подчас является определяющим для правильного выбора клинической мишени для того или иного препарата. В этих условиях выбор препарата осуществляется почти исключительно на основании профиля его побочных эффектов, что не отвечает клиническим потребностям врача.
Тем не менее предлагаемая книга безусловно представляет интерес для широкого круга специалистов, работающих с психически больными, и не только потому, что в ней содержится масса практических сведений справочного характера, но и потому, что эти сведения корректно и методически строго систематизированы и позволяют познакомиться нашим врачам с оригинальным и прагматичным взглядом на фармакотерапию психических заболеваний современных американских психиатров.
Книга выдержала 4 издания в США, настоящее вышло в 2001 году. За прошедшее время появились новые научные данные, новые препараты, новые лекарственные формы и т. д. Там, где это возможно, мы старались обновить имеющуюся информацию в виде примечаний. Прежде всего это касалось отдельных препаратов, в том числе торговых наименований, лекарственных форм и показаний, зарегистрированных в Российской Федерации, а также побочных эффектов и лекарственных взаимодействий. Большинство предлагаемых в книге справочных таблиц были дополнены отечественными и зарубежными, не упомянутыми авторами, но разрешенными к применению в России препаратами, чтобы практический врач имел, по возможности, наиболее полную картину имеющегося в его распоряжении арсенала психотропных средств. Кроме того, комментарии давались в отношении спорных вопросов или имеющихся оригинальных отечественных данных. Надеюсь, что большая работа, проделанная по переводу и редактированию настоящего руководства, окажется полезной для наших врачей и будет способствовать повышению эффективности и качества лечения психически больных.
Руководитель Научно-методического центра терапии психических заболеваний МЗ РФ,
профессор С. Н. Мосолов
Глава 1. Введение в психофармакологию.
Практическая психофармакология — крайне сложная область. Психические расстройства часто имеют непредсказуемое течение, коморбидные соматические расстройства или симптомы, которые нарушают контакт с пациентом (например, вследствие отрицания болезни, подозрительности или различных нарушений личности). Кроме того, у многих больных проводимое лечение недостаточно эффективно. Хотя при многих заболеваниях, таких как большой депрессивный эпизод, биполярное расстройство, паническое расстройство, фармакотерапия помогает большинству пациентов, у некоторых больных остается резидуальная симптоматика или развивается резистентность к терапии. При других заболеваниях, таких как шизофрения, проводимая терапия является лишь паллиативной и может приводить только к устранению отдельных симптомов. Искусство врача заключается в умении выбрать правильный баланс между фармакотерапевтическими и психотерапевтическими подходами. Квалифицированное применение имеющихся в настоящее время психотропных лекарственных препаратов значительно повышает вероятность благоприятного исхода при многих психических расстройствах.
Хотя психофармакотерапия является наиболее эффективным методом лечения большинства психических расстройств (например, биполярного расстройства, панических атак и большого депрессивного эпизода), она должна проводиться с соответствующей психотерапией. Например, некоторые больные, страдающие паническим расстройством с агорафобией, смогли избавиться при помощи лекарственной терапии от панических атак, но без поведенческой психотерапии не могли справиться с агорафобией. Депрессии хорошо реагируют на тимоаналептическую терапию, но при комбинированном применении с психотерапией развивается более полноценная и быстрая ремиссия. С другой стороны, возможны ситуации (например, маниакальные состояния), при которых психотерапия может быть неэффективна до момента ухода острых симптомов.
В целом предпочтение только фармакологической или психосоциальной составляющей терапии в реальной психиатрической практике неэффективно и приносит пациенту мало пользы. Стандарт лечения психических расстройств предусматривает точную диагностическую оценку перед началом применения терапии, а эффективность выбранной терапии должна быть документально подтверждена. Этот стандарт оставляет широкие возможности для принятия клинического решения. Клиницист должен осознавать, что полученные в контролируемых исследованиях результаты не всегда оправданы в реальных клинических ситуациях. Больные, отбираемые в научные исследования, составляют лишь часть всех больных, нуждающихся в лечении. Обычно они относительно молоды, не получают другой лекарственной терапии, не имеют серьезных заболеваний и согласны получать плацебо в течение нескольких недель.
Высказанные противоречия подтверждаются коллективным опытом разработки Международных стандартов лечения психических расстройств. После долгих дебатов выяснилось, что за исключением первого этапа алгоритма веских научных данных в пользу последующего выбора терапии нет. Очень немного исследований посвящались неудачам начала терапии, резистентным больным или курсам лечения, прерванным из-за возникновения побочных эффектов. Для панического расстройства, например, большинство доступных в литературе исследований поддерживало использование имипрамина в качестве первого курса терапии. Собравшиеся эксперты, однако, решили рекомендовать ингибиторы обратного захвата серотонина, несмотря на то, что контролируемых исследований в то время было еще недостаточно. В итоге специалисты решили создать алгоритм, фактически отражающий их клиническое предпочтение, но дополнительно определили степень доказательности подтверждения того или иного выбора: «А» — подтвержденные в нескольких контролируемых исследованиях; «В» — подтвержденные в открытых и пилотных (предварительных) исследованиях и «С» — описанные в виде отдельных клинических наблюдений. Этот компромисс соответствует философии настоящей книги — представить клиническую психофармакологию с позиции реальной практики, используя в качестве информационных источников строгие научные данные.
В духе практицизма вначале мы излагаем основные принципы терапии, которыми следует руководствоваться при лечении психических заболеваний и которые являются общими при проведении любой психофармакотерапии.
Перед началом лечения.
1. Перед назначением психотропной терапии важно быть уверенным в диагнозе. Если диагноз не был установлен, должны быть определены основные диагностические гипотезы и разработан систематический подход для выяснения диагноза. Например, депрессивные, психотические или кататонические состояния могут быть следствием не только психического, но и соматического заболевания, злоупотребления психоактивными веществами или побочного действия проводимой психофармакотерапии.
2. Перед назначением психотропной терапии важно знать соматические заболевания или лекарственные взаимодействия, которые:
а) могут быть ответственными за развитие психических симптомов;
б) могут увеличивать токсичность назначенных лекарственных средств (например, диуретики или нестероидные противовоспалительные препараты могут увеличивать содержание лития в крови) или
в) снижать эффективность проводимой терапии (например, карбамазепин может ускорять метаболизм некоторых трициклических антидепрессантов).
3. Необходимо осознавать возможные последствия злоупотребления алкоголем или другими психоактивными веществами, которые могут исказить результаты лечения. Поэтому перед началом терапии необходимо провести детоксикационные мероприятия.
4. Перед назначением психофармакотерапии необходимо обязательно определить симптомы-мишени (например, нарушения сна, панические атаки или галлюцинации), за которыми нужно следить во время курса терапии для контроля успешности лечения. Не менее важно контролировать изменения качества жизни пациента (например, удовлетворение домашней и семейной жизнью, работоспособность, а также общее ощущение благополучия). В качестве альтернативы для больных, которые не могут описать свои собственные симптомы (например, при деменции или остром психозе) можно обращаться к родственникам с просьбой оценить его поведение (например, по простой ежедневной шкале из 10 пунктов). Определение симптомов-мишеней и оценка качества жизни особенно важны при эмпирическом (пробном) назначении препарата, когда диагноз неясен.
5. Принципы подбора оптимального лекарственного препарата приведены в соответствующих разделах настоящей книги. Однако, если прежнее лечение было эффективным и хорошо переносилось пациентом, то разумно и клинически оправдано использовать те же препараты, даже если имеются более современные средства.
6. Если требуется коррекция диагноза или терапии, необходимо проводить дополнительные консультации со специалистами. Реакция врача на рекомендации консультантов (включая согласие или несогласие) должна быть документально оформлена.
Применение психофармакотерапии.
1. При выборе определенного лекарственного средства следует проводить полный его курс в адекватной дозировке и продолжительности лечения, чтобы при отсутствии улучшения симптоматики не возникала необходимость снова возвращаться к данному препарату. Неадекватная дозировка и продолжительность лечения являются основными причинами неэффективности лечения антидепрессантами у больных с правильно установленным диагнозом.
2. Следует предвидеть возможность возникновения побочных эффектов и своевременно предупреждать пациентов об этом (например, о дневной сонливости при применении бензодиазепинов, сухости во рту или нарушении аккомодации при применении трициклических антидепрессантов). Нужно четко представлять себе, при каких побочных эффектах следует успокоить больного (например, при сухости во рту), назначить дополнительное лечение (например, при паркинсонизме, вызванном нейролептиками) или прекратить терапию (например, при интерстициальном нефрите, вызванном применением лития). Необходимо разъяснять больному, что побочные эффекты некоторых психотропных средств могут быть похожими на симптомы тех нарушений, которые вызваны заболеванием (например, нейролептическая акатизия может проявляться в виде ажитации, а акинезия бывает трудно отличима от кататонии).
3. Следует по возможности соблюдать простую схему приема препаратов, как для улучшения соблюдения больным режима терапии так и для снижения риска токсичных взаимодействий. Соблюдение режима терапии нередко улучшается, если используются простые схемы приема (например, литий один или два раза в день вместо трех или четырех раз в день), а также, если с больным обсуждаются длительность и предполагаемая эффективность курса лечения или жалобы на побочные эффекты. Больные с психотической симптоматикой, слабоумием или заторможенностью для соблюдения режима терапии могут нуждаться в тщательной опеке.
4. Дозу препарата следует подбирать таким образом, чтобы на каждой стадии заболевания она была минимальной эффективной. Особенно это касается психотических расстройств, при которых требования к дозировке часто меняются со временем. Например, при шизофрении доза антипсихотика, требующаяся для лечения обострений, выше, чем при проведении длительной противорецидивной терапии.
5. У пациентов пожилого возраста лечение следует начинать с низких доз. Изменения дозировки должны быть менее частыми, так как для достижения стабильной концентрации препарата требуется больше времени.
6. Динамическое наблюдение за больным включает оценку эффективности лечения, выявление и коррекцию побочных эффектов и клинически значимых последствий стрессовых событий, сопутствующих соматических и психических нарушений, мониторинг лабораторных показателей и при необходимости изменение схемы терапии.
Прекращение психофармакотерапии.
1. Продолжение неэффективного курса терапии часто ведет к накоплению препаратов в организме, появлению побочных симптомов и дополнительным расходам. В некоторых случаях эффективна комбинированная терапия. Однако, если необходимость проведения дальнейшей терапии отсутствует, то ее целесообразно отменить. Иногда бывает сложно правильно оценить эффективность терапии, особенно если лечащий врач не следил за динамикой симптомов-мишеней с начала лечения.
2. Даже после достижения отчетливого терапевтического эффекта отмена психотропных препаратов в большинстве случаев зависит от особенностей течения конкретного заболевания. Прекращение лечения следует проводить постепенно для предотвращения появления симптомов отмены. Клиническое значение имеет различие между симптомами отдачи (чаще всего возникают после отмены быстродействующих бензодиазепинов), имеющими кратковременный и преходящий, но иногда выраженный характер; рецидивом заболевания, при котором исходные проявления болезни возвращаются на длительное время; и симптомами отмены, при которых появляются новые симптомы, характерные для конкретного препарата. В целом расстройства с хроническим или рецидивирующим течением или возникшие в пожилом возрасте чаще нуждаются в проведении длительной поддерживающей терапии.
Прочие вопросы психофармакологии.
1. Для оптимизации клинического ведения осложненных заболеваний необходимо документировать состояние пациента (включая психический статус в начале терапии и изменения в результате лечения) и побочные эффекты. Особое внимание следует уделять документальному отражению риска суицидального или агрессивного поведения, а также риску развития серьезных побочных эффектов, таких как поздняя дискинезия. Также важно указывать, что пациент осознает причину лечения, возможный риск и пользу, знает о существовании альтернативных методов и понимает риск отказа от терапии. Если способность пациента принимать собственные решения вызывает сомнения, то врачу следует получить согласие пациента на привлечение членов семьи к решению важных вопросов лечения. Если больной явно неспособен принимать решения, необходимо использовать официальный формальный механизм.
2. Некоторые из лекарственных средств, описываемых в данной книге, еще не получили одобрения в Управлении по контролю за лекарственными средствами и пищевыми продуктами США (FDA) в отношении новых показаний (например, флуоксетин при паническом расстройстве). Однако врач свободен в выборе любого подходящего препарата даже при незарегистрированном показании. В истории болезни следует отразить основание данного решения, которое в идеале должно демонстрировать полное понимание и осознание всех имеющихся данных.
3. Стоимость препарата, а также соотношение цена/эффективность являются важными моментами в вопросе выбора терапии. Лекарственный препарат, который в начале терапии кажется наиболее приемлемым в стоимостном отношении, в конечном счете может оказаться далеко не оптимальным вследствие недостаточного клинического эффекта или снижения качества жизни. Цена развития побочных эффектов в ряде случаев может превысить ожидаемую экономию. При более высокой эффективности, безопасности и снижении риска развития рецидива первоначально более дорогостоящий препарат может оказаться более приемлемым в ценовом отношении. Однако, если препараты обладают сходной эффективностью и переносимостью, то цена может являться веским основанием при выборе терапии.
Глава 2. Антипсихотические препараты.
Антипсихотические препараты являются основными средствами лечения шизофрении и других психозов, таких как шизоаффективное расстройство или органические психозы. Антипсихотические препараты впервые появились в клинической практике с 1950-х годов прошлого века, когда во Франции был синтезирован хлорпромазин, производное фенотиазина. Хотя изначально хлорпромазин разрабатывался в качестве антигистаминового препарата, при его клиническом использовании были выявлены антипсихотические свойства. Хлорпромазин явился моделью для разработки большого количества химически различных соединений для лечения психозов. Однако все препараты первого поколения (за исключением клозапина) вызывали развитие побочных экстрапирамидных симптомов (ЭПС) благодаря выраженному антагонизму к D2-дофаминовым рецепторам. Помимо влияния на психотические симптомы, свойство данных препаратов блокировать D2-дофаминовые рецепторы используется в других областях медицины (например, в качестве противорвотных средств или для лечения некоторых гиперкинетических двигательных расстройств). Блокаторы D2-дофаминовых рецепторов называются типичными антипсихотиками, в отличие от клозапина и других атипичных антипсихотиков, которые в меньшей степени вызывают экстрапирамидные симптомы. 1 Свойство классических антипсихотических препаратов вызывать при их применении экстрапирамидную симптоматику привело к появлению термина «нейролептики», так как данные средства буквально вызывали неврологические расстройства. Кроме того, длительное применение классических нейролептиков сопровождается высоким риском развития поздней дискинезии. Даже при краткосрочном применении типичные антипсихотические препараты могут вызывать симптомы паркинсонизма, а также другие нейролептические побочные симптомы (например, акатизию или акинезию), способные сами по себе симулировать или усиливать психотические симптомы, для лечения которых эти лекарства были первоначально назначены. Более чем за 40 лет клинического применения типичные антипсихотические средства показали свою эффективность при лечении психотических расстройств, но развитие серьезных двигательных нарушений служило значительным ограничением при их использовании.
Появление в последние годы новой группы антипсихотических препаратов, обладающих значительно меньшей способностью вызывать экстрапирамидные симптомы (ЭПС), так называемых атипичных антипсихотиков, открыло новый этап в лечении психотических расстройств. Первым из атипичных антипсихотиков был синтезирован клозапин — препарат, обладающий минимальной способностью вызывать экстрапирамидные расстройства и при этом доказавший свою эффективность при лечении шизофрении. Однако длительное время его применение было ограничено вследствие риска развития агранулоцитоза, требующего еженедельного контроля лейкоцитарной формулы. Кроме того, клозапин вызывает и другие побочные симптомы (седация, увеличение массы тела и снижение порога судорожной активности). Однако эффективность клозапина у многих больных шизофренией с недостаточным терапевтическим эффектом других антипсихотиков перевешивает риск развития побочных явлений. Новые препараты — рисперидон, оланзапин, кветиапин и зипразидон — показали свою эффективность при лечении шизофрении и других психозов, а также мании. Эти препараты в меньшей степени вызывают экстрапирамидные расстройства и в целом имеют более благоприятный профиль побочных симптомов по сравнению с клозапином. В частности, у них отсутствует риск развития агранулоцитоза. Вследствие этого они быстро стали препаратами выбора при лечении психотических расстройств. В контролируемых клинических исследованиях длительностью от 4 до 20 недель новые антипсихотические средства показали равную эффективность с классическими антипсихотиками, хотя и не удалось получить столь же убедительных данных, как для клозапина, об их эффективности у терапевтически резистентных больных.
Высокий аффинитет к D2-дофаминовым рецепторам среди типичных антипсихотиков четко коррелирует с их способностью вызывать экстрапирамидные симптомы. Меньшая способность новых антипсихотических препаратов вызывать ЭПС может быть связана с различными механизмами и пока полностью не изучена. Атипичный антипсихотик рисперидон обладает высоким аффинитетом к D2-рецепторам, сходным с галоперидолом (табл. 2.1), но его высокий аффинитет к серотониновым рецепторам (5-HT2А), возможно, уменьшает частоту развития ЭПС при использовании его в низких дозах ( 2
Таблица 2.1. Аффинитет к различным рецепторам у атипичных антипсихотиков в сравнении с галоперидолом
Источник