- Что такое лечебный патоморфоз 4 степени молочной железы
- Материалы конгрессов и конференций
- X РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
- 15-ЛЕТНИЙ ОПЫТ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ С ИСПОЛЬЗОВАНИЕМ НЕОадъювантНОЙ ХИМИОТЕРАПИИ
- Тройной негативный рак молочной железы
- Тройной негативный рак молочной железы
- Что такое тройной негативный рак молочной железы?
- Предоперационная терапия при тройном негативном раке молочной железы
- Нарушение процессов восстановления ДНК — мишень при лечении тройного негативного рака молочной железы
- Тройной негативный рак молочной железы и мутации BRCA
Что такое лечебный патоморфоз 4 степени молочной железы
хирург-онколог, маммолог, кандидат медицинских наук
+7 921 945 33 18
+7 981 710 40 41
Ленинградская область, Всеволожский район, пос.Кузьмоловский, Заозерная ул., 2
Врач в третьем поколении. Закончил в 1998 году с отличием Санкт-Петербургскую государственную медицинскую академию им. И.И. Мечникова, после чего сразу же поступил в клиническую ординатуру по хирургии этой же академии. Во время обучения в клинической ординатуре, которую с отличием закончил в 2000 году, получил специализацию по онкологии (1999). Начиная с 1999 года, обучение проводилось на базе Ленинградского областного онкологического диспансера (отделение общей онкологии). С 2000 по 2004 год проходил обучение в аспирантуре и в 2004 году защитил кандидатскую диссертацию на тему «Хирургическое и адъювантное лечение ранних форм рака молочной железы». Имею действительные сертификаты по хирургии (2021) и онкологии (2018), реконструктивной и пластической хирургии (2019)
В в клинике онкологических решений ЛУЧ (юридический адрес — Санкт-Петербург, Петровская коса, 1), также работаю с 2002 года в отделении заболеваний молочной железы ГБУЗ ЛОКОД. В 2007 году проходил обучение по онкологии в МАПО. С 2007 года являюсь действительным членом ЕВРОПЕЙСКОГО ОБЩЕСТВА МАММОЛОГОВ (EUSOMA) и ЕВРОПЕЙСКОГО ОБЩЕСТВА МЕДИЦИНСКОЙ ОНКОЛОГИИ (ESMO).
С 2004 года являюсь главным исследователем и координатором международных клинических исследований по раку молочной железы в Ленинградском областном клиническом онкологическом диспансере.
Имею более 10 печатных работ, в том числе в центральной зарубежной печати.
Рабочий телефон +7921 945 33 18
Мобильный телефон +7 921 945 33 18
Телефон администратора +7 981 710 40 41
Источник
Материалы конгрессов и конференций
X РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
15-ЛЕТНИЙ ОПЫТ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ МЕСТНО-РАСПРОСТРАНЕННЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ С ИСПОЛЬЗОВАНИЕМ НЕОадъювантНОЙ ХИМИОТЕРАПИИ
Э.К. Возный, Н.Ю. Добровольская
ФГУ РНЦРР
Хирургическое лечение больных местно-распространенным раком молочной железы обеспечивает 5-летнюю выживаемость только у 27-30% пациентов. Использование предоперационной химиотерапии в комбинации с операцией и лучевой терапией позволяет увеличить этот показатель до 40-80%.
Индукционная химиотерапия позволяет увеличить число органосохраняющих операций, определить индивидуальную чувствительность опухоли к цитостатикам для назначения адъювантного лекарственного лечения, а также продлить безрецидивный период.
С 1985 по 1996 гг. 336 женщин с местно-распространенной формой рака молочной железы получали комплексное лечение в Российском научном центре Рентгенорадиологии. В первой группе (231 больная) на первом этапе проводилась только химиотерапия по схемам CMF,CMFVP,CAF; во 2 группе (105 больных) в предоперационном периоде проводились те же режимы химиотерапии, а затем — лучевая терапия. Продолжительность наблюдения колебалась от 10 лет и более. Метастазы в лимфатические узлы были подтверждены цитологически у 298 (88,7%) больных: N1 имело место у 170 (50,6%) больных, N2 — у 128 (38,1%).
Методика комплексного лечения состояла из трех этапов. На первом этапе всем 336 больных проводилась неоадъювантная лекарственная терапия по схемам CMF, CAF, CMFVP. В последующем 105 из 336 пациентам назначалась предоперационная лучевая терапия. На втором этапе лечения выполнялось радикальное хирургическое лечение. На третьем этапе в послеоперационном периоде проводилась адъювантная лучевая терапия и химиогормонотерапия.
Индукционная химиотерапия при местно-распространенном раке молочной железы оказалась эффективной при всех изученных режимах как в целом, так и по подгруппам. Общий лечебный эффект отмечался у 168 (50%) пациентов, стабилизация процесса наступила у 164 (48,8%) больных и только в 4 (1,2%) случаях наблюдалось прогрессирование заболевания. Если говорить о группах, то общий лечебный эффект имел место у 50,2% пациентов в 1 группе и 49,5% пациентов во 2 группе.
Мы не выявили зависимости эффекта химиотерапии от стадии опухолевого процесса при всех режимах химиотерапии, что свидетельствует о зависимости эффекта не столько от распространенности опухолевого процесса, сколько от биологических особенностей опухоли. В 1 группе эффект наблюдался при Т2 у 29 (49,2%) больных, при Т3 – у 43 (48,3%) больных и при Т4 – в 44 (53,1%) случаев; во 2 группе при Т2 — у 5 (41,7%) больных, при Т3 – у 28 (52,8%) и при Т4 — у 19 (47,5%) пациентов.
Полная регрессия опухоли, подтвержденная морфологическим исследованием, при ее размерах Т2 и Т3 составила 6%, при Т4 — 2,4%. Важно, что у больных с лимфатическими узлами, оцененными индексом N1-2, снижение статуса до N0 имело место в 24,7%.
У большинства больных — 156 (46,4%) — зарегистрирована II степень лечебного патоморфоза. Одинаково часто имел место патоморфоз I и III степени: в 81 (24,1%) и 85 (25,3%) случаях соответственно. И только у 14 (4,2%) пациенток наблюдался патоморфоз IV степени. Патоморфоз III и IV степени в обеих группах чаще встречался при использовании схемы CAF и достигал 63,6%.
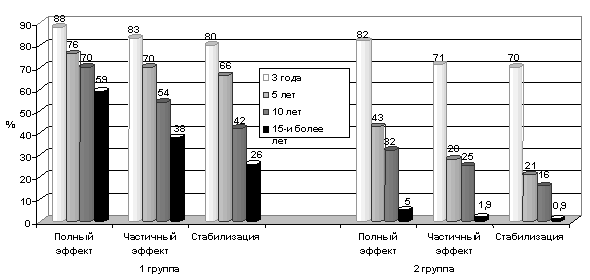
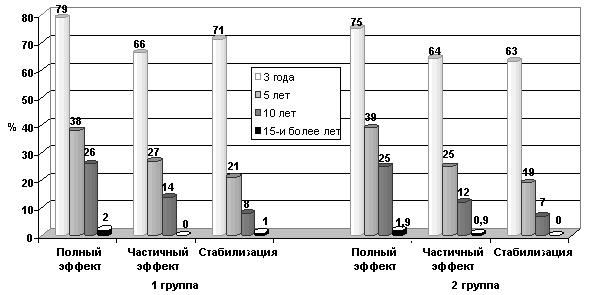
Выявлено, что в ранние сроки наблюдения местная распространенность опухоли не влияет на общую и безрецидивную выживаемость больных обеих групп, а в поздние сроки выживаемость зависит не только от значения индекса Т и N, но и, скорее всего, от клинического и морфологического эффекта (рис. 1, 2).
Сочетание неоадъювантной терапии с лучевой терапией у больных РМЖ с III+IV степенью патоморфоза по выживаемости и продолжительности безрецидивного периода не имело преимуществ по сравнению проведением только индукционной химиотерапии.
В группе больных с III и IV степенями патоморфоза, достигнутыми после неоадъювантной химиотерапии, при проявлении метастазов также сохранялась чувствительность к противоопухолевой лекарственной терапии.
Следует подчеркнуть, что пациенты, имевшие положительные РЭ и РП в 79,5% случаев переживали 3-летний период, в 63,6% случаев — 5-летний период и в 34,1% случаев — 10-летний период, что может быть объяснено проводимой адъювантной эндокринной терапией. При отрицательных значениях рецепторов общая выживаемость по периодам была ниже и распределялась следующим образом: в 25% и 10,7% случаев. Никто из больных не пережил 10- и 15-летний период.
Более четкая зависимость имела место в отношении наличия РЭ. Так, в тех группах, где они определялись в клетках опухоли, общая выживаемость была достоверно выше, чем у пациентов имеющих РП. При 3-летней выживаемости это соотношение было 63,6% против 27,8%, при 5-летней – 45,5% против 19,4%, при 10-летней – 27,3% против 2,8%.
Патоморфоз III+IV степени был зарегистрирован у 42,9% женщин, у которых рецепторы эстрогенов и прогестерона в ткани опухоли отсутствовали, и только у 4,5% пациенток с положительным рецепторным статусом. Следует отметить, что при отрицательном рецепторном статусе патоморфоз III+IV степени чаще имел место у пациенток с лекарственной аменореей (50% против 42,3%).
Таким образом, с учетом полученных нами данных, можно утверждать, что неоадъювантная химиотерапия увеличивает безрецидивный период и продолжительность жизни больных с местно-распространенным раком молочной железы за счет снижения значения таких прогностических факторов как индексы Т и N и патоморфологический эффект и должна быть неотъемлемым компонентом комплексного лечения таких пациентов.
Наличие рецепторов стероидных гормонов в тканях опухоли является положительным прогностическим признаком, свидетельствующим о возможности более благоприятного течения заболевания в отношении отдаленных результатов (общей и безрецидивной выживаемости). Поэтому, возможно, у больных с положительными РЭ и РП предоперационное лечение следует начинать с эндокринной терапии.
Индуцируемая неоадъювантной химиотерапией аменорея имеет благоприятное прогностическое значение, особенно у пациенток с положительным рецепторным статусом.
Источник
Тройной негативный рак молочной железы
Тройной негативный рак молочной железы
Что такое тройной негативный рак молочной железы?
В большинстве случаев рост клеток рака молочной железы зависит от наличия в организме женских половых гормонов, эстрогена и прогестерона, кроме того, во многих случаях в злокачественных клетках выявляется большое количество белка HER2 (гиперэкспрессия HER2). И рецепторы эстрогена/прогестерона и HER2 являются мишенями, на которые можно воздействовать с целью подавления роста опухоли и уничтожения раковых клеток (подробнее про разновидности рака молочной железы) [1].
Опухоли, в которых отсутствует экспрессия рецепторов эстрогена и прогестерона, а также не выявляется повышенной выработки белка HER2, относятся к так называемому тройному негативному раку молочной железы. Для обозначения этой разновидности рака может также использоваться термин «базально-подобный рак молочной железы». Рост клеток опухолей, которые относятся к этому подтипу, не зависит от стимулирующего влияния женских половых гормонов и белка HER2, по этой причине для лечения этого вида рака молочной железы не применяется ни гормонотерапия, ни анти-HER2 препараты. Тройной негативный рак молочной железы характеризуется агрессивным течением, его клетки склонны к быстрому делению, что сопровождается высокими темпами роста опухоли. Как правило, эти опухоли также характеризуются большим значением индекса Ki-67. Отсутствие трех основных мишеней для лечения и дало название этой разновидности рака молочной железы. На его долю приходится 10-20% случаев злокачественных опухолей молочных желез.
Предоперационная терапия при тройном негативном раке молочной железы
Тем не менее, этот вариант опухоли наиболее чувствителен к химиотерапии, во многих случаях на фоне её проведения можно достичь полной гибели всех злокачественных клеток. Высокая агрессивность тройного негативного рака молочной железы, а также его нечувствительность к вышеуказанным препаратам вынуждают врачей и ученых применять для его лечения особые методы лечения и искать новые лекарства, которые бы эффективно воздействовали на раковые клетки. Этот материал посвящен некоторым наиболее важным особенностям тройного негативного рака молочной железы.
В настоящее время для лечения тройного негативного рака молочной железы все шире применяется проведение предоперационной (или неоадъювантной) химиотерапии. В этом случае пациентке проводится необходимое количество курсов химиотерапии, после – оперативное лечение (удаление опухоли или всей молочной железы) и, при необходимости – лучевая терапия. Проведение лекарственного лечения до операции не только позволяет уменьшить размеры опухоли и облегчить выполнение оперативного вмешательства, но и имеет еще одно важное преимущество. Такой вид лечения позволяет оценить, насколько эффективно лекарственные препараты воздействуют на опухоль.
Достаточно часто после проведения такого лечения опухоль резко уменьшается в размерах, что является показателем эффективности предоперационной терапии. После завершения запланированного объема лечения проводится хирургическое удаление опухоли и врач-патологоанатом, изучив ткань опухоли, может сказать, насколько хорошо сработало лечение. Во многих случаях в послеоперационном материале не остается жизнеспособных опухолевых клеток – это означает, что лекарственное лечение убило все клетки, которые были в опухоли. Если предоперационная терапия оказалась высокоэффективной это свидетельствует в пользу благоприятного прогноза дальнейшего течения болезни и того, что терапия смогла или сможет убить все клетки опухоли, которые могли разнестись по организму. Это называется «полный лечебный патоморфоз» (или «патоморфоз четвертой степени»), что является благоприятным прогностическим признаков и резко снижает риск развития рецидива и появления метастазов (подробнее про пред- и послеоперационную химиотерапию).
Нарушение процессов восстановления ДНК — мишень при лечении тройного негативного рака молочной железы
У тройного негативного рака молочной железы тоже есть «уязвимое место». В клетках этих опухолей часто обнаруживается выраженное нарушение работы систем, восстанавливающих ДНК, содержащую всю основную генетическую информацию клеток и являющуюся «матрицей» для выработки всех структур и белков клетки. Клетки опухоли быстро делятся, но не могут восстанавливать свою ДНК, что делает их уязвимыми к воздействию лекарственных препаратов, повреждающих ДНК. К ним относятся алкилирующие препараты (например, циклофосфамид), а также препараты платины. Последние образуют связки между нитями ДНК (поперечные сшивки), что нарушает функционирование её функционирование и приводит к гибели опухолевых клеток. В настоящее время проводится множество исследований, посвященных изучению роли препаратов платины в лечении тройного негативного рака молочной железы. Например, в одном из исследований было показано, что добавление карбоплатина к стандартной терапии этого заболевания повышает вероятность полного уничтожения клеток опухоли на 17% [2].
В настоящее время также изучается роль препаратов, подавляющих активность PARP (ферментов, играющих важную роль в процессах восстановления ДНК) в лечении тройного негативного рака молочной железы. Функция PARP особенно важна для раковых клеток в тех случаях, когда не работают другие системы, ответственные за поддержание целостности ДНК – например, если в клетке присутствует мутация BRCA. Подавление активности PARP приводит к нарушению работы системы восстановления ДНК, что лишает клетки опухоли возможности восстановить свое ДНК после повреждения. Это приводит к очень быстрому накоплению в них мутаций и последующей гибели опухолевых клеток. Предполагается, что добавление ингибиторов PARP позволит повысить эффективность терапии. В одном из ранних исследований было показано, что применение PARP-ингибитора велипариба позволяет увеличить вероятность достижения полного патоморфоза с 26% до 51% [3].
Тройной негативный рак молочной железы и мутации BRCA
Кроме того, необходимо отметить, что во многих случаях развитие тройного негативного рака молочной железы связано с наличием мутаций в генах BRCA1 или BRCA2, особенно при развитии опухолей у пациенток молодого возраста (≤50 лет). Исследования показали, что до от 9% до 28% пациенток с этим диагнозом являются носительницами мутаций в гене BRCA1, от 3% до 17% — в гене BRCA2. Наиболее часто носительство этих мутаций встречается у пациенток, относящихся к евреям-ашкенази. Гены BRCA принимают активное участие в процессах восстановления ДНК после повреждения. Наличие этих мутаций значительно повышает риск возникновения раковой опухоли во второй молочной железе, а также злокачественных опухолей яичников.
По этой причине в настоящее время многим больным с наличием мутаций BRCA, с целью снижения риска второй злокачественной опухоли, предлагают выполнение удаления обеих молочных желез, а также, во многих случаях – профилактическое удаление яичников (придатков матки), особенно у пациенток в постменопаузе или не планирующих деторождение. Проведенные исследования показали, что проведение профилактического удаления обеих молочных желез у пациентов-носительниц мутаций в генах BRCA снижает риск развития рака молочной железы на 93%. Профилактическое удаление яичников снижает риск развития рака яичников, маточных труб и брюшины на 80%, рака молочной железы – на 50-64% [4, 5].
Кроме того, получение информации о носительстве мутации в генах BRCA важно не только для самой пациентки, но и для её близких родственников, особенно, в тех случаях, когда в семье отмечалось развитие злокачественных опухолей молочных желез, яичников и других органов. В этих случаях кровным родственникам пациентки (особенно матери, сестрам, дочерям) целесообразно пройти генетическое консультирование.
Источник