- Журнал «ПАРТНЕР»
- Персонализированная медицина: Основные принципы и методы
- Немного истории
- Суть персонализированной медицины
- Отличия нового подхода от ныне существующего
- Ранняя диагностика важна во всех случаях персонализированной медицины!
- Эксперт персонализированной медицины: кто сможет лечить будущие болезни
- Кто такой эксперт персонализированной медицины
- Чем занимается эксперт персонализированной медицины
- Тренды и направления профессии
- Откуда придет профессия
- Ключевые навыки эксперта персонализированной медицины
- Как стать экспертом персонализированной медицины
- Персонализированная медицина: перспективы использования нанобиотехнологий
- Персонализированная онкология
- Персонализированная кардиология
- Заключение
- Литература
- Персоналізована медицина: перспективи застосування нанобіотехнологій
- Рersonalized medicine: perspectives used of the nanobiotechnology
Журнал «ПАРТНЕР»
Персонализированная медицина: Основные принципы и методы
Немного истории

К настоящему времени в медицине сложился принцип лечениянепосредственно самой «болезни» как комплекса симптомов и синдромов у некоего среднестатистического человека без учета индивидуальных особенностей его физиологии, наследственных факторов, психосоциального статуса. Подобная схематизация лечебного процесса в ряде случаев приводит к безуспешной борьбе с «заболеванием», при которой индивидуальные особенности пациента не учитываются в полной мере, а иногда просто противодействуют эффективности терапии, изменяя прогноз и течение болезни.
Суть персонализированной медицины
Но вот появился «свет в конце тоннеля»: в современную медицину, благодаря новейшим достижениям молекулярной биологии, уверенно входит понятие «персонализированная медицина». Это дает надежду, что индивидуальный подход к медицинской помощи, поистине выстраданный человечеством, наконец, станет доминирующим.
Толчком для развития персонализированной медицины стали успехи, достигнутые за последние десятилетия в молекулярной биологии.
Отправной точкой явился знаменитый международный проект «Геном человека», стартовавший в 1990 г. Результаты этого проекта выразились, в том числе, и в бурном развитии технологий массового секвенирования (распознавания) ДНК, позволили медицинской генетике вплотную приблизиться к клинической практике. Так, геном пациента помогает определить оптимальный подход к оказанию индивидуальной медицинской помощи, будь она профилактической, диагностической или терапевтической.
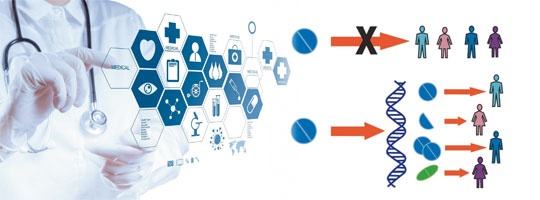
Ознакомившись с информацией, содержавшейся в наследственном материале, можно в любой момент жизни человека определить, какие генетические неполадки имеются в организме человека и какова вероятность того, что они однажды дадут о себе знать. Более того, такой анализ позволяет прогнозировать, как наш организм будет реагировать на определенные лекарства.
Персонализированная,или предсказательная, индивидуализированная медицина – это совокупность методов профилактики (предупреждения) болезни, диагностики и лечения в случае ее возникновения, основанных на индивидуальных особенностях пациента. К подобным индивидуальным особенностям относят целый комплекс различных генетических маркеров в сочетании с присущими данному организму разнообразными фенотипическими признаками.
Что такое фенотипические признаки? Это совокупность всех внешних характеристик человека, включая различные физиологические, биохимические и молекулярные характеристики, которые могут изменяться в результате действия генов.
Таким образом, персонализированная медицина – это прежде всего интегральная медицина, которая включает в себя разработку персонализированных средств лечения, тестирование на предрасположенность к болезням, профилактику, а также объединение диагностики с лечением и мониторингом лечения.
К основным принципам персонализированной медицины относятся:
— Возможность «предсказать» болезнь (предикативность).
— Принятие конкретных мер, предотвращающих заболевание (профилактика).
— Индивидуальное лечение каждого (персонализация).
— Возможность непосредственного участия самого пациента в процессе профилактики и лечения (партисипативность).
Составление многофакторной базы данных на каждого пациента предполагает учет всех его биологических и психосоциальных особенностей. При этом общая картина складывается из множества пазлов: результатов анализа работы различных систем организма (в том числе и на молекулярном уровне), наличия наследственных патологий и даже описания особенностей отношений в семье.
Новое направление неразрывно связано с молекулярной медициной и биологией, которые во многом обеспечивают развитие соответствующих инновационных технологий: клеточные и биомолекулярные методы и средства диагностики, профилактики, лечения и реабилитации.
Отличия нового подхода от ныне существующего
К таким отличиям в первую очередь относятся:
— Профилактическая направленность (возможность «предсказать» заболевание, составить его прогноз и, соответственно, принять меры, чтобы его предотвратить);
— Использование высокотехнологичных методов, с помощью которых можно не только определять диагноз на ранних стадиях, но и назначать лекарственные препараты индивидуально, то есть в зависимости от тех или иных характеристик человека.
Существенным фактором является то, что основным инструментом персонализированной медицины остается врач, который изучает историю болезни человека, анализирует жалобы, используя свой опыт и профессионализм. Методы персонализированной медицины – это сочетание высокого профессионализма врача, принципов доказательной медицины, «обычных» инструментальных исследований при необходимости, а также современной лабораторной диагностики.
Инновационным для персонализированной медицины является попытка понять болезнь или предрасположенность к ней на клеточном уровне, оценить «молекулярные пути» заболевания, найти соответствующие биомаркеры – вещества, которые являются «знаками» той или иной болезни. Для этого используется генетика, геномика (раздел молекулярной генетики, посвященный изучению генома и генов), протеомика (наука об изучении белков, их функций и взаимодействия в живых организмах), а также метаболомика (наука об изучении уникальных химических «отпечатков пальцев», специфичных для процессов, протекающих в живых клетках).
Все ли заболевания можно предотвратить с помощью персонализированной медицины? Главным образом это –мультифакторные заболевания, при которых у человека есть предрасположенность к определенному заболеванию, но проявится болезнь или нет, зависит от факторов внешней среды – питания, спортивных нагрузок и т.п., то есть образа жизни. На сегодняшний день возможно определить предрасположенность к большому количеству патологий – начиная от панкреатита и заканчивая некоторыми видами онкологии. Это и сахарный диабет 2-го типа, и гипертоническая болезнь; существуют маркеры, свидетельствующие о возможности возникновения инфаркта миакарда.
Персонализированная медицина, несмотря на значительный объем используемой информации, на самом деле экономит время и пациента, и врача. Полное обследование пациента в клинике персонализированной медицины занимает, как правило, всего 2-3 дня, включая медико-генетическое консультирование и необходимые лабораторные и инструментальные методы. А определение биомаркеров и генетическое тестирование может занять всего 10 минут – для этого требуется сдать анализ крови или слюны.
Ранняя диагностика важна во всех случаях персонализированной медицины!
Не существует «легких» или «тяжелых» болезней, для каждого человека болезнь – это стресс и снижение качества жизни. В случае с неясным или редким диагнозом прояснить ситуацию помогает медико-генетическое консультирование. Можно диагностировать наследственные заболевания, включая онкологические заболевания, предсказывать спортивные достижения, определять переносимость и эффективность определенных лекарств.
Персонализированный подход необходим людям, которые пожизненно или длительно принимают лекарственные средства, для подбора дозировки с помощью методов новой науки – фармакогенетики. Например, если дело касается препаратов, разжижающих кровь – антикоагулянтов. Многие из нас знают, что риск тромбоза после любого оперативного вмешательства существует всегда, с этой целью назначают препараты, препятствующие тромбообразованию. Как правило, определение лекарства и его дозировка – это выбор врача, основанный на действующих медицинских стандартах. Однако каждому пациенту присуща индивидуальная скорость метаболизма, т.е. скорость, с которой препарат начнет свое действие и будет выводиться из организма. Методы фармакогенетики позволяют оценивать скорость метаболизма у каждого пациента, выбрать определенное лекарство, его дозу персонально.
Таким образом, персонализированная медицина – это уникальное сочетание накопленного исторического опыта мировой медицины и достижений современной науки, симбиоз опыта и высокого профессионализма врачей и совершенных высокоэффективных технологий. Есть ли у нее проблемы и «теневые» стороны? Об этом – в следующем номере.
Д-р Ольга Грищенко (Хеппенхайм)
Источник
Эксперт персонализированной медицины: кто сможет лечить будущие болезни
Кто такой эксперт персонализированной медицины
Это врач, который проводит лечение, диагностику и профилактику болезней на основе индивидуальных показателей организма пациента. Эти показатели называют биомаркерами.
К традиционным биомаркерам относят биохимические показатели из лабораторных анализов и клинические показатели, например, пульс или значение артериального давления. Они показывают состояние организма пациента «здесь и сейчас» и помогают отследить динамику.
Современными биомаркерами считают геномные или молекулярно-генетические биомаркеры. По мутациям внутри генетического кода врач может понять, как эти биомаркеры влияют на метаболизм (обмен веществ), и выявить «ошибки», которые приводят к заболеваниям. Все три группы биомаркеров помогают врачу быстро подобрать наиболее эффективный и безопасный препарат, выбрать подходящую дозировку или предупредить развитие болезни пациента.
Пример персонализации препаратов на основе генетических биомаркеров — «Герцептин». Его используют для борьбы с раком молочной железы [1]. Другой случай — препарат «Ивакафтор». Его назначают для лечения заболевания желез внешней секреции, которое происходит из-за мутации в генах [2].
Чем занимается эксперт персонализированной медицины
Такой специалист работает как обычный лечащий врач. Он принимает пациентов, выбирает методы диагностики заболевания, назначает лечебный или профилактический комплекс, занимается документами.
Отличие эксперта персонализированной медицины от обычного врача в том, что он разбирается в генетических тестах и может самостоятельно интерпретировать их результаты. Кроме того, он может обратиться за помощью к клиническому фармакологу или нейросети для подбора лекарства. При этом решение о назначении препарата и его дозировки остается за врачом.
Эксперт персонализированной медицины — одна из профессий будущего.
Тренды и направления профессии
Фармакогенетические тесты, которые помогают понять, как организм пациента отреагирует на тот или иной препарат, становятся более доступными. Поэтому врачи с такими компетенциями все более востребованы.
Благодаря фармакогенетическим тестам, уже сегодня можно определить генетическую предрасположенность к появлению опухолей, в том числе злокачественных, к проблемам с сердечно-сосудистой системой, склонность к неврозам, депрессии и другим психическим заболеваниям.
«Генетические технологии дешевеют с каждым годом, что, в общем-то, может служить хорошей надеждой для более широкого внедрения подобного рода технологий в реальную клиническую практику в будущем», — отмечал в интервью «Постнауке» Дмитрий Сычев, доктор медицинских наук, профессор, член-корреспондент РАН [3].
В будущем сдача фармакогенетического анализа будет нормой, вся информация из него станет частью единых медицинских информационных систем. Это будет своеобразный генетический паспорт, по которому врач сможет отслеживать историю болезни, быстрее назначать лечение и эффективную профилактику. Накопление генетических данных в биобанках поможет развивать доказательную медицину, потому что данные о безопасности и эффективности препаратов станут точнее.
Еще одно крупное направление профессии — поиск новых биомаркеров для будущего тестирования эффективности препаратов. Например, сейчас во всем мире исследуют генетические комбинации, влияющие на более тяжелое течение COVID-19 [4].
Откуда придет профессия
В мире персонализированная медицина становится все более востребованным направлением как в исследованиях, так и в практике. По данным Grand View Research, мировой рынок персонализированной медицины в 2020 году оценивали в $493,1 млрд. Эксперты прогнозируют рост рынка со среднегодовым темпом в 6,2% до 2028 года [5]. При этом в клинических рекомендациях российских врачей уже есть генетические тесты. По их результатам врачи назначают пациентам препараты.
Ключевые навыки эксперта персонализированной медицины
Такому эксперту важно разбираться в областях медицины, фармакологии и генетики. Ему потребуется умение работать с программами для анализа данных, медицинским оборудованием и развитые soft skills для работы с коллегами и пациентами.
Как стать экспертом персонализированной медицины
В России нет отдельной специальности по этому профилю. Компетенция эксперта персонализированной медицины относится к программам повышения квалификации. Ее могут получить врачи клинических специальностей или специалисты с высшим образованием по направлениям «Лечебное дело», «Педиатрия», «Стоматология», «Медицинская биофизика», «Медицинская биохимия», «Медицинская кибернетика». Две таких программы организует ФГБОУ ДПО РМАНПО Минздрава России [6].
Источник
Персонализированная медицина: перспективы использования нанобиотехнологий
Резюме. Обзор посвящен обсуждению перспективных направлений персонализированной диагностики и терапии в кардиологии и онкологии при использовании инновационных нанобиотехнологий. Приведены результаты основных исследований по данному вопросу.
Персонализированная (индивидуализированная, персонифицированная) медицина (ПМ) — сравнительно новое направление современной медицины, получившее развитие благодаря использованию методов направленного пациентассоциированного лечебно-диагностического воздействия, на основе учета влияний генетических, внешнесредовых и региональных факторов (Jain K.K., 2009a). Другими словами, это целевая диагностика (геномно-протеомная, метаболомная, транскриптомная) и лечение (индивидуально ориентированные воздействия, в том числе лекарственная, клеточная терапия) больного в соответствии с исходными результатами исследования его генетического профиля (Willard H.F., Ginsburg G.S. (Eds), 2009).
ПМ также является перспективной областью интеграции современных биотехнологических подходов в медицинской практике, оптимизирующих понимание патофизиологической основы развития заболеваний, а также особенностей их молекулярной диагностики и терапии. Кроме того, такие активно развивающиеся направления медико-биологических исследований, как фармакогеномика, фармакогенетика, метаболомика и другие «омики», в частности фармакопротеомика, фармакометаболомика, фармакоцитомика, вносят свой вклад в развитие ПМ (Zhou S.F. et al., 2008; Nordström A., Lewensohn R., 2010; Trent R.J., 2010).
Сегодня ПМ — бурно развивающаяся область медицинских знаний. Оценка Бостонской консалтинговой группы (Boston Consulting Group — BCG) свидетельствует, что до 2020 г. темпы роста ПМ составят 37% ежегодно (Jain K.K., 2009b).
Важно отметить, что современное развитие наномолекулярной медицины рассматривается в связи с применением нанобиотехнологий (Залесский В.Н., 2009). В то же время нанобиотехнологии вносят существенный вклад в развитие ПМ благодаря использованию инновационных методик для лечебно-диагностических целей (Hess H., Jaeger L., 2010).
В основе развития ПМ лежит анализ особенностей генома человека. Так, в клиническом плане в первую очередь речь идет о том, чтобы с помощью генного анализа установить, стоит ли вообще принимать тот или иной препарат. Это необходимо потому, что даже незначительные индивидуальные различия в ДНК у двух пациентов могут привести к тому, что одно и то же лекарственное соединение будет действовать на них совершенно по- разному (Willard H.F., Ginsburg G.S. (Eds), 2009).
В ПМ роль биомаркеров в качестве референтных точек для диагностики и терапии общеизвестна (Saito M., Yoshino T., 2010; Sharon D. et al., 2010). С помощью биомаркерных молекул определяют, в частности, состояние процессов повреждения клетки, ДНК, РНК, а также наличие метаболитов или белков-предшественников, которые детектируются благодаря инновационным нанобиотехнологиям (Archakov A.I., Ivanov Y.D., 2007; Hess H., Jaeger L., 2010).
Наноматериалы, используемые с целью создания биометок, являются важнейшей составляющей биомаркерных исследований (Розенфельд Л.Г. и соавт., 2008). Внутриклеточные биомаркерные молекулы, отличающиеся хорошей водорастворимостью, биосовместимостью и флюоресцентными свойствами, а также высокой стабильностью в составе серебряно-дендримерных нанокомпозитов, широко применяются для лечения клеток in vitro (Lesniak W. et al., 2005; Stofik M. et al., 2009).
Квантовые точки — довольно устойчивые наноструктуры, которые используются как молекулярные метки в целях выявления поражений, в частности, на ранних стадиях развития процессов онкогенеза (Lee J. et al., 2010) и микрометастазирования (Mahmoud W. et al., 2010), а также позволяют оценивать их эффективность в качестве соединений-мишеней при индукции клеточной альтерации в процессе развития многих заболеваний (Derfus A.M. et al., 2007).
Протеомные технологии имеют существенное значение для выделения и идентификации биомаркерных молекул. Использование нанобиотехнологий для протеомного, нанопротеомного анализа в значительной степени оптимизирует современную протеомную базу исследований и облегчает выявление следовых количеств белковых аналитов, а также протеинов в чрезвычайно малых объемах исследуемых образцов.
Постоянное совершенствование инновационных нанобиотехнологий позволит широко использовать поверхностные характеристики наночастиц на этапах их взаимодействия с биомаркерными молекулами и последующего их разделения на основе использования методов высокочувствительного протеомного тестирования (Geho D.H. et al., 2006; Jain K.K., 2007). По-видимому, нанобиотехнологии будущего позволят создавать наноразмерные устройства для ускоренного скрининга биомаркерных молекул, идентифицирующих этапы развития сравнительно редко отмечающихся заболеваний человека (Archakov A.I., Ivanov Y.D., 2007).
Существенная роль отведена нанобиотехнологиям в персонифицированной диагностике. Сегодня становятся очевидными высокие темпы оптимизации методов направленной диагностики ДНК, РНК и белков. Отмечается повышение их точности и чувствительности, превышающее общепринятые методы молекулярного анализа. Начиная с диагностики простых белковых молекул, ДНК, РНК и их функциональных субъединиц в наношкальном формате, нанобиотехнологические подходы обеспечивают высокую прецизионность протеомных методов исследования (Hess H., Jaeger L., 2010).
Нанобиотехнологии помогают преодолевать ограничения методов современной молекулярной диагностики и содействуют установлению быстрого, точного и наиболее полного диагноза, а также интеграции диагностических программ исследования с терапевтическими мероприятиями в рамках персонализированных подходов к пациенту (Jain K.K., 2007).
Развитие ПМ напрямую связано с информацией о геноме человека. Известно, что для расшифровки генома в 1990 г. правительство США санкционировало проект «Геном человека». Стоимость секвенирования (идентификации нуклеиновых оснований в молекуле ДНК) генома примата составила порядка 20 млн дол. США, его проведение потребовало 3–5 мес. Для удешевления процедуры секвенирования генома человека до порядка 1 тыс. дол. был открыт проект «Персональный геном», инициированный Гарвардским университетом (Davies K., 2010).
Одним из наиболее перспективных методов секвенирования оказался метод, основанный на использовании физических различий между 4 нуклеотидами (Mirsaidov U.M. et al., 2010). Благодаря этим различиям оказалось возможным зарегистрировать, транспортируя ДНК через нанопору, электрический сигнал, возникающий в ее электронной структуре (Mirsaidov U.M. et al., 2010). Такой метод не предполагает использования процедуры амплификации, что значительно удешевляет технологию секвенирования до 1 тыс. дол. и повышает быстродействие процедуры. В созданном устройстве подсчета единичных олигонуклеотидов регистрируется изменение во времени электрического сопротивления стенок нанопоры с диаметром несколько нанометров при прохождении через нее молекулы ДНК (Xu M. et al., 2009).
Длительное время исследователи имели затруднения в тестировании последовательности оснований, поскольку ДНК совершала обратные (вперед, назад) движения в пределах нанопоры. Для удержания процесса перемещения ДНК в пределах нанопоры интенсивно разрабатываются способы стабилизации молекулы с применением электрической «ловушки» (Pettersson E. et al., 2009).
Современные инновационные технологии секвенирования генома (ДНК) позволяют сравнительно быстро и эффективно считывать геномную информацию непосредственно от этих молекул благодаря замедлению и контролю скорости движения молекул через поры наноразмерного формата (Mirsaidov U.M. et al., 2010).
Быстрое и эффективное секвенирование молекул ДНК человека сегодня стало реальным благодаря новаторской технологии декодирования молекул ДНК при их транслокации через нанопоры, размещенные на кремниевом чипе (Archakov A.I., Ivanov Y.D., 2007). Эта технология доступна для широкомасштабного геномного анализа с помощью серийно выпускаемых систем (454 Sequencing System), которые генерируют сотни тысяч высококачественных данных о секвенс-последовательностях за считанные часы. При этом платформа 454 Sequencing System может стать первой технологией секвенирования нового поколения, разработанной для применения в клинических условиях (Davies K., 2010).
Особенно перспективным оказалось устройство, в котором измерения осуществляются на отдельной молекуле ДНК благодаря созданию мельчайших нанопор в графене (слое углерода толщиной всего в 1 атом) для регистрации перемещения отдельных молекул ДНК, проходящих через наноразмерную пору (Schneider G.F. et al., 2010). Оказалось, что находящуюся в водном растворе молекулу ДНК можно транспортировать через графеновую нанопору, и, что особенно важно, отдельно каждую молекулу ДНК можно выявить по падению электрического тока в области нанопоры. Такая нанопора позволяет считывать всю последовательность (основание за основанием) перемещающейся через пору молекулы ДНК. Авторы считают, что графеновые нанопоры открывают новые, гораздо большие, чем только секвенирование ДНК, возможности. Они включают область разработки новых сенсоров для осуществления как фундаментальных, так и прикладных научных исследований (Liu A. et al., 2010).
В целом активно разрабатываемые новые биотехнологии секвенирования ДНК на основе использования нанобиотехнологических решений имеют широкие перспективы для применения в здравоохранении. Они могут позволить оптимизировать персонализированную диагностику, способствуя получению данных о предрасположенности к развитию сердечно-сосудистых заболеваний, рака, сахарного диабета и др.
Молекулярная визуализация — важнейшая диагностическая модальность, которая позволяет комбинировать лечебные и диагностические подходы и является базовой биотехнологией ПМ (Chen K., Chen X., 2010). Наночастицы в составе суперпарамагнитных контрастных соединений и перфлюороуглеродных нанокомпозиций используются в качестве инструмента для формирования молекулярного изображения, что позволяет проводить отбор пациентов для персонализированной терапии (Caruthers S.D. et al., 2006; Chen K., Chen X., 2010).
Развитие многофункциональных транспортных наноплатформ для наноассоциированной доставки визуализирующих меток оптимизирует такие современные молекулярные визуализирующие технологии, как оптическая когерентная томография, рентгеновская компьютерная томография, магнитно-резонансная томография, однофотонная компьютерная томография, позитронно-эмиссионная томография (Дынник О.Б., Залесский В.Н., 2005; Залесский В.Н., Дынник О.Б., 2005; Залесский В.Н., Дынник О.Б., 2006; Cai W., Chen X., 2007; Залесский В.Н., 2009).
Мишеньассоциированные лиганды, визуализирующие метки, наноплатформы и многие другие нанобиоконструкции позволяют проводить таргетную наномолекулярную персонализированную диагностику в условиях клиники (Залесский В.Н., 2009). Сравнительно недавно разработан метод молекулярной визуализации с использованием наночастиц золота для диагностики состояния уязвимости атеросклеротических бляшек коронарных артерий при использовании многоцветной компьютерной томографии. Данная инновация может способствовать проведению надежной персонализированной диагностики и лечения кардиальных событий у пациентов в клинических условиях (Lukianova-Hleb E.Y. et al., 2009).
Некоторые биоконструкции (нанобиосенсоры, нанобиочипы), создаваемые на основе современных наноматериалов, помогают в процессах создания и доставки новых лекарственных препаратов (Jain K.K., 2007; Marcato P.D., Durán N., 2008).
Доставка лекарственных соединений стала важнейшей стратегией современных нанофармакологических исследований (Marcato P.D., Durán N., 2008; Farokhzad O.C., Langer R., 2009). Таргетная доставка к целевому органу или ткани, а также преодоление биологических барьеров крайне важны для безопасного и эффективного использования лекарственных соединений. Конъюгаты наночастиц со специфическими лигандами и аптамерами дают возможность проводить специфическое таргетирование с высокой клинической эффективностью (Debbage P., 2009).
Нанобиотехнологии также вносят существенный вклад в проведение процедур клеточной и генной терапии, которые являются составными частями персонализированного лечения (Guo K.T. et al., 2008; Wolf S.M. et al., 2009).
Удачным примером доставки терапевтического материала в составе наноконструкций послужило создание наночастиц, начиненных малыми интерферирующими РНК (small interfering RNA — siRNA), что позволило им эффективно проникать внутрь раковых клеток и непосредственно индуцировать подавление экспрессии гена-мишени (Tian Z. еt al., 2010).
Феномен РНК-интерференции, заключающийся в способности двухцепочечной молекулы siRNA прицельно блокировать синтез определенных белков, сегодня рассматривается в качестве перспективного подхода к разработке новых лекарственных препаратов (Corydon T.J., Mikkelsen J.G., 2006). Однако доставка терапевтических молекул siRNA в клетки-мишени оказалась довольно сложной задачей. После введения в организм siRNA быстро выводились почками, поэтому для обеспечения их эффективности потребовались нетоксические частицы-носители, способные доставлять содержимое в клетки-мишени, не вызывая при этом иммунного ответа.
Впервые осуществлено системное введение терапевтических siRNA, заключенных внутрь специальным образом сконструированных наночастиц, в клинических тестовых исследованиях для лечения больных макулярной дегенерацией сетчатки глаза и инфекционным поражением легких, вызванным респираторно- синцитиальным вирусом (Tiemann K., Rossi J.J., 2009; Tokatlian T., Segura T., 2010). Молекулярный маркер на поверхности таких наночастиц специфически связывается с рецепторами мембран злокачественных клеток и обеспечивает внутриклеточное проникновение siRNA.
Помещенные в наночастицы молекулы siRNA блокируют синтез рибонуклеотидредуктазы М2 (ribonucleotide reductase M2 — RRM2) — фермента, управляющего восстановлением повреждений ДНК. Выбор данного гена в качестве мишени (вернее, комплементарной ему информационной РНК-матрицы, на которой синтезируется собственно белок) был необходим для повышения вероятности положительного эффета терапии (гиперэкспрессия RRM2 отмечена именно в том регионе, на который прицельно воздействовали тестируемой siRNA (Tokatlian T., Segura T., 2010).
Персонализированная онкология
Нанобиотехнологии выполняют важную роль в персонализированных онкологических исследованиях. Они способствуют оптимизации процесса идентификации опухольассоциированных биомаркерных молекул, используемых в качестве основы для осуществления специфической молекулярной онкодиагностики и проведения таргетной терапии. Так, avβ3-таргетные парамагнитные наночастицы прошли успешную клиническую апробацию при их использовании в неинвазивной визуализации крайне малых очагов ангиогенеза, ассоциированных с растущей опухолевой (меланома кожи) тканью (Schmieder A.H. et al., 2005). Оказалось, что наночастицы, содержащие металлы переменной валентности, способствовали повышению контрастности изображения при магнитно-резонансном сканировании, формируя молекулярный формат изображения. Присоединенные к поверхности наночастиц белковые молекулы фиксировались к эндотелию новообразованных микрососудов, идентифицируя участки роста опухолевой ткани. Молекулярный формат изображения позволял зарегистрировать участки неоангиогенеза в зонах роста опухоли, по сравнению с остающимися «немыми» в анатомическом формате изображениями при проведении стандартной магнитно-резонансной томографии. Также раннее обнаружение роста опухоли повышало эффективность персонализированной терапии меланомы кожи.
Другим примером использования металлсодержащих наночастиц в онкологии может служить применение их в составе платформ-переносчиков высоких доз противоопухолевых антибиотиков в бластомную ткань (без развития признаков системной токсичности) (Upadhyay K.K. et al., 2009). Наночастицы для магнитно-резонансной томографической визуализации позволяют клиницисту быстрее оценить эффективность лечения по сравнению с использованием стандартной магнитно-резонансной томографии до и после терапевтических воздействий. В целом для персонализированной противоопухолевой терапии важнейшими являются следующие составляющие: раннее выявление процесса, комбинация диагностических и лечебных процедур, а также мониторирование эффективности лечения (Roukos D.H., 2009).
Дендримеры являются сравнительно новым классом 3D наноразмерных структур с довольно обширной областью применения в медицине, включая персонализированную онкологию, благодаря уникальным физико-химическим свойствам их поверхности (Baker J.R. Jr., 2009; Medina S.H., El-Sayed M.E., 2009). Они чаще стали использоваться для доставки лекарств наряду с применением в процессах синтеза новых фармакологических соединений. Известно, что поливалентные дендримеры взаимодействуют одновременно со многими лекарственными мишенями и могут быть использованы для создания новых таргетных противоопухолевых соединений (Medina S.H., El-Sayed M.E., 2009; Sajja H.K. et al., 2009).
Конъюгирование дендримеров с различными биологическими соединениями, в частности фолиевой кислотой, в сочетании с комплементарными ДНК- олигонуклеотидами, позволило создать «гроздевидные» молекулы для таргетирования опухолевых клеток, со сверхэкспрессированными на их поверхности высокоаффинными фолатными рецепторами (Choi Y. et al., 2005; Baker J.R. Jr., 2009).
Мультифункциональные и многокомпонентные наноструктуры интенсивно исследуются и способствуют оптимизации персонализированной противоопухолевой терапии (Cho K. et al., 2008; de Dios A.S., Diaz-Garcia M.E., 2010). Конъюгаты наночастиц с лигандами (моноклональными антителами, пептидами или малыми молекулами) применяются для таргетирования злокачественных новообразований с высокой специфичностью. Эти данные свидетельствуют о формировании нового направления — персонализированной онкологии (Wang M.D. et al., 2007; Stambuk K.S. et al., 2010; Roukos D.H., 2010).
Персонализированная кардиология
Будущее наномолекулярной диагностики сердечно-сосудистых заболеваний существенным образом зависит от развития мультифункциональных наносистем в качестве визуализирующих агентов (Залесский В.Н., 2009; Pan D. et al., 2010). Одновременно с этим постепенно расширяется сфера использования наноплатформ в кардиологии для доставки лекарственных препаратов (Wickline S.A. et al., 2006; Iverson N. et al., 2008). Параллельное применение перфлюороуглеродных наночастиц для таргетной доставки лекарств и с целью формирования молекулярного профиля изображения в области атеросклеротических поражений стенки коронарных сосудов существенно оптимизирует потенциал персонализированной кардиологии в целом (Lanza G.M. et al., 2006; Kaneda M.M. et al., 2009).
В результате развития персонализированной диагностики сердечно-сосудистых заболеваний совершенствование стратегий усиления индуцируемых сигналов в тканях на основе использования нанобиотехнологических инновационных решений привело к быстрому развитию современных визуализирующих систем (коронарной магнитно-резонансной томографии и оптической коронарной томографии, оптической когерентной томографии) сверхвысокого разрешения (Jaffer F.A., Weissleder R., 2004; Залесский В.Н., Дынник О.Б., 2005; Залесский В.Н., 2009).
В этом контексте молекулярная визуализация на основе применения наноконтрастных меток, корреспондирующих изображение молекул-мишеней (in vivo), может оказаться полезным инструментом исследования молекулярных звеньев патогенеза атеросклероза в рамках персонализированной диагностики, включая локальное воспаление, апоптоз и ангиогенез.
Структурная трансформация фиброзной покрышки атеросклеротической бляшки, сопровождающаяся высоким риском возникновения ее разрыва, может быть успешно отслежена с помощью метода магнитно-резонансной томографии, компьютерной томографии или внутрисосудистой ультразвуковой визуализации, что позволяет получать наиболее полную анатомическую характеристику бляшко-ассоциированной атеросклеротической поверхности венечного сосуда сердца. Однако лишь молекулярная визуализация позволяет уточнить степень активности альтеративных процессов на атерогенной поверхности венечных сосудов и обосновать реальный прогноз возможного развития осложнений атеросклероза, что оптимизирует процесс персонализированной диагностики в кардиологии (Залесский В.Н., 2009).
Подробно изучен процесс активизации макрофагов, выступающих в качестве клеточных эффекторов воспаления, а их присутствие расценивается как предиктор высокого риска возникновения уязвимости атеросклеротической бляшки (Naghavi M. et al., 2003). Установлено, что магнитные наночастицы (окись железа) связываются с макрофагами атеросклеротически измененной сосудистой стенки и преимущественно накапливаются в бляшках a. carotis (Kooi M.E. et al., 2003; Trivedi R.A. et al., 2004). В этих двух независимых исследованиях выполненное магнитно-резонансное сканирование на фоне введения наночастиц, при проведении каротидной эндартерэктомии, позволило визуализировать очаги локального воспаления в пределах атеросклеротической бляшки. Более тонкие механизмы атеросклеротического процесса были раскрыты при использовании методики наноассоциированной магнитофлюоресценции. Необходимо отметить, что оптимизация молекулярного профиля изображения кардиоваскулярных структур и адресной доставки лекарств на основе использования нанобиотехнологий позволит сегодня значительно ускорить развитие персонализированной кардиологии будущего (Ginsburg G.S. et al., 2005; Schoenhagen P., Conyers J.L., 2008; Lee S.H. et al., 2009).
Заключение
На протяжении уже ближайших нескольких лет могут возникнуть и получат стремительное развитие ряд новых направлений персонализированной диагностики и терапии в условиях работы специализированных клиник и центров ПМ (Corsi F., Prosperi D., 2010). Это позволит повысить интерес практических врачей к молекулярным звеньям патогенеза заболеваний, а также методам наномолекулярной диагностики и терапии. Значительный прогресс следует ожидать в создании мультимодальных наносоединений, повышающих контрастность молекулярного изображения, а также новых технических средств и алгоритмов оптимизации визуализации молекулярных процессов в наношкальном формате с помощью современных биоконструкций. Это создает предпосылки для базовой инфраструктуры и повысит эффективность методов ПМ в целом.
Принимая во внимание наблюдаемый в последние годы процесс развития высокоспециализированных, высокоточных и наукоемких нанобиотехнологий для решения лечебно-профилактических и диагностических задач практически во всех областях медицины, не вызывает сомнений дальнейший интенсивный рост их использования в широкой клинической практике. Все это свидетельствует о назревшей необходимости организации Национального научного центра персонализированной медицины с одновременным созданием сети специализированных научно-исследовательских институтов по проблемам геномики, протеомики, метаболомики, транскриптомики, цитомики, а также наномолекулярной визуализации для диагностики и терапии заболеваний человека, при государственной поддержке со стороны НАН Украины, НАМН Украины и Министерства здравоохранения Украины с участием частных инвесторов в целях координации и планирования данного направления исследований в нашей стране.
Литература
- Дынник О.Б., Залесский В.Н. (2005) Внутрикоронарная ультразвуковая томографическая визуализация (проблемы и перспективы). Укр. мед. часопис, 5(49): 89–94.
- Залесский В.Н. (2009) Наномолекулярная медицина: современные биотехнологии наномолекулярной диагностики, лучевые томографические методы визуализации, наномодифицированная клеточная и лекарственная терапия. ВИПОЛ, Київ, 320 с.
- Залесский В.Н., Дынник О.Б. (2005) Внутрисосудистая оптическая когерентная томография: возможности визуализации коронарной патологии. Укр. мед. часопис, 6(50): 42–46.
- Залесский В.Н., Дынник О.Б. (2006) Визуализация кальциноза методом спиральной компьютерно-томографической коронароангиографии. Укр. мед. часопис, 3(53): 78–83.
- Розенфельд Л.Г., Москаленко В.Ф., Чекман І.С., Мовчан Б.О. (2008) Нанотехнології, наномедицина: перспективі наукових досліджень та впровадження їх результатів у медичну практику. Укр. мед. часопис, 5(67): 63–68.
- Archakov A.I., Ivanov Y.D. (2007) Analytical nanobiotechnology for medicine diagnostics. Mol. Biosyst., 3(5): 336–342.
- Baker J.R. Jr. (2009) Dendrimer-based nanoparticles for cancer therapy. Hematology Am. Soc. Hematol. Educ. Program, 708–719.
- Cai W., Chen X. (2007) Nanoplatforms for targeted molecular imaging in living subjects. Small, 3(11): 1840–1854.
- Caruthers S.D., Winter P.M., Wickline S.A., Lanza G.M. (2006) Targeted magnetic resonance imaging contrast agents. Methods Mol. Med., 124: 387–400.
- Chen K., Chen X. (2010) Design and development of molecular imaging probes. Curr. Top. Med. Chem., 10(12): 1227–1236.
- Cho K., Wang X., Nie S. et al. (2008) Therapeutic nanoparticles for drug delivery in cancer. Clin. Cancer Res., 14(5): 1310–1316.
- Choi Y., Thomas T., Kotlyar A. et al. (2005) Synthesis and functional evaluation of DNA-assembled polyamidoamine dendrimer clusters for cancer cell-specific targeting. Chem. Biol., 12(1): 35–43.
- Corsi F., Prosperi D. (2010) Molecular nanoclinics: Dream or reality? Pharmacol. Res., 62(2): 55–56.
- Corydon T.J., Mikkelsen J.G. (2006) RNA interference — towards individualized genetic medicine. Ugeskr. Laeger, 168(50): 4401–4404.
- Davies K. (2010) The $1,000 Genome: The Revolution in DNA Sequencing and the New Era of Personalized Medicine. FREE PRESS, New York, 340 p.
- de Dios A.S., Díaz-García M.E. (2010) Multifunctional nanoparticles: analytical prospects. Anal. Chim. Acta, 666(1–2): 1–22.
- Debbage P. (2009) Targeted drugs and nanomedicine: present and future. Curr. Pharm. Des., 15(2): 153–172.
- Derfus A.M., Chen A.A., Min D.H. et al. (2007) Targeted quantum dot conjugates for siRNA delivery. Bioconjug Chem., 18(5): 1391–1396.
- Farokhzad O.C., Langer R. (2009) Impact of nanotechnology on drug delivery. ACS Nano, 3(1): 16–20.
- Geho D.H., Jones C.D., Petricoin E.F., Liotta L.A. (2006) Nanoparticles: potential biomarker harvesters. Curr. Opin. Chem. Biol., 10(1): 56–61.
- Ginsburg G.S., Donahue M.P., Newby L.K. (2005) Prospects for personalized cardiovascular medicine: the impact of genomics. J. Am. Coll. Cardiol., 46(9): 1615–1627.
- Guo K.T., Ziemer G., Paul A., Wendel H.P. (2008) CELL-SELEX: Novel perspectives of aptamer-based therapeutics. Int. J. Mol. Sci., 9(4): 668–678.
- Hess H., Jaeger L. (2010) Nanobiotechnology. Curr. Opin. Biotechnol., 21(4): 373–375.
- Iverson N., Plourde N., Chnari E. et al. (2008) Convergence of nanotechnology and cardiovascular medicine: progress and emerging prospects. BioDrugs, 22(1): 1–10.
- Jaffer F.A., Weissleder R. (2004) Seeing within: molecular imaging of the cardiovascular system. Circ. Res., 94(4): 433–445.
- Jain K.K. (2007) Applications of nanobiotechnology in clinical diagnostics. Clin. Chem., 53(11): 2002–2009.
- Jain K.K. (2009a) Textbook of Personalized Medicine. Springer, New York, 419 p.
- Jain K.K. (2009b) The role of nanobiotechnology in drug discovery. Adv. Exp. Med. Biol., 655: 37–43.
- Kaneda M.M., Caruthers S., Lanza G.M., Wickline S.A. (2009) Perfluorocarbon nanoemulsions for quantitative molecular imaging and targeted therapeutics. Ann. Biomed. Eng., 37(10): 1922–1933.
- Kooi M.E., Cappendijk V.C., Cleutjens K.B. et al. (2003) Accumulation of ultrasmall superparamagnetic particles of iron oxide in human atherosclerotic plaques can be detected by in vivo magnetic resonance imaging. Circulation, 107(19): 2453–2458.
- Lanza G.M., Winter P.M., Caruthers S.D. et al. (2006) Nanomedicine opportunities for cardiovascular disease with perfluorocarbon nanoparticles. Nanomedicine (Lond, 1(3): 321–329.
- Lee J., Choi Y., Kim K. et al. (2010) Characterization and cancer cell specific binding properties of anti-EGFR antibody conjugated quantum dots. Bioconjug Chem., 21(5): 940–946.
- Lee S.H., Shin D.J., Jang Y. (2009) Personalized medicine in coronary artery disease: insights from genomic research. Korean Circ. J., 39(4): 129–137.
- Lesniak W., Bielinska A.U., Sun K. (2005) Silver/dendrimer nanocomposites as biomarkers: fabrication, characterization, in vitro toxicity, and intracellular detection. Nano Lett., 5(11): 2123–2130.
- Liu A., Zhao Q., Guan X. (2010) Stochastic nanopore sensors for the detection of terrorist agents: current status and challenges. Anal. Chim. Acta, 675(2): 106–115.
- Lukianova-Hleb E.Y., Mrochek A.G., Lapotko D.O. (2009) Method for disruption and re-canalization of atherosclerotic plaques in coronary vessels with photothermal bubbles generated around gold nanoparticles. Lasers Surg. Med., 41(3): 240–247.
- Mahmoud W., Sukhanova A., Oleinikov V. et al. (2010) Emerging applications of fluorescent nanocrystals quantum dots for micrometastases detection. Proteomics., 10(4): 700–716.
- Marcato P.D., Durán N. (2008) New aspects of nanopharmaceutical delivery systems. J. Nanosci. Nanotechnol., 8(5): 2216–2229.
- Medina S.H., El-Sayed M.E. (2009) Dendrimers as carriers for delivery of chemotherapeutic agents. Chem. Rev., 109(7): 3141–3157.
- Mirsaidov U.M., Wang D., Timp W., Timp G. (2010) Molecular diagnostics for personal medicine using a nanopore. Wiley Interdiscip. Rev. Nanomed. Nanobiotechnol., 2(4): 367–381.
- Naghavi M., Libby P., Falk E. et al. (2003) From vulnerable plaque to vulnerable patient: a call for new definitions and risk assessment strategies: Part I. Circulation, 108(14): 1664–1672.
- Nordström A., Lewensohn R. (2010) Metabolomics: moving to the clinic. J. Neuroimmune Pharmacol., 5(1): 4–17.
- Pan D., Caruthers S.D., Chen J. et al. (2010) Nanomedicine strategies for molecular targets with MRI and optical imaging. Future Med. Chem., 2(3): 471–490.
- Pettersson E., Lundeberg J., Ahmadian A. (2009) Generations of sequencing technologies. Genomics, 93(2): 105–111.
- Roukos D.H. (2009) Personalized cancer diagnostics and therapeutics. Expert. Rev. Mol. Diagn., 9(3): 227–229.
- Roukos D.H. (2010) Systems medicine: a real approach for future personalized oncology? Pharmacogenomics, 11(3): 283–287.
- Saito M., Yoshino T. (2010) Clinical development of biomarkers for personalized medicine. Nippon Rinsho, 68(6): 1111–1116.
- Sajja H.K., East M.P., Mao H. et al. (2009) Development of multifunctional nanoparticles for targeted drug delivery and noninvasive imaging of therapeutic effect. Curr. Drug Discov. Technol., 6(1): 43–51.
- Schmieder A.H., Winter P.M., Caruthers S.D. et al. (2005) Molecular MR imaging of melanoma angiogenesis with alphanubeta3-targeted paramagnetic nanoparticles. Magn. Reson. Med., 53(3): 621–627.
- Schneider G.F., Kowalczyk S.W., Calado V.E. et al. (2010) DNA translocation through graphene nanopores. Nano Lett., 10(8): 3163-3167.
- Schoenhagen P., Conyers J.L. (2008) Nanotechnology and atherosclerosis imaging: emerging diagnostic and therapeutic applications. Recent Pat. Cardiovasc. Drug Discov., 3(2): 98–104.
- Sharon D., Chen R., Snyder M. (2010) Systems biology approaches to disease marker discovery. Dis. Markers, 28(4): 209–224.
- Stambuk S., Sundov D., Kuret S. et al. (2010) Future perspectives of personalized oncology. Coll. Antropol., 34(2): 763–769.
- Stofik M., Strýhal Z., Malý J. (2009) Dendrimer-encapsulated silver nanoparticles as a novel electrochemical label for sensitive immunosensors. Biosens. Bioelectron, 24(7): 1918–1923.
- Tian Z., Wang H., Jia Z. et al. (2010) Tumor-Targeted Inhibition by a Novel Strategy — Mimoretrovirus Expressing siRNA Targeting the Pokemon Gene. Curr. Cancer Drug Targets, 10(8): 932–941.
- Tiemann K., Rossi J.J. (2009) RNAi-based therapeutics-current status, challenges and prospects. EMBO Mol. Med., 1(3): 142–151.
- Tokatlian T., Segura T. (2010) siRNA applications in nanomedicine. Wiley Interdiscip. Rev. Nanomed. Nanobiotechnol., 2(3): 305–315.
- Trent R.J. (2010) Pathology practice and pharmacogenomics. Pharmacogenomics, 11(1): 105–111.
- Trivedi R.A., U-King-Im J.M., Graves M.J. et al. (2004) In vivo detection of macrophages in human carotid atheroma: temporal dependence of ultrasmall superparamagnetic particles of iron oxide-enhanced MRI. Stroke, 35(7): 1631–1635.
- Upadhyay K.K., Agrawal H.G., Upadhyay C. et al. (2009) Role of block copolymer nanoconstructs in cancer therapy. Crit. Rev. Ther. Drug Carrier Syst., 26(2): 157–205.
- Wang M.D., Shin D.M., Simons J.W., Nie S. (2007) Nanotechnology for targeted cancer therapy. Expert Rev. Anticancer Ther., 7(6): 833–837.
- Wickline S.A., Neubauer A.M., Winter P. et al. (2006) Applications of nanotechnology to atherosclerosis, thrombosis, and vascular biology. Arterioscler. Thromb. Vasc. Biol., 26(3): 435–441.
- Willard H.F., Ginsburg G.S. (Eds) (2008) Genomic and Personalized Medicine. Academic Press, 1558 p.
- Wolf S.M., Gupta R., Kohlhepp P. (2009) Gene therapy oversight: lessons for nanobiotechnology. J. Law Med. Ethics., 37(4): 659–684.
- Xu M., Fujita D., Hanagata N. (2009) Perspectives and challenges of emerging single-molecule DNA sequencing technologies. Small, 5(23): 2638–2649.
- Zhou S.F., Di Y.M., Chan E. et al. (2008) Clinical pharmacogenetics and potential application in personalized medicine. Curr. Drug Metab., 9(8): 738–784.
Персоналізована медицина: перспективи застосування нанобіотехнологій
В.М. Залеський, Б.О. Мовчан
Резюме. Огляд присвячений обговоренню перспективних напрямів персоналізованої діагностики і терапії в кардіології та онкології при використанні інноваційних нанобіотехнологій. Наведено результати основних досліджень з цього питання.
Ключові слова: персоналізована медицина, нанобіотехнології, кардіологія, онкологія.
Рersonalized medicine: perspectives used of the nanobiotechnology
V.N. Zalessky, B.A. Movchan
Summary. Perspective diagnostic and therapeutic methods of the personalized medicine in cardiology and oncology with used of innovation nanobiotechnology are examineted in the review. The results of the principal trials regarding this question are provided.
Key words: personalized medicine, nanobiotechnology, cardiology, oncology.
Адрес для переписки:
Залесский Вячеслав Николаевич
03151, Киев, ул. Народного ополчения, 5
Национальный научный центр «Институт кардиологии имени Н.Д. Стражеско» НАМН Украины
Источник