Метаболизм лекарственных веществ в организме
ЛС, поступившие в организм, являются для него ксенобиотиками, т. е. чужеродными агентами, следовательно, они подлежат выведению. Комплекс физико-химических и (или) биохимических реакций, в результате которых ЛС превращается в более полярное (водорастворимое) соединение, т. е. продукт, который легче выводится из организма, называется биотрансформацией.
Как правило, химические соединения, образовавшиеся в результате биотрансформации ЛС, менее активны и менее токсичны, однако возможно образование как более токсичных, так и более фармакологически активных соединений (в результате биотрансформации кортизола образуется фармакологически более активный гормон — гидрокортизон, а в результате биотрансформации противокашлевого препарата кодеина образуется наркотический анальгетик морфин).
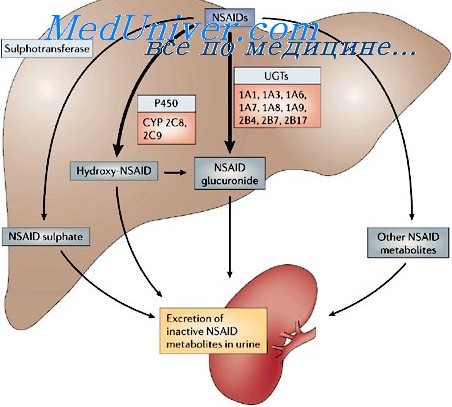
Биотрансформация лекарств почти исключительно (на 90–95%) протекает в печени. Остальные количества инактивируются в тканях ЖКТ, легких, коже и плазме крови. Некоторое количество ЛС выводится из организма в неизмененном виде.
Выделяют 2 основных вида превращения лекарственных препаратов :
Метаболическая трансформация (реакции I фазы, несинтетические реакции метаболизма).
Конъюгация (реакции II фазы, синтетические реакции метаболизма).
Метаболическая трансформация— это превращение лекарственных веществ за счет окисления, восстановления, гидролиза и др.
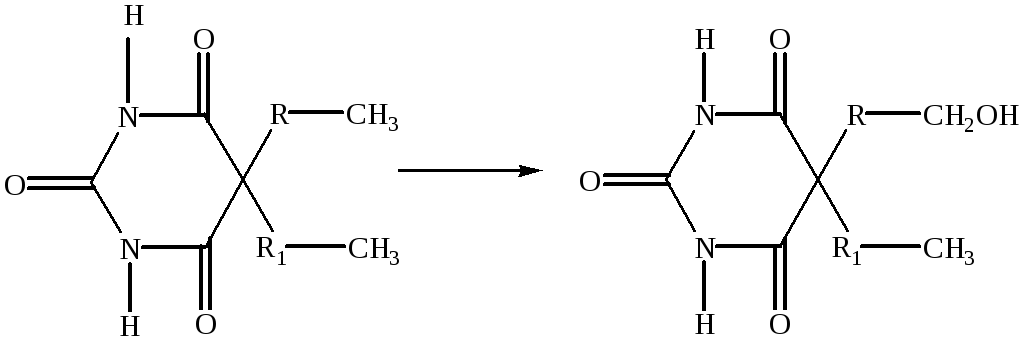
Окисление— один из наиболее характерных и частых путей инактивации препаратов. Осуществляется в гепатоцитах системой микросомальных ферментов оксидаз (основной представитель — цитохром Р-450).
барбитурат Окисление заместителей
Восстановление— сравнительно редкий путь превращения. Он характерен, в частности, для гормонов стероидной структуры и их аналогов.
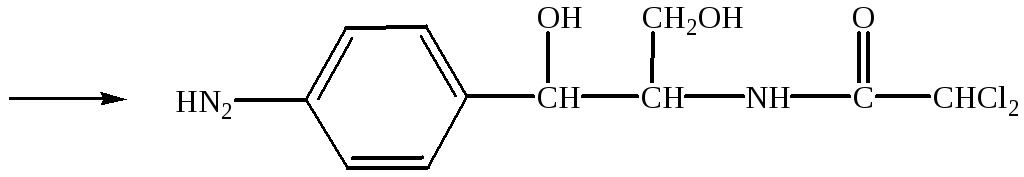
восстановление нитрогруппы в аминогруппу
Гидролиз — очень важный путь инактивации сложных эфиров и амидов, к которым относятся многие ЛС. В процессе гидролиза происходит расщепление сложной эфирной или амидной связи с присоединением воды.
парааминобензойная кислота диэтиламиноэтанол
Конъюгация— это биосинтетический процесс, сопровождающийся присоединением к лекарственному веществу или его метаболитам ряда химических группировок или молекул эндогенных соединений (метилирование, ацетилирование, взаимодействие с глюкуроновой кислотой, сульфатами, глутатионом).
На биотрансформацию ЛС оказывает непосредственное влияние достаточно большое количество факторов:
Возраст (у новорожденных система микросомальных ферментов печени очень несовершенна).
Пол (в опытах на крысах показано, что самцы быстрее метаболизируют лекарственные вещества, что связывают со стимулирующим действием мужских половых гормонов на синтез микросомальных ферментов).
Генетические факторы (генетически обусловленный уровень активности псевдохолинэстеразы).
Вредные привычки (никотин и алкоголь повышает активность микросомальных ферментов и, следовательно, скорость метаболизма одновременно применяемых веществ).
Функциональное состояние печени (при патологии печени нарушается метаболизм лекарственных веществ).
Источник
Что такое конъюгация лекарственных веществ
Конъюгация — ферментативное присоединение химических радикалов к молекуле лекарства или к метаболиту, образовавшемуся во время фазы 1.
Реакции фазы 2, называемые конъюгацией, происходят в самых разнообразных тканях. Чаще всего эти реакции заключаются в опосредованном ферментами присоединении гидрофильных компонентов, таких как глюкуроновая кислота, сульфат, глутатион и ацетат, к функциональной группе родительской молекулы и/или метаболиту, образовавшемуся во время фазы 1. Глюкуроновая кислота сначала активируется, соединяясь с уридиндифосфатом (УДФ). Затем активированное соединение УДФ-глюкуроновая кислота переносится на лекарство с помощью фермента глюкуронозилтрансферазы. Образовавшиеся в результате таких реакций конъюгаты обычно более гидрофильны, чем родительское лекарство или его метаболиты фазы 1, поэтому они легче экскретируются почками.
В целом конъюгаты фармакологически менее активны, чем родительское лекарство, однако не всегда. Иногда в реакциях конъюгации участвуют такие замещающие группы, как глицин, метильные группы и сахара глюкоза и рибоза.
Конъюгация обычно повышает водорастворимость, а ацетилирование приводит к образованию метаболитов, менее растворимых в воде, чем неконъюгированный предшественник (например, в случае ацетилирования сульфонамидных антибиотиков). Ацетилирование функциональной основной аминогруппы превращает основное лекарство в слабую кислоту (амид). Это химическое изменение влияет на распределение и элиминацию образующегося метаболита.
Реакции конъюгации обычно рассматривают как процесс инактивации, но существует несколько исключений. Например:
• ацетилирование антиаритмического лекарства прокаинамида приводит к образованию N-ацетилпрокаинамида, также обладающего антиаритмическими свойствами, хотя и отличающегося по спектру действия, блокирующего ионные каналы, от родительского лекарства;
• морфин-6-глюкуронид представляет собой анальгетик с более продолжительным действием, чем родительское лекарство, морфин.
Нарушение функции почек отражается на терапевтических и токсических эффектах обоих метаболитов.
Конъюгация с сульфатами может представлять собой реакцию активации. Миноксидил, антигипертензивное лекарство, должен быть сульфатирован в N-оксидной позиции, чтобы вызывать эффект вазодилатации. Миноксидил также способствует росту волос, однако в меньшей степени, чем его сульфатированный метаболит, поэтому наблюдаемые вариации роста волос отчасти могут быть связаны с различной способностью организма сульфатировать миноксидил в волосяных фолликулах.
Открыты множественные изоформы конъюгирующих ферментов и определена их относительная специфичность в отношении различных субстратов и метаболитов. Описаны по меньшей мере 2 семейства и 3 подсемейства глюкуронозилтрансфераз, а также продукты многих генов, выполняющие функции ацетилирования и сульфатирования.
Доза изониазида, прокаинамида и гидралазина зависит от способности организма ацетилировать эти лекарства. Чем выше скорость ацетилирования, тем большая доза необходима для поддержания терапевтической концентрации лекарства в плазме. Фенотипически медленные ацетиляторы могут стать быстрыми ацетиляторами, если некоторые лекарства принимают внутрь вместе с этанолом. Это происходит, если пациенты, принимающие прокаинамид или сульфаметазин, одновременно употребляют алкоголь.
Дефицит одной или нескольких изоформ конъюгирующих ферментов может повлиять на выбор лекарства. В связи с этим определение способности организма метаболизировать прототипичные субстраты дает возможность подобрать лекарственную терапию для конкретного пациента. Можно привести два клинически значимых примера:
• больным раком и с дефицитом тиопуринметилтрансферазы необходимо в 10-15 раз снизить дозу 6-меркаптопурина, чтобы уменьшить риск токсического воздействия лекарства на гемопоэз;
• больным раком и с недостаточностью экспрессии изоформы UGTIA1 глюкуронозилтрансферазы следует снизить дозу иринотекана, ингибитора топоизомеразы I, чтобы уменьшить вероятность возникновения миелосупрессии и диареи.
Источник
1.4. Биотрансформация лекарственных веществ
Биотрансформация (метаболизм) — изменение химической струк- туры и физико-химических свойств ЛВ под действием ферментов организма. Основная направленность этого процесса — удаление чужеродных соединений, в том числе ЛВ, из организма путем пре- вращения неполярных липофильных веществ в полярные гидрофильные соединения. Так как полярные гидрофильные вещества в отличие от липофильных не реабсорбируются в почечных канальцах, они быстро выводятся почками, а некоторые из них выводятся с желчью в просвет кишечника.
Биотрансформация липофильных ЛВ в основном происходит под действием ферментов печени, локализованных в мембране эндо- плазматического ретикулума гепатоцитов. Эти ферменты называются микросомальными, так как они оказываются связанными с мелкими субклеточными фрагментами гладкого эндоплазматическо- го ретикулума(микросомами), которые образуются при гомогенизации печеночной ткани или тканей других органов и могут быть выделены центрифугированием (осаждаются в так называемой «микросомальной» фракции). Основное место локализации микросомальных фер- ментов — гепатоциты, но обнаружены они также и в других органах (кишечнике, почках, легких, головном мозге).
В плазме крови, а также в печени, стенке кишечника, почках, лег- ких, коже, слизистых оболочках и других тканях имеются н е м и к — росомальные ферменты, локализованные в цитозоле или митохондриях.
Различают два основных вида метаболизма ЛВ:
• несинтетические реакции (метаболическая трансформация);
• биосинтетические реакции (конъюгация).
Большинство ЛВ сначала метаболизируется при участии реакций метаболической трансформации с образованием реакционноспо- собных метаболитов, затем вступающих в реакции конъюгации.
При конъюгации к ЛВ или их метаболитам присоединяются остатки эндогенных соединений (глюкуроновой кислоты и др.) или химичес- кие группировки (ацетильные, метильные), поэтому реакции конъюгации обозначают термином«биосинтетическая трансформация».
Реакции метаболической трансформации включают окисление, восстановление, гидролиз.
Окисление. Многие липофильные соединения подвергаются окислению в печени под действием микросомальной системы ферментов, известных как оксидазы смешанных функций (или монооксигеназы), основным компонентом которой является цитохром Р-450 (гемопротеин, связывающий ЛВ и кислород в своем активном центре). Реакция протекает при участии цитохром Р-450 редуктазы и НАДФН, который является донором электронов. В результате после восстановления молекулярного кислорода происходит присоединение одного атома кислорода к субстрату (ЛВ) с образованием окисленного метаболита и включение другого атома кислорода в молекулу воды.
RH + O2 + НАДФН + H + → ROH + H2O + НАДФ + ,
где RH — лекарственное вещество, а ROH — метаболит.
Кислород может быть включен в молекулу субстрата в составе гид- роксильной группы (реакция гидроксилирования),эпоксидной группы (реакция эпоксидации), может замещать аминогруппу (реакция дезаминирования) или атом серы. В реакциях дезалкилирования метаболиты образуются при включении кислорода в алкильную группу, которая отделяется от молекулы субстрата. Примеры реакций микросомаль- ного окисления приведены в табл. 1-1.
Оксидазы смешанных функций в целом обладают низкой суб- стратной специфичностью и могут метаболизировать многие химические соединения. В то же время отдельные изоформы (изоферменты) цитохрома Р-450 (Cytochrome P-450, CYP)отличаются определенной специфичностью (каждая из них участвует в метаболизме относительно небольшого количества веществ). В настоящее время известно более тысячи изоферментов цитохрома Р-450, подразделяемых на семейства и подсемейства. Изоформы, имеющие более 40% общего аминокислотно-
Основные реакции метаболизма (биотрансформации) лекарственных веществ
Реакции биотрансформации Лекарственные вещества
Фенобарбитал, фенитоин, пропранолол, варфарин
Толбутамид, ибупрофен, дигитоксин, барбитураты
Морфин, хинидин, парацетамол
Диазепам, амфетамин, эфедрин
Морфин, кодеин, кофеин, теофиллин
Прокаин, ацетилсалициловая кислота, эналаприл, суксаметония бромид
Амидов Прокаинамид, индометацин
Конъюгация с остатком глюкуроновой кислоты (образование эфиров, тиоэфиров или амидов глюкуроновой кислоты)
Парацетамол, хлорамфеникол, диазепам, морфин, дигоксин, салициловая кислота
Конъюгация с остатком серной кислоты (образование сульфатов)
Конъюгация с глицином
Конъюгация с глутатионом
Этакриновая кислота, доксорубицин
го состава, объединены в семейства и обозначаются арабскими цифрами (CYP1, CYP2, CYP3 и т. д.). Подсемейства, обозначаемые латинскими буквами, объединяют изоформы с идентичностью аминокислотного
состава более 55% (CYP2D, CYP3A и т.д.) Отдельные изоферменты обозначают арабскими цифрами, следующими за латинскими буквами (CYP1A2, CYP2D6, CYP3A4). ЛВ могут быть субстратами двух и более изоферментов, при этом различные изоферменты способны метаболизировать одно вещество в различных участках его молекулы. В табл. 1-2 приведены основные изоферменты цитохрома Р-450 печени человека, принимающие участие в метаболизме ЛС, и примеры ЛВ, являющихся субстратами этих изоферментов. Наибольшее количество ЛВ метаболизируется при участии CYP3A4.
Окисление некоторых ЛВ происходит при участии немикросомальных ферментов, локализованных в цитозоле, митохондриях, лизосомах и цитоплазматических мембранах клеток. Для этих ферментов характерна субстратная специфичность. Так, моноаминоксидаза типа А (МАО-А) осуществляет окислительное дезаминирование катехоламинов (норадреналина, адреналина, серотонина и др.), под действием алкогольдегидрогеназы этанол окисляется до ацетальдегида, под действием ксантиноксидазы происходит гидроксилирование пуриновых соединений (аллопуринола, теофиллина).
Восстановление лекарственных веществ заключается в присоединении к его молекуле атома водорода или удалении атома кислорода. Эти реакции могут протекать при участии микросомальных (восстановление хлорамфеникола) и немикросомальных (восстановление хлоралгидрата) ферментов. Некоторые ЛВ (например, месалазин) восстановливаются в кишечнике под действием редуктаз, продуцируемых кишечными бактериями.
Гидролиз большинства ЛВ осуществляют немикросомальные фер- менты (эстеразы, амидазы, фосфатазы) в плазме крови и тканях (в основном в печени). Вследствие присоединения воды происходит разрыв эфирных, амидных и фосфатных связей в молекулах ЛВ. Гидролизу подвергаются сложные эфиры (суксаметоний, прокаин, бензокаин, ацетилсалициловая кислота) и амиды (прокаинамид, индометацин). Некоторые ЛВ гидролизуются под действиеммикросомальных ферментов, например амидаз (местные анестетики из группы амидов). Микросомальный фермент эпоксидгидролаза гидролизует высокореактивные метаболиты, образующиеся при микросомальном окислении некоторых ЛВ (например, карбамазепина) с образованием неактивных соединений.
В процессе метаболической биотрансформации обычно происходит снижение активности и токсичности исходных веществ. Однако метабо-
Основные изоферменты цитохрома Р-450, участвующие в метаболизме лекарственных веществ, их индукторы и ингибиторы
Кофеин, теофиллин, парацетамол, варфарин, тамоксифен, кломипрамин
Фенобарбитал, омепразол, рифампицин, вещества, содержащиеся в сигаретном дыме и жареной пище (бензопирены, метилхолантрены), броколли, брюссельская капуста
Ципрофлоксацин, циметидин, кларитромицин, эритромицин
Ибупрофен, фенитоин, толбутамид, варфарин
Диклофенак, сульфаниламиды циметидин, этанол (однократно)
Диазепам, напроксен, пропранолол, омепразол
Кодеин, клозапин, омепразол, метопролол, тимолол, галоперидол, трициклические антидепрессанты
Амиодарон, галоперидол, флуоксетин, хини- дин, циметидин
Этанол, парацетамол, галотан, энфлуран
Этанол (хронический прием), изониазид
Амиодарон, варфарин, верапамил, диазепам, дилтиазем, кетоконазол, кортикостероиды, кокаин ловастатин, лидокаин, лозартан, макролиды, мидазолам, нифедипин, прогестерон, ритонавир, спиронолактон, сульфаметоксазол, тестостерон, циклоспорин, хинидин, этинилэстрадиол
Барбитураты, рифампицин, фенитоин, карбамазепин, глюкокортикоиды, фенилбутазон, трава зверобоя
Кетоконазол, метронидазол, омепразол, циметидин, хинидин, ципрофлоксацин, эритромицин, кларитромицин, хинидин, фуранокумарины сока грейпфрута
литы, образуемые в результате несинтетических реакций, могут обладать такой же, а иногда и более высокой активностью, чем исходные соединения. Образование активных метаболитов обеспечивает длительное действие некоторых ЛВ (например, диазепама). Примером ЛВ, неактивных в исходном состоянии и активируемых в процессе метаболизма, являются предшественники лекарств (пролекарства). Например, антигипертензивные средства из группы ингибиторов ангиотен-превращающего фермента (эналаприл, фозиноприл) гидролизуются в организме с образованием активных соединений. С помощью пролекарств могут решаться проблемы с доставкой ЛВ к месту его действия. Так, предшественник дофамина леводопа в отличие от дофамина проникает в ЦНС, где под влиянием ДОФА-декарбоксилазы превращается в дофамин.
В некоторых случаях в процессе метаболической трансформации образуются токсичные соединения. Примером является образование промежуточного токсичного метаболита (N-ацетил-пара-бензохино- нимина) при микросомальном окислении анальгетика парацетамола. Инактивация этого метаболита происходит в результате связывания с глутатионом, однако при истощении запасов глутатиона (в основном вследствие передозировки препарата) он оказывает токсическое действие на печень.
В процессе б и о с и н т е т и ч е с к и х р е а к ц и й к функциональным группировкам (аминогруппам, гидроксильным, карбоксильным группам) молекул ЛВ или их метаболитов присоединяются остатки эндогенных соединений (глюкуроновой или серной кислоты, глутатиона, глицина др.) или высокополярные химические группы (ацетильные, метильные). Эти реакции протекают при участии ферментов (в основном, трансфераз) печени, а также ферментов других тканей (легких, почек). Содержатся ферменты в эндоплазматическом ретикулуме гепатоцитов (микросомальные ферменты) или в цитозольной фракции.
Наиболее общей реакцией является конъюгация с глюкуроновой кислотой. Присоединение остатков глюкуроновой кислоты (образование глюкуронидов) происходит при участии микросомального фермента уридилдифосфат-глюкуронилтрансферазы (цитохром Р-450-содержащий фермент), обладающего низкой субстратной специфичностью, вследствие чего этот фермент метаболизирует многие ЛВ
и их метаболиты (а также некоторые эндогенные вещества, например билирубин).
В реакцию конъюгации с глутатионом вступают некоторые реакционноспособные вещества (эпоксиды, хиноны), в том числе проме- жуточные метаболиты, образующиеся в результате микросомального окисления (например, парацетамола), в результате чего резко снижается их токсичность.
В процессе конъюгации образуются высокополярные гидрофильные соединения, которые быстро выводятся почками или с желчью в просвет кишечника. Конъюгаты, как правило, менее активны и ток- сичны, чем исходные ЛВ или их метаболиты.
Факторы, влияющие на биотрансформацию лекарственных веществ
Активность ферментов, метаболизирующих ЛВ, а следовательно, скорость их биотрансформации зависит от пола, возраста, состояния организма, одновременного назначения других ЛС, а также от некоторых веществ, содержащихся в продуктах питания.
У мужчин активность микросомальных ферментов выше, чем у женщин, так как синтез этих ферментов стимулируется мужскими половыми гормонами. Такие вещества, как этанол, эстрогены, бензодиазепины, салицилаты метаболизируются быстрее у мужчин, чем у женщин.
В эмбриональном периоде отсутствует большинство ферментов метаболизма ЛВ. У новорожденных в первые 2-4 нед жизни активность многих ферментов (в частности, ферментов, участвующих в реакциях конъюгации) снижена и достигает достаточного уровня лишь через 1-6 мес. Поэтому детям в первые недели жизни не рекомендуется назначать такие ЛВ, как хлорамфеникол, так как вследствие недостаточной активности микросомальных ферментов, замедлены процессы конъюгации его токсичного метаболита.
В старческом возрасте снижается активность некоторых микросомальных ферментов, печеночный кровоток и масса печени, вследствие чего уменьшается скорость метаболизма многих ЛВ (лицам старше 60 лет, такие препараты назначают в меньших дозах).
При заболеваниях печени снижается активность микросомальных ферментов и замедляется биотрансформация многих ЛВ, что приводит к усилению и удлинению их действия. Уменьшение скорости кровото-
ка также существенно замедляет метаболизм некоторых ЛВ (морфина, лидокаина), поэтому при сердечной недостаточности обычные дозы этих препаратов могут вызвать токсические эффекты. Нарушения функций щитовидной железы повышают (при гипертиреозе) или снижают (при гипотиреозе) биотрансформацию ЛВ. Сахарный диабет и другие нарушения функции эндокринной системы также влияют на лекарственный метаболизм.
Синтез микросомальных ферментов может повышаться (индукция ферментов) под действием различных ЛВ, некоторых веществ, содержащихся в продуктах питания, сигаретном дыме, окружающей среде и т.д. Индукции могут подвергаться ферменты, участвующие как в несинтетических реакциях, так и в реакциях конъюгации (в основном, с глюкуроновой кислотой).
При воздействии индукторов микросомальных ферментов повышается скорость биотрансформации ЛВ, которые метаболизируются этими ферментами (см. табл. 1-2), что приводит к ослаблению их тера- певтического действия. Поскольку CYP3A4 участвует в метаболизме многих ЛВ (более 60% препаратов, применяемых в клинической практике), индукция этого изофермента достаточно часто может иметь нежелательные последствия. Некоторые ЛВ (например, фенобарбитал, рифампицин) являются универсальными индукторами, повышая активность нескольких изоферментов цитохрома Р-450, в том числе CYP3A4 и, как следствие, ослабляют терапевтический эффект многих ЛВ. Например, эффективность пероральных контрацептивов может снизиться на фоне лечения рифампицином или фенобарбиталом из-за ускорения метаболизма входящих в их состав эстрогенов и прогестинов.
Если в процессе биотрансформации ЛВ образуются токсичные метаболиты, индукция метаболизирующих это вещество ферментов приводит к повышению риска его токсического действия. Так, индукция CYP2E1 при хроническом употреблении алкоголя (см. табл. 1-2) увеличивает токсичность парацетамола.
Как правило, действие индукторов синтеза микросомальных ферментов (в том числе фенобарбитала) развивается медленно (в течение нескольких недель). Рифампицин оказывает более быстрый эффект, существенно повышая активность ферментов уже через несколько дней от начала применения.
Препараты некоторых лекарственных растений могут ускорять метаболизм ЛВ. Например, препараты зверобоя, применяемые в
качестве легких антидепрессантов, вызывают индукцию изофермента CYP3A4 и поэтому ослабляют или предупреждают действие ЛВ, которые метаболизируются при участии этого изофермента.
Полициклические ароматические углеводороды (бензопирены, метилхолантрены), содержащиеся в табачном дыме, некоторые вещества, применяемые в промышленности (например, полихлорированные бифенилы) или побочные продукты химического синтеза (диоксин) вызывают индукцию изофермента CYP1A2. Индукция изофермента CYP2E1 развивается при хроническом употреблении алкоголя (см. табл. 1-2).
В некоторых случаях может увеличиваться скорость метаболизма самого индуктора (аутоиндукция), вследствие чего ослабляются его фармакологические эффекты. Аутоиндукция весьма характерна для барбитуратов (в частности, фенобарбитала) и является причиной развития толерантности при их длительном приеме.
Некоторые ЛВ снижают активность микросомальных ферментов, в результате повышается концентрация в крови веществ, метаболизируемых этими ферментами. Это может привести к развитию токсических эффектов. Например, циметидин, некоторые макролидные антибиотики, кетоконазол, ципрофлоксацин, ингибируя цитохром CYP3A4/3А5, замедляют микросомальное окисление варфарина, что может усилить его антикоагулянтный эффект и спровоцировать кровотечение. Токсическое действие теофиллина, который метаболизируется при участии цитохрома CYP1A2, резко усиливается при его одновременном назначении с антибактериальным препаратом ципрофлоксацином, ингибирующим этот фермент. Фуранокумарины, содержащиеся в грейпфрутовом соке, ингибируют CYP3A4/3А5, в результате может усилиться действие многих
В отличие от индукторов метаболизма ингибиторы ферментов действуют быстрее (эффект ингибирования отмечен через 24 ч после приема соответствующего препарата).
При одновременном применении ЛВ с индукторами или ингибиторами их метаболизма необходимо корректировать назначаемые дозы этих веществ.
Изменение активности ферментов метаболизма ЛВ могут определяться генетическими факторами. Такие изменения имеют в своей основе передающиеся из поколения в поколение мутации генов, кодирующих синтез данных ферментов. Данный феномен носит название
генетического полиморфизма и имеет следствием значительные межиндивидуальные различия в метаболизме ЛВ. При этом у определенного процента больных, принимающих данное ЛВ, активность метаболизирующих ферментов может быть повышена, процесс биотрансформации ЛВ ускоряется, и его действие снижается. И наоборот, активность ферментов может быть снижена (недостаточность ферментов), вследствие чего биотрансформация ЛВ будет происходить медленнее, и действие его будет усиливаться вплоть до появления токсических эффектов. Часто отмечают генетический полиморфизм изоферментов цитохрома Р-450.
Известны случаи генетического полиморфизма ферментов, не имеющих отношения к системе цитохрома Р-450. Например, при аце- тилировании противотуберкулезного препарата изониазида у определенного процента больных в популяции выявляют недостаточность фермента N-ацетилтрансферазы («медленные ацетиляторы»), а у других больных активность этого фермента повышена («быстрые ацетиляторы»). У «медленных ацетиляторов» концентрация изониазида в плазме крови в 4-6 раз выше, чем у «быстрых ацетиляторов», что может быть причиной токсического действия препарата. Примеры влияния генетической недостаточности некоторых ферментов на действие ЛВ приведены в табл. 1-3.
Реакции организма на лекарственные вещества при генетической недостаточности некоторых ферментов
Источник