- Без признаков лечебного патоморфоза что означает
- Без признаков лечебного патоморфоза что означает
- Реферат
- Введение. Неоадъювантная химиотерапия — перспективный метод лечения больных колоректальным раком, однако данные об эффективности такого подхода и частоте ответа на лечение пока недоступны.
- Методы. В ретроспективное исследование были включены больные раком ободочной кишки, находившиеся на лечении в отделении онкопроктологии ФГБНУ «РОНЦ им. Н.Н. Блохина» в 2007-2014 годах, которым на дооперационном этапе проводилось 2 или более курсов химиотерапии. Основным оцениваемым параметром был лечебный патоморфоз. Проводился анализ выраженности лечебного патоморфоза в зависимости от схемы и количества курсов химиотерапии, наличия регионарных метастазов.
- Результаты. В исследование было включено 9 мужчин и 9 женщин. 9 пациентов с местно-распространенным раком T4N0-2M0 и 9 с отдаленными метастазами T3-4N0-2M1. Выраженность лечебного патоморфоза опухоли, соответствующая 1 и 2 степени по Dworak, была выявлена у 6 (33,3%) и 10 (55,5%) больных, соответственно. У 2 (11,1%) больных признаки лечебного патоморфоза в опухоли отсутствовали. Наиболее часто выраженный лечебный патоморфоз (2 степени) отмечался у больных, получавших химиотерапию c включением оксалиплатина — у 6 из 10 пациентов.
- Выводы. Неоадъювантная химиотерапия позволяет достичь лечебного патоморфоза у большинства пациентов. Клиническое значение этого фактора необходимо изучить в проспективных исследованиях.
- Ключевые слова: предоперационная химиотерапия, рак толстой кишки, патоморфоз опухоли.
- Целью нашего исследования была оценка эффективности неоадъювантной химиотерапии по показателям лечебного патоморфоза.
- Материалы и методы
- Результаты
- Таблица 1. Распределение пациентов в зависимости от частоты лечебного патоморфоза в первичной опухоли и вида используемой программы предоперационной химиотерапии
- Обсуждение
- Литература
Без признаков лечебного патоморфоза что означает
Вопрос о структуре самого лечебного патоморфоза болезни продолжает оставаться дискуссионным. Как известно, этиология н патогенез подавляющего большинства опухолевых болезней точно не установлены, а потому эти элементы не могут служить достоверными показателями патоморфоза. Наиболее значимыми являются изменения клинических и морфологических проявлений болезни.
Именно эти изменения входят в число существенных признаков, раскрывающих содержание понятия. В разряд патоморфоза следует отнести изменчивость н другие элементы болезни, в частности, ее осложнения, неходы н непосредственные причины смерти.
Часто возникает вопрос о том, все ли изменения болезни и опухоли можно отнести к патоморфозу. Отвечая на этот вопрос, следует заметить, что к патоморфозу могут быть отнесены лишь типовые и стойкие изменения болезни (опухоли) Я. Л. Раппопорт (1962) подчеркивал, что нозоморфоз — это не эксцесс, выходящий за рамки клинико-анатомических вариаций, свойственных данной опухоли. Нозоморфоз представляет собой типичное для данной опухоли (либо для данного метода лечения) явление.
Следует при этом, однако, помнить, что «типичное», «стандартное» для опухоли весьма относительно, как относительна и сама клиническая и морфологическая характеристика патоморфоза. Вместе с тем патоморфоз — это не беспорядоч ное н хаотичное изменение. Изучение проявлений и механизмов патоморфоза позволяет выделить его общую и главную черту — перестройку закономерностей происхождения и развития болезни (родовое понятие) на уровне вида, популяции и индивидуума (видовое отличие).
Иными словами, в понятие «патоморфоз» входят типичные явления, повторяющиеся существенные отношения, отражающие определенные и во многом пока еще не установленные закономерности возникновения, развития и проявления опухолевого процесса.
Следует отметить, что по мере усовершенствования лучевых методов лечения и увеличения числа лекарственных средств с усилением их лечебных свойств при химиотерапии возрос не только лечебный потенциал врача-онколога, но также возросло и количество повреждений различных органов и тканей. Ятрогенные патологические процессы не только изменяют клинико-анатомические проявления опухолевой болезни, но и могут быть непосредственной причиной смерти. Однако разнообразные неблагоприятные реакции на медикаментозные средства, а также осложнения, вызванные хирургическими и терапевтическими вмешательствами, в проявление патоморфоза включать не следует.
Установление патоморфоза опухолевых болезней представляет интерес с точки зрения практики и теории медицины. Данные о патоморфозе опухолей используют на практике для сравнения разных методов лечения, для оценки эфектквкости проводимого (или уже законченного) лечения для объективного обоснования прогноза и его критериев, для оптимизации сроков диспансерного наблюдения и экспертизы трудоспособности, а также для других целей. Наблюдения патоморфоза в клинике одновременно являются основой для теоретических разработок в различных областях онкологии, патологии, радиобиологии и т. д.
Сюда можно отнести разработку принципов лечения злокачественных новообразований, изучение сущности биологического действия ионизирующих излучений, взаимоотношения опухоли и организма в условиях лечения, восстановления повреждений нуклеиновых кислот и клеточных органелл и т. д.
В качестве примера важности изучения лечебного патоморфоза опухолей достаточно привести данные ВОЗ (Женева, 1982) из доклада «Оптимизация лучевой терапии». Различия в характере используемых методов противораковой терапии свидетельствуют о том, что даже в развитых странах еще не удалось добиться повсеместной оптимизации ее программ. Около одной трети всех больных раком нуждаются в лучевой терапии либо отдельно, либо в сочетании с хирургическим лечением, тогда как потребность в хирургическом лечении отдельно или в сочетании с другими методами выявляется в половине случаев заболевания раком.
Менее одной десятой всех больных раком подвергаются химиотерапии, гормонотерапии и другим видам лечения, а около четверти всех больных либо не получают специфического лечения, либо находятся на слишком поздних стадиях заболевания для применения соответствующих методов лечения. Следовательно, знание особенностей патоморфоза болезни и патоморфоза опухоли необходимо для оптимизации лечения. Решение этой проблемы требует решения многих частных вопросов, например, определяет ли гистологическое строение опухоли ее чувствительность к лечебному фактору (излучению, хнмиопрепарату, гормону и т. д.). В широком плане вопрос должен решаться в рамках проблемы взаимоотношения общего и частного с тем, чтобы не уклониться в морфологизм, функционализм и другие крайности.
В зависимости от клинической ситуации и цели исследования для выявления и оценки патоморфоза можно использовать любые доступные методы и подходы клинические, морфологические, радиологические, рентгено логические, биохимические и др. Неуклонно возрастает роль цитологических исследований в оценке патоморфоза. Каждый метод используемся либо самостоятельно, либо в комплексе. Объектом морфологического исследования может быть биопсийныи, операционный и секционный материал. Морфологическое исследование леченых опухолей не отличается от общих правил обработки онкологического материала.
Следует лишь подчеркнуть 3 момента. Во-первых, на всех этапах исследования должно руководствоваться клинико-анатомическнм принципом, который подразумевает тесный контакт патологоанатома и клинициста на практике и в познании. Приступая к исследованию материала, патологоанатом должен располагать необходимыми клиническими сведениями о больном, о цели и об особенностях проведенного лечения (метод лечения, доза облучения или химиопрепарата, вид и сроки оперативного лечения и т. п. ). Без данных о характере лечения производить оценку патоморфоза не рекомендуется ввиду возможных ошибок и дискредитации морфологического метода и самого исследования.
Во-вторых, максимального внимания заслуживают те случаи, в которых после лечения визуально опухоли не находят. При предоперационной лучевой и/или химиотерапии с видимым исчезновением опухоли операционный материал приходится исследовать иногда повторно с обработкой большого числа биоптатов. Снять диагноз «рака» почти всегда бывает труднее, чем его установить. В-третьих, при оценке патоморфоза обязателен сравнительный метод. Сравнение может быть либо на уровне конкретного больного (повторные пункции опухоли и биопсии в процессе лечения, сравнение биопсийного и операционного материала и т.д.), либо на уровне группы больных одной нозологической формой (сравнение типичных проявлений болезни).
— Вернуться в оглавление раздела «гистология»
Источник
Без признаков лечебного патоморфоза что означает
© А.О. Расулов, В.М. Кулушев, В.С. Ананьев, М.Ю. Федянин, Н.А. Козлов, 2015
А.О. Расулов, В.М. Кулушев, В.С. Ананьев, М.Ю. Федянин, Н.А. Козлов
ФБГНУ «Российский онкологический научный центр им. Н.Н. Блохина», г. Москва
Кулушев Вадим Маратович — заведующий операционным блоком
115478, г. Москва, Каширское шоссе, д. 23, тел. +7-903-758-70-42, e-mail: Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Реферат
Введение. Неоадъювантная химиотерапия — перспективный метод лечения больных колоректальным раком, однако данные об эффективности такого подхода и частоте ответа на лечение пока недоступны.
Методы. В ретроспективное исследование были включены больные раком ободочной кишки, находившиеся на лечении в отделении онкопроктологии ФГБНУ «РОНЦ им. Н.Н. Блохина» в 2007-2014 годах, которым на дооперационном этапе проводилось 2 или более курсов химиотерапии. Основным оцениваемым параметром был лечебный патоморфоз. Проводился анализ выраженности лечебного патоморфоза в зависимости от схемы и количества курсов химиотерапии, наличия регионарных метастазов.
Результаты. В исследование было включено 9 мужчин и 9 женщин. 9 пациентов с местно-распространенным раком T4N0-2M0 и 9 с отдаленными метастазами T3-4N0-2M1. Выраженность лечебного патоморфоза опухоли, соответствующая 1 и 2 степени по Dworak, была выявлена у 6 (33,3%) и 10 (55,5%) больных, соответственно. У 2 (11,1%) больных признаки лечебного патоморфоза в опухоли отсутствовали. Наиболее часто выраженный лечебный патоморфоз (2 степени) отмечался у больных, получавших химиотерапию c включением оксалиплатина — у 6 из 10 пациентов.
Выводы. Неоадъювантная химиотерапия позволяет достичь лечебного патоморфоза у большинства пациентов. Клиническое значение этого фактора необходимо изучить в проспективных исследованиях.
Ключевые слова: предоперационная химиотерапия, рак толстой кишки, патоморфоз опухоли.
Удаление рака ободочной кишки в пределах здоровых тканей является ключевым фактором, влияющим на прогноз пациента [5, 9, 15]. Но, даже при выполнении резекций в объеме R0, прогрессирование рака после радикального лечения остается актуальной и нерешенной проблемой, а механизмы, ответственные за эти процессы — остаются неясными.
Использование предоперационной химиотерапии имеет ряд теоретических предпосылок: эрадикация микрометастазов, уменьшение диссеминации опухолевых клеток при хирургическом лечении, а также возможность уменьшения первичной опухоли в размерах и снижения стадии заболевания. Более того пациенты лучше переносят химиотерапию, проводимую до операции, нежели после хирургического вмешательства, за счет чего может увеличиться общее количество пациентов, которые получат такое лечение в необходимом объеме [11]. Кроме этого можно изучить ответ опухоли на проводимое предоперационное лечение, на основании чего определить необходимость проведения или изменения схемы адъювантной химиотерапии.
В ряде исследований авторы предположили, что риск диссеминации заболевания значительно повышается периоперационно за счет активного синтеза различных факторов роста и цитокинов в ответ на хирургическую агрессию [10, 16].
Также возможно воздействие химиотерапии на микрометастазы в тканях, не удаляемые при стандартных объемах оперативных вмешательств [18] .
Проведение адъювантной химиотерапии позволяет улучшить показатели выживаемости пациентов с III стадией и II стадией болезни при наличии неблагоприятных факторов прогноза (операция на фоне кишечной непроходимости, инфильтрация опухолью лимфатических и кровеносных сосудов, низкая дифференцировка опухоли, показатель Т4, удаление при операции менее 12 лимфоузлов) [2, 4, 20].
Таким образом, проведение неоадъювантной химиотерапии имеет хорошее теоретическое обоснование. Главным вопросом остается то, сколько пациентов не ответят на такое лечение и каков риск отсрочки радикального хирургического лечения в этой группе.
Целью нашего исследования была оценка эффективности неоадъювантной химиотерапии по показателям лечебного патоморфоза.
Материалы и методы
Материалом для данного ретроспективного анализа послужил архив ФГБНУ «РОНЦ им. Н.Н. Блохина». В исследование включались все больные раком ободочной кишки, проходившие хирургическое лечение в отделении хирургическом № 3 в период с 2007 по 2014 гг. и получавшие на дооперационном этапе химиотерапевтическое лечение.
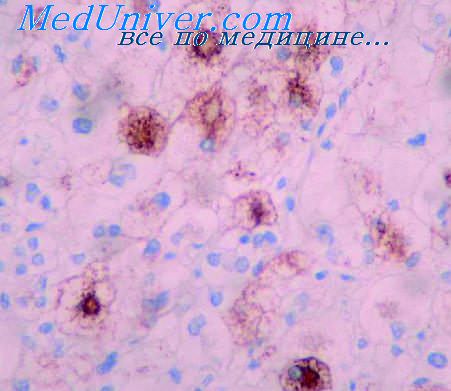
В исследование были включены только морфологически верифицированные случаи аденокарциномы ободочной кишки. Все гистологические препараты пересматривались одним морфологом, лечебный патоморфоз оценивался по шкале Dworak [8]: от «0 баллов — отсутствие признаков лечебного патоморфоза в опухоли» до «4 балла — резидуальная опухолевая ткань отсутствует». В связи с низкой репрезентативностью материала предоперационных биопсий, все опухоли с признаками высокой (G1) или умеренной (G2) степени дифференцировки были объединены в общую группу низкой степени злокачественности (low grade). В свою очередь, аденокарциномы с преобладанием перстневидноклеточного, или неспецифичного солидного компонентов были объединены в группу высокой степени злокачественности (high grade/G3).
Результаты
Проанализированы истории болезни 18 больных раком ободочной кишки, находившихся на лечении в отделении онкопроктологии ФГБНУ «РОНЦ им. Н.Н. Блохина» в 2007-2014 гг. Мужчин и женщин было поровну. 9 пациентов с местно-распространенным раком T4N0-2M0 и 9 с отдаленными метастазами T3-4N0-2M1 (по классификации TNM 7-й редакции). Большая часть пациентов получила химиотерапию фторпиримидинами и оксалиплатином. По одному случаю химиотерапия проводилась по схеме Мейо, капецитабином, фторафур + лейковорин, FOLFOX + бевацизумаб и FOLFIRI. Количество предоперационных курсов колебалось от 2 до 8.
Все 18 случаев были представлены аденокарциномами низкой степени злокачественности. У 13 из 19 пациентов опухоль локализовалась в сигмовидной кишке. Среди 18 первичных опухолей насчитывалось 16 (88,9%) аденокарцином высокой или умеренной дифференцировки и 2 (11,1%) муцинозные аденокарциномы. Макроскопически, в 17 (94,4%) случаях при исследовании операционного материала хорошо визуализировалась резидуальная опухолевая ткань. Выраженность лечебного патоморфоза опухоли, соответствующая 1 и 2 степени по Dworak, была выявлена у 6 (33,3%) и 10 (55,5%) больных, соответственно. У 2 (11%) больных признаки лечебного патоморфоза в опухоли отсутствовали. У 6 больных, имевших регионарные метастазы на момент проведения операции, выраженность лечебного патоморфоза соответствовала 0, 1 и 2 баллам в 2 (33,3%), 1 (16,7%) и 3 (50,0%) случаях, соответственно. Лечебного патоморфоза 3 и 4 степени отмечено не было (табл. 1).
Таблица 1. Распределение пациентов в зависимости от частоты лечебного патоморфоза в первичной опухоли и вида используемой программы предоперационной химиотерапии
XELOX либо FOLFOX
Лечебный патоморфоз ― 1 балл
1 (6%)
1 (6%)
1 (6%)
Лечебный патоморфоз ― 2 балла
1 (6%)
1 (6%)
1 (6%)
1 (6%)
1 (6%)
1 (6%)
Лечебный патоморфоз ― 3 балла
Лечебный патоморфоз ― 4 балла
Лечебный патоморфоз ― 0 баллов
Как следует из таблицы 1 большинство пациентов получили предоперационную химиотерапию, включающую оксалиплатин и один из препаратов фторпиримидинового ряда. У 5 (27,7%) параморфоз 2 степени был выявлен при проведении только двух курсов предоперационной химиотерапии.
Чаще всего применялась схема лечения с оксалиплатином и фторпиримидинами. При использовании схем с одними фторпиримидинами у 2 из 3 пациентов был выявлен лечебный патоморфоз в опухоли 2 степени. При анализе в нашем исследовании зависимости частоты курсов химиотерапии (до 3 и 3 и более) и достижением более выраженного патоморфоза опухоли, статистически значимой зависимости получено не было (р=0,55).
Обсуждение
Проведение неоадъювантной химиотерапии позволяет не только сразу оказать системное противоопухолевое воздействие, но и определиться с необходимостью коррекции послеоперационного лечения, с учетом данных о полученном лечебном патоморфозе [14].
Выбор препаратов для неоадъювантной химиотерапии должен основываться на опыте проведения адъювантного лечения, где эффективность показали только 2 группы препаратов — фторпиримидины и оксалиплатин. Иринотекан, а также моноклональные антитела в режимах адъювантной химиотерапии не показали эффективности [1, 7, 17, 19, 21-23].
Длительность предоперационной химиотерапии при раке ободочной кишки до конца не определена. Однако в исследованиях больных метастатическими опухолями толстой кишки наиболее часто эффект химиотерапии реализуется в первые 2-3 месяца, в дальнейшем же частота объективного ответа нарастает не значимо [6, 13]. Таким образом, для дальнейшего изучения достаточным может быть проведение не более 2-3 курсов предоперационной химиотерапии с последующим проведением после операции адъювантной химиотерапии с суммарной длительностью лечения не менее 6 месяцев.
Подобный подход с изучением неоадъювантного режима химиотерапии FOLFOX у больных раком ободочной кишки используется в исследовании FOxTROT в сравнении только с адъювантной терапией. В данном исследовании уже после 3 курсов химиотерапии по схеме FOLFOX-6 был выявлен выраженный или значительный морфологический регресс опухоли у 30% пациентов, а снижение стадии болезни достигнуто у 20% больных. Отдаленные результаты по выживаемости пациентов ожидаются [12]. Интересно отметить, что аналогичные результаты по достижению лекарственного патоморфоза достигаются и в метастазах рака толстой кишки в печень после проведенного предоперационного лечения [3]. Результаты исследования FOxTROT демонстрируют обнадеживающие данные, позволяющие рекомендовать дальнейшее исследование данного подхода.
Следует учитывать ряд возможных недостатков проведенного нами исследования. Поскольку исследование носит ретроспективный характер выявить показания к проведению неоадъювантной химиотерапии у данной группы пациентов не представилось возможным, равно как и оценить понятие «операбельности» опухоли, что затрудняет анализ такого факта как перевод опухоли в операбельное состояние. Полученные показатели лечебного патоморфоза в нашем исследовании значительно ниже, нежели в FOxTROT. Возможно, это было связано как с неадекватностью химиотерапевтического режима (24% больных — не получали оксалиплатин) и с тем, что ряд пациентов получил только 2 курса химиотерапии.
Тем не менее, на основании проведенного анализа, можно говорить о том, что неоадъювантная химиотерапия приводит к развитию лечебного патоморфоза у подавляющего большинства пациентов. Данный подход имеет хорошее теоретическое обоснование и должен стать объектом для дальнейшего изучения. Для выбора оптимальной схемы и продолжительности лечения необходимо проведение более крупных проспективных исследований. Окончательное суждение об эффективности неоадъювантной химиотерапии возможно только после завершения мультицентровых рандомизированных работ.
Литература
1. Alberts S.R. Adjuvant mFOLFOX6 with or without Cetuximab (Cmab) in KRAS wild-type (WT) patients (pts) with resected stage II colon cancer (CC): result from NCCTG Intergroup Phase III Trial N0147 / S.R. Alberts, D.J. Sargent, T.C. Smyrk et al. // J. Clin. Oncol. — 2010. — 28 (Suppl 18). — P. 959s.
2. Andre` T. Improved overall survival with oxaliplatin, fluorouracil and leucovorin as adjuvant treatment in stage II or III colon cancer in the MOSAIC trial / T. Andre`, C. Boni, M. Navarro et al. // J. Clin. Oncol. — 2009. — 27. — P. 3109-16.
3. Chan G. Pathological response grade of colorectal liver metastases treated with neoadjuvant chemotherapy / G. Chan, M. Hassanain, P. Chaudhury et al. // HPB. — 2010. — № 12. — P. 277-284.
4. Connell M.J. Oxaliplatin or irinotecan as adjuvant therapy for colon cancer: the results are in / M.J. Connell // J. Clin. Oncol. — 2009. — № 27. — P. 3082-4.
5. Costa S.R. En-bloc pancreatoduodenectomy and right hemicolectomy for treating locally advanced right colon cancer (T4): a series of five patients / S.R. Costa, A.C. Henriques, S.H. Horta et al. // Arq. Gastroenterol. — 2009. — Apr-Jun. — 46 (2). — P. 151-3.
6. de Gramont A. Leucovorin and fluorouracil with or without oxaliplatin as first-line treatment in advanced colorectal cancer / A. de Gramont, A. Figer, M. Seymour et al. // J. Clin. Oncol. — 2000. — № 18. — P. 2938-47.
7. de Gramont A. AVANT: Results from a randomized three-arm multinational phase III study to investigate bevacizumab with either XELOX or FOLFOX4 versus FOLFOX4 alone as adjuvant treatment for colon cancer / A. de Gramont, E. Van Cutsem, J. Tabernero et al. // J. Clin. Oncol. — 2011. — 29 (suppl 4; abstr 358).
8. Dworak O. Pathological features of rectal cancer after preoperative radiochemotherapy / O. Dworak, L. Keilholz, A. Hoffmann // Int. J. Colorectal. Dis. — 1997. — 12 (1). — P. 19-23.
9. Faculdade de Medicina do ABC, São Bernardo do Campo. En bloc pancreaticoduodenectomy and right hemicolectomy for locally advanced right colon cancer treatment // Rev. Col. Bras. Cir. — 2010. — Jun. — 37 (3). — P. 247-9.
10. Fahmy R.G. Transcription factor Egr-1 supports FGF-dependent angiogenesis during neovascularization and tumor growth / R.G. Fahmy, C.R. Dass, L.Q. Sun et al. // Nat. Med. — 2003. — Т. 9, № 8. — C. 1026-32.
11. Fernandez-Martos C. Phase II, randomized study of concomitant chemoradiotherapy followed by surgery and adjuvant capecitabine plus oxaliplatin (CAPOX) compared with induction CAPOX followed by concomitant chemoradiotherapy and surgery in magnetic resonance imaging-defined, locally advanced rectal cancer: Grupo cancer de recto 3 study / C. Fernandez-Martos, C. Pericay, J. Aparicio et al. // J. Clin. Oncol. — 2010. — № 28. — P. 859-865
12. Foxtrot Collaborative Group. Feasibility of preoperative chemotherapy for locally advanced, operable colon cancer: the pilot phase of a randomised controlled trial // Lancet Oncol. — 2012. — 13. — P. 1152-60.
13. Giacchetti S. Phase III multicenter randomized trial of oxaliplatin added to chronomodulated fluorouracil-leucovorin as first-line treatment of metastatic colorectal cancer / S. Giacchetti, B. Perpoint, R. Zidani et al. // J. Clin. Oncol. — 2000. — № 18. — P. 136-47.
14. Hong Y.S. Adjuvant chemotherapy with oxaliplatin/5-fluorouracil/leucovorin (FOLFOX) versus 5-fluorouracil/leucovorin (FL) for rectal cancer patients whose postoperative yp stage 2 or 3 after preoperative chemoradiotherapy: Updated results of 3-year disease-free survival from a randomized phase II study (The ADORE) / Y.S. Hong, B.H. Nam, K.P. Kim et al. // J. Clin. Oncol. — 2014. — 32. — 5s. — (suppl; abstr 3502).
15. Landmann R.G. Surgical management of locally advanced and locally recurrent colon cancer / R.G. Landmann, M.R. Weiser // Clin. Colon. Rectal. Surg. — 2005. — № 18 (3). — Р. 182-9.
16. Miki C. Perioperative host-tumor inflammatory interactions: a potential trigger for disease recurrence following a curative resection for colorectal cancer / C. Miki, K. Tanaka, Y. Inoue et al. // Surg. Today. — 2008. — Т. 38, № 7. — P. 579-84.
17. Nordlinger B. Perioperative et al. FOLFOX4 chemotherapy and surgery versus surgery alone for resectable liver metastases from colorectal cancer (EORTC 40983): long-term results of a randomised, controlled, phase 3 trial / B. Nordlinger, H. Sorbye, B. Glimelius et al. // Lancet. — 2013. — 14. — P. 1208-15.
18. Pantel K. Detection and clinical importance of micrometastatic disease / K. Pantel, R.J. Cote, O. Fodstad // J. Natl. Cancer Inst. — 1999. — Т. 91, № 13. — P. 1113-24.
19. Saltz L. Irinotecan plus fluorouracil/leucovorin (IFL) versus fluorouracil/leucovorin alone (FL) in stage III colon cancer (Intergroup Trial CALGB C89903) / L. Saltz, D. Niedzwiecki, D. Hollis et al. // Journal of Clinical Oncology. — 2004. — 22. — P. 245s.
20. Van Cutsem E. Progress in the adjuvant treatment of colon cancer. Has it influenced clinical practice? / E. Van Cutsem, F. Costa // JAMA. — 2005. — 7. — P. 2758-60.
21. Van Cutsem E. Randomized phase III trial comparing biweekly infusional fluorouracil/leucovorin alone or with irinotecan in the adjuvant treatment of stage III colon cancer: PETACC-3 / E. Van Cutsem, R. Labianca, G. Bodoky et al. // J. Clin. Oncol. — 2009. — 27. — P. 3117-25.
22. Ychou M. Randomized phase III trial comparing infused 5-fluorouracil/folinic acid (LV5FU) versus LV5FU+irinotecan (LV5FU+IRI) as adjuvant treatment after complete resection of liver metastases from colorectal cancer (LMCRC). (CPT-GMA-301) / M. Ychou, W. Hohenberger, S. Thezenas et al. // J. Clin. Oncol. — 2008. — 26 (Suppl). — LBA4013
Источник