Аденома простаты: 5 полезных советов мужчинам
Аденома простаты — это опухоль. Но не стоит бояться: опухоль доброкачественная — просто разрастаются ткани этого органа. Ее появление и развитие связано с изменениями гормонального фона мужского организма, которые наблюдаются практически у всех представителей сильного пола после 40-45 лет. Это состояние называют андропаузой, или мужским климаксом. В это время начинает снижаться выработка полового гормона — тестостерона. Так что в какой-то мере это заболевание даже закономерное.
Когда идти к врачу?
Первые признаки аденомы связаны с затруднением мочеиспускания. Анатомически простата как бы охватывает мочеиспускательный канал и, когда она увеличивается, то, во-первых, пережимает его, а во-вторых, давит на мочевой пузырь. Из-за этого струя мочи теряет напор, прерывается, а мочиться приходиться чаще (в норме человек мочится 5-8 раз в день, при аденоме — 9 и чаще). Нередко, сходив один раз, через пару минут человек чувствует новый позыв. Что характерно, появляются позывы ходить по-маленькому по ночам. При этом, чувство полного опорожнения мочевого пузыря при аденоме бывает редко — обычно кажется, что еще что-то осталось.
К сожалению, даже заподозрив, что у них аденома, большинство мужчин рассуждают, что «все это возраст», и поэтому за медицинской помощью не обращаются. И потом расплачиваются более тяжелыми последствиями.
Если отток мочи постоянно затруднен, в мочевыводящих путях создаются благоприятные условия для развития инфекции, и начинают появляться осложнения — цистит, пиелонефрит, камни в мочевом пузыре. Со временем развивается хроническая почечная недостаточность, что проявляется постоянной головной болью, жаждой, сухостью во рту, слабостью, раздражительностью. Наиболее же грозным острым осложнением аденомы является острая задержка мочи (когда моча вообще перестает выделяться) и развитие почечной недостаточности — это состояние угрожает жизни и требует вызова «неотложки». В любом случае, чем раньше мужчина обратится за помощью, тем больше шансов у него победить болезнь.
Но бывают и «молчаливые» аденомы. На ранних стадиях опухоль уже может быть, а симптомов — еще нет. Поэтому, чтобы не пропустить начало заболевания, мужчинам за 40 нужно раз в год для профилактики проходить обследование у уролога, и не дать развиться раку предстательной железы.
Специалист, к которому нужно обратиться — это врач уролог. Чтобы установить степень аденомы, он проведет мужчине несколько исследований. Часто пациенты спрашивают, можно ли для постановки диагноза обойтись без пальцевого исследования простаты через прямую кишку, которого многие стесняются. Но это и есть самое важное исследование при аденоме, заменить его ничем нельзя. Еще обязательно нужно сделать УЗИ органов малого таза. Имея на руках результаты этих анализов, специалист может определиться с лечением, подходящим конкретному пациенту.
Группа риска
У некоторых мужчин аденома предстательной железы развивается раньше. К группе риска по возникновению этого заболевания, в первую очередь, можно отнести тех мужчин, чья работа предполагает сидячий образ жизни. В первую очередь, это занимающиеся исключительно умственным трудом. В прессе также нередко звучит информация, что к развитию аденомы предрасполагают злоупотребление алкоголем и табаком, перенесенные воспалительные и венерические заболевания, и даже нетрадиционная половая ориентация. Но достоверной связи между этими факторами и опухолью простаты не выявлено.
Как избавиться от проблемы
Все способы лечения аденомы простаты можно разделить на две группы: консервативные и хирургические. Первые применяются на начальных стадиях болезни. Это прием одного или нескольких препаратов, обычно в виде таблеток. Чаще всего это лекарства из группы альфа-адреноблокаторов, они расслабляют мышечные стенки различных органов, в т. ч. и мочеиспускательного канала. Конечно, опухоль они никуда не уберут, но мочеиспускание нормализуют. Также уролог может назначить дополнительное лечение — гормональные средства (ингибиторы 5-альфа редуктазы), фитопрепараты (например, на основе крапивы, тыквы, каштана, плодов американской карликовой пальмы и др.), гомеопатию, которые могут приостановить рост опухоли, а также противовоспалительные препараты — если аденома уже успела осложниться циститом или другим воспалением мочевыводящих путей.
Но если аденома уже «в расцвете», то такое лечение малоэффективно — помочь избавиться от неприятных симптомов можно только с помощью хирургии. Традиционная операция для больных с аденомой — это частичное или полное удаление — аденэктомия предстательной железы. У этой операции есть свои недостатки — нужно делать разрез передней брюшной стенки, идет кровопотеря, остается рубец. На западе от таких операций уже отказались, там практикуют намного более щадящую методику с минимальным вмешательством (т. н. малоинвазивную операцию) — трансуретральную резекцию. У нас ее также делают, но она не так распространена. Ее осуществляют без разреза передней брюшной стенки, доступ идет через мочевыводящий канал (уретру). В него вводят резктоскоп — мини-зонд с видеокамерой и режущими инструментами. Хирург-уролог видит изображение на экране и, ориентируясь по нему, удаляет кусочки ткани предстательной железы и прижигает кровоточащие сосуды. Единственный общий минус обеих операций — обе они требуют госпитализации и имеют относительно продолжительный послеоперационный период.
5 полезных советов мужчинам
Делайте зарядку. Длительное сидение приводит к застою крови в органах малого таза, что способствует развитию аденомы. Поэтому возьмите себе за правило вставать каждый час — если не для разминки, то хотя бы, чтобы просто пройтись.
Ведите регулярную половую жизнь. Одно из лучших средств борьбы с застоем крови — регулярная близость. Интим может, как замедлять появление аденомы, так и сдерживать ее прогресс. Поэтому, женщины, не отказывайте своим мужчинам в этом приятном и полезном способе лечения.
Замените лекарства. Есть ряд лекарств, которые могут ухудшить симптомы аденомы: некоторые антигистаминные, мочегонные и противоотечные (включая спреи для носа). Спросите у своего лечащего врача, не принимаете ли вы таких препаратов и, если да, то замените их на более подходящие.
Не пейте на ночь. Если у вас все-таки появилась аденома, не пейте воду и другие напитки в течение нескольких часов перед сном, чтобы ночью реже вставать в туалет.
Раз в год делайте онкопроверку. У кого увеличена предстательная железа, надо раз в год сдавать анализ крови на ПСА (простатический специфический антиген) — специальный маркер злокачественного процесса.
Записаться на прием к урологу вы можете в любое удобное для вас время, просто позвонив по телефонам слева в блоке контакты.
Источник
Атония мочевого пузыря
Причины
Причинами атонии мочевого пузыря являются такие факторы:
- недостаточное влияние нервной системы на сократительные мышечные волокна образования;
- травма крестцового отдела спинного мозга;
- аденома предстательной железы;
- дегенеративные заболевания позвоночника;
- повреждения задних корешков спинного мозга.
Атония мочевого пузыря у женщин встречается чаще, чем у мужчин. Иногда главная причина заболевания – частые циститы.
Симптомы атонии мочевого пузыря
Симптомами атонии мочевого пузыря являются следующие проявления:
- неконтролируемое мочеиспускание у пациента;
- задержка начала мочеиспускания;
- слабая струя при мочеиспускании;
- мочеиспускание без позывов.
Если Вы обнаружили у себя схожие симптомы, незамедлительно обратитесь к врачу. Легче предупредить болезнь, чем бороться с последствиями.
Диагностика
Для диагностики атонии мочевого пузыря следует выполнить следующие шаги:
- пройти обследование у врача — уролога;
- посетить специалиста узкого профиля (невропатолога, гинеколога, сексопатолога, хирурга и т.д.);
- выполнить УЗИ органов мочеполовой системы;
- сделать компьютерную томографию (КТ);
- сдать общие анализы мочи.
Полноценную диагностику и лечение можно пройти в любом современном медицинском центре урологии.
Лечение атонии мочевого пузыря
При лечении атонии мочевого пузыря актуальны следующие манипуляции:
- прием лекарственных препаратов для терапии нейрогенных функций (миотропные спазмолитические релаксанты,
- антихолинергические препараты, бета-адреноблокаторы);
- прием простогладинов Е;
- использование поддерживающих средств народной медицины;
- применение специальных катетеров.
Опасность
При борьбе с астонией мочевого пузыря главное – определить причину заболевания. В случае если проблема, приведшая к астонии, излечима – прогноз благоприятен. При других проблемах, когда основная причина – неизлечима, можно воспользоваться современными средствами гигиены, чтобы частично ликвидировать последствия астонии мочевого пузыря.
Профилактика
Для профилактики астонии мочевого пузыря следует принимать превентивные меры по отношению к заболеваниям, которые могут привести к первой проблеме. Для женщин, например, – это соблюдение правил личной гигиены, избегание переохлаждений и инфекционных заболеваний.
Источник
Лечение функциональных нарушений опорожнения мочевого пузыря
Лечение больных с функциональными нарушениями опорожнения мочевого пузыря является насущной проблемой нейроурологии. Это связано с тем, что до настоящего времени не разработано эффективных и этиопатогенетически обоснованных методов лечения таких больных
Лечение больных с функциональными нарушениями опорожнения мочевого пузыря является насущной проблемой нейроурологии. Это связано с тем, что до настоящего времени не разработано эффективных и этиопатогенетически обоснованных методов лечения таких больных.
Выделяют нейрогенные, миогенные (миопатии) и психогенные (неврозы, шизофрения, истерия и др.) факторы, лежащие в основе функциональных нарушений опорожнения мочевого пузыря. Нейрогенные нарушения и повреждения — основная причина таких нарушений. В отсутствие причины функциональных нарушений опорожнения мочевого пузыря следует думать об идиопатических формах заболевания.
Согласно классификации Международного общества по удержанию мочи, функциональные нарушения опорожнения мочевого пузыря — это результат недостаточной функции мочевого пузыря, гиперактивности уретры или следствие комплексного воздействия обоих нарушений [1]. Недостаточная функция мочевого пузыря возникает вследствие снижения или отсутствия сократительной способности детрузора (арефлексия), которые встречаются при локализации повреждения или неврологического поражения в области фронтальных долей и моста головного мозга, сакрального отдела спинного мозга, при повреждении волокон конского хвоста, тазового сплетения и нервов мочевого пузыря, а также при рассеянном склерозе. Гиперактивность уретры — это следствие наружной детрузорно-сфинктерной диссинергии (ДСД) или нерасслабляющегося (спастического) поперечно-полосатого (п/п) сфинктера уретры, также может проявиться как вариант синдрома Фоулера у женщин. При этом наружная ДСД наблюдается при супрасакральном уровне поражения спинного мозга.
В литературе имеются лишь единичные сообщения о распространенности функциональных нарушений опорожнения мочевого пузыря. Так, P. Klarskov и соавт., оценивая обращаемость в лечебные учреждения Копенгагена, выявили, что ненейрогенные формы нарушения опорожнения мочевого пузыря встречаются в среднем у 7 женщин на 100 000 населения [2]. По данным T. Tammela и соавт., после оперативных вмешательств на органах брюшной полости нарушения опорожнения мочевого пузыря встречаются у 2,9 % пациентов, а после проктологических операций — у 25% больных [3]. Многие авторы считают данную проблему особенно значимой у неврологических больных.
Клиническим проявлением снижения сократительной способности детрузора и нерасслабляющегося п/п сфинктера уретры являются симптомы нарушения опорожнения мочевого пузыря, к которым относятся затрудненное мочеиспускание тонкой, вялой струей, прерывистое мочеиспускание, необходимость прилагать усилия и натуживаться, чтобы начать мочеиспускание, ощущение неполного опорожнения мочевого пузыря.
При отсутствии сократительной способности детрузора в сочетании с паралитическим состоянием п/п сфинктера уретры больные опорожняют мочевой пузырь, искусственно увеличивая внутрибрюшное давление, что клинически проявляется мочеиспусканием слабой струей мочи. При отсутствии сократительной способности детрузора в сочетании со спастическим состоянием наружного сфинктера уретры в большинстве случаев самостоятельное мочеиспускание невозможно и отмечается хроническая задержка мочи.
Нерасслабляющийся п/п сфинктер уретры приводит к инфравезикальной обструкции с симптомами нарушения опорожнения мочевого пузыря.
Клинические проявления наружной ДСД (непроизвольное сокращение п/п сфинктера уретры во время мочеиспускания или непроизвольного сокращения детрузора) включают два вида симптомов, а именно: нарушения опорожнения и накопления мочи в мочевом пузыре. Последние включают учащенное и ургентное мочеиспускание нередко в сочетании с ургентным недержанием мочи и никтурией. Для наружной ДСД характерно неполное опорожнение мочевого пузыря и развитие пузырно-мочеточникового рефлюкса.
Таким образом, различные формы нарушения опорожнения мочевого пузыря могут иметь во многом сходную клиническую картину. В связи с этим правильная и своевременная диагностика функциональных нарушений опорожнения мочевого пузыря является залогом успешного лечения.
Диагностика функциональных нарушений опорожнения мочевого пузыря складывается из сбора жалоб и анамнеза, урологического и неврологического обследования, а также дополнительных методов обследования, среди которых основное место занимает уродинамическое исследование. На начальном этапе обследования обязательна оценка симптомов нижних мочевых путей на основании вопросника I-PSS (Internanional Prostate Symptom Score). Вопросник I-PSS был предложен для оценки нарушений акта мочеиспускания вследствие заболеваний предстательной железы, однако в настоящее время он с успехом применяется и в случаях проявления симптомов заболеваний нижних мочевых путей, вызванных различными факторами, в том числе и неврологического характера.
Для уточнения поведения детрузора и его сфинктеров в фазу опорожнения мочевого пузыря наиболее информативным методом исследования больных является комплексное уродинамическое исследование.
Уродинамическими признаками наружной ДСД, характерной для надкрестцовой локализации патологического процесса, особенно в шейном отделе спинного мозга, являются регистрируемые с помощью электромиографии во время мочеиспускания «всплески» сократительной активности п/п сфинктера уретры и мышц тазового дна. Сокращение мышц тазового дна затрудняет или полностью прерывает поток мочи. Для нерасслабляющегося сфинктера уретры характерно отсутствие снижения электромиографической активности п/п сфинктера уретры во время мочеиспускания. Снижение или отсутствие сократительной способности детрузора уродинамически проявляется отсутствием плавного повышения детрузорного давления в ходе цистометрии или отсутствием позыва к акту мочеиспускания.
Следует подчеркнуть, что только уродинамическое обследование дает возможность достоверно установить форму нарушения функции нижних мочевых путей, приводящих к нарушению опорожнения мочевого пузыря, и во многом определить выбор метода лечения.
Ультразвуковое исследование почек и мочевого пузыря, также как и экскреторная урография, позволяет уточнить анатомическое состояние верхних мочевых путей и количество остаточной мочи в мочевом пузыре. По количеству остаточной мочи в мочевом пузыре после акта мочеиспускания (в норме до 50 мл) можно косвенно судить о функциональном состоянии детрузора и наличии инфравезикальной обструкции.
В таблице перечислены методы лечения больных с функциональными нарушениями опорожнения мочевого пузыря, из которых только медикаментозная терапия и дорзальная ризотомия с электростимуляцией передних корешков могут действительно считаться методами лечения, тогда как другие скорее являются способами опорожнения мочевого пузыря. При этом даже медикаментозная терапия во многом является симптоматическим методом лечения. Несмотря на это, назначение лекарственных средств представляет собой первый этап лечения больных с функциональными нарушениями опорожнения мочевого пузыря. Выбор медикаментов зависит от вида нарушения функции нижних мочевых путей. Так, в случае нарушения сократительной способности детрузора применяют антихолинэстеразные средства и М-холиномиметики, а при гиперактивности уретры — центральные миорелаксанты и α-блокаторы.
У 22 больных со сниженной сократительной способностью детрузора использовали дистигмина бромид (убретид) в дозе 5 мг через день за 30 мин до завтрака в течение 2 мес. При этом через каждые 2 нед делали 7-дневный перерыв в приеме препарата. Механизм действия дистигмина бромида заключается в блокировании ацетилхолинэстеразы, что сопровождается увеличением концентрации ацетилхолина в синаптической щели и соответственно приводит к облегчению передачи нервного импульса.
У всех больных терапевтический эффект развивался в первую неделю приема препарата и выражался в снижении среднего балла I-PSS c 15,9 до 11,3, а количества остаточной мочи — с 82,6 до 54,3 мл. Субъективно пациенты отмечали усиление ощущения позыва и облегчение начала акта мочеиспускания.
Следует отметить, что до настоящего времени остается открытым вопрос о продолжительности лечения антихолинэстеразными средствами. По нашим данным, у 82% больных в разные сроки после окончания 2-месячного курса лечения отмечалось возобновление симптомов, потребовавшее повторного назначения препарата.
К сожалению, мы не накопили собственного опыта применения бетанехола у больных со сниженной сократительной способностью детрузора, так как данный препарат не зарегистрирован для клинического применения в нашей стране и соответственно отсутствует в аптечной сети. Механизм действия бетанехола аналогичен действию ацетилхолина на гладкие миоциты. Данные других авторов показывают, что бетанехол может применяться при лечении больных с легкой степенью нарушения сократительной способности детрузора [4, 5].
α1-адреноблокатор доксазозин (кардура) использовали в ходе лечения 30 больных с гиперактивностью уретры, в том числе 14 пациентов с наружной ДСД и 16 с нарушением произвольного расслабления п/п сфинктера уретры. Доксазозин назначали в дозе 2 мг/сут на ночь.
Через 6 мес средний балл по шкале I-PSS у больных с наружной ДСД снизился с 22,6 до 11,4, количество остаточной мочи уменьшилось с 92,6 до 32,4 мл, а максимальная скорость потока мочи увеличилась с 12,4 до 16,0 мл/сек.
Кроме того, через 6 мес у больных с нарушением произвольного расслабления п/п сфинктера уретры средний балл I-PSS снизился с 14,6 до 11,2, количество остаточной мочи — с 73,5 до 46,2 мл, а максимальная скорость потока мочи увеличилась с 15,7 до 18,4 мл/сек.
Баклофен и тизанидин (сирдалуд) являются центральными миорелаксантами. Они снижают возбуждение моторных нейронов и интернейронов и могут ингибировать передачу нервного импульса в спинном мозге, уменьшая спастичность п/п мышц. По нашим данным, после применения баклофена в дозе 20 мг/сут и тизанидина в дозе 4 мг/сут не было выявлено существенной динамики субъективных и объективных симптомов как у больных с наружной ДСД, так и у пациентов с нарушением расслабления п/п сфинктера уретры. Выраженная слабость мускулатуры конечностей на фоне приема этих препаратов не позволяет увеличивать дозу препаратов, что существенно ограничивает их применение в клинической практике.
Следует отметить, что медикаментозная терапия эффективна у больных с начальными и легкими формами нарушения опорожнения мочевого пузыря. Тем не менее ее целесообразно использовать в качестве первого этапа лечения. В случае недостаточной эффективности медикаментозной терапии необходимо искать новые пути решения проблемы адекватного опорожнения мочевого пузыря.
Предложенная Lapides и соавт. в 80-е гг. прошлого столетия интермиттирующая аутокатетеризация мочевого пузыря до настоящего времени остается одним из основных методов опорожнения мочевого пузыря [6]. Однако этот метод имеет ряд осложнений, к которым относятся инфекции нижних мочевых путей, стриктуры уретры и, самое главное, значительное снижение качества жизни. При невозможности выполнения (неврологические больные с тетраплегией, больные с ожирением) или отказе пациента от аутокатетеризации, у лиц с наружной ДСД и нерасслабляющимся сфинктером уретры, а также со сниженной сократительной способностью детрузора для адекватного опорожнения мочевого пузыря применяют в последние годы имплантацию специальных стентов (производства фирм Balton, Mentor, МедCил) и инъекции ботулинического токсина в зону п/п сфинктера уретры.
 |
| Рисунок 1. Временный уретральный стент |
Временные уретральные стенты имеют форму цилиндра, выполненного из проволочной спирали толщиной 1,1 мм, изготовлены они на основе полимолочной и полигликоликовой кислот с различным периодом разрушения (от 3 до 9 мес) посредством гидролиза (рис. 1). Механические свойства и время разрушения временных стентов зависят от степени поляризации, места и формы зоны имплантации.
Мы имеем опыт применения временных уретральных стентов у семи мужчин с наружной ДСД и у четырех пациентов, у которых отсутствовала сократительная способность детрузора. Временный уретральный стент устанавливали при уретроцистоскопии таким образом, чтобы он «шинировал» как простатический, так и мембранозный отделы уретры. Такое положение стента обеспечивает адекватное опорожнение мочевого пузыря.
У всех больных отмечалось восстановление самостоятельного мочеиспускания сразу после имплантации уретрального стента. Пациенты с наружной ДСД осуществляли мочеиспускание по позыву, а больные с отсутствием сократительной способности детрузора с интервалом 4 ч (6 раз в сутки) с использованием приема Креда. По данным ультразвукового сканирования, через 10 нед после установки стента у больных с наружной ДСД не отмечалось остаточной мочи, а у больных с отсутствием сократительной способности детрузора среднее количество остаточной мочи составило 48 мл и зависело от адекватности выполнения приема Креда. Очень важно, что у больных с наружной ДСД было выявлено снижение максимального детрузорного давления во время мочеиспускания в среднем с 72 до 35 см вод. ст. (профилактика развития пузырно-мочеточникового рефлюкса).
Мы считаем, что временные уретральные стенты обеспечивают адекватное опорожнение мочевого пузыря и показаны тем больным с нарушением опорожнения мочевого пузыря, которым не может быть выполнена интермиттирующая катетеризация мочевого пузыря или которые воздерживаются от нее по различным причинам. Временные стенты могут являться методом отбора больных для установки постоянных (металлических) стентов.
В последние годы в литературе появились сообщения об успешном использовании ботулинического токсина у больных с функциональными нарушениями опорожнения мочевого пузыря. В нашей клинике ботулинический токсин применялся у 16 больных с нарушением опорожнения мочевого пузыря, в том числе у девяти с наружной ДСД, у трех с нерасслабляющимся п/п сфинктером уретры и у четырех с нарушением сократительной способности детрузора. Мы использовали ботулинический токсин типа А фармацевтической фирмы Allergan. Коммерческое название препарата — ботокс (Botox), он представляет собой лиофилизированный порошок белого цвета в вакуумных стеклянных флаконах объемом 10 мл, закрытых резиновой пробкой и герметичным алюминиевым затвором. В одном флаконе содержится 100 ЕД ботулинического токсина типа А.
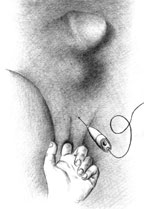 |
| Рисунок 2. Введение ботулинического токсина у мужчин |
Механизм действия ботокса заключается в блокировании выброса ацетилхолина из пресинаптической мембраны в нервно-мышечном синапсе. Фармакологическим эффектом этого процесса является стойкая хемоденервация, а клиническим проявлением — расслабление мышечных структур.
Согласно рекомендациям фирмы-производителя, лиофилизированный порошок разводили 8 мл стерильного 0,9% раствора натрия хлорида без консервантов (1 мл полученного раствора содержит 12,5 ЕД ботокса). Использовали трансперинеальную методику введения препарата. У мужчин под контролем указательного пальца, введенного в прямую кишку, специальную иглу с изоляционным покрытием вводили в точку, находящуюся на 2 см латеральнее и выше анального отверстия (рис. 2). У женщин иглу под контролем указательного пальца, введенного во влагалище, вводили в точку на 1 см латеральнее и выше наружного отверстия уретры на глубину 1,5–2,0 см (рис. 3). Во всех случаях положение иглы контролировали электромиографически по характерному звуку динамика электромиографа. В каждую точку вводили по 50 ЕД ботокса.
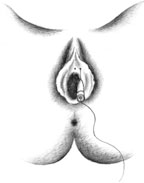 |
| Рисунок 3. Введение ботулинического токсина у женщин |
У всех больных через 10 дней после введения ботулинического токсина исчезла остаточная моча и было отмечено увеличение максимальной скорости потока мочи. Важно, что хемоденервация сфинктера уретры после инъекции ботокса у всех пациентов с нерасслабляющимся п/п сфинктером и наружной ДСД приводила к снижению детрузорного давления, а у больных с нарушением сократительной способности детрузора — к снижению максимального абдоминального давления, вызывающего выделение мочи из наружного отверстия уретры. Это наблюдение представляется крайне важным в отношении профилактики развития пузырно-мочеточникового рефлюкса и сохранения функциональной способности почек. Только у одного больного клинический эффект после инъекции ботокса продолжал сохраняться на протяжении 16 мес, остальным пациентам потребовались повторные инъекции препарата с периодичностью 3–8 мес.
В отдельных случаях, при выраженной инвалидизации больных с нарушением опорожнения мочевого пузыря, используют трансуретральную инцизию или резекцию наружного сфинктера уретры, дренируют мочевой пузырь постоянным уретральным катетером или выполняют цистостомию.
Таким образом, нарушение опорожнения мочевого пузыря может быть следствием различных форм дисфункции нижних мочевых путей. Требуются проведение комплексного уродинамического обследования для уточнения функционального состояния мочевого пузыря и его сфинктеров и выбор адекватного метода опорожнения мочевого пузыря. Отсутствие высокоэффективных и универсальных способов лечения больных с функциональными нарушениями опорожнения мочевого пузыря диктует необходимость поиска новых методов терапии таких больных.
Г. Г. Кривобородов, доктор медицинских наук
М. Е. Школьников, кандидат медицинских наук
РГМУ, Москва
Источник