5. Лекарственные вещества, содержащие первичную ароматическую аминогруппу
Первичная ароматическая аминогруппа (ПАА) – это группа – NH2, связанная с ароматическим радикалом.
Её содержат производные п-аминобензойной кислоты (анестезин, новокаин, новокаинамид), этакридина лактат, сульфаниламиды (стрептоцид, сульфацил-натрий, норсульфазол и др.), производные п-аминосалициловой кислоты (натрия п-аминосалицилат).
Ряд лекарственных веществ образуют соединения с ПАА при гидролитическом разложении, это бепаск, производные п-аминофенола (фенацетин, парацетамол), бензодиазепина (нозепам, феназепам, нитразепам).
Электронная пара азота первичной аминогруппы находится в сопряжении с π-электронами ароматической системы, что приводит к перераспределению электронной плотности и активизации ароматического кольца в о- и п- положениях. Смещение электронной плотности с атома азота приводит к снижению его основности: как правило, ЛВ из группы первичных ароматических аминов являются слабыми основаниями.
На основе свойств ПАА и связанного с ней ароматического радикала в анализе используют следующие реакции:
— реакция диазотирования с последующим азосочетанием;
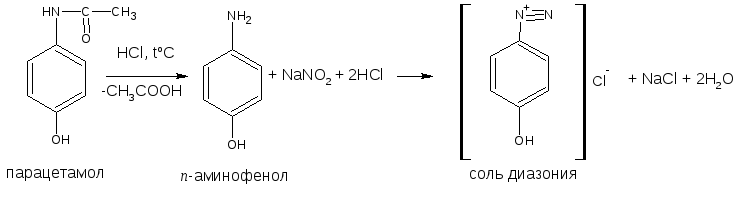
5.1. Реакция диазотирования с последующим азосочетанием
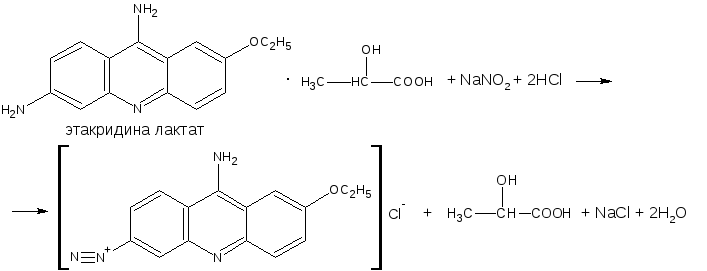
В основе реакции лежит взаимодействие соединений, содержащих незамещённую ПАА, с нитритом натрия в кислой среде. В результате образуются бесцветные или слабо-жёлтого цвета соли диазония.
Исключение составляет этакридина лактат, в результате диазотирования которого по аминогруппе в образуется диазосоединение, имеющее вишнёво-красную окраску.
Ацильные производные ароматических аминов дают реакцию диазотирования после предварительного гидролитического разложения (парацетамол, фенацетин, тримекаин, фталазол, нозепам и др.).
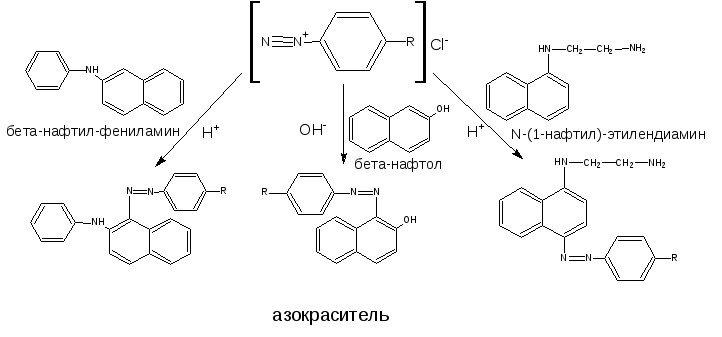
Полученные диазосоединения сочетают с фенолами или ароматическими аминами: β-нафтолом (нозепам, тримекаин, новокаин, сульфаниламидные препараты), резорцином (феназепам), N-(1-нафтил)-этилендиамином (нитразепам).
Азосочетание с фенолами и нафтолами наиболее благоприятно проходит в слабощелочной среде, а с аминами в слабокислой. При этом образуются азокрасители вишнёво- или красно-оранжевого цвета.
Реакция диазотирования с последующим азосочетанием включена в раздел «Общие реакции на подлинность» ГФ ХI и широко используется во внутриаптечном контроле.
5.2. Реакции окисления
Лекарственные вещества, содержащие ПАА, легко окисляются даже кислородом воздуха с образованием окрашенных продуктов.
Появление окраски может быть обусловлено не только продуктами окисления, но и веществами, образующимися в результате последующей их конденсации с избытком ароматического амина.
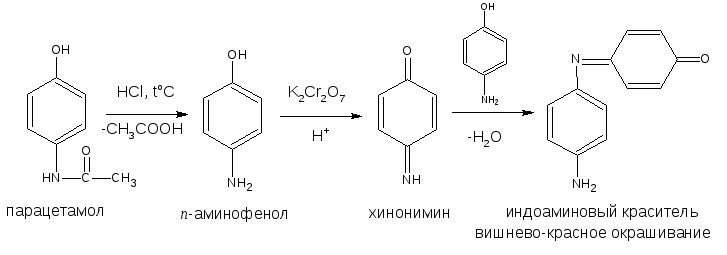
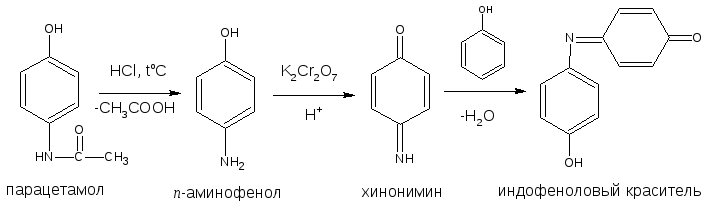
Эта реакция является официнальной для фенацетина и парацетамола.
В случае парацетамола появляется фиолетовое окрашивание, фенацетина – фиолетовое, переходящее в вишнёво-красное.
Индофеноловые красители образуются также при окислении сульфаниламидов хлорамином в щелочной среде (в случае стрептоцида образуется синий, переходящий в сине-зелёный; норсульфазола – жёлтый). В этом случае, вероятно, образуются индофеноловые красители о-хиноидной структуры в отличие от п-хиноидной, приведённой выше.
Реакции окисления рекомендуются ГФ при идентификации анестезина (извлекающийся в эфирный слой продукт окисления хлорамином жёлтого цвета), новокаина (обесцвечивание калия перманганата), уросульфана (рубиново-крсное окрашивание при действии натрия нитрита при нагревании), норсульфазола (жёлто-розовое окрашивание при окислении перекисью водорода и хлоридом железа).
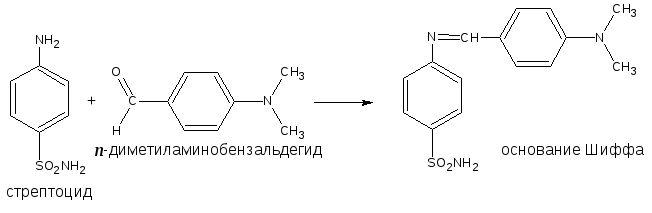
5.3. Реакция конденсации с альдегидами
При взаимодействии в кислой среде с ароматическими альдегидами (п-диметиламинобензальдегид, ванилин и др.) первичные ароматические амины образуют окрашенные в жёлтый или оранжевый цвет основания Шиффа:
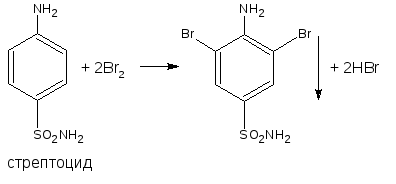
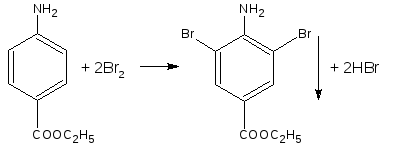
5.4. Реакция галоидирования
В частности, бромирование, основана на электрофильном замещении атомов водорода бензольного кольца на галоген. Образуются аморфные осадки белого или желтоватого цвета.
5.5. Нитритометрический метод
Основан на свойстве лекарственных веществ, содержащих ПАА, диазотироваться нитритом натрия в кислой среде. Ацильные производные ароматических аминов предварительно гидролизуют. Титрование проводят в присутствии калия бромида (катализатора) при пониженной температуре и медленном добавлении титранта.
Индикация конечной точки титрования проводится:
— с помощью внутренних индикаторов, например, тропеолин 00 или его смесь с метиленовым голубым, нейтральный красный. Избыток титранта окисляет индикатор и его окраска изменяется.
— с использованием внешнего индикатора – йодкрахмальной бумаги (пропитанной водными растворами крахмала и калия йодида фильтровальной бумаги), на неё в конец титрования наносят каплю раствора из колбы, в которой находится анализируемый раствор, по окончании диазотирования на бумаге проявляется синее пятно от выделившегося йода. Это свидетельствует о появлении в титруемом растворе некоторого избытка титранта и наступлении точки эквивалентности.
2NaNO2 + 2KI + 4HCl → I2 + 2NO + 2KCl + 2NaCl + 2H2O
I2 + KI + крахмал → синее окрашивание
5.6. Методы галоидирования
Основаны на электрофильном замещении атомов водорода ароматического кольца, активированного первичной аминогруппой, атомами галогена.
Броматометрический метод, способ прямого титрования
Методом прямого бромирования определяют анестезин, новокаин, стрептоцид, хотя в целом метод имеет ограниченное применение в анализе рассматриваемой группы лекарственных веществ в связи со свойством последних окисляться избытком брома.
Йодхлорметрический метод, способ обратного титрования. Избыток йодмонохлорида определяют йодометрически.
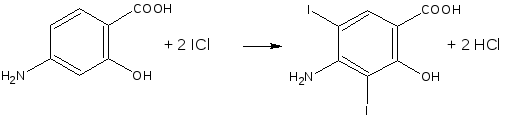
ICl + KI → I2 + KCl
Метод используется для количественного определения производных ПАБК, натрия п-аминосалицилата, сульфаниламидных препаратов (стрептоцид, сульгин, сульфадимезин и др.).
5.7. Фотоколориметрия и спектрофотометрия в видимой области
На основе реакций образования азокрасителя или шиффовых оснований.
Источник
9. Лекарственные вещества, содержащие амидную группу
Амидная группа включает остаток кислоты и амина (ароматического или алифатического).
Её содержат производные салициловой кислоты (салициламид, оксафенамид), п-аминофенола (парацетамол), анилиды аминокарбоновых кислот (ксикаин, тримекаин), производные никотиновой кислоты (никотинамид, никодин, диэтиламид никотиновой кислоты), новокаинамид, бепаск, левомицетин, кальция пантотенат, ЛВ из группы β-лактамидов.
На основе химических свойств амидной группы в анализе содержащих её ЛВ используются следующие реакции:
— гидроксамовая реакция, т. е. такие же, как и при анализе сложных эфиров.
9.1. Гидролиз в присутствии кислоты и щёлочи
Продукты гидролиза доказывают аналитическими реакциями или по их физическим свойствам (характерный запах, Тпл). Если образовавшийся амин летуч, то его определяют по запаху или с помощью лакмусовой бумажки.
— гидролиз в присутствии кислоты (его продукты – соответствующая кислота и амин):
— гидролиз в присутствии щёлочи(его продукты – натриевая соль соответствующей кислоты и амин):
9.2. Гидроксамовая реакция
9.3. Метод Кьельдаля
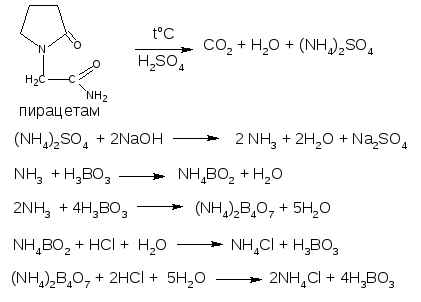
Основан на минерализации амидов конц. серной кислотой. Образующийся сульфат аммония разлагают щёлочью до аммиака, который улавливают борной кислотой. Полученные аммонийные соли борной кислоты (метабораты и тетрабораты) оттитровывают хлористоводородной кислотой.
Метод является фармакопейным для оксафенамида, пирацетама.
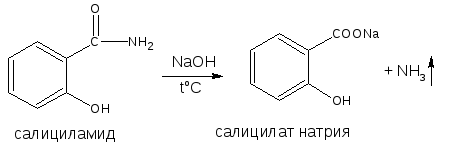
9.4. Гидролитическое разложение амидов в присутствии гидроксида натрия и дальнейшее определение образовавшегося аммиака по методу Кьельдаля.
Вариант метода является фармакопейным для салициламида.
9.5. Гидролитическое разложение в присутствии серной кислоты с образованием соли амина, которую разлагают щёлочью до летучего амина и далее определяют по методу Кьельдаля.
Таким методом возможно определение диэтиламида никотиновой кислоты. М.э. = М.м.
9.6. Фотоколориметрия и спектрофотометрия
На основе гидроксамовой реакции.
Лекарственные вещества, содержащие лактамную группу
Образуются из аминокислот и являются внутримолекулярным (циклическим) амидом.
Лекарственные вещества, содержащие лактамную группу: антибиотики группы β-лактамидов (бензилпенициллина натриевая, калиевая, новокаиновая соли, феноксиметилпенициллин, оксациллина натриевая соль, ампициллин, цефалексин, цефалотин).
Лактамы более реакционноспособны, чем амиды, поэтому реакции гидролитического разложения и гидроксамовая проба протекают легче и даже при комнатной температуре.
Гидроксамовая реакция является фармакопейной для антибиотиков β-лактамной группы – гидроксамовую кислоту доказывают по образованию гидроксамата меди.
Гидролитическое разложение в присутствии кислоты или щёлочи для идентификации препаратов, содержащих лактамную группу не используется, но находит применение в количественном анализе.
Способ обратного титрования. Метод основан на гидролитическом разложении лактамов в присутствии избытка титрованного раствора щёлочи, который далее оттитровывают кислотой. М.э. = М.м.
Метод является фармакопейным для оксациллина натриевой соли.
Источник
Ароматические кислоты. Аминокислоты и их производные
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Ароматические кислоты. Аминокислоты и их производные
Ароматические кислоты и их производные
К данной группе ЛС относятся кислота бензойная и ее натриевая соль, кислота салициловая и ее натриевая соль, сложные эфиры кислоты салициловой – фенилсалицнлат, кислота ацетилсалициловая; амиды кислоты салициловой — салициламид, оксафенамид; производные кислоты иара-аминосалициловой – натрия пара-аминосалицилат; производные орто- замешенного амина — кислота мефенамовая и натрия диклофенак.
Среди них ЛС природного происхождения (кислоты бензойная, салициловая, ацетилсалициловая), а также синтетические соединения.
Перечисленные ЛС оказывают разнообразное фармакологическое действие; антисептическое (кислота бензойная, натрия салицилат, фенилсалицилат), противовоспалительное (кислота ацетилсалициловая, кислота мефенамовая, натрия диклофенак), желчегонное (оксафенамид), месгноанестезируюшее (анестезин, новокаин).
Свойства лекарственных веществ данной группы представлены в табл. 42.


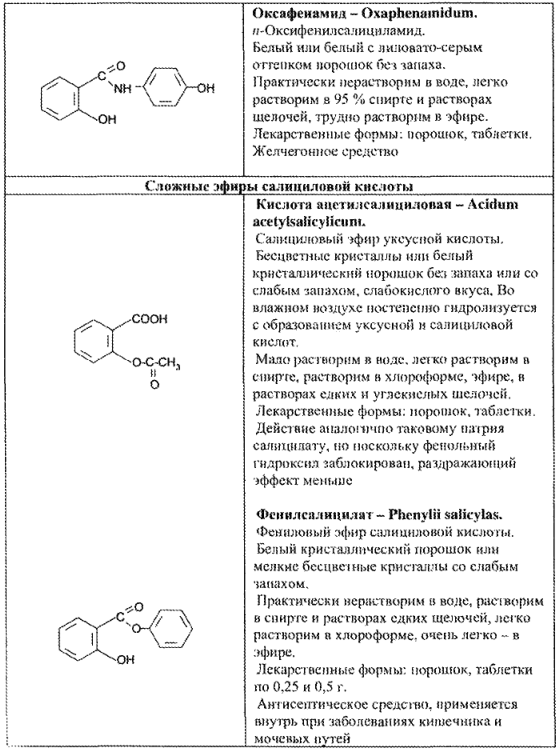
Исследуемые лекарственные препараты имеют характерные спектры поглощения в УФ-области. Например, 0,007% раствор кислоты ацетилсалициловой в хлороформе имеет максимум при /тине волны 278 нм; 0,02% раствор кислоты мефенамовой в смеси метанола и кислоты хлороводородной — при 279 и 350 нм.
Растворимость
Нерастворимы в воде кислоты (бензойная, салициловая), их эфиры (фенилсалицилат, кислота ацетилсалициловая, анестезин) и амиды.
Растворимы в воде соли щелочных металлов (натрия бензоат, натрия салицилат, натрия n-амияосалицилат), соль органического основания и минеральной кислоты (новокаин). Исключение — натрия диклофенак, который, являясь солью, трудно растворим в воде.
Ароматические кислоты и их производные
Кислотные свойства
Кислотные свойства ароматических кислот более выражены, чем γ- кислот жирного ряда и угольной кислоты. Это объясняется влиянием ароматического ядра. Кислотные свойства обусловлены подвижностью протона водорода к карбоксильной группе, при этом образуется резонансный стабилизированный анион, у которого отрицательный заряд распределяется поровну между электроотрицательными атомами кислорода:
Значение рКa кислот следующее: угольная — 6,12, уксусная — 4,76, бензойная – 4,18, салициловая – 3,00.
Ароматические кислоты взаимодействуют со щелочами, а также (в отличие от фенолов) — с гидрокарбонатами щелочных металлов, В медицине применяются натриевые соли бензойной и салициловой кислот.
Если на соль подействовать кислотой азотной, происходит вытеснение ароматической кислоты и выпадение ее в осадок. ГФ рекомендует определять их Тпл:
С солями тяжелых металлов изучаемые вещества образуют окрашенные осадки или окрашенные комплексы различного состава. Кислотные формы предварительно переводят в хорошо диссоциируемую соль путем добавления эквивалентного количества щелочи. Необходимо избегать избытка реактива, так как гидроксид тяжелого металла маскирует окраску комплекса:
Часто окраска и состав комплекса зависят от соотношения реактива и препарата, а также от pH среды.
При pH 2,0-3,0 образуется окрашенный в фиолетовый цвет моносалицилат
который разрушается при добавлении кислоты хлороводородной; при добавлении кислоты уксусной окраска сохраняется.
При pH 3,0-8,0 образуется дисалицилат красного цвета:
При pH 8,0— 10,0 образуется трисалицилат желтого цвета:
Реакции используются и для открытия примеси кислоты салициловой, натрия салицилата и фенола в фемилсалипилате. Последний практически нерастворим в воде, поэтому указанные примеси открываются в водной вытяжке, полученной из препарата.
Примесь свободной кислоты салициловой в кислоте ацетилсалициловой определяется по образованию окрашенного комплекса е ионами железа (III).
Реакции электрофильного замещения
Кислота салициловая, являясь полифункциональным соединением, вступает в реакции, которые характерны для фенолов:
– образование азокрасителя с солями диазония
Образование азокрасителя сопровождается чаще всего появлением красного окрашивания или красного осадка. У кислоты салициловой и ее соли наблюдается желтое окрашивание, переходящее в розовое.
Соль диазония из-за нестойкости готовят непосредственно перед проведением реакции, используя соединения, содержащие первичную ароматическую аминогруппу.
Реакции конденсации и окисления
Образование арилметанового красителя происходит в присутствии реактива Марки, при этом концентрированная Н2SО4 на 1-й стадии является водоотнимающим агентом, а на 2-й – окислителем:
Анализ чистоты
В кислоте бензойной определяется примесь фталевой кислоты. Препарат растворяют в бензоле. Появление мути доказывает наличие нерастворимой в бензоле фталевой кислоты.
На наличие примеси фенола и оксидифенила проверяется кислота салициловая. Определение фенола проводят по цвету сухого остатка, полученного после испарения спирта из раствора препарата в данном растворителе.
Примеси оксидифенила не должно быть больше 0,1%. Препарат переводят в натриевую соль, для этого его помешают в раствор натрия карбоната. Оксидифенил, являясь производным фенола, не взаимодействует с натрия карбонатом. Затем примесь извлекают эфиром, эфир выпаривают, сухой остаток оксидифенила взвешивают.
Количественное определение
Количественное определение ароматических кислот проводят методом алкалиметрии с индикатором фенолфталеином. В результате реакции образуется соль сильного основания и слабой органической кислоты. Такая соль легко гидролизуется, поэтому окраска индикатора может измениться до наступления точки эквивалентности. Для подавления гидролиза в анализе используют спирт.
Количественный анализ бензоата и салицилата натрия проводят ацидиметрически по метиловому оранжевому:
Титрование проводят в присутствии эфира для удаления из реакционной среды кислот, с pH 2,5—3,0, которые могут изменить окраску индикатора до наступления точки эквивалентности.
Ароматические аминокислоты
Кислотно-основные свойства
Натрия пара-аминосалицилат — амфотерное соединение, поскольку не только характеризуется кислотными функциями, но и имеет первичную ароматическую аминогруппу, которая обладает основными свойствами:
Препарат образует комплекс красно-фиолетового цвета с железа (III) хлоридом.
Эта реакция используется для открытия токсичной примеси 5- аминосалициловой кислоты. Примесь также образует комплекс красно-фиолетового цвета, но при стоянии выпадает в осадок.
Анестезия и новокаин проявляют лишь основные свойства за счет первичной ароматической аминогруппы. Основные свойства новокаина выражены сильнее вследствие наличия третичной алифатической аминогруппы. Соль новокаина-основания и кислоты хлороводородной выпускается промышленностью. Реакция среды раствора такой соли кислая, а при действии щелочи выделяется органическое основание новокаина, нерастворимое в воде (бесцветные маслянистые капли):
Новокаин образует соли и с общеалкалоидными осадительными реактивами: кислота пикриновая, кислота фосфорно-вольфрамовая.
У кислоты мефенамовой, диклофенака натрия выраженные кислотные свойства, поэтому препараты образуют соли со щелочами и с тяжелыми металлами.
Диклофенак с натрия гидроксидом образует устойчивую соль. При добавлении к раствору соли минеральной кислоты выпадает осадок кислотной формы диклофенака и индолинона:
Окислительно-восстановительные свойства
Лекарственные соединения, содержащие первичную ароматическую аминогруппу, относительно легко окисляются. В структуре натрия n-аминосалицилата, кроме аминогруппы, имеется фенольный гидроксил, поэтому он особенно легко окисляется как кислородом воздуха, так и окислителями.
Устойчивая окраска образуется при окислении анестезина хлорамином, продукты окисления в эфире окрашены в оранжевый цвет.
Обесцвечивание раствора калия перманганата происходит при действии его на раствор новокаина.
В структуре кислоты мефенамовой, натрия диклофенака имеется остаток дифениламина, за счет которого происходит окисление в жестких условиях (калия дихроматом в кислоте серной концентрированной Н2SО4; натрия нитритом в той же кислоте).
Реакция образования азокрасителя
При действии на анестезин и новокаин натрия нитритом в кислой среде образуется соль диазония, которая вступает в реакцию с азосоставляющей с образованием азокрасителя.
В качестве азосоставляющей могуг быть:
1) фенолы (в щелочной среде);
2) ароматические амины (в кислой среде):
Образование азокрасителя определяется по появлению красного окрашивания или красного осадка. Реакция используется для установления подлинности препаратов и количественного определения.
Токсичную примесь м-аминофенола в натрия n-аминосалицилате выявляют также по этой реакции. Поскольку препарат образует азокраситель (следовательно, мешает определению примеси), проводят разделение. Для этого препарат растворяют в метаноле, затем добавляют эфир. Раствор оставляют до выпадения осадка, в котором остается примесь.
Реакции гидролитического расщепления
Анестезин и новокаин — эфиры n-амииобензойной кислоты, легко гидролизуются в кислой и щелочной среде. Образующиеся после гидролиза вещества открывают соответствующими реакциями. Например, этиловый спирт – по реакции образования йодоформа (анестезин):
Гидроксамовая проба используется при анализе качества анестезина, новокаина:
Количественное определение
Количественное определение новокаина, анестезина, натрия пара-аминосалицилата проводят по первичной ароматической аминогруппе методом нитритометрии.
Титрование натрия нитритом проводят медленно, так как образование соли диазония идет во времени. В реакционную среду для стабилизации соли добавляют калия бромид; рекомендуемая температура — ниже комнатной.
В качестве индикатора используют тропеолин 00 (внутренний) или йодкрахмальную бумагу (внешний),
В точке эквивалентности на йодкрахмальной бумаге выделяется йод, который окрашивает крахмал в синий цвет:
Содержание кислоты мефенамовой определяется кислотно-основным титрованием в неводной среде (диметнлформамида). Мефенамовая кислота обладает слабыми кислотными свойствами, которые усиливают путем ее растворения в протофильном растворителе. Препарат в среде диметнлформамида депротоиируется. Титрантом служит раствор натрия гидроксида в смеси бензола и метанола. Индикатор – тимоловый синий:
Натрия диклофенак определяется неводным титрованием с использование протогенного растворителя — кислоты уксусной ледяной. Титруют раствором кислоты хлорной, индикатор — кристаллический фиолетовый:
Источник