- Антагонизм для лекарственных препаратов
- Модели молекулярных механизмов действия агонистов и антагонистов
- Антагонизм для лекарственных препаратов
- 28. Антагонизм. Лекарственных средств: виды, механизмы взаимодействия препаратов, клиническое значение .
- 1.Местные анестетики
- 23) Антагонизм лекарственных средств: виды, механизмы взаимодействия препаратов, клиническое значение.
- 24) Значение синергизма и антагонизма лекарственных средств в анестезиологии. Значение синергизма и антагонизма при совместном применении антибиотиков.
Антагонизм для лекарственных препаратов
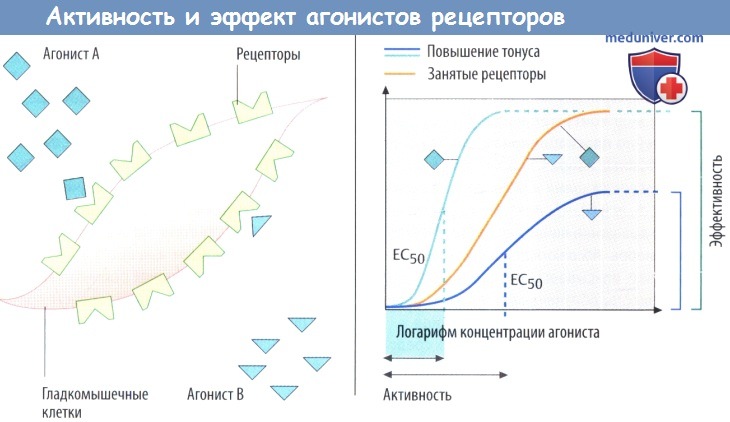
Агонисты способны прикрепляться к белкам-рецепторам, изменяя функцию клетки, т. е. обладают внутренней активностью. Биологический эффект агониста (т. е. изменение функции клетки) зависит от эффективности внутриклеточной передачи сигнала в результате активации рецептора. Максимальный эффект агонистов развивается уже тогда, когда связанной оказывается только часть доступных рецепторов.
Другой агонист, обладающий такой же аффинностью, но меньшей способностью активировать рецепторы и соответствующую внутриклеточную передачу сигнала (т. е. обладающий меньшей внутренней активностью), вызовет менее выраженный максимальный эффект, даже если связанными окажутся все рецепторы, т. е. имеет меньшую эффективность. Агонист В является частичным агонистом. Активность агонистов характеризуется концентрацией, при которой достигается половина максимального эффекта (EC50).
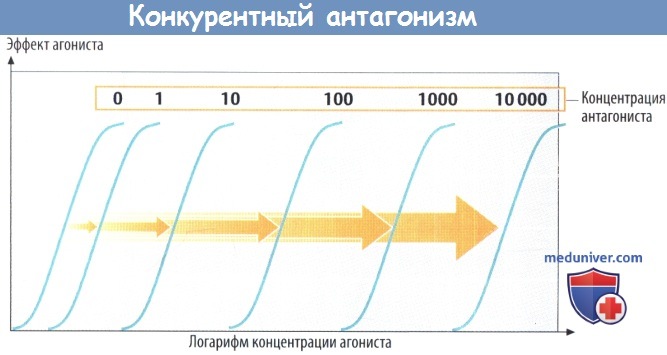
Антагонисты ослабляют эффект агонистов, противодействуя им. Конкурентные антагонисты обладают способностью связываться с рецепторами, но при этом функция клетки не изменяется. Другими словами, они лишены внутренней активности. Находясь в организме одновременно, агонист и конкурентный антагонист соперничают за связывание с рецептором. Химическое сродство и концентрация обоих соперников определяют, кто будет связываться активнее: агонист или антагонист.
Увеличивая концентрацию агониста, можно преодолеть блок со стороны антагониста: в этом случае кривая зависимости эффекта от концентрации сдвигается вправо, к более высокой концентрации с сохранением максимальной эффективности препарата.
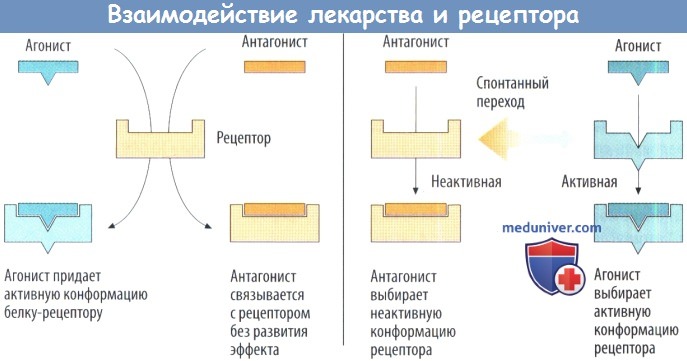
Модели молекулярных механизмов действия агонистов и антагонистов
Агонист вызывает переход рецептора в активированную конформацию. Агонист связывается с рецептором в неактивированной конформации и вызывает его переход в активированное состояние. Антагонист прикрепляется к неактивному рецептору, не изменят его конформацию.
Агонист стабилизирует спонтанно появившуюся активированную конформацию. Рецептор способен спонтанно переходить в состояние активированной конформации. Однако обычно статистическая вероятность такого перехода настолько мала, что спонтанное возбуждение клеток определить не удается. Селективное связывание агониста происходит только с рецептором в активированной конформации и тем самым благоприятствует этому состоянию.
Антагонист способен связываться с рецептором, находящимся только в неактивном состоянии, продлевая его существование. Если у системы невысокая спонтанная активность, добавление антагониста не оказывает особого влияния. Однако, если система демонстрирует выэсокую спонтанную активность, антагонист может вызывать эффект, противоположный эффекту агониста, — такназываемый обратный агонист. «Истинный» агонист без внутренней активности (нейтральный агонист) обладает одинаковой аффинностью к активированным и неактивированным конформациям рецептора и не изменяет базальную активность клетки.
Согласно этой модели, частичный агонист обладает меньшей селективностью по отношению к активированному состоянию: однако в некоторой степени он связывается также с рецептором в неактивированном состоянии.
Другие виды антагонизма. Аллостерический антагонизм. Антагонист связывается за пределами места прикрепления агониста к рецепторуи вызывает снижениеаффинностиагони-ста. Последняя нарастает в случае аллостерического синергизма.
Функциональный антагонизм. Два агониста, действующие через различные рецепторы, изменяют одну и ту же переменную (диаметр бронхов) в противоположных направлениях (адреналин вызывает расширение, гистамин — сужение).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Антагонизм для лекарственных препаратов
Обратный агонизм — это инициация явного клеточного ответа путем торможения спонтанной активации рецептора.
Молекулярный ответ на обратный агонизм может быть:
• инактивацией активированного рецептора;
• стабилизацией рецептора в неактивной конформации.
Данная модель выглядит как R R и I+R IR, где R — активированное состояние, I — обратный агонист.
Антагонизм — это предотвращение действия агониста. Многие лекарства связываются с рецептором, образуя комплекс лекарство-рецептор, который не вызывает клеточного ответа. Более того, оккупация рецептора антагонистом препятствует либо связыванию агониста, либо возникновению клеточного ответа при связывании агониста с рецептором. Таким образом, антагонизм может быть результатом различных молекулярных механизмов. Математическое описание эффектов различных типов антагонистов приведено далее. Кратко — антагонизм может возникать вследствие:
• связывания антагониста в том же участке рецептора, который в норме занимает агонист. Связывание антагониста препятствует оккупации центра агонистом (конкурентный антагонизм);
• связывания антагониста с участком рецептора, который в норме не оккупирует агонист (аллостерический центр), ведущего к конформационным изменениям связывающего центра агониста, что либо препятствует связыванию агониста, либо делает невозможным возникновение молекулярного ответа.
Антагонист, связывающийся с аллостерическим центром только в отсутствие агониста, называют неконкурентоспособным антагонистом. Если антагонист может связываться с аллостерическим центром даже в присутствии связанного агониста, его называют неконкурентным антагонистом. В данном случае центр часто называют лиганд-связывающим (где лигандом может быть агонист, антагонист, частичный агонист и др.).
Связывание антагониста может быть обратимым или необратимым. Различают как минимум шесть возможных типов антагонизма. Эффекты, проявляемые антагонистом в ответ на действие агониста, детально описаны далее.
Физиологический антагонизм отличается от фармакологического антагонизма. Часто термин «физиологический (или функциональный) антагонизм» используют некорректно. Этот термин описывает способность агониста (чаще, чем антагониста) тормозить ответ на другой агонист путем активации разных, физически разделенных рецепторов. Это может происходить, если рецепторы двух агонистов объединены одинаковыми компонентами клеточного ответа, но по-разному действуют на них, или связаны разными компонентами клеточного ответа, которые вызывают противоположные тканевые ответы.
Наглядным примером служит взаимодействие между норадреналином и ацетилхолином в артериолах. Норадреналин вызывает сокращение, а ацетилхолин — расслабление. Конечно, бессмысленно описывать норадреналин как антагонист ацетилхолина, поскольку также можно ацетилхолин расценивать как антагонист к норадреналину, поэтому термины «агонист» и «антагонист» становятся взаимозаменяемы и не имеют смысла. Термин «антагонист» лучше всего подходит для описания лекарств, которые тормозят молекулярный ответ на действие агониста. Термин «функциональный антагонист» лучше не использовать.
Источник
28. Антагонизм. Лекарственных средств: виды, механизмы взаимодействия препаратов, клиническое значение .
Два лекарственных препарата при совместном применении уменьшают эффекты друг друга.
использование при отравлении лекарственными препаратами;
для устранения побочных эффектов.
Во всех остальных случаях стараются избегать этого явления.
физический или механический— один препарат сорбирует на себе другой ,не вступая в химическую реакцию *:активированный уголь + алкалоиды.
химический -два вещества вступают в химическую реакцию с образованием нетоксического соединения *:KMnO4+алкалоиды( морфин, атропин)=окисление; или I2+тиосульфат Na=KI-не опасен
Прямой- два вещества действуют на один орган-мишень, чаще он бывает конкурентным. Конкурентный- это когда на один рецептор действуют два вещества, один из них обладает внутренней активностью, а второй не обладает (агонист-антагонист).*:морфин (агонист)-налоксон(антагонист).Среди примеров конкурентного антагонизма может встречаться односторонний конкурентный антагонизм *:атропин (м-блокатор) и мускарин(м-миметик)-один из них более сильный конкурент; как правило, блокаторы обладают большим сродством к рецепторам.
ККосвенный –два препарата вызывают противоположные эффекты, действуя, например, на разные физиологические системы; *:ацетилхолин приводит к брадикардии, а адреналин и норадреналин- к тахикардии. Такие явления практически не применяют.
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ВЛИЯЮЩИЕ НА АФФЕРЕНТНУЮ ИННЕРВАЦИЮ.
1.Местные анестетики
Местные анестетики (греч.an — отрицание, aesthesis — чувствительность) обратимо снижают возбудимость чувствительных нервных окончаний и блокируют проведение импульсов в нервных стволах в месте непосредственного применения, используются для устранения боли.
Механизм действия местных анестетиков
Местные анестетики представляют собой третичные азотистые основания. Они состоят из гидрофильной и липофильной частей, соединенных эфирной или амидной связями. Механизм действия определяет липофильная часть, имеющая ароматическую структуру. Для нанесения на слизистые оболочки и кожу и парентерального введения применяют водные растворы хлористоводородных солей местных анестетиков. В слабощелочной среде тканей (рН=7,4) соли гид-ролизуются с освобождением оснований, растворяющихся в липидах мембран нервных окончаний и стволов. Основания местных анестетиков проникают к внутренней поверхности мембраны, превращаются в ионизированную катионную форму и нарушают проницаемость потенциалозависимых быстрых каналов, пропускающих ионы натрия. Местные анестетики во время потенциала действия связываются с открытыми натриевыми каналами и вызывают их инактивацию. Препараты не взаимодействуют с закрытыми каналами в период потенциала покоя и инактивированными каналами в период ре-поляризации. Рецепторы для местных анестетиков локализованы в Sg-сегменте IV-ro домена внутриклеточной части натриевых каналов.Таким образом, в зоне нанесения местных анестетиков не развиваются потенциалы действия, что сопровождается блоком проведения нервных импульсов. Избирательное влияние местных анестетиков на чувствительные афферентные нервы обусловлено генерацией в них длительных (более 5 миллисекунд) потенциалов действия с высокой частотой.В первую .очередь местные анестетики блокируют безмиелиновые и тонкие миелиновые волокна (афферентные пути, проводящие болевые и температурные раздражения; вегетативные нервы). Напротив, толстые миелиновые волокна (афферентные пути, проводящие тактильные раздражения; двигательные нервы) не реагируют на местные анестетики. Кроме того, устойчивость двигательных нервов к анестезии обусловлена низкочастотными короткими (менее 5 миллисекунд) потенциалами действия. На волокна, окруженные миелиновой оболочкой, местные анестетики действуют в области перехватов Ранвье.В очаге воспаления в условиях ацидоза нарушаются диссоциация хлористоводородных солей местных анестетиков и образование их свободных липидорастворимых оснований, поэтому обезболивающее влияние утрачивается. Например, местная анестезия может оказаться неэффективной при удалении зуба в случае тяжелого периодонтита.
Препараты местных анестетиков
Местные анестетики классифицируют на сложные эфиры и замещенные амиды.
/. Сложные эфиры ароматических кислот и аминоспиртов: •КОКАИН — эфир бензойной кислоты и аминоспирта метилэкгонина
(последний близок по химическому строению атропину); •НОВОКАИН (ПРОКАИНА ГИДРОХЛОРИД) — эфир парааминобензой-ной кислоты и диметиламиноэтанола, обладающего самостоятельной слабой местноанестезирующей активностью; • ДИКАИН (ТЕТРАКАИНА ГИДРОХЛОРИД) — химический аналог новокаина, имеет алифатический радикал в ароматическом кольце, по активности в 10 раз превосходит кокаин, но в 2-5 раз токсичнее кокаина и в 10-20 раз токсичнее новокаина; •АНЕСТЕЗИН (БЕНЗОКАИН) — этиловый эфир парааминобензойной кислоты, не образует соль с хлористоводородной кислотой и поэтому плохо растворим в воде.
2. Замещенные амиды кислот:
•ЛИДОКАИНА ГИДРОХЛОРИД (КСИЛОКАИН) — производное амино-этиламида, при поверхностной анестезии его активность вдвое меньше, чем у кокаина, в 20-40 раз меньше по сравнению с эффективностью дикаина, при проводниковой и инфильтрационной анестезии действует в 2-4 раза сильнее новокаина, превосходит по токсичности новокаин в 1,5-2 раза (активные метаболиты лидокаина -моноэтилглицинксиламид и глицинксиламид вызывают судороги);
•БУПИВАКАИНА ГИДРОХЛОРИД (АНЕКАИН, МАРКАИН) — химический аналог лидокаина, имеет в составе бутилпиперидиновый гетероцикл, один из самых эффективных и длительно действующих местных анестетиков, обладает кардиотоксичностью;
•ТРИМЕКАИН — близок по строению лидокаину (отличается присутствием ме-тильной группы в положении 4 фенильного ядра), при поверхностной анестезии в 2,5 раза слабее кокаина и в 25-50 раз дикаина, при проводниковой и инфильтрационной анестезии в 2,5-3,5 раза превосходит новокаин, несколько токсичнее новокаина;
•ПИРОМЕКАИН (БУМЕКАИНА ГИДРОХЛОРИД) — аналог тримекаина, имеет пир-ролидоновое кольцо, проявляет высокую местноанестезирующую активность;
• МЕПИВАКАИН (КАРБОКАИН, МЕПИКАТОН) — аналог лидокаина с более дли-
тельным (на 20%) действием;
•РОПИВАКАИН — аналог лидокаина, смесь R- и S-энантиомеров, действует слабее бупивакаина, характеризуется низкой кардиотоксичностью, пригоден для спинномозговой анестезии;
• АРТИКАИН (УЛЬТРАКАИН) — амидный препарат с тиофеновым кольцом, оказы-
вает сильное, быстрое и продолжительное действие, в том числе при спинномозговой анестезии.
Местные анестетики — сложные эфиры подвергаются гидролизу псев-дохолинэстеразой крови и действуют в течение 30-60 минут. Их эффект пролонгируют антихолинэстеразные средства (прозерин). Продукт гидролиза — парааминобензойная кислота ослабляет бактериостатичес-кое влияние сульфаниламидов.
Замещенные амиды кислот инактивируются монооксигеназной системой печени в течение 2-3 часов. Бупивакин вызывает местную анестезию продолжительностью 3-6 часов, после ее прекращения длительно сохраняется анальгетический эффект.
Источник
23) Антагонизм лекарственных средств: виды, механизмы взаимодействия препаратов, клиническое значение.
Антагонизм – способность одного вещества в той или иной степени уменьшать эффект другого.
Прямой — два вещества действуют на один орган-мишень, чаще он бывает конкурентным. Конкурентный — на один рецептор действуют два вещества, один из них обладает внутренней активностью, а второй не обладает (агонист-антагонист). Например морфин (агонист) -налоксон (антагонист).
Косвенный – два препарата вызывают противоположные эффекты, действуя, например, на разные физиологические системы (ацетилхолин приводит к брадикардии, а адреналин и норадреналин- к тахикардии).
Физический или механический — один препарат сорбирует на себе другой, не вступая в химическую реакцию (активированный уголь + алкалоиды).
Химический — два вещества вступают в химическую реакцию с образованием нетоксического соединения.
Физиологический ( функциональный) – прямой или косвенный.
Синергоантагонизм — при котором одни эффекты комбинируемых веществ усиливаются, а другие ослабляются. Так, на фоне А-адреноблокаторов стимулирующее действие адреналина на а-адренорецепторы сосудов уменьшается, а на В-адренорецепторы — становится более выраженным.
Использование при отравлении лекарственными препаратами; для устранения побочных эффектов.
24) Значение синергизма и антагонизма лекарственных средств в анестезиологии. Значение синергизма и антагонизма при совместном применении антибиотиков.
Некоторые препараты изменяют чувствительность рецепторов тканей к другим препаратам.
Совместное введение миорелаксанта панкурония бромида и фентанила. Первый препарат обладает ваголитическим действием и при монотерапии вызывает тахикардию. Ваготоническое действие фентанила нейтрализует этот нежелательный эффект и обеспечивает сбалансированную ЧСС при вводном наркозе у большинства пациентов с заболеваниями сердца.
Кетамин потенцирует действие недеполяризующих миорелаксантов. совместное применение с препаратами теофиллина может вызывать судороги. бензодиазепины ослабляют обусловленную кетамином стимуляцию кровообращения и психотомиметические эффекты, удлиняют период его полусуществования в фазе элиминации. кетамин на фоне действия фторотана вызывает депрессию миокарда. препараты лития пролонгируют действие кетамина.
Синергизм — это усиление бактерицидного действия а\б при их совместном применении. Синергизм определяют как уменьшение числа бактерий на 99% (в 100 раз) после инкубации в течение ночи с обоими препаратами по сравнению с инкубацией с каждым из них в отдельности. Примером может служить сочетание препаратов, препятствующих синтезу клеточной стенки, и аминогликозидов. Препараты, подавляющие образование клеточной стенки (бензилпенициллин, ампициллин, ванкомицин), в отношении энтерококков в лучшем случае оказывают медленный бактерицидный эффект. Аминогликозиды действуют на эти микроорганизмы только бактериостатически. Сочетание же препарата, подавляющего синтез клеточной стенки, и аминогликозида облегчает проникновение последнего в бактериальные клетки и приводит к быстрой гибели бактерий. Указанные препараты синергично действуют и в отношении гемолитических стрептококков, Staphylococcus aureus, многих грамотрицательных палочек.
В некоторых случаях антимикробные препараты действуют антагонистически. Например, в присутствии препарата, подавляющего размножение бактерий, бактерицидное действие b-лактамных антибиотиков, направленное на делящиеся микроорганизмы, может смениться бактериостатическим.
25) Принципы лечения угрожающих жизни состояний в результате поражения токсическими веществами (острые отравления, химические ожоги, отравления грибами, поражения ядовитыми животными с опасностью развития угрожающих жизни состояний).
Основная задача при лечении острых отравлений заключается в удалении из организма вещества, вызвавшего интоксикацию.
1)Задержка всасывания токсичного в-ва в кровь.
Очищение желудка – вызывание рвоты (концентрированный NaCl/Na2SO4) или промывание. При отравлении кислотами и щелочами рвоту не вызываем (в-ва повреждают слизистую). Эффективно промывание желудка ч/з зонд. Дают адсорбенты и слабительные (солевые слабительные, вазелиновое масло).
При подкожном введении в-ва, вводят адреналин вокруг места введения в-ва, охлаждение этой области, м/о наложить жгут.
2) Удаление токс в-ва из орг-ма.
Метод форсированного диуреза – водная нагрузка+мочегонные, поддержание электролитного баланса.
Гемодиализ – кровь пр-т ч/з диализатор с полупроницаемой мембраной и освобождается от не связанных с белками токс в-в (барбитураты).
Перитонеальный диализ – промывание полости брюшины раствором электролитов, вводят антибиотики.
Гемосорбция – токс в-ва адсорбируются на сорбентах (актив уголь с покрытием белками крови).
Замещение крови – кровопускание+донорская кровь.
Плазмаферез – производится удаление плазмы без потери форм элементов + донорская плазма.
3) Устранение д-я всосавшегося токс в-ва.
Антидоты при отравлении тяж Ме (унитол, CaNa2).
Фармакологические антагонисты (атропин при отравлении антихолинэстеразными ср-ми).
4) Симптоматическая терапия острых отравлений.
Поддержание жизненно важных функций. Применяют кардиотоники, в-ва, регулирующие уровень АД, улучшающие микроциркуляцию в периферических тканях.
5) Профилактика острых отравлений.
ВЕГЕТОТРОПНЫЕ (СИНАПТОТРОПНЫЕ) ЛЕКАРСТВЕННЫЕ
Источник