- Какие стандарты обеспечивают качество упаковки фармацевтической продукции?
- Международные стандарты на упаковку фармацевтической продукции
- Национальные / региональные стандарты и нормы
- Подробнее о фармацевтической упаковке
- Сохранение безопасности лекарств после извлечения из упаковки через стерилизацию
- Анализ упаковки лекарственных препаратов
Какие стандарты обеспечивают качество упаковки фармацевтической продукции?
Международные стандарты на упаковку фармацевтической продукции
При этом руководящие органы и организации по стандартизации по всему миру устанавливают правила упаковки фармизделий, которым надлежит соответствовать фармацевтическим компаниями.
В частности, упоминания заслуживают несколько добровольных основанных на консенсусе стандартов от Международной организации по стандартизации (ИСО), которые большинство правительств использует в качестве руководства при разработке собственных норм.
Как пример можно привести стандарт ИСО 15378:2017 «Первичные упаковочные материалы для лекарственных препаратов — Частные требования по применению ИСО 9001:2015, учитывая правила организации производства и контроля качества лекарственных средств».
Данный документ касается «первичных упаковочных материалов для лекарственных средств» и детализирует принципы управления качеством на базе другого стандарта ИСО 9000:2015 «Системы менеджмента качества – Базовые принципы и вокабулярий», которые следует применять во время производства.
Как правило, эти руководства в значительной степени касаются надлежащей производственной практики и отчетности, обеспечивая основу, которая может применяться как к обычному, так и к специализированному производству.
Дополнительные стандарты могут применяться к конкретным продуктам и процессам, являющимся объектами углубленного контроля. Например, в ситуации, когда из стерильных флаконов отбираются образцы и проверяются на стерильность во время и после производства.
Сразу несколько стандартов могут применяться на определенных стадиях данного процесса. Как пример можно привести документы из серии ИСО 11137-1, касающиеся радиационной стерилизации медицинских изделий:
- ИСО 11137-1:2006 «Стерилизация медицинских изделий – Радиация — Часть 1: Требования к разработке, валидации и текущему контролю процесса стерилизации медицинских изделий»;
- ИСО 11137-2:2013 «Стерилизация медицинских изделий – Радиация — Часть 2: Установление стерилизующей дозы»;
- ИСО 11137-3:2017″Стерилизация медицинских изделий – Радиация — Часть 3: Руководство по дозиметрическим аспектам разработки, валидации и текущего контроля»;
Внимания заслуживает и серия ИСО 11737, включающая стандарты, посвященные оценке изделий медицинского назначения после стерилизации на предмет наличия микроорганизмов:
- ИСО 11737-1:2018 «Стерилизация изделий медицинского назначения — Микробиологические методы — Часть 1: Определение количества микроорганизмов на изделиях».
- ИСО 11737-2:2019 «Стерилизация изделий медицинского назначения — Микробиологические методы — Часть 2: Испытания на стерильность, выполняемые при определении, валидации и поддержании процесса стерилизации».
- ИСО 11737-3:2004 «Стерилизация изделий медицинского назначения — Микробиологические методы — Часть 3: Руководство по оценке и интерпретации данных о микробиологической нагрузке».
Лекарства, требующие стерильности, могут размещаться внутри первичной упаковки в «чистой комнате» в соответствии с многочисленными дополнительными стандартами, которые устанавливают правила обеспечения надлежащего качества и чистоты воздуха внутри помещения.
Национальные / региональные стандарты и нормы
Стандарты и нормы, применимые к тому или иному фармпродукту, зависят от страны, в которой он производится и распространяется. Хотя стандарты ИСО предоставляют полезные рекомендации, они не являются заменой правительственными нормам, которые действуют на территории страны или региона (например, Евросоюза). Стандарты ИСО фактически не определяют лимиты — особенно в отношении химикатов и их концентраций в продуктах.
Например, максимально допустимая концентрация фенилфенола, разрешенного для использования в косметике в качестве консерванта, установлена Европейским Союзом на уровне 0,2% (2018 г.), в то время как американский регулятор FDA (Комиссия по контролю за пищевыми продуктами и лекарственными средствами) не ввел соответствующего запрета в отношении косметики. Однако FDA ограничивает использование этого химического вещества (не более 0,08%) в изделиях, контактирующих с пищевыми продуктами.
В Соединенных Штатах Америки FDA регулирует лекарства и их упаковку, а Европейская комиссия устанавливает правила для стран ЕС. В большинстве других юрисдикций / региональных геополитических блоков имеются аналогичные агентства, устанавливающие правила и нормы. Так, в Китае есть Национальное управление по медицинским изделиям, а в России – Министерство здравоохранения Российской Федерации.
Подробнее о фармацевтической упаковке
Фармацевтическая упаковка обычно делится на два-три уровня:
- Первичная упаковка, которая вступает в прямой контакт с лекарством;
- Вторичная упаковка, видимая конечному пользователю;
- Третичная упаковка, которая обычно используется только на стадии хранения и транспортировки для защиты продукта.
К каждому слою применяется несколько стандартов, первый из которых в наибольшей степени связан с химической стабильностью лекарственного средства – в основном за счет обеспечения инертности контейнера, воздухо- и влагонепроницаемости, а также непрозрачности для УФ-излучения.
Второй уровень часто предназначен просто для повышения привлекательности продукта для конечного потребителя, предлагая необходимую маркировку и информацию, видимые клиенту и помогающие обдумать целесообразность приобретения / сравнить предложенные варианты между собой перед покупкой.
Как правило, подобная информация дублируется на первичной упаковке, чтобы гарантировать использование продукта по назначению за счет наличия хорошо читаемой маркировки, заметной после извлечения из вторичной упаковки.
Многие нормативные акты, касающиеся упаковки фармацевтических продуктов, связаны с надлежащей маркировкой, чтобы гарантировать полную прослеживаемость изделий (от места производства до пункта продажи), а также обеспечить осведомленность потребителей и конечных пользователей о содержимом и четко обозначить любые источники опасности.
Материал, используемый для печати этикеток фармацевтических препаратов, и клей, с помощью которого этикетки прикрепляются, также подлежат регулированию с применением стандартов и законодательных норм.
Подобный подход гарантирует читаемость и фиксацию этикетки даже после многих месяцев или лет нахождения в освещенном месте и под воздействием иных погодных условий, а также отсутствие опасности для здоровья конечного пользователя со стороны материалов, используемых при изготовлении и наклеивании этикетки.
Неправильная маркировка лекарств потенциально может представлять серьезный риск для здоровья. Например, некорректное указание концентрации лекарства при маркировке способно вызвать передозировку.
По этой причине многие руководящие органы ввели правила, снижающие вероятность такой ошибки. Так, если используются автоматизированные методы маркировки, то нормативные акты обязывают производителей устанавливать / настраивать оборудование таким образом, чтобы неправильная этикетка физически не могла быть прикреплена к продукту.
Законодательство большинства стран требует соблюдения ряда мер безопасности при упаковке фармацевтических препаратов. Например, колпачки для защиты от детей и другие подобные упаковочные изделия разрабатываются и испытываются в соответствии со стандартом ИСО 8317:2015 «Упаковка с защитой от вскрытия детьми – Требования и процедуры испытаний для повторно закрываемых упаковок».
Документ позволяет заинтересованным сторонам оцениваться легкость, с которой дети могут открыть повторно закрывающуюся упаковку и получить доступ к ее содержимому. Некоторые препараты могут требовать или не требовать защиты от детей – в зависимости от токсичности. Например, в Великобритании лекарства, содержащие более 25% парацетамола по весу, должны иметь колпачок, препятствующий вскрытию упаковки детьми.
Сохранение безопасности лекарств после извлечения из упаковки через стерилизацию
Важно помнить и о необходимости обеспечения безопасности фармпрепаратов вроде тех же пропитанных бинтов в после извлечения из упаковки. Минимизация рисков достигается, помимо прочего, через стерилизацию. Данный процесс используется медработниками и фармацевтами в ходе получения стерильных лекарственных форм для освобождения продукции, оборудования, вспомогательных веществ и упаковки от живых микроорганизмов, а также от спор подобных существ.
Недавно специалисты ИСО опубликовали новое тематическое руководство по стерилизации медицинских изделий. Авторы документы отмечают, что устранение микробиологической угрозы требует повышенного внимания при анализе любых возможных источников загрязнения, включая окружающую среду и персонал.
Факторов и требований много – в зависимости от того, где используется конкретный медицинский продукт. В новой технической спецификации содержится первый в своем роде набор согласованных на международном уровне требований к стерилизаторам.
Документ именуется ИСО / ТС 22421 «Стерилизация изделий медицинского назначения — Общие требования к стерилизаторам для окончательной стерилизации изделий медицинского назначения в учреждениях здравоохранения».
Как следует из названия, документ содержит общие требования и описывает соответствующие методы испытаний, а также закладывает основу для дальнейшей публикации более подробных стандартов, которые будут применяться для минимизации рисков. Авторы документа учли многочисленные факторы, которые способствуют безопасному и эффективному использованию медицинских изделий по назначению.
Источник
Анализ упаковки лекарственных препаратов
Потребительные свойства упаковки лекарственных средств (ЛС) являются одним из основных элементов при создании стратегических, визуальных и тактических инструментов обеспечения конкурентоспособности лекарственных препаратов (ЛП). При этом общая маркетинговая концепция удобства использования упаковки обосновывает полезность конкретного решения с точки зрения преимуществ, рассчитывая на «интуитивную понятность» потребителю не только выгоды, но и социально-экономических следствий ее неполучения. Последнее характерно и для государственного бюджета. Например, в США дополнительные издержки на медицинские расходы из-за неточного соблюдения врачебных предписаний ежегодно составляют 290 млрд долларов. До 5 % этих затрат рассматривается как следствие забывчивости потребителей и затруднений, связанных с пользованием упаковок. Поэтому медицинские специалисты отмечают роль приданных потребительных свойств упаковки в формировании лекарственного комплаенса, от которого зависит не только эффективность терапии, но и экономия бюджетно-страховых средств. Однако эти данные имеют фрагментарный характер, что затрудняет возможность рассмотрения удобства пользования упаковкой в качестве дополнительного социально-экономического инструмента при оптимизации затрат, связанных с нарушением режима приема ЛП [2, 4, 8].
Цель работы ‒ систематизация приданных потребительных свойств упаковки, влияющих на лекарственный комплаенс.
Объектом исследования являлись потребительные свойства упаковки ЛП, а предметом – лекарственный комплаенс. Составляющими исследования являлись:
– понятийные темы – удобство применения; удобство использования; комфортность применения; упаковка и комплаенс; факторы некомплаентности, дозирующие устройства; напоминающие устройства; информационные сигналы;
– метод анализа – неколичественный контент-анализ, основанный на изучении нечастотной модели содержания текстов и позволяющий выявить типы качественных моделей содержания;
– материальный носитель информации – специальная медицинская литература;
– поисковый инструмент информации – набор технических средств и программ.
Информация, относящаяся к регуляторному полю – графическое оформление и требования к инструкции-вкладышу ‒ в выборку не включалась.
Результаты контент-анализа показали, что вопросам влияния вида и типа упаковки, конструкции укупорочных и дозирующих устройств как факторов обеспечения удобства использования ЛП в большей мере посвящены маркетинговые сообщения, в которых позиционируются пластиковые упаковки, флаконы и аэрозоли с дозирующими устройствами. Специалисты в области медицины тоже отмечают влияние этих признаков на формирование комплаенса. Например, приводятся данные о положительном влиянии на комплаенс пациентов, страдающих заболеваниями суставов, увеличения размера колпачка упаковки мази «Хондроксид», замена круглой на треугольную форму крышки «Вольтарен эмульгеля». Акцентируется внимание на упаковки, позволяющие принимать ЛП без растворителя, например, гели и суспензии в пакетиках, полиэтиленовые одно- и мультидозированные ампулы. Подобные и портативные пластиковые упаковки рассматриваются как элемент формирования лекарственного комплаенса, особенно в период социальной активности больного [5, 7].
К одному из актуальных направлений развития упаковки как фактора комплаентности относится производство готовых шприцов, доля которых на мировом рынке увеличивается на 7–9 % ежегодно. Очевидными преимуществами данной формы упаковки в сравнении с концепцией «контейнер с препаратом + одноразовый шприц» является удобство и легкость обращения, а также повышение безопасности. Однако в России только завод «Сотекс» оборудован линией по выпуску преднаполненных шприцов, на которой производится препарат Эральфон® для лечения анемии [9].
Болезненность инъекций, особенно для детей или их большого количества взрослым, также рассматривается как один из факторов некомплаентности, что определяет поиск новых менее болезненных вариантов. Британец Оливер Блэкуэлл представил новый тип иглы, названной им «безболезненной». К обычному шприцу изобретатель добавил содержащую анестетик дополнительную иглу, которая чуть длиннее и много тоньше основной. Перед обычной иглой в кожу вводится игла намного меньшего диаметра, содержащая 0,2 мл анестетика, вторая игла войдёт почти в ту же точку. Кроме снижения болезненности такой вариант способствует комплаентности, когда рекомендуется перед инъекцией ЛС делать инъекцию с обезболивающим – анестетиком. Другим вариантом повышения комплаентности при парентеральном введении ЛС служит техническое решение американских ученых, которыми разработан прибор, доставляющий ЛС при помощи крошечных реактивных струй, проникающих через поры кожи. Новинка обходится без иглы и может доставлять препарат на разную глубину, так как позволяет программировать мощность его выброса [6, 10].
Одним из вариантов нивелирования лекарственной некомплаентности по причине забывчивости, особенно при терапии хронических заболеваний и больных пожилого возраста, служит придание упаковке информационных средств напоминания. Приводятся данные об использовании микро-таблетниц и упаковок таблеток с индивидуальными отделениями для каждого дня недели и надписями на внешней поверхности «утро», «день», «вечер», «ночь», что позволяет не только не забыть о времени приема ЛС, но и заметить, когда прием был пропущен. Их эффективность, по данным исследований, составляет до 20 % [2, 3].
В последние годы для некоторых стандартных полимерных и стеклянных упаковок ЛП используют мигающий колпачок в комплектации с беспроводным передатчиком. Когда подходит время принимать очередную дозу препарата, он мигает и далее через каждые пять минут подает с повышением громкости звуковые сигналы. Разработки более сложных устройств позволяют упаковке не только напоминать о приеме ЛС, но и контролировать соблюдение режима назначений врачом. Система представляет собой электронный модуль с датчиками, напечатанными на бумаге специальными проводящими красками, и обладает уникальной возможностью регистрировать время приема ЛП каждый раз, когда нарушается целостность оболочки. Данные сохраняются при помощи микроэлектронного сенсора, интегрированного в картон, и могут быть считаны лечащим врачом больного при помощи сканера, подключенного к персональному компьютеру. Особенно важны такие упаковки для ЛС, препятствующих отторжению трансплантированных органов [1, 4].
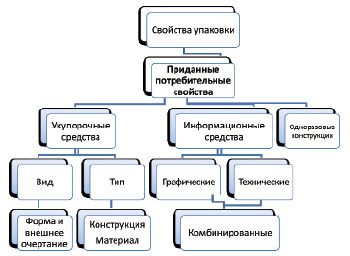
Анализ и сопоставление данных специальной литературы позволили систематизировать приданные потребительные свойства упаковки ЛП, влияющие на лекарственный комплаенс (рисунок).
Номенклатура приданных потребительных свойств упаковки,влияющих на лекарственный комплаенс
Из анализа данных рисунка следует, что на этапе потребления минимизируется значимость одного из основных маркетинговых признаков – дизайна упаковки ‒ и возрастает роль свойств, обеспечивающих комфортность пользования и информационных средств напоминания. Проведенное исследование имеет свои ограничения, носит субъективный, преимущественно качественный характер и требует количественного подтверждения полученных результатов при решении сложной социально-экономической проблемы – формирования лекарственного комплаенса.
1. Результаты систематизации данных литературы позволили обозначить номенклатуру приданных потребительных свойств упаковки, влияющих на лекарственный комплаенс.
2. Обозначена дополнительная возможность формирования лекарственного комплаенса и оптимизации дополнительной затратной части медицинской помощи путем обеспечения доступности ЛП в упаковках, обладающих рациональной совокупностью приданных потребительных свойств.
Рецензенты:
Данилова-Волковская Г.М., д.т.н., профессор, зав. кафедрой бухгалтерского учета, анализа и аудита Пятигорского филиала Российского государственного торгово-экономического университета, г. Пятигорск;
Гришин А.В., д.фарм.н., профессор, зав. кафедрой фармации Омской государственной медицинской академии Министерства здравоохранения Российской Федерации, г. Омск.
Источник