Acinetobacter baumannii

Acinetobacter baumannii широко распространены в природе, а также во внутрибольничной среде и обладают множественными механизмами резистентности к антибиотикам. Acinetobacter baumannii могут колонизировать желудочно-кишечный тракт, кожу пациента, рото- и носоглотку, конъюнктиву, влагалище и уретру.
В то же время Acinetobacter baumannii могут являться причиной пневмонии, трахеобронхита, сепсиса, инфекций мочевыводящих путей, эндокардита, раневой и хирургической инфекции, инфекций кожи и мягких тканей (включая некротизирующий фасциит), менингита, вентрикулита, абсцессов мозга, интраабдоминальных абсцессов, хориоамнионита, остеомиелита, артрита, синусита и перитонита.
Acinetobacter baumannii — возбудитель внутрибольничных инфекций
Проблема нозокомиальных (внутрибольничных) инфекций, вызываемых Acinetobacter baumannii, становится всё более актуальной из-за растущей резистентности данных микроорганизмов к антибактериальным препаратам. Резистентность Acinetobacter baumannii к цефтазидиму и ампициллину/сульбактаму за 5 лет увеличилась в 2–2,5 раза, к амикацину и ципрофлоксацину — в 8–9 раз. Встречаются штаммы, резистентные ко всем применяемым антибактериальным препаратам. Появление таких устойчивых внутрибольничных микроорганизмов связано с необоснованным и неограниченным использованием антибиотиков.
Acinetobacter baumannii вызывает 2-10 % всех грамотрицательных инфекций в Европе и США и до 1% всех внутрибольничных инфекций. В России Acinetobacter baumannii, наряду с Pseudomonas aeruginosa и Klebsiella pneumoniae, относится к трём самым часто происходящим и опасным возбудителям нозокомиальных инфекций. Во внутрибольничных условиях вспышки инфекций, вызываемые Acinetobacter baumannii в 60% случаев происходят во «взрослых» отделениях реанимации и интенсивной терапии. Оставшиеся 40% приходятся на отделения реанимации и интенсивной терапии новорожденных, ожоговые, нейрохирургические, хирургические, онкологические и гематологические отделения. Способствующими факторами являются: организация работы в этих отделениях – широкое использование инвазивных диагностических и лечебных мероприятий (катетеризация магистральных сосудов, искусственная вентиляция лёгких, длительная инфузионная терапия, энтеральное питание, методы внепочечного очищения крови), высокая концентрация больных с тяжелыми заболеваниями и сниженной иммунологической защитой, широкое и часто нерациональное использование антибактериальных и кортикостероидных препаратов, цитостатиков. Acinetobacter baumannii в большинстве случаев вызывает заболевания у тяжелобольных иммуноскомпрометированных пациентов (Ю.Л. Горбич, И.А. Карпов, 2012).
Acinetobacter baumannii относится к основными возбудителями раневых инфекций (Д.О. Вагнер).
Acinetobacter baumannii в систематике бактерий
Антибиотики, активные в отношении Acinetobacter baumannii
В течение многих лет основой терапии инфекций, вызванных Acinetobacter baumannii, были бета-лактамные антибиотики, часто в сочетании с аминогликозидами в случаях тяжелых инфекций. Однако большинство внутрибольничных Acinetobacter baumannii в настоящее время устойчивы к этим препаратам. Фторхинолоны, тетрациклины и глицилциклин, триметоприм-сульфаметоксазол, карбапенемы (за исключением эртапенема), полимиксины могут сохранять активность в отношении некоторых внутрибольничных штаммов. Однако в большинстве стран наблюдается быстрое нарастание резистентности к этим группам антибиотиков. В настоящее время наиболее клинически и финансово эффективным является использование монотерапии ампициллином/сульбактамом в дозах 24 г/сут или комбинированных режимов, включающих карбапенемы и ампициллин/сульбактам или карбапенемы и цефоперазон/сульбактам и нетилмицин. Последняя комбинация является экономически менее выгодной (Н.Д. Дмитриева и др., 2012).
По данным отечественного проекта «РЕЗОРТ», наибольшую активность в отношении 459 протестированных нозокомиальных штаммов Acinetobacter baumannii проявляли цефоперазон/сульбактам, имипенем и меропенем (2,2, 2,2 и 3,5% устойчивых изолятов соответственно), наименьшую – цефоперазон, гентамицин и пиперациллин (97,8, 89,1 и 91,7% соответственно) (Козлов С.Н., Белькова Ю.А. ).
Из представленных в данном справочнике антимикробных средств в отношении Acinetobacter baumannii (в общем) активны: левофлоксацин, нифурател, доксициклин. Acinetobacter baumannii устойчив к рокситромицину.
Источник
Acinetobacter baumannii — главная причина внутрибольничных инфекций
Acinetobacter baumannii — главная причина внутрибольничных инфекций
После открытия пенициллина человечество решило, что с инфекционными болезнями покончено. Но были проигнорированы правила эволюции и дрейфа генов. Человек изобретает всё новые антибиотики, а микроорганизмы укрепляют свои стенки, ускоряют процессы репликации и маскируются под клетки хозяина.
Проблема нозокомиальных инфекций, устойчивых к антибиотикам, стала настолько серьёзной, что недавно ей посвятили заседание Генеральной Ассамблеи ООН. Согласно представленным данным, из-за лекарственно-устойчивых инфекций ежегодно умирают более 700 000 человек. Не поддающиеся системам биологической защиты и лекарствам микробы встали в один ряд с глобальным изменением климата.
Во многих странах наблюдается рост заражения внутрибольничными инфекциями в стационарах лечебных учреждений, что существенным образом связано с распространением штаммов микроорганизмов, устойчивых к различным антибактериальным препаратам и системам биологической защиты.
Acinetobacter baumannii — самый распространенный больничный возбудитель благодаря широкому спектру природной и приобретенной резистентности.
В отделениях реанимации и интенсивной терапии, а также в ожоговых отделениях данный микроорганизм может явиться причиной развития разнообразных инфекционных осложнений: от госпитальной пневмонии до сепсиса.
Эта бактерия обладает механизмами, обеспечивающими устойчивость к подавляющему большинству антибиотиков, к дезинфицирующим средствам, высушиванию, а также к ультрафиолетовому облучению. Ее патогенность обусловлена суммарным действием ряда факторов на системы биологической защиты. Одним из таких факторов являются капсульные полисахариды – поверхностные структуры, формирующие толстую клеточную стенку.
Естественные природные враги Acinetobacter baumannii — это вирусы. Свойство определенных штаммов вирусов убивать специфичные виды бактерий исследовали ещё в начале XX века. Бактериофаги были открыты в 1915 году британским микробиологом Фредериком Туортом. Появление антибиотиков затормозило исследования в данном направлении, но с появлением мультирезистентных бактериальных штаммов поиск других способов борьбы возобновился.
Ученые исследовали литические бактериофаги, которые после заражения бактериальной клетки и периода размножения разрушают бактерию изнутри. Литические фаги не влияют на нормальную микрофлору, не активируют системы биологической защиты, соответственно, не вызывают развития дисбактериозных процессов. Бактериофаги способны реплицироваться до уничтожения всех бактерий.
Актуальность проблемы заражения внутрибольничными инфекциями заставляет искать новые и эффективные методы решения этой проблемы на международном уровне. При совместной работе российских и белорусских микробиологов была изучена организация геномов vB_AbaP_AS11 и vB_AbaP_AS12, описана стратегия взаимодействия систем биологической защиты, вирусов и бактериальных клеток. В результате были найдены эффективные с широким спектром природной и приобретенной резистентности бактериофаги (AS11 и AS12) рода Fri1virus, подсемейства Autographivirinae семейства Podoviridae. Литическая активность бактериофагов была протестирована на 100 клинических антибиотикоустойчивых штаммах Acinetobacter baumannii из 53 больниц и 32 городов России и Белоруссии. Для этих фагов характерны быстрая адсорбция к бактериальной клетке-хозяину и высокая плодовитость.
Для лечения внутрибольничных инфекций необходимы самые современные лекарства, к которым опасная бактерия еще «не привыкла». Таким образом, антибактериальная терапия превращается в бесконечную гонку, в которой, как показывает совместная работа российских и белорусских ученых, у человечества есть шанс одержать победу.
Источник
Ацинетобактер
Автор: врач – клинический фармаколог Трубачева Е.С.
Автор: врач – клинический фармаколог Трубачева Е.С.
Если еще каких-то 7 лет назад ацинетобактер была зверем, о котором знали реаниматологи крупных больниц да клинические фармакологи, то менее пяти лет назад ситуация кардинально изменилась – теперь про ацинетку знают все, кто в том или ином виде работает в стационарах. Она очень быстро заместила собой всю предыдущую внутрибольничную микрофлору и фактически вышла на первый план самых проблемных внутрибольничных микробов, заняв чуть ли не основную нишу ВБИ.
Автор сразу хотел бы предупредить, что речь здесь пойдет не столько об Acinetobacter baumannii, сколько о семействе ацинетобактеров, ибо клиническую значимость имеет не только вышеупомянутый возбудитель.
Ацинетобактеры являются представителями тройки основных опасных возбудителей согласно определению ВОЗ. Двух других представителей из этого списка мы уже обсудили: это синегнойная палочка и энтеробактерии (клебсиелла, кишечная палочка, энтерококки). Именно для этой могучей тройки в первую очередь и должны разрабатываться новые антибиотики, но пока с этим как-то не очень.
Микробиологические аспекты
Ацинетобактер (или ацинетка, как любит обзывать ее автор), является фактически «кровной родней» другого общеизвестного неферментера – синегнойной палочки. Но, в отличие от синегнойки, природно-устойчивого ацинетобактера вам могут принести прямо с улицы. То есть в природе имеются штаммы, и в очень большом количестве, которые изначально природно-устойчивы фактически ко всему арсеналу имеющихся в медицине антибиотиков. А еще таких же, но уже внутрибольничных мутантов не менее «удачно» выращивают в отделениях с высокой частотой использования антибактериальных препаратов. И это при том, что принести такого микроба в больницу, а также занести его в больного, может вообще любой человек, так как изначально ацинетка, как и синегнойка, является почвенным микробом, а потому горшки с цветами, садоводы-огородники, зимой растящие рассаду, летом ковыряющиеся на даче, а потом, нормально не отмыв руки, начинающие перевязывать раны или менять катетеры, да просто посетители с пылью на ботинках – все они в каждый момент времени приносят в больницы миллиарды подобных микробов. И это как раз то, о чем автор упоминал в разговоре о клебсиелле – вывести ацинетку, в отличие от синегнойки, несопоставимо труднее. Напомню, синегнойка предпочитает мокрую теплую грязь, поэтому ее проще отсечь от заноса в чистые отделения и внутри самой больницы проще выбить. А теперь представьте, чего будет стоить избавиться от пыли, комнатных растений, любителей-огородников и ломящихся, теперь уже даже в реанимации, посетителей. Практически нереально, если это только не ламинарный бокс.
Поэтому будем изучать врага в лицо
Общее представление о том, что из себя представляют дикие и непуганые антибиотиками ацинетобактеры, можно составить на EUCAST. Для тех, кто никогда не пользовался данным ресурсом, небольшая подсказка – тыкаем мышкой (или пальцем, смотря откуда читаете этот опус) в плашку «Species», выбираем один из 25-ти ацинетобактеров и наслаждаемся изучением. Общую антибиотикочувствительность семейства Acinetobacter spp. можно рассмотреть тут. Небольшое пояснение для тех, кто здесь впервые, – клинически значимыми минимальными подавляющими концентрациями (MIC), которыми можно и нужно пользоваться в клинической практике (а также как маркер того, какие антибиотики будут работать, а какие нет – их MIC указаны с чисто исследовательскими целями), являются показатели, отмеченные синими клеточками. На эти же показатели настроены аппараты для определения антибиотикочувствительности, с помощью которых продемонстрированы антибиотикограммы в наших статьях.
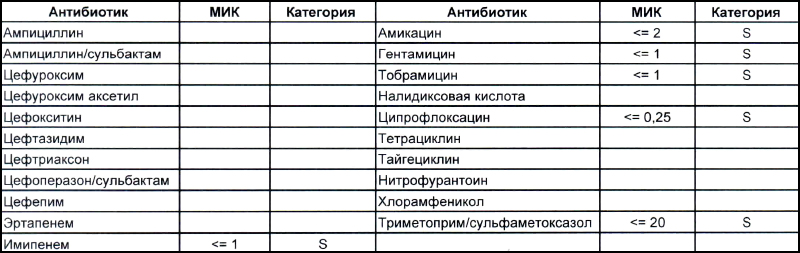
Теперь посмотрим на, можно сказать, типичных представителей семейства Acinetobacter spp. Необходимо отметить, что продемонстрированные ниже возбудители выделены из ран, полученных в результате ДТП в летнее время, причем у пациентов, которые длительное время не лечились антибиотиками, то есть оба зверя являются дикими.
На первом фото лечащему врачу повезло, так как ему достался возбудитель, чувствительный ко всему возможному арсеналу антибиотиков, которые в принципе могут повлиять на данный микроб.
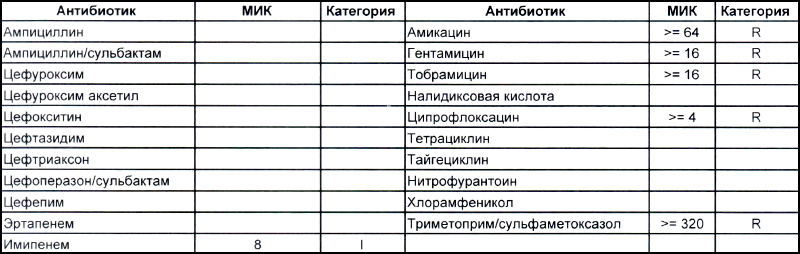
На второй антибиотикограмме возбудитель тоже получен из раны, ни разу не леченной антибиотиками, а также сам больной длительное время ничего антибактериального не употреблял. Данный случай очень хорошо демонстрирует то, что мы обсудили раньше, – только по антибиотикограмме в случае ацинеток трудно сказать, внутрибольничный возбудитель вызвал гнойно-воспалительный процесс или дикий уличный.
В научно-исследовательском институте, который может провести генетическое исследование возбудителя, смогут выяснить полностью, дикий это штамм или внутрибольничный, а мы, работающие на земле, скорее всего, не ответим на этот вопрос. Правда, у нас теперь СК все про всех знает, и автор уже давно ждет, когда очередного несчастного еще и в такого рода заражении обвинят.
Следует отметить, что обе эти картинки не отменяют факта наличия внутрибольничного заражения как первым штаммом (горшки с цветами помним?), так и вторым, в который под действием использующихся в больнице антибиотиков может выродиться первый. Ациентка, как и предыдущие обсуждаемые возбудители ВБИ, так же не имеет крылышек и ножек, ее точно так же переносят на руках и плохо обработанном медицинском оборудовании (эндоскопы, точнее, бронхоскопы, это просто бич крупных стационаров). Поэтому только внутриведомственный микробиологический надзор и работа над соблюдением санэпидрежима помогает удержать и эту зверюгу в хоть каких-то приемлемых рамках.
Клинические аспекты
Что способен вызвать ацинетобактер?
- Раневую инфекцию
- Инфекции кровотока
- Инфекции дыхательных путей – в первую очередь, внутрибольничную пневмонию, часто вентилятор-ассоциированную, особенно так называемую позднюю (более семи суток на ИВЛ). Здесь он делит пальму первенства с синегнойкой и MRSA
- Внутрибольничные менингиты
- Инфекции мочевыводящих путей, чаще всего ассоциированные с использованием эндоскопического оборудования
- Перитониты у пациентов на перитонеальном диализе
- Почти полный набор инфекций, связанных с установкой имплантов или протезов
В общем, как вы можете видеть, ацинетка способна загубить на корню любой врачебный труд, так как инфекции, ей вызванные, имеют высокий процент летальности у пациентов, имеющих факторы риска развития подобной инфекции.
К факторам риска относятся:
- пациенты мужского пола
- наличие сопутствующих заболеваний, особенно в стадии декомпенсации
- отдельно отметим сахарный диабет
- пожилой возраст
- длительное нахождение в стационаре/стационарах
- использование массированной терапии антибиотиками без явных показаний или использование комбинированной антибиотикотерапии там, где она так же не показана – вспоминаем пословицу «свято место пусто не бывает» и не даем селективных преимуществ подобным убийцам
- предшествующая текущему заболеванию госпитализация в реанимацию
- и лично от автора – ДТП в сухой теплый период, если не сделать нормальное ПХО сразу, шанс получить ацинетобактерную инфекцию рану достаточно высок
Чем лечить?
Хороший вопрос. Точно такой же, как «чем лечить внутрибольничную клебсиеллу», которым мы задавались ранее.
Как вы могли убедиться, лечить ацинетку эмпирически (а это возможно только при тщательном внутрибольничном мониторинге), и даже с использованием диско-диффузионного метода, не очень-то и получится. Точнее, не получится совсем. Нужны аппаратные методы диагностики, чтобы точно знать, с чем вы имеете дело. И внутрибольничный мониторинг тоже крайне необходим, особенно если неферментеры сеются массово, чтобы знать — заполз ли возбудитель с улицы или уже свой зверинец развели. Во втором случае только мыть-мыть и еще раз мыть всю больницу полностью, а не только одно отделение, а также переходить на полностью одноразовые расходники, и к аппаратам ИВЛ тоже. Автор понимает, что при этих словах или в монитор захочется плюнуть, или помидором тухлым швырнуть, благо сезон пока не закончен.
Так как лечить?
В рамках клинических рекомендаций по той нозологии, которая у вашего пациента имеется, выложенных здесь, всегда только комиссионно, с привлечением клинических фармакологов и клинических микробиологов. И мойте руки после каждого подобного пациента очень тщательно — это ваша личная техника безопасности.
Источник